茶花粉水提物对酒精性肝损伤大鼠模型肝脏组织中COL1A1、α-SMA表达水平的影响
刘晓红,王菊梅*,闫伦春,单慧明,谭壮忱,杨立波
长期过度饮酒会使肝细胞反复发生脂肪变性甚至坏死,同时导致酒精性肝损伤,最终导致肝癌[1]。使用保肝药物可以有效缓解酒精肝,但是大量使用药物会对肾脏等其他器官造成较大的负担。补充维生素、矿物质等可以提高自身免疫力达到缓解酒精性肝损伤功效[2]。茶花粉水提物的成分复杂,包含有蛋白质、氨基酸、糖类、脂类、维生素、微量元素及大量的生物活性物质[3],服用茶花粉水提物可以补充蛋白质、脂肪充维生素、矿物质等有效缓解酒精性肝损伤[4]。目前对茶花粉水提物成分的研究较多,但有关茶花粉水提物对酒精肝的影响的研究相对较少。本文旨在研究茶花粉水提物对酒精性肝损伤大鼠模型肝脏组织中胶原蛋白Ⅰ(collagen, type I, alpha 1,COL1A1)、α-平滑肌肌动蛋白(alpha-smooth muscle actin,α-SMA)表达水平的影响,以期了解茶花粉水提物对酒精性肝损伤大鼠模型肝脏组织中COL1A1、α-SMA表达水平的作用机理,从而为酒精性肝损伤的治疗提供一定的理论依据。
1 材料
1.1 动物
选取60只雄性SD大鼠,体重200±30 g,由北京维通利华实验动物技术有限公司提供,动物许可证号SCXK(京)2017-0022,分12个笼子饲养,每个笼子5只。在本院动物中心实验室,饲养温度20~25 ℃,相对湿度50%~65%,无噪音条件下自由饮水进食。
1.2 药物与试剂
茶花粉水提物购自扬州同人生物工程有限公司;谷丙转氨酶检测试剂盒、谷草转氨酶试剂盒购自上海恪敏生物科技有限公司、超氧化物歧化酶试剂盒及丙二醛试剂盒均购自上海恒远生物科技有限公司;COL1A1和α-SMA抗体购自武汉博士得生物有限公司;中性福尔马林、酒精、二甲苯购自天津科密欧有限公司;红星二锅头购自武商量贩。
1.3 仪器
BS-124s 型电子天平购自北京赛多斯仪器系统有限公司;TDL-5 型台式离心机购自上海安亭科学仪器厂;光学显微镜购自东莞市同创仪器有限公司;切片机购自德国Leica公司;低温离心机购自湖南恒诺离心机有限公司;蛋白电泳及转膜仪购自美国Bio-Rad公司。
2 方法
2.1 建立模型
大鼠适应性喂养1 周后,使用 56°红星二锅头灌胃,第一周灌胃计量为:6 mL/kg;第二周灌胃计量为:8 mL/kg;第三周灌胃计量为:10 mL/kg,第四至十周灌胃剂量为:11 mL/kg。具体造模方法和判断模型是否成功参考梁惠等[5]研究。
2.2 分组及药物干预
60只FPS级雄性SD大鼠随机分为4组,每组15只,其中45只大鼠制成酒精性肝损伤模型,建立模型和判断模型是否建立成功参考梁惠等[5]研究。将制成模型的大鼠分为模型组、低剂量茶花粉水提物组和高剂量茶花粉水提物组,剩下15只作为对照组;低剂量茶花粉水提物组大鼠使用50 mg/kg·d-1的茶花粉水提物灌胃,高剂量茶花粉水提物组大鼠使用100 mg/kg·d-1的茶花粉水提物灌胃,对照组和模型组分别以等量的生理盐水灌胃处理,每天一次,持续21 d。
2.3 检测项目
2.3 1 测量大鼠肝脏质量并计算肝指数
使用脊椎脱臼法处死大鼠后,取大鼠肝脏并准确称量大鼠肝脏质量,计算大鼠肝指数。
2.3.2 检测大鼠血清ALT、AST水平、肝组织SOD、MAD水平
药物治疗结束后24 h,给予3%戊巴比妥钠(生产厂家:上海依赫生物科技有限公司;生产批号:20180212)麻醉,腹主动脉取血0.5 mL,使用离心分离血清谷丙转氨酶(glutamic pyruvic transaminase,ALT)、谷草转氨酶(glutamic oxaloacetic transaminase,AST)试剂盒子检测其ALT及AST水平,操作方法严格按照试剂盒子说明书操作。
取大鼠肝组织,在冷生理盐水中漂洗后滤纸拭干。加入肝组织重量9倍的生理盐水并置入匀浆器中在冰水中匀浆5 min,使用恒温离心机在4℃、3 000 r/min条件下离心10 min。分别吸取0.1 mL上清液,严格按照超氧化物歧化酶(total superoxide disumutase,T-SOD)和丙二醛(malondialdehyde,MDA)试剂盒子说明书上的操作方法测定SOD活性和MDA含量。
2.3.3 Western blot 检测蛋白表达水平
按照Western blot 检测方法操作,使用蛋白质条带用扫描仪进行扫描,以β-actin为内参,应用Imagaquent 5.1软件对COL1A1和α-SMA蛋白质条带灰度进行相对定量分析。以目的蛋白条带与 β-actin 灰度比值表示蛋白相对表达水平。实验重复 3 次,取平均值为最终结果。
2.3.4 HE染色观察大鼠肝组织
使用HE染色,具体步骤为:使用二甲苯浸泡10~15 min,分别使用100%、95%、80%、70%、50%酒精的酒精依次冲洗2~3 min,使用蒸馏水冲洗1 min后使用苏木精浸泡10~15 min,再使用蒸馏水冲洗20 min。使用盐酸酒精分化后再次使用水冲洗10~20 min后使用氨水冲洗一次,在此重复酒精冲洗过程(100%、95%、80%、70%、50%酒精的酒精依次冲洗2~3 min),完成后使用伊红染色30s后使用95%酒精Ⅰ和95%酒精Ⅱ浸泡1~2 min后再次使用100%酒精Ⅰ和100%酒精Ⅱ浸泡10~15 min,分别使用二甲苯Ⅰ和二甲苯Ⅱ浸泡10~15 min最后中性树胶封片即可。在电子显微镜下使用10×40的倍镜观察肝组织情况。
2.4 统计学方法
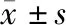
3 结果
3.1 大鼠肝脏质量及肝指数
由表1可以看出,相比对照组,模型组大鼠体质量无显著差异(T=0.083,P=0.935),模型组大鼠肝质量(T=5.748,P=0.000)及肝指数(T=15.257,P=0.000)显著升高。相比模型组,低剂量茶花粉水提物组大鼠体质量无显著差异(T=0.527,P=0.595),大鼠肝质量(T=4.156,P=0.000)及肝指数(T=12.952,P=0.000)显著降低。相比低剂量茶花粉水提物组,高剂量茶花粉水提物组大鼠体质量无显著差异(T=0.540,P=0.592),肝质量(T=0.614,P=0.534)及肝指数(T=2.738,P=0.016)显著降低。
3.2 大鼠血清ALT、AST水平及肝组织SOD、MAD水平
由图1可以看出,相比对照组大鼠血清ALT(30.21±2.32)U/L、AST(62.36±2.87)U/L、SOD(138.21±6.32)U/mL、MAD(5.81±1.08)mmol/mL,模型组大鼠血清ALT显著升高(79.32±2.89)U/L(T=52.105,P=0.000),AST显著升高(115.35±5.01)U/L(T=35.544,P=0.000),SOD显著降低(70.21±29.32)U/mL(T=8.780,P=0.000);MAD显著升高(13.01±1.80)mmol/mL(T=18.25,P=0.000)。相比模型组,低剂量茶花粉水提物组ALT显著降低(53.21±3.21)U/L(T=23.414,P=0.000),AST显著降低(80.37±4.01)U/L(T=21.11,P=0.000),SOD显著升高(120.32±12.39)U/mL(T=6.097,P=0.000),MAD显著降低(9.85±1.70)mmol/mL(T=6.076,P=0.000)。相比低剂量茶花粉水提物组,高剂量茶花粉水提物组ALT显著降低(44.87±2.49)U/L(T=7.950,P=0.000),AST显著降低(74.36±4.65)U/L(T=3.790,P=0.007),SOD显著升高(135.28±8.23)(T=3.895,P=0.006),MAD显著降低(7.72±2.31)mmol/mL(T=2.876,P=0.007)。

表1 大鼠肝脏质量及肝指数
注:与对照组相比,**P<0.01;与模型组相比##P<0.01

图1大鼠血清ALT、AST水平及肝组织SOD、MAD水平 与对照组相比**P<0.01;与模型组相比##P<0.01;A为各组大鼠ALT含量水平;B为各组大鼠AST含量水平;C为各组大鼠SOD含量水平;D为各组大鼠MAD含量水平
3.3 大鼠肝组织COL1A1和α-SMA蛋白表达水平
由图2可以看出,相比对照组COL1A1和α-SMA蛋白相对表达量(0.40±0.11)、(0.51±0.12),模型组COL1A1蛋白表达量(1.49±0.17)显著升高(T=20.184,P=0.000),α-SMA蛋白表达量(1.50±0.16)显著升高(T=19.171,P=0.000)。相比模型组,低剂量茶花粉水提物组COL1A1蛋白表达量(0.85±0.15)显著降低(T=10.933,P=0.000),α-SMA蛋白表达量(1.15±0.14)显著降低(T=6.375,P=0.000)。相比低剂量茶花粉水提物组,高剂量茶花粉水提物组COL1A1蛋白表达量(0.65±0.12)显著降低 (T=4.032,P=0.004),α-SMA蛋白表达量(0.84±0.14)显著降低(T=6.064,P=0.000)。
图2大鼠肝组织COL1A1和α-SMA蛋白表达水平 与对照组相比**P<0.01;与模型组相比##P<0.01;A为蛋白质印记观察COL1A1和α-SMA蛋白表达情况;B为COL1A1和α-SMA蛋白相对表达情况
3.4 HE染色观察结果
对照组大鼠肝细胞较为完整,且细胞核清晰可见,细胞核与细胞浆呈鲜明对比;模型组大鼠细胞出现较多的细胞核坏死,且细胞出现纤维化状态,部分细胞质间出现空隙,低剂量茶花粉水提物组大鼠,细胞核出现坏死的数目降低,且细胞纤维化显著降低;高剂量茶花粉水提物组大鼠肝细胞无显著纤维化,且细胞核、细胞质呈鲜明对比。
4 讨论
近年来,对花粉水提物的研究越来越多,其中茶花粉水提物因其含有丰富的营养物质和抗氧化等性质受到广泛的关注[6]。研究表明:花粉水提物具有降血脂、降血糖、抗动脉粥样硬化、治疗前列腺等功效[7-8]。茶花粉水提物中含有多酚和黄酮类化合物,这两类化合物是天然的抗氧化剂,可以降低人体内的过氧化反应,对人体健康有着非常重要的作用[9]。
酒精在肝脏中的分解代谢会促进活性氧的产生,使得ROS在人体内大量累积,引发肝细胞膜发生脂质过氧化而损伤肝细胞。夏婷研究表明:氧应激和脂质过氧化是酒精引起肝脏损伤的重要原因之一[10]。抗氧化体系主要包括酶系和非酶系两大类,酶体系中,最主要的是SOD,其含量多少可以直接反应氧化应激的程度[11]。本实验中发现,模型组大鼠体内SOD含量显著减少,说明其肝脏内的氧化应激反应显著增强,使用茶花粉水提物处理后,SOD含量显著增加,说明其氧化应激受到了抑制,且随着茶花粉水提物处理浓度增加,SOD含量显著升高,说明茶花粉水提物可以降低大鼠体内氧化应激反应且随着使用浓度增加,大鼠体内氧化应激反应抑制程度增加。赵高远[12]研究表明:SOD可以反映体内氧化应激能力的强弱,且升高SOD浓度可以有效抑制氧化应激反应,保护肝脏组织,与本研究得出的结论相一致。吴志刚等[13]研究表明:MAD含量增加会使得肝内大量脂质沉积并且会使得机体的抗氧化能力减弱。肝细胞膜和线粒体膜受损,引起血清丙氨酸转氨酶升高,同时也会使得大鼠的肝组织游离脂肪酸水平明显升高,诱发肝细胞死亡导致肝脏炎症反应和细胞功能障碍[14]。MAD的含量可以反映机体内发生脂质过氧化的程度,使自由基与生物膜中的多不饱和脂肪酸发生反应并使得氧化产物分解,由此可以得知MAD的含量可间接反映出细胞损伤的程度[15]。本实验中可以看出,模型组大鼠MAD含量显著升高,说明肝脏内脂质增加,且脂质氧化程度较高。使用茶花粉水提物处理后大鼠肝组织中MAD含量显著降低,说明大鼠肝脏组织中的脂质水平降低、脂质氧化程度也较低,肝脏得到了有效的保护,且随着茶花粉水提物处理剂量的增加,脂质的氧化反应逐渐降低。彭国霞等[16]研究表明:花粉具有较强的抗氧化活性可以明显改善酒精引起的肝细胞损伤,与本研究得出的结论相一致。

图3HE染色观察大鼠肝组织(×400) A为对照组(较为完整);B为模型组(严重纤维化);C为低剂量茶花粉水提物组(较轻纤维化);D为高剂量茶花粉水提物组(无显著纤维化)
血清ALT、AST活力的大小是检验肝脏损伤的重要指标之一。刘鑫等[17]研究表明:血清ALT、AST活力的大小,直接反映了肝细胞受损的程度。本实验中可以看出,模型组大鼠血清ALT、AST活力显著增加,说明大鼠肝脏受损程度显著增加。使用茶花粉水提物处理后大鼠血清ALT、AST活力显著降低,说明茶花粉水提物处理可以有效降低ALT、AST活力保护肝脏,且随着茶花粉水提物使用剂量增加,ALT、AST活力进一步降低,说明茶花粉水提物可以抑制ALT、AST活力且在一定浓度范围内呈浓度依赖性。赵燕平等[18]通过探讨破壁灵芝孢子粉对大鼠肝脏损伤研究表明:血清ALT、AST活力肝组织炎症程度关系密切,与本研究得出的结论相一致。
酒精还会损伤产生的细胞因子或炎性因子刺激肝星状细胞的活化[19],肝星状细胞活化后会伴有NF-kB等转录因子的激活及c-myb基因表达的增强,而c-myb蛋白可结合α-SMA基因调控区,表达平滑肌激动细胞骨架蛋白α-SMA,且α-SMA的表达程度与肝星状细胞活化的程度及数量呈正相关[20-21]。α-SMA阳性的肝星状细胞出现的NF-kB核转位活性同时有靶基因的表达,产生急性期蛋白、黏附因子、生长因子等,加速肝纤维化进程[22-23]。肝纤维化发生的主要变化是星状细胞的活化增殖,当肝星状细胞活化后,储存的维生素A脂滴含量明显减少,同时维甲酸及其受体含量也下降。活化的肝星状细胞增殖,并分泌大量胶原和一系列促纤维化细胞因子,使 COL1A1生成明显增加,同时抑制胶原降解因子生成,使胶原降解下降,最终导致胶原沉积,诱发肝脏纤维化。本研究发现,模型组大鼠COL1A1和α-SMA蛋白表达水平显著增加,使用茶花粉水提物处理后COL1A1和α-SMA蛋白表达水平显著降低,说明茶花粉水提物处理可以有效抑制COL1A1和α-SMA蛋白表达,同时防止肝脏的纤维化。毕晓娟等[24]研究表明:肝脏内的COL1A1和α-SMA蛋白表达与肝脏纤维化密切相关,与本研究得出的结论相一致。
综上所述,茶花粉水提物可以降低酒精性肝损伤,同时降低大鼠肝脏组织中COL1A1、α-SMA表达,有效缓解酒精性肝损伤,其作用机制可能与茶花粉水提物可以抑制肝脏组织的氧化应激反应有关。

