脑出血疾病患者脑脊液中NSE、S100β及miR-124-3p、miR-146a-5p检测的临床意义
杨 奇,史清海,牛莉莉,王 黎,李 凯,邓梦芸,胡慧婷,伏建峰△
(1.石河子大学医学院,新疆石河子 832002;2.新疆军区总医院全军临床检验诊断中心,新疆乌鲁木齐 830000;3.新疆昌吉州人民医院检验科,新疆昌吉 831100)
脑出血(ICH)占急性脑卒中的15%~20%,具有高发病率和高病死率[1]。ICH后,血脑屏障(BBB)损伤,脑水肿和炎症等病理生理过程被激活,参与相关过程的分子可能是诊断及病情评估潜在生物标志物[2]。脑脊液(CSF)是具有许多重要功能一种体液,并与中枢神经系统(CNS)的细胞外环境直接接触,是CNS各种物质代谢的媒介[3]。神经元特异性烯醇化酶(NSE)和酸性钙结合蛋白(S100β)属于CNS的结构蛋白质,被广泛用作CNS组织损伤的特异性生物标志物[4]。到目前为止,大多数研究主要集中在血液中,考虑到脑或脊髓与CSF之间的紧密解剖和功能关系,在CNS损伤时CSF中特异性结构蛋白浓度可能迅速且明显增加[5]。微小RNA(miRNA)是短的非编码RNA(20~24个核苷酸),其在脑组织中含量丰富,人体体液的基因表达谱和ICH实验模型已经提示miRNA是重要的基因调节因子且与神经系统疾病息息相关[6],而目前ICH患者CSF中miRNA表达变化的研究报道相对较少。本研究通过分析ICH患者CSF NSE、S100β表达水平及发生显著改变的miRNA,探讨其对脑出血疾病的诊断价值及对病情的评估。
1 资料与方法
1.1一般资料 选取2016年3月至2018年4月期间在新疆军区总医院神经外科确诊的新发ICH 26例患者作为病例组,其中基底节出血15例,丘脑出血4例,脑干出血4例,脑叶出血3例;男15例,女11例,年龄(56.70±14.50)岁,出血量35.00(23.25,65.45)mL。对照组22例;男14例,女8例,年龄(34.86±12.46)岁。诊断符合中国脑出血诊治指南(2014)诊断标准,并符合纳入标准:(1)均为原发性出血病例;(2)经临床医生系统评估(病史、神经系统检查、影像学检查(CT/MRI)符合自发性脑出血指针;排除标准:(1)先天性血管病、血管炎;自身免疫系统疾病;(2)颅脑手术史、外伤史、肿瘤史(肺癌、黑色素瘤)、血液病史、心脑卒中史;(3)近期口服抗凝、抗血小板药物;(4)无法配合抽取CSF患者。脑出血组病情严重程度按照格拉斯哥昏迷评分(GCS)分为轻度ICH组(高GCS评分组)、重度ICH组(低GCS评分组)各13例。对照组选取同期住院经头颅CT/MRI证实无CNS疾病(脑血管、感染、脱髓鞘、变性疾病)、无心脑血管病史,且CSF常规检查均在正常参考范围内。所有CSF样本的采集均经患者本人或家属同意,并签署知情同意书。用于本项目研究的临床样本已获得新疆军区总医院伦理委员会的审核。
1.2方法
1.2.1试剂与仪器 MiRNA的测定采用qRT-PCR法,主要试剂及仪器包括:miRcute miRNA提取分离试剂盒(离心柱型),miRcute miRNA cDNA第一链合成试剂盒,miRcute增强型荧光定量检测试剂盒(SYBR Green),外参引物(CR100-01,TIANGEN,北京),余miRNA引物均购自天根生化科技(TIANGEN,北京),见表1;β2-微球蛋白(β2-MG,货号:BM7513,北京利德曼)、天门冬氨酸氨基转移酶(AST,货号:05850819190,上海罗氏诊断)、乳酸(LAC,货号:05171881190,上海罗氏诊断)、乳酸脱氢酶(LD,货号:05169330190,上海罗氏诊断)、微量清蛋白(mAlb、货号:04469658190,上海罗氏诊断)、NSE(货号:12133113122,上海罗氏诊断)、S100β(货号:03175243190,上海罗氏诊断);Cobas全自动荧光定量PCR分析仪Z480、Cobas e701、Cobas e602全自动生化仪均购自罗氏公司;BIO-RED T100 PCR仪购自美国伯乐公司。
1.2.2CSF样本收集 收集研究对象入院48 h内CSF样本3~5 mL,使用无菌管收集,上下轻轻颠倒混匀8次后,立即置于4 ℃或冰盒中运送,将CSF转移至1.5 mL无RNA酶离心管中,2 000 r/min离心10 min;将上清转移至1.5 mL无RNA酶离心管中,弃去细胞及组织沉淀;每管吸入500 μL上清进行封装标记,并置于-80 ℃保存备用。

表1 miRNA成熟序列及对应引物
1.2.3数据采集 采集患者入院初的基本病历资料,包括姓名、年龄、既往史、初步诊断、CSF常规检查、GCS评分、出血量(入院时CT按多田公式计算[血量(mL)=π×长(cm)×宽(cm)×高(cm)/6])。收集研究对象入院48 h内血常规、凝血四项、清蛋白等检查结果。
1.2.4CSF游离miRNA提取、检测 提取及检测miRNA严格按照TIANGEN提取及检测试剂盒试验流程进行。佩戴一次性手套和口罩,所使用枪头、EP管均为RNASE Free,其余实验相关器材均经去RNA酶处理。由于CSF中miRNA含量低,提取出的RNA样本OD260/280的测定结果不可靠,本文未列出浓度。在待检测CSF标本中均加入外参1 μL(cel miRNA-39,TIANGEN提供,参考Ct值范围:6~8)为质检参考指标。提取:将200 μL CSF样本用miRcute miRNA提取分离试剂、氯仿、无水乙醇进行一系列的提取及分离,最终从离心柱洗脱获得20 μL提取物。检测方法:每份CSF样本提取物进行逆转录反应合cDNA第一链,总反应体系为20 μL,(反应条件:42 ℃ 60 min逆转录,95 ℃ 3 min酶失活),并使用特异性上游引物进行扩增,以2 μL的cDNA为模板(1∶4稀释),总反应体系为20 μL(反应条件:95 ℃预变性15 min,95 ℃变性20 s,65 ℃退火30 s,72 ℃延伸30 s,35个循环)。以扩增曲线和熔炼曲线综合评估Ct的可靠性,并采用2-ΔΔCt法计算miRNA的相对表达量。
1.2.5CSF生化指标的检测 按照自动生化仪、化学发光分析仪及相对应的试剂盒操作流程,检测CSF中下列生化指标:β2-MG、AST、LAC、LD、mAlb、NSE、S100β。
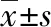
2 结 果
2.1一般资料 两组在糖尿病史、吸烟史、饮酒史、白细胞计数(WBC)、纤维蛋白原比较差异无统计学意义(P>0.05);而高血压史、高脂血症、GCS评分比较差异有统计学意义(P<0.05),且ICH组中高血压病和高脂血症人数明显多于对照组,见表2。
2.2CSF部分生化指标比较
2.2.1ICH组与对照组CSF生化指标比较 按照GCS评分将ICH组分为轻度ICH组、重度ICH组,与对照组相比,轻度ICH组、重度ICH组CSF 血糖(GLU)、血浆清除率(CL)、LD差异无统计学意义(P>0.05);轻度ICH组CSF尿蛋白(PRO)、清蛋白指数(QAlb,QAlb=CAlb/SAlb)、mAlb明显高于对照组;重度ICH组、轻度ICH组β2-MG、AST、LAC水平均明显高于对照组;而NSE、S100β在重度ICH组、轻度ICH组高于对照组,重度ICH组高于轻度ICH组,3组间差异有统计学意义(P<0.05)。见表3。
表2 病例组和对照组一般资料比较
注:-表示无数据

表3 ICH组与对照组CSF生化指标比较
注:Pa为对照组与轻度ICH组P值,Pb为对照组与重度ICH组P值,Pc为轻度ICH组与重度ICH组P值
2.2.2ICH患者出血量与CSF NSE、S100β水平相关性研究 为了研究改变的CSF NSE、S100β水平是否与脑出血量有关,笔者使用了Pearson相关系数来确定是否存在相关性。发现CSF NSE的水平与ICH患者出血量显著相关(r=0.86;P<0.01),见图1A;CSF S100β的水平与ICH患者出血量有相关性(r=0.49;P<0.05),见图1B。
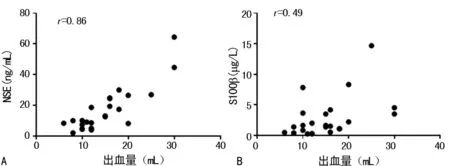
注:A为NSE,B为S100β
图1ICH组和对照组CSFNSE、S100β水平与出血量的相关性研究结果
2.3ICH患者CSF miRNA表达研究 本研究应用qRT-PCR方法检测文献报道的与中枢神经系统疾病相关的15个靶标miRNA,探索其在脑出血疾病中的潜在诊断与病情评估价值。与对照组比较,ICH组CSF miR-124-3p、miR-146a-5p显著上调(P<0.05),见图2;而miR-21-5P、miR-29c-3P、miR-214-3p、miR-9-5p、miR-16-5p、miR-30e-5p、miR-221-3P、miR-125b-5P、miR-320C、miR-26b-5p、miR-7c-5P、miR-29c-3P、miR-182-5p差异无统计学意义(P>0.05)。
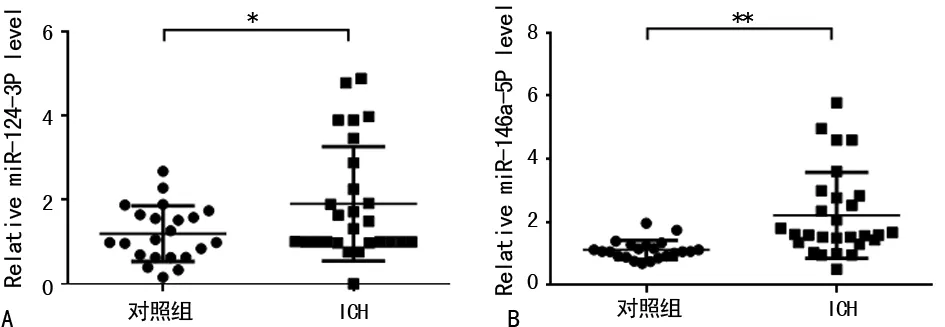
注:与对照组比较,ICH患者CSF miR-124-3p(A)、miR-124-3p(B)水平显著上调(*P<0.05,**P<0.01)
图2ICH组和对照组CSF中差异表达miRNA的研究结果
2.4CSF中 NSE、S100β、miR-124-3p、miR-146a-5p诊断ICH的效能研究 CSF中 NSE、S100β、miR-124-3p、miR-146a-5p诊断ICH的AUC分别为0.931[95%置信区间(95%CI):0.857~0.892]、0.795[95%CI:0.670~0.921]、0.667[95%CI:0.512~0.822]和0.878[95%CI:0.776~0.844]。CSF中NSE、S100β两者联合诊断ICH的AUC为0.965,灵敏度84.6%,特异度为98.2%。当NSE含达到0.62 ng/mL,诊断ICH的灵敏度为 80.8%,特异度为95.5%;当S100β的水平为0.43 μg/L,诊断ICH的灵敏度为76.9%,特异度为77.3%;当 miR-124-3p相对表达量是0.45时,其诊断ICH的灵敏度为80.8%,特异度为50.1%;当miR-146a-5p相对表达量是0.55时,其诊断ICH的灵敏度为81.8%,特异度为86.4%。见图3。

图3 ICH组和对照组CSF中NSE、S100β、miR-
3 讨 论
脑出血是一种病因复杂、病程进展迅速的一种疾病[7]。脑出血继发性损伤如细胞凋亡、血肿周围水肿、炎症细胞、因子激活、血管内皮损伤等严重危害着患者生存质量[8]。而依赖于CSF、影像学检查及神经功能评估的常规检查多反映疾病结局。CSF是直接接触脊髓、神经元细胞的并在脑室内循环的体液,当出现神经细胞损害后,某些神经特异性分子的变化可在一定程度上反映受损脑组织的局部事件,是包括ICH在内中枢神经系统疾病诊断标志物的理想来源[9]。因此基于疾病原发灶CSF的生化标志物或分子标志物的检测可直接、客观地为临床辅助诊断、病情评估提供参考,进一步挖掘CSF样本的潜在价值并为脑出血损伤机制的深入研究提供了可能。
S100β是一种主要位于中央(主要是星形胶质细胞)和周围神经系统的神经胶质细胞中的一种酸性糖蛋白,在细胞损伤或应激活化时释放,能反映神经元细胞、胶质细胞损伤[10]。NSE是在由神经元细胞形成的一种的水解酶,神经元细胞膜功能与结构受损时,NSE从胞质释放至细胞间隙和CSF中[11],并在CSF中有较高的浓度[12]。此外,NSE和S100β也可由一些神经外胚层来源的肿瘤细胞产生,如小细胞肺癌时血液中NSE水平可升高[13],恶性黑色素瘤时血液S100β的水平可升高[14],因此检测CSF中神经特异性蛋白更能特异、客观地反映脑损伤程度。文献报道,动脉瘤性蛛网膜下腔出血患者CSF高水平NSE、S100β提示脑损伤程度严重且更易出现不良结局(脑梗死、血管痉挛和颅内高压)[15],而本研究针对急性ICH病例,发现重度ICH组(低GCS评分组)CSF-S100β、NSE水平显著高于轻度ICH组(高GCS评分组),且ICH患者CSF S100β、NSE的水平与出血量均显著正相关,表明CSF NSE、S100β水平对判断患者病情严重程度具有积极意义,这与以往文献报道的研究结论基本一致。基础研究已证实NSE、S100β水平在脑损伤自适应调节后升高并参与神经损伤后的修复[16],是具有应用前景的脑损伤标志物。为了进一步检验CSF NSE、S100β对ICH的诊断效能,笔者又将NSE与S100β进行ROC分析,明确了两者联合检测可提高灵敏度至84.6%,提高特异度至98.2%,因此CSF NSE、S100β联合检测更能有效辅助诊断ICH及评估脑损伤程度。
miRNA是一类内源性非编码RNA加工成熟的,仅由20~24个核苷酸组成的短链RNA,其作为调节剂在CNS相关疾病的病理生理过程中发挥重要作用[17]。不断有研究揭示脑出血后miRNA表达谱发生改变并在一系列继发损伤中扮演着重要的角色。IWUCHUKWU等[18]通过检测ICH确诊患者CSF中的miRNA表达谱,发现211个差异表达miRNA,高表达的miRNA包括:miR-204-5p(2 075倍)、miR-125b-5p(108倍)、miR-9-5p(299倍)、miR-338-3p(146倍)、miR-187-3p(21倍)、miR-9-3p(299倍)。SØRENSEN等[19]研究发现ICH患者CSF中部分miRNA的水平明显高于血浆,而调控炎症相关基因的miRNA大量减少表明其可能受到系统调节影响。本研究针对ICH病例,选择了文献报道的与中枢神经系统疾病相关的15个靶标miRNA,实验结果表明:ICH患者CSF miR-124-3p、miR-146a-5p表达量显著高于对照组。研究表明,miR-124-3p过表达后可抑制神经毒性,包括减少神经细胞凋亡、神经炎症和氧化应激,并可在体外减弱甲基苯基吡啶碘化(MPP)诱导的神经损伤[20]。而miR-146a与ICH诱导的脑水肿发展相关的生物学过程有关,包括先天免疫反应、白细胞激活、转化生长因子-β信号传导和平滑肌细胞增殖[21]。因此,miR-124-3p、miR-146a-5p与出血所致脑组织损伤的病理生理过程是相关的,支持本研究的结果,其可作为诊断脑出血及评估脑损伤的生物标志物。同时也为miRNA参与脑损伤相关的机制研究提供了新的方向。
4 结 论
ICH后CSF蛋白水平(NSE、S100β)和基因水平(miR-124-3p、miR-146a-5p)标志物的检测可用于ICH的辅助诊断,NSE、S100β不仅可以反映脑组织损伤程度,也可用来评估ICH 出血严重程度。与此同时,本研究也具有一定的临床局限性,如CSF样本不易获取、CSF采集时机差异、miRNA水平个体差异、入组病例数较少等,仍需多中心、大样本加以验证。

