我院94例儿童中药注射剂不良反应调查分析
熊雪婷
湖北省荆州市妇幼保健院药剂科,湖北荆州 434020
中药注射剂因其成分复杂,生产工艺复杂,其安全性问题已成为备受关注的焦点[1],目前,已有多种中成药注射剂被国家药品监督管理局强制修改说明书。儿童因生理结构的特殊性,ADR的发生率比成人更高,ADR症状发展更快[2];然而,儿童中药注射剂ADR的研究资料相对缺乏[3],基层医院对儿童中药注射剂安全问题重视不足。我院临床药师为促进我院儿童合理安全的使用中药注射剂,进一步了解我院患儿发生中药注射剂ADR特点及一般规律,对我院2015年1月~2018年6月ADR监测小组收集并审核上报的94例中药注射剂致ADR报告进行回顾性分析,为今后儿童合理使用中药注射剂提供参考依据。
1 资料与方法
1.1 一般资料
资料来源于我院ADR监测小组2015年1月~2018年6月收集的中药注射剂致ADR报告表94份,纳入标准:(1)单独使用中药注射剂后发生的;(2)符合药品说明书用法的;(3)病历中有ADR症状描述的;(4)年龄在0~18岁之间。剔除标准:(1)同时使用多种药物的;(2)药品用法不合理的;(3)病历中无ADR症状记录的;(4)年龄超范围的。
1.2 方法
1.2.1 设计调查表 设计调查表,记录患者年龄、性别、ADR发生时间、引起ADR的药品名称、ADR涉及的器官或系统及临床表现、分类转规等信息,对符合标准的94份ADR报告逐份进行登记整理,录入Excel表格,进行汇总分析。
1.2.2 ADR判定标准 根据《药品不良反应报告和监测管理办法》(卫生部令第81号)进行判定。按ADR的严重程度分为一般、严重,严重是指导致死亡、危及生命,致癌致畸,致永久伤残或器官功能损伤,致住院或者住院时间延长。新的是指药品说明书未收载的不良反应,有描述但ADR反生频率与说明书描述不一致或更严重亦归为新的ADR。如同一报告是新的严重ADR则分别计算例次。
1.2.3 ADR分类方法 参照《WHO药品不良反应术语集》[4]对ADR所累及的系统/器官进行分类,对于同一报告累及多个系统/器官并涉及多个临床表现的分别计算例次。
1.3 统计学方法
采用SPSS19.0统计软件进行统计分析,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 ADR与患儿年龄和性别的关系
94 例ADR涉及的患儿中,总体男性发生ADR例数高于较女性,不同年龄段患儿性别构成比较差异无统计学意义(χ2=8.219,P>0.05)。发生例数最高的年龄段是2~5岁(P<0.01)。见表1。

表1 发生ADR患儿的年龄和性别分布[n(%)]
2.2 ADR发生时间
94例ADR的发生时间主要集中在静脉滴注给药后> 5min且< 30min、> 30min且< 60min,其次是静脉滴注给药后>60min且<24h,>24h且<3d,发生在用药后0~5min的ADR仅有6例。见表2。

表2 ADR发生时间分布
2.3 ADR临床表现分布特点
本研究中皮肤及附件损害占比最高,达到了80.85%,其次是全身性损害和消化系统损害,呼吸系统和神经系统损害较少,见表3。

表3 ADR临床表现分布特点
2.4 发生ADR中药注射剂品种排位及临床表现
本次调查中涉及4种中药注射剂,皆为清热解毒类,通过统计,热毒宁注射液的ADR发生例数最高,占43.62%,见表4。
2.5 ADR的分类和转规情况
本次调查的94例不良反应中,“新的”不良反应有8例,其中,热毒宁注射液引起4例,表现为眼痛、头痛、嗜睡、疲劳、烦躁、寒战;喜炎平注射液引起1例,表现为大汗淋漓、面色苍白,注射用炎琥宁引起2例,表现为冒冷汗、面色苍白、嗜睡;痰热清注射液引起1例,表现为胸闷。“严重”ADR2例,都来自于热毒宁注射液ADR,具体表现为寒战,四肢发绀,循环差,呕吐,经小抢救后均痊愈。所有ADR停药及对症治疗后,均治愈或好转,仅1例导致原患疾病延长。见表5。

表4 发生ADR排序中药注射剂品种排位及临床表现
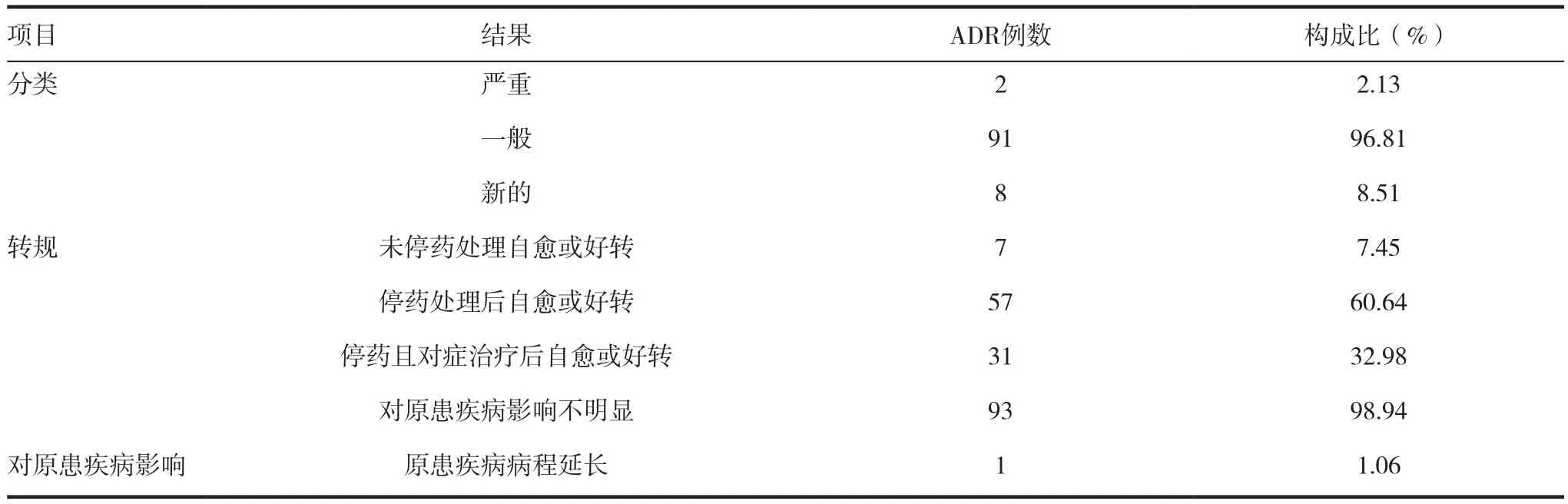
表5 ADR的分类和转规情况
3 讨论
3.1 中药注射剂ADR在儿童年龄性别上的分布特点
由表1可见,在>1~2岁、>2~5岁 两个年龄组ADR例数较多,可能原因:这两个年龄段的儿童是呼吸道疾病高发人群[5-7],患者基数大;该阶段的患儿免疫系统和各器官处于发育阶段,肝肾功能发育不全易导致药品蓄积发生ADR;某些药品说明书对于儿童用量含糊不清,儿科临床中存在广泛的超说明书用药[8-9]。而1岁以内的患儿ADR发生率反而低于1~5岁患儿,可能由于该时期的患儿大部分还处于哺乳期,因母乳中含有丰富的免疫球蛋白、细胞因子、生长因子等能够调节其免疫功能,促进其免疫系统的成熟[10-12],国外研究发现母乳中的成分如低聚糖可以有效降低婴幼儿变态反应的发病风险[13],从而降低发生ADR的风险,>5岁且<12岁儿童各器官系统发育较学龄前儿童更完善,故不良反应概率低,>12岁且<18岁儿童发生ADR仅为1例。
总体男性患儿发生ADR例数高于较女性患儿,但并不能说明男性比女性发生ADR的几率高,可能与本地人口男女出生性别构成比有关[14]。
3.2 中药注射剂ADR在儿童中发生的时间分布规律
由表2可见,因注射剂直接进入静脉,起效快,ADR症状主要在用药后5~30min,30~60min显现,而少数皮肤、神经系统损害则是在用药后,甚至数日后出现。故监测儿童ADR,除了用药过程中密切观察外,用药后的3~5d也不容忽视。我院ADR有一半以上是住院病区上报,能够有条件连续监测患儿用药数日内的ADR。
3.3 中药注射剂ADR在儿童中的临床表现特点及品种排位
本院儿童中药注射剂ADR与类似文献报道的分布特点大致相符[9,15],皮肤及附件损害占80.85%排首位,高于一般综合ADR调查中皮肤及附件损害的占比[16-17]。儿童的皮肤含有的免疫细胞对致敏原产生的效应比成人更敏感[18],对有过敏体质或有食物及药物过敏史的儿童应谨慎使用中药注射剂。
本次调查中5种中药注射剂的例数排位并不能反映ADR的发生率,在统计期间内,某一批次注射用炎琥宁被暂时召回停用,影响了其ADR发生例数;如何排除杂因、结合同期药品的使用率,平行比较同期不同药品的ADR发生率,是今后深入分析ADR的研究方向。
3.4 ADR分类和转规情况
本次调查中发现多数ADR来势迅猛,经及时处理,转规大都良好[19-20],目前,我院未发生因中药注射剂ADR造成严重后果或死亡的案例。得益于我院将中药注射剂纳入高危药品严格管理,住院请领、门诊取药均需专册登记,严格审核剂量,使用时护士专门看护,保证能够在第一时间处理ADR。对于“新的”ADR药及时上报促进药品说明书的修改,“严重”ADR应做好急救培训,能迅速处理,防止死亡案例的发生。
4 展望
我院是一所三级甲等妇幼保健院,有开展儿童ADR监测的样本优势,儿童临床研究资料十分珍贵,尤其是儿童ADR记录,我院ADR监测小组对收集的ADR表格会逐份调取病案,查阅病程记录、医嘱、护理记录单、检验单等进行核对,保证上报结果的真实性。临床药师在今后的工作中应不断总结更新儿童ADR的特点,给儿科医生给予更科学的建议;加强患儿家长用药教育和知情权工作,正视药品的ADR,积极配合科学处理不良反应;密切关注中药注射剂的动态,对总局发布的修改说明书召回等,有预案能科学应对。虽然,目前中药注射剂管理日益严格,但是临床使用中不必杯弓蛇影,应将关注点落在如何科学合理的使用减少ADR,及时有效地应对避免造成严重ADR。因此,持续监测儿童中药注射剂ADR,对促进临床合理用药具有极大的现实意义。

