‘保罗兰’睡莲花粉离体萌发及花粉管生长的研究
毛立彦,唐毓玮,谢振兴,龙凌云,黄秋伟,陆祖正,於艳萍,苏 群,丁丽琼*
(1.广西壮族自治区亚热带作物研究所,广西 南宁 530001;2.广西壮族自治区农业科学院 花卉研究所,广西 南宁 530007)
【研究意义】睡莲NymphaeaL.是睡莲科睡莲属植物的总称,属于多年生草本植物[1],花态多样,花色艳丽,具有观赏价值,主要用于城市水景绿化。睡莲属植物主要以生态学为基础进行分类,可分为Nymphaea、Anecphya、Brachyceras、Hydrocallis、Lotos等5个亚属[2-5]。其中,Brachyceras亚属睡莲的种、变种和栽培品种甚多[6],是重要的种质资源,对其花粉的研究对杂交育种的成败具有指导意义。【前人研究进展】Brachyceras亚属睡莲‘保罗兰’Nymphaea‘Paul Stetson’适宜广西的气候环境,群体花期长达10个月以上,目前在广西武宣县小规模种植。花粉的活力是指花粉具有萌发和生长发育的能力[7-8],鉴定花粉生活力的方法主要有花粉离体培养法、染色法(如I2-KI染色、TTC染色),花粉离体培养法是最准确的鉴定花粉活力的方法[9-11]。关于睡莲花粉离体培养的研究报道较少,赵其龙等[12]对Lotos亚属的柔毛齿叶睡莲花粉萌发的研究发现,最适宜的离体培养基是60 mg/L蔗糖+15 mg/L H3BO3。5 %蔗糖+15 mg/L H3BO3+20 mg/L CaCl2+1 %琼脂为Nynphaea亚属睡莲花粉离体萌发的最佳培养基[13]。杨梦飞等[14]采用离体培养法测定了不同亚属睡莲的花粉活力,其中埃及蓝睡莲(Brachyceras亚属)在各个组分的培养液中均无法萌发。睡莲花粉活力的研究可为睡莲杂交亲和性,新品种培育,基因库的保存等研究提供参考依据[15-16]。【本研究切入点】目前,有关测定‘保罗兰’Nymphaea‘Paul Stetson’花粉在不同培养基中的萌发率和花粉管长度,观测花粉管的生长过程的研究较少报道。【拟解决的关键问题】旨在筛选出适宜Nymphaea‘Paul Stetson’睡莲花粉萌发的培养基,为睡莲的花粉活力检测和的杂交育种的亲本选择提供参考依据。
1 材料与方法
1.1 试验材料
试验材料为广西壮族自治区亚热带作物研究所的睡莲种质资源圃的‘保罗兰’睡莲Nymphaea‘Paul Stetson’。
1.2 试验方法
共种植‘保罗兰’睡莲25株,株距2 m,在花蕾时期做套袋处理,避免昆虫携带花粉干扰试验。‘保罗兰’睡莲具有早上绽放,夜间闭合的特性,花开后第2天再开时,于早上8:00-9:00采摘花粉成熟的花朵带回实验室内,从每朵花中选择3枚成熟的花药,将其中的花粉均匀抖落在干燥培养皿中并混匀,等待检测。
1.3 测定项目及方法
1.3.1 离体培养基最佳组分 采用双因素试验筛选最佳培养基[17]。培养基用水为双蒸馏水,蔗糖设置3个浓度梯度:0、100和200 g/L;H3BO3设置3个浓度梯度0、20和40 mg/L,共9个处理。花粉离体培养4 h后进行镜检,根据9个处理的培养基培养效果,确定蔗糖和H3BO3的较佳配比,在此基础上分别加入0、20、60和100 mg/L的CaCl2,进一步对比花粉萌发率,探讨CaCl2对花粉活力的影响,并筛选出最佳的培养基。
1.3.2 花粉的收集与离体萌发 在含有700 μl液体培养基的1 mL离心管中加入适量新鲜花粉,置于30 ℃培养室中,光照条件下自然培养6 h,每隔1 h观测1次。将离心管摇匀,用移液枪吸取50 μl花粉液滴在载玻片上,进行镜检。
1.3.3 花粉萌发率统计以及花粉管长度测定 每个玻片随机选取7个不重复的视野,每个视野花粉数量不少于40粒,以花粉管长度大于花粉粒直径视为萌发。使用Image-Pro Plus 6.0进行花粉粒的计数以及测量花粉管的长度。
萌发率(%)=(视野内萌发花粉数/视野内花粉总数)×100
1.3.4 花粉离体培养的最佳时间 镜检最佳培养基培养1、2、3、4、5和6 h的花粉,分析花粉萌发率和花粉管生长的趋势,确立最佳的培养时间。
1.4 统计分析
试验数据采用Excel 2013 进行统计与制图,采用SPSS 18.0进行双因素方差分析。
2 结果与分析
2.1 不同浓度的蔗糖和H3BO3对花粉离体萌发的影响
9组花粉离体培养基的试验结果如表1所示,花粉离体萌发率非常低,均不足10 %,在仅有蔗糖或仅有H3BO3处理的单因素作用下,花粉管生长有限,平均长度不足60 μm。100 g/L蔗糖+20 mg/LH3BO3的培养基中,睡莲花粉的萌发率较高,达到8.34 %;100 g/L蔗糖+40 mg/L H3BO3的培养基中,睡莲花粉管的平均长度较长,达到179.9 μm。
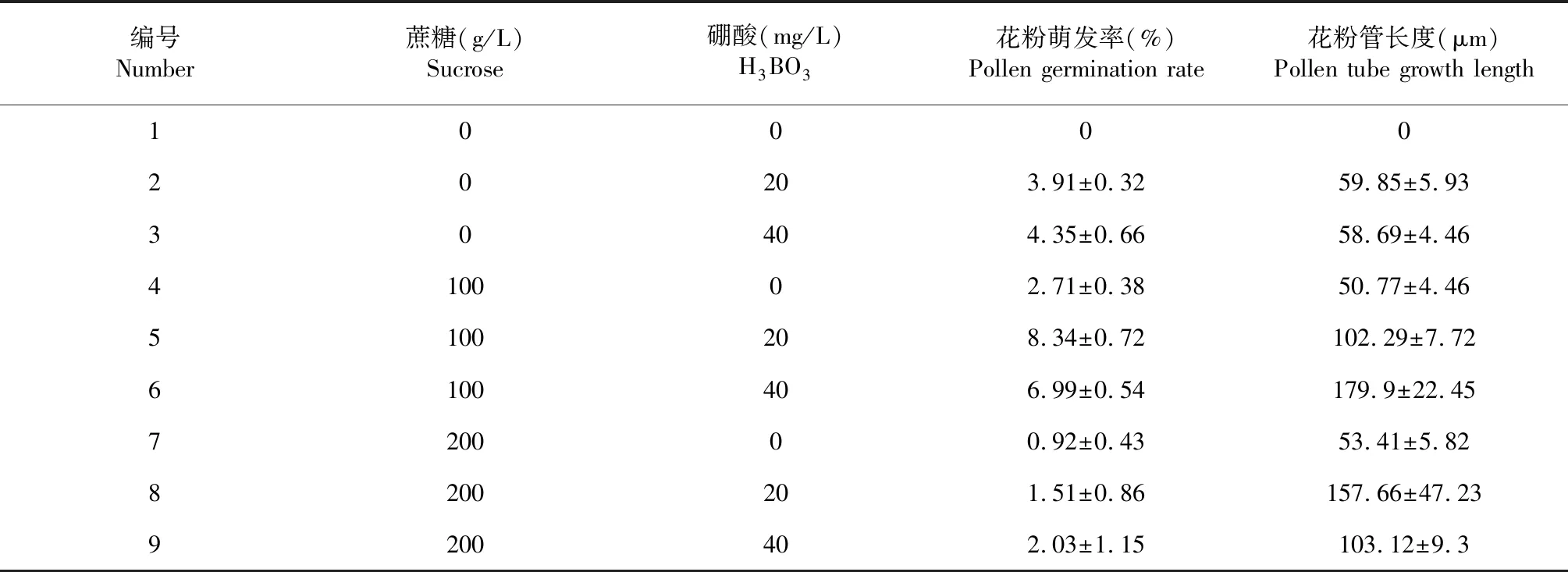
表1 蔗糖和H3BO3对花粉萌发率和花粉管生长的影响
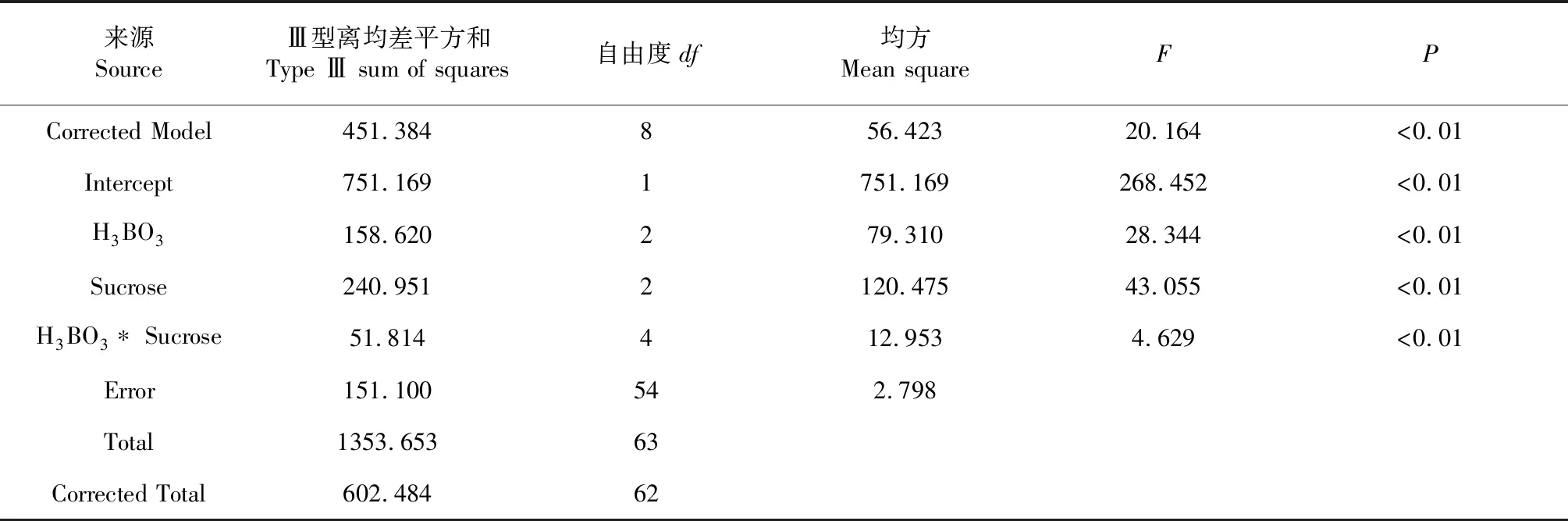
表2 H3BO3和蔗糖的主体间效应检验结果
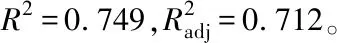
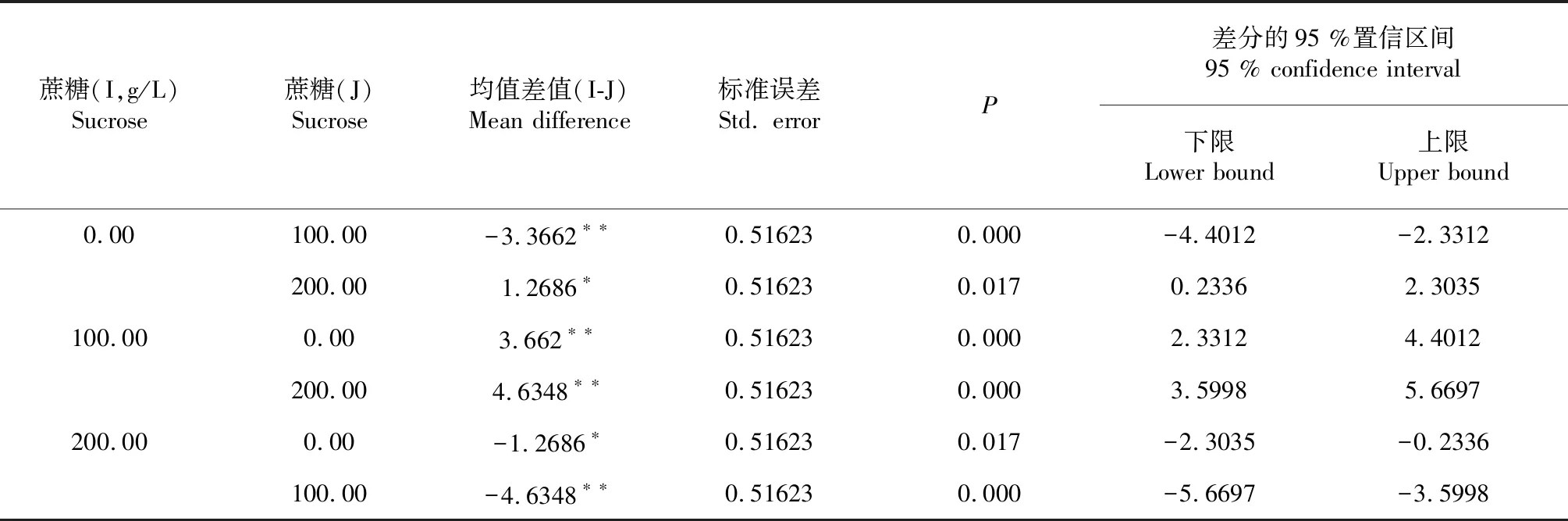
表3 LSD比较结果(主效应Sucrose)
注:*表示均值差值在0.05级别上显著,**表示均值差值在0.01级别上显著。
Note:,* mean difference is significant at 0.05 level, ** mean difference is significant at 0.01 level.

表4 LSD比较结果(主效应H3BO3)
注:*表示均值差值在0.05级别上显著,**表示均呈差值在0.01级别上显著。
Note: * mean difference is significant at 0.05 level, ** mean difference is significant at 0.01 level.
采用SPSS 18.0进行不同浓度的蔗糖和H3BO3处理对花粉萌发率影响的双因素方差分析,如表2所示,不同浓度的蔗糖或H3BO3处理对花粉的离体萌发存在极显著的影响(P<0.01,下同),并且2个因素的交互作用极显著。

表5 H3BO3和CaCl2对花粉萌发率和花粉管生长的影响

表6 H3BO3和CaCl2主体间效应检验结果
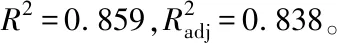
再进一步采用LSD检验法进行多重比较,主效应分析结果表明,在试验范围内,100 g/L的蔗糖处理适宜花粉萌发,与0及200 g/L的蔗糖处理之间均存在极显著差异,200 g/L的蔗糖处理存在抑制作用(表3);0 mg/L H3BO3的处理与20、40 mg/L H3BO3的处理之间均存在极显著差异,20与40 mg/L H3BO3的处理之间无显著差异。H3BO3的加入能显著促进花粉的萌发,20和40 mg/L的H3BO3的处理均适宜睡莲花粉的萌发(表4)。
2.2 不同H3BO3和CaCl2的浓度对花粉萌发的影响
根据蔗糖、H3BO3的主效应分析结果(表3、表4),进一步进行H3BO3和CaCl2处理的双因素试验,硼酸浓度设置2个水平:20、40 mg/L,CaCl2浓度设置4个水平:0(CK)、20、60及100 mg/L。试验结果如表5所示。采用SPSS 18.0进行不同浓度的H3BO3和CaCl2处理对花粉萌发率影响的双因素方差分析(表6),不同浓度的H3BO3或CaCl2处理对花粉的离体萌发存在极显著的影响,并且两个因素存在极显著的交互作用。
再进一步采用LSD检验法对不同浓度的CaCl2处理进行简单的主效应分析(表7),在不同H3BO3浓度的水平上,对CaCl2进行简单主效应分析,结果表明:CaCl2能促进花粉的萌发,在试验范围内,20 mg/L的CaCl2处理较适宜花粉的离体萌发,在不同浓度的H3BO3水平上,与0、60和100 mg/L的CaCl2的处理均存在极显著的差异,在20 mg/L H3BO3的水平上,随着CaCl2浓度的增高,促进花粉萌发的效果逐步减弱。
2.3 离体萌发过程中花粉萌发率及花粉管长度的变化情况
如图1所示,花粉萌发率在1~4 h内快速上升,从11.30 %±1.24 %上升至20.66 %±0.56 %,4~6 h时,萌发率相对平稳,维持在20 %左右。花粉管的平均长度在培养1~2 h时迅速增长,从97.84 μm上升至145.22 μm,2~4 h时,花粉管平均长度不变,4 h以后花粉管平均长度略有下降。综上所述,最佳的镜检时间可以设置为4 h。
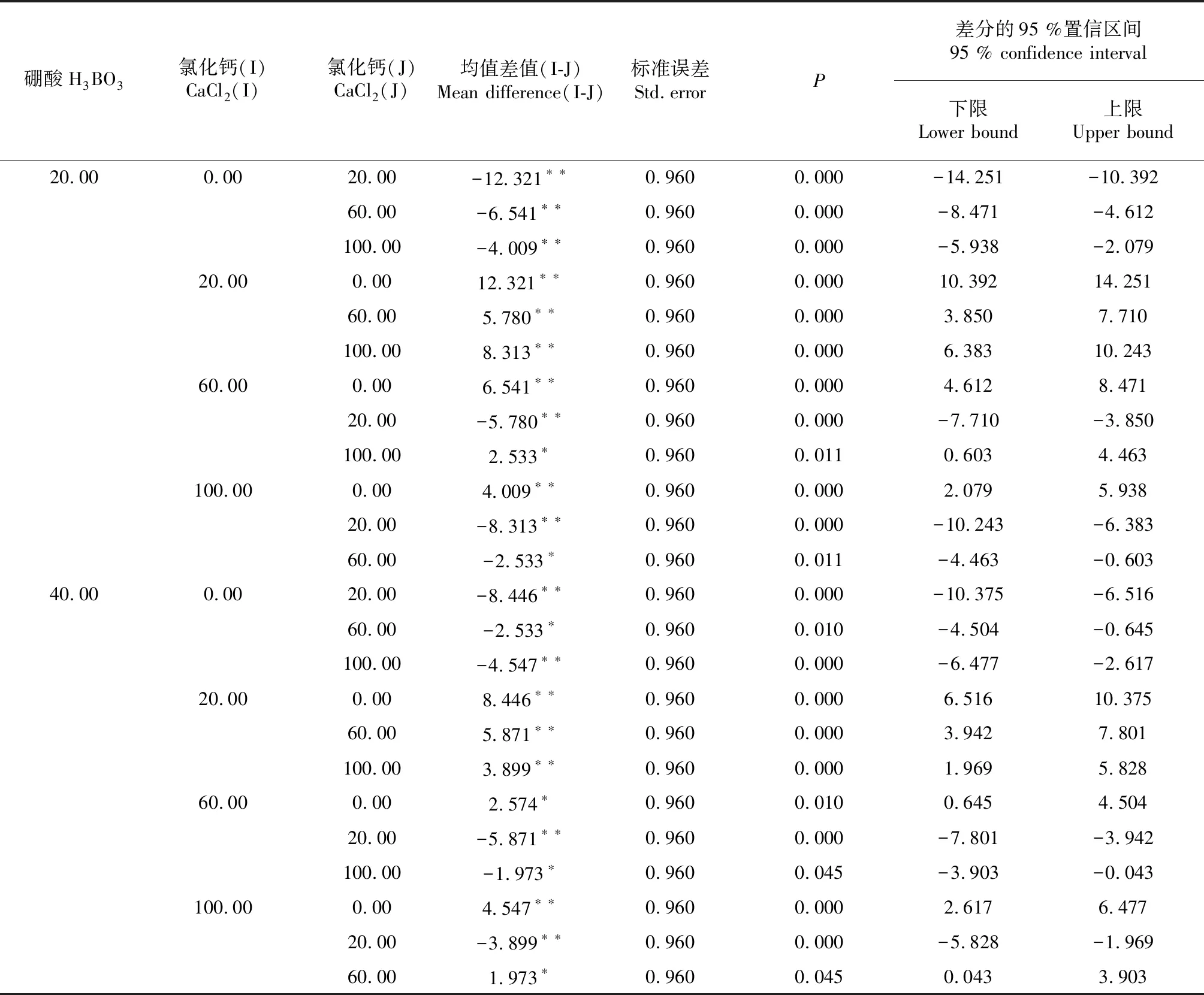
表7 LSD比较结果(主效应CaCl2)
注:CaCl2单位为mg/L,*表示均值差值在0.05级别上较显著,**表示均呈差值在0.01级别上显著。
Note: CaCl2unit mg/L, * means that difference is significant at 0.05 level, ** means that difference is significant at 0.01 level.
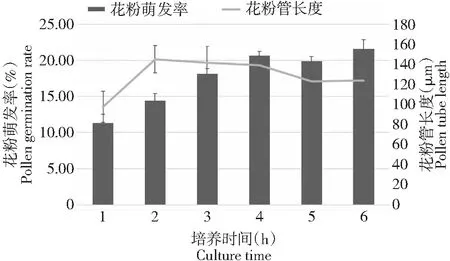
图1 培养时间对花粉萌发和花粉管生长的影响Fig.1 Effect of culture times on pollen germination and pollen tube growth
在镜检中观察到,睡莲的花粉粒呈圆形(图2-a),直径大约25~50 μm,一粒睡莲花粉通常只萌发出一束花粉管(图2-b)。萌发的初始阶段,花粉粒的一侧会凸起,突起物透明(图2-c)。随后突起部位不断伸长,形成花粉管。随着花粉管的伸长,花粉粒中的内含物逐步进入花粉管,花粉管渐渐填充满内含物(图2-d)。在下一个阶段的生长过程中,内含物均匀分布在花粉粒和花粉管之中,此外还会出现以下几种情况;花粉粒变透明,花粉管中部和末端充满内含物;内含物分别集中分布在花粉管各个部分,透明与不透明的部分界限鲜明(图2-f)。此外,花粉萌发过程中,花粉管还会出现细小、扭曲的现象(图2-e)。
3 讨 论
3.1 培养基组分和花粉萌发及花粉管生长的关系
适宜浓度的蔗糖对睡莲花粉萌发有明显的促进作用,蔗糖是花粉萌发和花粉管生长主要的营养物质,同时也是花粉代谢和跨膜运输的碳源[18]。10 %的蔗糖能有效促睡莲花粉萌发,过高浓度会产生抑制。杨梦飞等[14]的研究也得到同样的结果,10 %的蔗糖浓度适用于睡莲花粉的离体培养。李佛莲等[8]对山玉兰花粉的研究表明,蔗糖浓度高于10 %会抑制山玉兰花粉的萌发,5 %蔗糖是最适宜耐寒睡莲花粉萌发的浓度。邓衍明等[20]的研究表明,在BK培养基[19]中添加8 %蔗糖最适宜花粉管的萌发,而薄壳山核桃花粉萌发的最佳蔗糖浓度为20 %~30 %[18]。因此,不同植物的花粉离体萌发适宜的蔗糖浓度不同,这可能与不同植物花粉对蔗糖浓度形成的渗透压的适应能力不同有关。在今后的睡莲花粉研究中,可以将试验对象扩展至其它亚属的睡莲花粉,以进一步探讨不同亚属的睡莲花粉对蔗糖浓度的适应能力的差异性。

a.睡莲花粉在蒸馏水中培养4 h的状态;b.睡莲花粉在培养基中培养4 h的状态;c.睡莲花粉萌发的初始阶段;d.睡莲花粉管开始伸长,内含物质进入花粉管;e.花粉管扭曲异常;f.花粉管伸长后,内含物在花粉管的分布情况a. The condition of pollen in distilled water for 4 hours; b. The condition of pollen in medium for 4 hours; c. The initial stage of pollen germination; d. pollen tube begins to elongate and inclusion enters pollen tube; e. Abnormal distortion of pollen tube; f. Distribution of inclusions in pollen tube after elongation of pollen tube 图2 花粉萌发及花粉管生长的动态变化Fig.2 The dynamic changes of pollen germination and pollen tube growth
H3BO3能刺激并增加花粉对糖类的吸收、运转和代谢[21],参与花粉管顶端细胞壁合成,对花风管中果胶的合成有着重要作用[22],使酸性果胶转变呈酯化果胶,而酯化果胶存在于花粉管顶端,有助于提高花粉管顶端的延展性[8]。硼离子对质外体结合钙离子和游离钙离子有影响,可以增加细胞内的游离钙离子,使其达到启动花粉萌发的最佳浓度[23]。硼离子的加入能有效促进Nymphaea‘Paul Stetson’睡莲花粉的萌发和花粉管的生长,20 mg/L的硼离子更适宜睡莲花粉的萌发,在10 %蔗糖+20 mg/L CaCl2的基础上,花粉萌发率达到20.66 %。
Ca2+是花粉萌发、花粉管生长不可缺少的,外源施加的Ca2+能促进花粉的萌发[23],Bednarska[24]通过在培养基中加入Ca2+通道阻塞剂发现花粉萌发受到抑制,证明了Ca2+对花粉萌发的影响。杨梦飞等[14]的试验中,培养基未加入Ca2+,除埃及白睡莲外,其余睡莲花粉萌发率均不到10 %,这与本试验的结果较一致。在浓度适宜的蔗糖、H3BO3的培养基中,补充少量的外源Ca2+能显著提高Nymphaea‘Paul Stetson’睡莲花粉的萌发率,过高的Ca2+会造成Ca2+中毒,反而抑制花粉的萌发[25]。龚明和曹宗巽[26]研究结果认为,Ca2+能启动花粉萌发和调节花粉管生长。本研究结果表明,Nymphaea‘Paul Stetson’睡莲花粉在缺少Ca2+的培养基中,萌发率非常低,随着Ca2+的加入,萌发率大幅度提高。
3.2 花粉管的生长情况
4 h以前,睡莲花粉萌发率会随着培养时间显著增加,4 h以后趋于稳定,花粉管长度在培养2 h以前迅速增加,2 h后达到一个相对稳定的水平,此结果与杨梦飞等[14]的研究结果基本一致。
试验中所观察到的睡莲花粉粒或花粉管中的内含物质可能是生殖核及营养核或微丝骨架[27]。游韩莉等[28]研究发现花粉在离体萌发过程中,营养核和生殖核会陆续进入到花粉管内,微丝骨架排列与花粉细胞核的移动存在一定的关系,随着花粉的萌发,微丝骨架逐渐聚集,推动营养核和生殖核向花粉管内移动。花粉管中的细胞核行为及花粉管内的微丝骨架的分布是一个复杂的过程[29],对此次试验中观察到的花粉中的内含物质需要进一步进行荧光标记,才能进行更准确和深入的研究分析。
4 结 论
最适合‘保罗兰’睡莲的花粉离体萌发的培养基为10 %蔗糖+20 mg/L或40 mg/L H3BO3+20 mg/L CaCl2,花粉离体萌发率为15.76 %~20.66 %,花粉管生长长度为139.28~141.11 μm,最佳镜检时间为4 h。

