钴掺杂增强二硫化钼纳米片的电驱动析氧性能研究
位兵伟,申永庆,赵 敏,张 华
(太原理工大学 新材料工程技术研究中心,太原 030024)
随着工业的快速发展,人们对能源的需求量也不断增加。然而化石能源的大量使用会引发一系列问题,如温室效应、环境污染等[1-4]。因此,人们迫切需要开发清洁能源以降低对于传统化石能源的依赖,电驱动裂解水作为一种制备H2和O2的有效手段,有望实现清洁能源的高效利用[5]。电解水的核心包括两个电化学过程:阴极的H2析出反应(HER)和阳极的O2析出反应(OER).相比较于HER,OER需要施加更大的过电位,才能产生一个氧气分子。因此,OER被认为是整个电化学裂解水过程的速控步[6],OER进行的是多步电子转移过程,其反应速率缓慢且过电位高,严重制约了电解水的发展。OER机理通常被认为[7]:
在酸性电解质中:
M+H2O→M—OH+H++e-,
(1)
M—OH→M—O+H++e-.
(2)
2M—O→O2+2M或
M—O+H2O→MOOH+H++e-,
(3)
MOOH+H2O→M+O2+H++e-.
(4)
在碱性电解质中:
M+OH-→M—OH-,
(1)
M—OH+OH-→M—O+H2O+e-.
(2)
2MO→O2+2M或
MO+OH-→MOOH+e-,
(3)
MOOH+OH-→M+H2O+O2+e-.
(4)
其中,M代表金属元素,在不同的电解质中均能产生金属-氧(M—O)中间体,该中间体可通过两种不同的方式形成O2,第一种方式是2个M—O中间体结合产生O2,另一种是M—O先形成M—OOH中间体,再形成O2.O2析出涉及4个电子转移过程,M—O键断裂过程的动力学非常缓慢,在电解水阳极反应中具有较高的过电位,消耗的能量较高,根据Sabatier原理,当电催化剂表面与O的成键强度太弱时,不易形成中间产物HO*;当电催化剂表面与O的成键强度太强时,不利于HO*进一步反应生成HOO*;只有电催化剂表面与O的成键强度适中才有利于提高OER活性[8]。因此高效的电解水析氧的关键因素是催化剂的制备,使反应在较低过电势下进行,从而有效降低反应过程所需的能耗。开发高效的电催化剂成为可持续能源技术探索的重中之重。目前,RuO2和IrO2等被认为是最好的商业OER电催化剂,由于这些贵金属在地壳中的储量有限,价格昂贵且稳定性较差,不利于大规模生产限制了其在OER催化反应中的应用[9]。因此,廉价、高效、耐用、绿色的OER催化剂的开发尤为迫切。近年来,石墨烯、MoS2等二维材料,因具有较大的比表面积、良好的导电性等特点而备受关注[10]。例如,戴黎明等在热解含六氟磷酸铵(AHF)的聚苯胺(PANi)图层的氧化石墨烯(GO-PANi)实验中得到了对水裂解及氧还原反应均具有良好催化性能的N,P和F三元掺杂石墨烯非金属催化剂[11]。二维层状结构的MoS2最近也广泛用于电催化的研究中,ZHENG et al[12]使用一种简便的方法,将MoS2纳米片限制在石墨烯(RGO)片之间,合成一种尺寸可控的MoS2/RGO复合材料。该材料具有良好的HER催化性能,因为GO的引入为MoS2提供了更多含氧官能团,并在GO层插入MoS2,易于控制MoS2的尺寸,防止MoS2纳米片堆叠,从而使得MoS2暴露更多的活性边缘位点,提高了析氢反应活性。然而这些研究主要集中在探索其HER催化性能,MoS2在OER中的催化性能还面临很多挑战,非贵金属掺杂作为一种有效的调控手段,被广泛应用于提升电催化剂的催化性能,如JIN et al[13]报道了采用复合共沉淀技术制备了一种Ni-Fe氧化物基纳米管阵列电极,实验结果表明Fe的引入将促进具备催化活性的NiOOH中间体的形成,提高其OER活性。推测采用非贵金属掺杂调控MoS2纳米片的OER催化性能是一种有效的方式。
因此,本文采用钴掺杂调控MoS2纳米片的结构进而调控其OER催化性能,由于前期的研究多是利用水热法制备MoS2,该方法耗时较长且受热不均匀等缺点[14-15]。与水热法相比,微波辅助加热法是通过极性分子可以选择性吸收微波将电磁能转换为内能和热能,形成高效的“内加热”,从而使反应物被快速加热,该方法用时较短且受热均匀。因此采用微波加热法制备了不同含量Co的掺杂的MoS2纳米片(MoS2-Co-1,MoS2-Co-2,MoS2-Co-3对应n(Mo)∶n(Co)的摩尔比分别为:10∶1,2∶1,1∶1),并使用X射线衍射(XRD)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)等表征手段,对其形貌、结构进行系统的表征,进一步测试了这些样品在析氧反应(OER)中的催化性能,研究了不同的Co掺杂量对MoS2纳米片结构其OER催化性能的影响。最终发现MoS2-Co-2具有最佳的催化性能,其在10 mA/cm2的过电势为220 mV,Tafel斜率为128 mV,并且该样品具有很好的稳定性。
1 实验部分
1.1 催化剂的制备
不同Co含量的MoS2催化剂具体制备过程如下:将0.026 g (0.1 mmol)(NH4)2MoS4和0.012 g (0.05 mmol) CoCl2·6H2O加入到40 mL超纯水中搅拌20 min,在微波反应釜中220 ℃加热反应1 h;随后,冷却至室温,洗涤、离心、干燥。所得产物为掺杂Co的MoS2,命名为MoS2-Co-2.改变CoCl2·6H2O的量为0.002 4 g (0.01 mmol)和0.024 0 g (0.1 mmol)分别命名为MoS2-Co-1,MoS2-Co-3.
1.2 催化剂的表征
催化剂的X射线衍射(XRD)表征采用丹东通达科技有限公司TD-3500型X射线粉末衍射仪测定分析。Cu/Kα作为辐射源,管压为30 kV,管电流为100 mA,扫速为2(°)/min对样品进行广角度范围(10°~90°)扫描测试。催化剂的扫描电子(SEM)图像通过泰思肯有限公司生产的FIB-SEM,TESCAN S-4800型扫描电子显微镜获得。通过JEM-2010型高分辨透射电子显微镜在加速电压为200 kV下获得透射电子图像。X射线光电子能谱采用了超高真空装置,配有单色铝钾的X射线源和一个高分辨的Gammadata-Scienta SES 2002分析仪,对实验样品的元素组分结构进行分析。
1.3 催化剂的性能测试
催化剂的性能评价是用电化学工作站CHI760E(上海辰华仪器有限公司)测得。OER电化学性能是在三电极体系下测定,其中,Ag/AgCl电极和石墨棒分别用作参比电极和对电极,将5 mg样品分散到1 mL乙醇和水的混合溶剂(体积比乙醇∶水=4∶1)中取5 μL滴在玻碳电极上用作工作电极。所有的极化曲线包括循环伏安曲线(CV)和线性循环伏安曲线(LSV)均在扫速为2 mV/s,电解液为1.0 mol/L KOH中测得。每个样品的交流阻抗谱(EIS)是在一定外加电压下测得。所得的曲线是以标准氢电极(RHE)为参比并经过iR补偿所得。
2 结果与讨论
2.1 催化剂表征分析
图1为催化剂MoS2-Co-x(x=1、2、3)的XRD图谱。由图1可知,该催化剂在2θ=31.5°,35.3°,38.9°,53.5°,55.8°出现明显的衍射峰,分别对应于MoS2的(100),(101),(102),(103),(105),(110)晶面,表明制备的样品为2H相MoS2晶体[16]。随着Co含量的增加,观察到样品在2θ=26.8°,28.6°,55.3°,57.2°处出现明显的衍射峰,分别对应于MoCoS4的(204),(021),(040),(208)晶面,从而证明

图1 MoS2-Co-x的XRD谱图 Fig.1 XRD spectrum of MoS2-Co-x
了Co成功掺杂入MoS2纳米片中。为了确定Co在MoS2中的价态,对OER催化性能最好的样品(MoS2-Co-2)进行了X射线光电子谱(XPS)测试,通过宽谱扫描,在图2(a)中明显观察到MoS2-Co-2中Co,S,Mo元素的存在,图2(b)为S的精细扫谱图,其中结合能为159.9 eV和160.9 eV分别对应着MoS2的S2p1/2和S2p3/2.此外,在167.0 eV出现S2p特征峰,结合能为161.4 eV和162.4 eV分别对应于的Co—Mo—S键,这表明,Co成功掺杂入MoS2的晶体中[4,7,17]。Mo3d光谱(图2(c))显示在227.1 eV和230.1 eV处呈现出两个主要Mo4+的自旋轨道峰,即Mo3d5/2和Mo3d3/2.而在231.3 eV和234.2 eV处出现的峰则对应的是Mo6+,主要归结于样品表面的部分氧化。此外,224.2 eV 处出现的峰则是MoS2的S2s特征峰。Co2p谱图(图2(d))中位于777.0 eV和 792.0 eV处的峰分别对应于Co2p3/2和Co2p1/2[3]。从Mo3d,S2p和Co2p的X射线光电子能谱给出的Mo,S,Co的价态变化进一步证明成功制备了Co掺杂的MoS2[18]。图3为所制备材料的SEM图,图3(a)中可以看出在未加入Co时,产物为片状MoS2,随着Co加入量的不断增加,催化剂的形貌也发生了明显变化,图3中(b)、(c)、(d)分别对应n(Mo)∶n(Co)为10∶1,2∶1,1∶1,可以明显看出随着Co含量的增加MoS2由纳米片状逐步过渡到纳米颗粒状。主要是由于Co的引入导致的MoS2的电子结构发生改变,这一结果与 XRD图谱相对应。从图3(c)的EDS图谱进一步确定Co成功掺杂到MoS2纳米片中。图4中(a),(b)和(c),(d)分别为MoS2和MoS2-Co-2的TEM和HRTEM图,从图4(a)中可以明显看出该样品为MoS2的层状形貌,图4(b)中可以清晰的看出MoS2的分层结构且层晶面间距为0.64 nm对应MoS2的(002)晶面,而且层数为6~8层,进一步确定产物为二维MoS2[19]。从图4(c)中可以看出MoS2-Co-2为掺杂Co的MoS2,其中MoS2-Co-2的高分辨透射电子显微图像(图4(d))显示出0.26 nm和0.64 nm分别对应于MoCoS4的(223)晶面和MoS2的层间距[20]。SEM和TEM图表明Co的掺杂只是导致MoS2形貌的变化而并未引起MoS2的晶体结构的改变,即掺杂后的MoS2仍然为2H型。

图2 MoS2-Co-2的XPS谱图 Fig.2 XPS spectrum of MoS2-Co-2

图3 SEM表征 Fig.3 SEM characterizations

图4 TEM表征 Fig.4 TEM characterizations
2.2 催化剂的性能测试
图5(a),(b)分别为各个样品的LSV极化曲线及其相应的Tafel曲线。从测试结果中可以得出,样品MoS2在电流密度为10 mA/cm2时显示出非常大的过电位,其值为350 mV.相比MoS2,掺杂Co以后的样品MoS2-Co-1、MoS2-Co-2和MoS2-Co-3表现出较好的OER性能,在同样的电流密度下其过电势分别为280 mV、220 mV和250 mV且低于商业RuO2(320 mV)的过电势,其中MoS2-Co-2的过电势最低,催化性能最好。相比于最近报道的通过化学气相沉积法在泡沫钴上生长的二硫化钼复合物(过电势为350 mV),我们制备的MoS2-Co-2的过电势有明显的降低[21]。Tafel斜率是评估电极与电解液界面处的OER机制的一个关键参数,对Tafel斜率的详细分析可以用来确定催化反应的限速步骤。通常OER的动力学过程主要由四个电化学步骤组成,每一步都有一个质子转移过程发生。碱性溶液中的OER机制描述如下[22]:
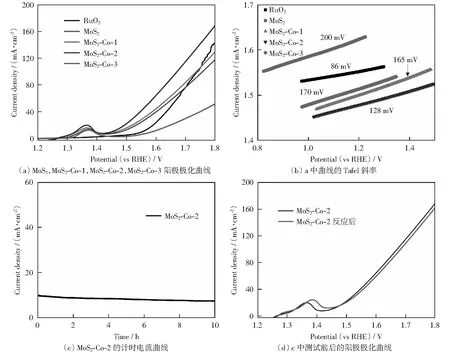
图5 电化学性能测试结果 Fig.5 Electrochemical performance
OH-+*HO*+e-.
(1)
HO*+OH-O*+H2O+e-.
(2)
O*+OH-HOO*+e-.
(3)
HOO*+OH-O2*+H2O+e-.
(4)
O2**+O2(g) .
(5)
式中:*代表催化剂的一个反应活性位点;O*、OH*和OOH*是吸附在活性位点上的中间体。已有文献报道过渡金属的3d轨道和中间体的相互作用力决定了过渡金属的OER活性。对于样品MoS2-Co而言,由Co向MoS2的电荷转移将会优化活性位点上的含氧中间体的吸附,因而提升电极材料的OER活性。根据SEM结果可以看出,MoS2-Co-2结构既具有MoS2的层状结构,同时有具有含量相对较高的Co,从而保证了足够的活性位点。而MoS2-Co-1中的Co的含量较少,MoS2-Co-3由于形貌完全变为球形,从而导致其催化性能相对较差。较低的Tafel斜率进一步证实了MoS2-Co-2催化剂的动力学过程更有利于实现OER反应。长期的稳定性是评价电催化剂的另一个关键参数,通过析氧催化剂的计时电流曲线(CA)来测定其析氧反应的稳定性。图5(c)显示了电位为0.5 V条件下的计时电流曲线。测试过程中使用旋转圆盘电极转速为1 000 r/min,所以i-t曲线没有出现明显波动。催化剂MoS2-Co-2的电流密度至少保持10 h没有明显变化,并对经过10 h阳极极化曲线测试后的样品进行OER性能测试,从图5(d)中可以看出,经过10 h阳极极化曲线测试后的样品仍能保持几乎不变的OER催化活性,并且反应前后其形貌也没有明显的变化,以上结果均证明MoS2-Co-2具有良好的化学稳定性。良好的催化活性和稳定性是因为反应形成的Co—S键使得电极材料在高电位极化下保持稳定不被分解。我们进一步通过电化学双电层电容来考察其电化学活性面积,对同一催化剂而言,其Cdl值与电化学活性表面积(ECSA)是成正比的。图6(a)显示的是MoS2-Co-2在不同扫速下测得的CV曲线。根据图6(a)的结果,就可以算出该材料的双电层电容为21.5 mF/cm2,说明该材料具有很高的电化学活性表面积。此外,为了研究材料的导电性,我们对该样品的电化学阻抗谱进行了测试(图6(b)),各个样品均在OER过电位为220 mV下测定。从图中可以看出,与MoS2相比,MoS2-Co-1、MoS2-Co-2和MoS2-Co-3具有较小的半圆直径,证明Co的掺入有效降低了MoS2的电荷转移电阻,而MoS2-Co-2具有最低的欧姆损耗[4],表明其具有最好的OER催化活性。该结果与图5(a)相对应,进一步解释了Co的掺入使得具有大量催化活性位点的MoS2具有更强的导电性,因而具有更好的OER催化活性。
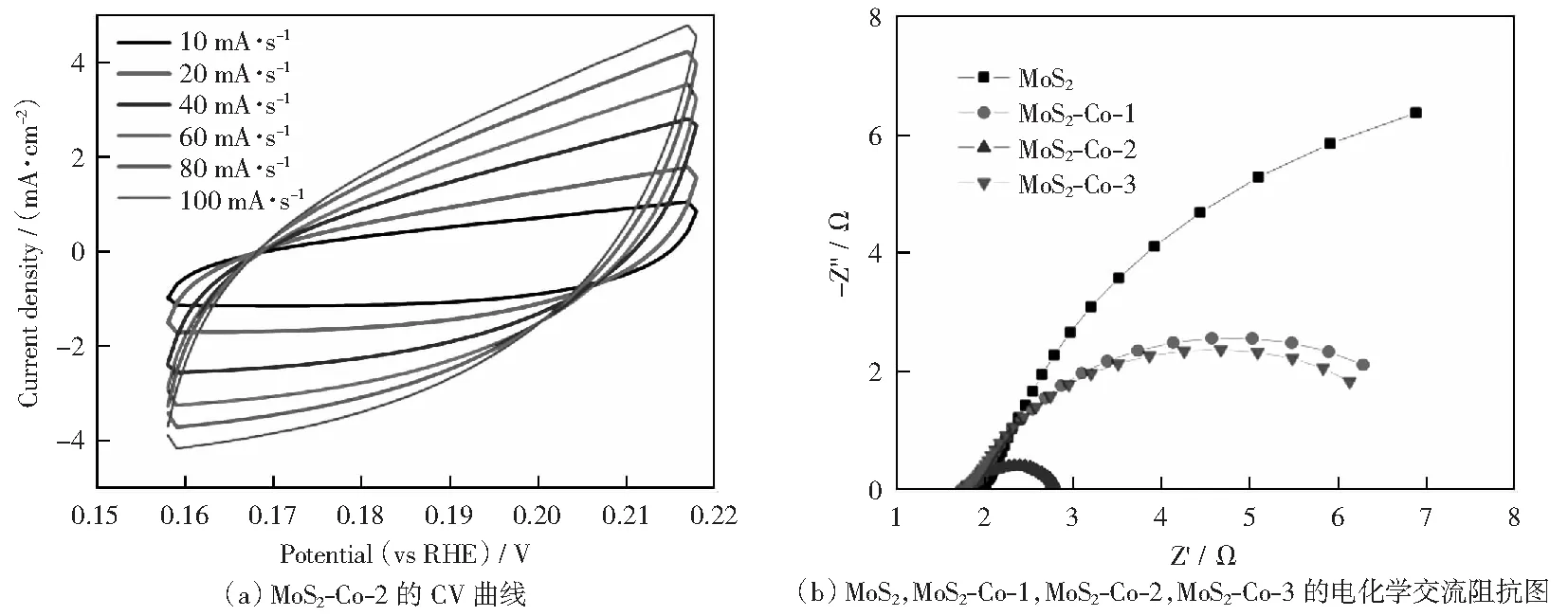
图6 MoS2-Co-2的导电性测试 Fig.6 Conductivity test of MoS2-Co-2
3 结论
本文介绍了一种微波辅助加热法快速制备Co掺杂的MoS2纳米片的方法,研究了Co掺杂量对MoS2的形貌及OER催化性能影响。结果表明:Co的掺入可以显著提升MoS2的OER催化活性,MoS2-Co-2(n(Mo)∶n(Co)=2∶1)催化剂具有最佳催化性能,在10 mA/cm2的过电势为220 mV,Tafel斜率为128 mV/dec,并且该样品具有很高的稳定性,其催化性能的提高主要是由于Co原子的掺杂有效改变了二维MoS2纳米片的电子结构和导电性。该研究对新型过渡金属电催化剂的设计、制备和催化性能调控具有一定的借鉴意义。

