CT引导下经皮肺穿刺活检诊断早期肺癌的意义及其与超声的对比分析
李 雪 张申众 袁秀敏 门桐林 张 璐 王 艳
肺癌是近年来世界范围内死亡率、发病率最高的恶性肿瘤,其发病率逐年上升,2011年世界新增患者高达160万,在所有恶性肿瘤新增患者中占13%左右,肺癌致死共140万例,占恶性肿瘤致死例数的23%[1]。肺癌5年生存率仍不足20%,这与肺癌确诊时间较晚,患者错失最佳治疗时机以及缺乏根治方法密切相关。目前该病的诊断金标准为病理学诊断,主要采用支气管镜、CT引导经皮肺穿刺活检、经胸腔镜胸膜活检以及超声内镜下支气管针吸活检[2-3]。CT引导经皮肺穿刺活检费用低、创伤小、恢复快、敏感度高,因此在临床广泛使用。本研究分析了CT引导经皮肺穿刺在早期肺癌中的诊断价值,并与超声进行对比,分析年龄、病灶大小、穿刺深度对CT引导经皮肺穿刺活检诊断肺癌敏感度的影响,报告如下。
1 资料与方法
1.1 一般资料
回顾性分析医院2011年1月至2017年6月1940例疑似肺癌患者资料。男性1106例,女性834例;年龄28~75岁,平均(65.01±8.12)岁。按获取活检组织方法不同分为2组,CT组970例,男性541例,女性429例;年龄28~72岁,平均(64.21±7.91)岁。超声组:男性565例,女性405例;年龄33~75岁,平均(66.98±9.12)岁。2组均经手术获取病理组织活检确诊,2组患者年龄、性别无统计学差异,P均>0.05,有研究可行性。纳入标准[4-5]:①胸CT提示有块状、结节状,且直径>5 mm的可穿刺病灶;②凝血功能、血常规、心电图正常,HIV、梅毒检测为阴性;③患者家属及其本人了解本研究的意义、穿刺的风险及必要性,自愿行穿刺活检,签署知情同意书。排除标准[6]:①心、肺、肝、肾等严重功能障碍;②无>5 mm的可穿刺病灶;③患者不配合研究。
1.2 方法
术前准备:在穿刺活检前充分评估各种安全因素,例如病灶位置、病灶大小、与邻近血管的关系;活检前必须获得最近的凝血功能信息,排除凝血异常;要充分了解病灶位置、大小、血管走形及活检部位结构,进行高质量阅片。CT引导下经皮肺穿刺活检:采用高清128层CT机(Optima CT660;美国GE),活检枪、17G及16G活检针。行常规CT平层扫描,明确患者病症位置,根据时机情况选择体位,层厚为1.5~3 mm,进行病灶局部扫描,将十字光标横线对准病灶最大径做标记,将横向光标与距病灶的最近的金属丝交点作为穿刺位点,常规消毒,行利多卡因(2%)局部麻醉,患者屏气时进针,针尖刺入病灶内,患者再次屏气,采集样品:使用甲醛(10%)固定样本,行病理组织学检查和细胞学检查;结合患者实际情况进行药敏实验和细菌学培养,术毕封闭穿刺位点,在20 min后再次扫描,主要观察患者病灶、气胸、针刀周围实时性出血等发生情况。使用全自动生化分析仪(Roche公司;MODULAR)测量血清NSE、CEA、CYFRA21-1,严格按试剂盒说明书操作,其阳性界值分别为15.0 μg/l,3.3 μg/l,5.0 μg/l。超声引导下经皮肺穿刺活检:根据胸CT确定病灶位置,超声探查病变部位以及病变与周围组织的关系,与胸壁的距离,确定穿刺位置、路径、进针角度、进针深度。穿刺位置经常规消毒铺巾,麻醉处理后用消毒穿刺引导探头再次核对上述信息,实施超声动态检测和引导下穿刺活检,活检组织2~3次,获取组织经10%甲醛溶液固定并送检。均以手术取样活检结果为标准。
1.3 观察指标
以手术取样获得的病理组织学诊断结果为准,对比2组特异度、敏感度、误诊率、漏诊率。对比2组并发症。进一步分析CT引导下经皮肺穿刺活检受年龄、病灶大小及穿刺深度的影响情况,根据年龄不同分组,≤30岁、>30~40岁、>40~50岁、>50~60岁、>60~70岁、>70岁,对比各组CT引导经皮肺穿刺活检诊断该病敏感度;根据病灶大小不同分为<2 cm、2~3 cm、4~5 cm、6~7 cm、>7 cm;按穿刺深度不同分为<3 cm、3~5 cm、6~9 cm、>9 cm,对比各组敏感度。
1.4 统计学分析

2 结果
2.1 检测结果对比
2.1.1 2组诊断结果及其各自手术取样病理确诊结果比较 CT组诊断结果:肺癌患者为585例,其中腺癌303例、鳞癌212例、小细胞肺癌61例、间叶来源恶性肿瘤9例;经手术取样病理组织检查确诊584例为阳性(肺癌),386例为阴性(肉芽肿性炎症277例、炎性104例、其它5例)。超声组诊断结果:肺癌共580例,其中腺癌303例、鳞癌211例、小细胞肺癌59例、叶间来源恶性肿瘤7例;经手术取样病理组织检查确诊:595例为阳性(肺癌),375例为阴性(非肺癌)(肉芽肿性炎症273例,炎性灶98例,其它4例)。
2.1.2 2组特异度、敏感度、误诊率、漏诊率对比 2组特异度、敏感度、误诊率、漏诊率比较,P均>0.05,见表1。

表1 CT与超声引导经皮肺穿刺活检诊断肺癌特异度、敏感度、误诊率、漏诊率对比
2.2 2组并发症发生情况对比
CT组共有125例患者发生并发症,发生率为12.89%;其中气胸共69例,56例为病灶及针刀周围实质性出血。超声组129例发生并发症,发生率为13.30%;其中气胸63例,病灶及针刀周围实质性出血共66例。
2.3 CT引导下经皮肺穿刺活检诊断肺癌敏感度与年龄、病灶大小及穿刺深度的关系
各年龄段敏感度比较,P>0.05;各病灶大小范围诊断敏感度对比,P>0.05;各穿刺深度组诊断敏感度比较,P>0.05。见表2。
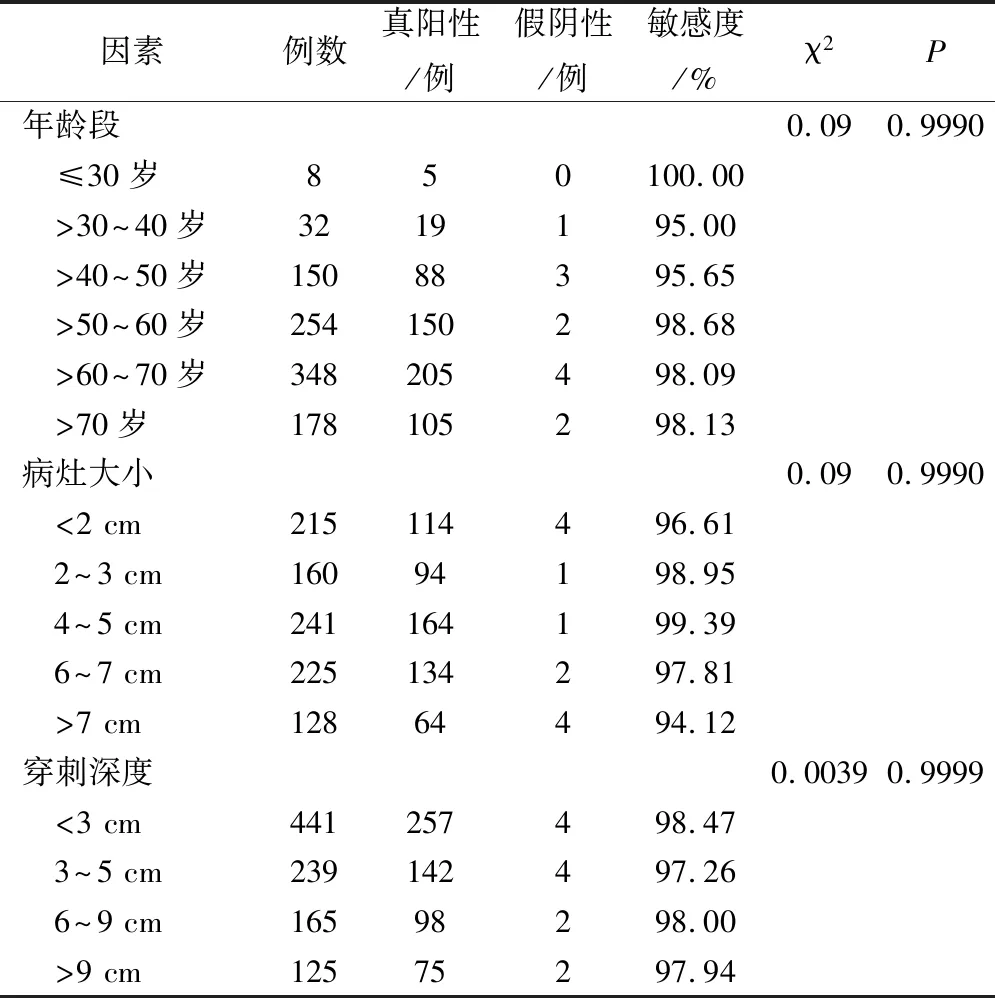
表2 不同特征下诊断敏感度对比
3 讨论
肺部病灶组织病理标本活检方式较多,包括开胸肺活检、纤维支气管镜下活检、胸腔镜活检、肺穿刺活检等。胸腔镜活检和开胸肺活检创伤较大,风险较高,不适合有心肺功能障碍和年龄较高的患者[7]。纤支镜检查在周围型病灶中难以窥及远端,活检难度大;对部分中央型病灶,纤支镜检查显示管腔外压性狭窄,因此获取病理组织难度也较高,纤支镜活检受限范围大[8]。经皮肺穿刺活检相对于以上活检方法,具有费用低、创伤小、患者痛苦小等优势,一些医院肺穿刺活检后患者可当天出院,穿刺第二天能正常生活[9]。在CT引导下经皮肺穿刺能清晰了解病灶位置、大小、形态及病灶与毗邻组织的重要关系,尤其在纵膈旁、心影后、脊柱旁的小病灶能清晰显影;若增强CT扫面则能更好观察病灶血供及其与大血管的重要关系,能有效区分坏死区,分析病灶周围组织,例如叶间裂、肺大泡等。而超声引导下经皮肺穿刺活检在肺癌诊断中应用已久,能实时观察并调整进针深度,同时无辐射,对体位要求低,创伤小,诊断准确性高[10-11]。本研究将CT用于肺癌早期诊断中,并与超声引导下经皮肺穿刺活检进行对比,发现二者均有较高诊断价值。
CT引导下肺穿刺活检能诊断肺癌,并利于病理组织检查准确分型。陈轸等[12]报道,CT引导经皮肺穿刺活检在肺部良性病变中的诊断符合率为80%及以上,在恶性肿瘤中的诊断符合率高达99.1%,特异度高达96.0%以上。王志敏等[13]在<15 mm肺结节中CT引经皮肺穿刺活检准确率为93%,特异性为100%。本研究结果发现CT诊断特异度(96.63%)、敏感度(97.75%)、误诊率(3.37%)、漏诊率(2.05%),基本与上述研究结果一致,说明CT引导下肺穿刺活检敏感度高,能有效诊断肺癌。通过与超声进行对比发现,CT组与超声组特异度(92.00%)、敏感度(92.44%)、误诊率(8.00%)、漏诊率(7.56%)比较,P>0.05。但仍然可见CT组的特异度、敏感度略高于超声组,误诊率和漏诊率略低于超声组。考虑可能是因为CT引导,对<1 cm的病变也能准确定位,同时在超声无法探及的周围型病灶中能有效操作。但是,与超声相比,CT对体位要求较高,有放射辐射伤害,其价格更贵[14]。2组在穿刺并发症发生率上无统计学差异,其中 CT组共有125例患者发生并发症,其中气胸共69例,病灶及针刀周围实质性出血56例,提示气胸和出血是主要并发症,但仍然是可控风险,需要提高穿刺技术,加强并发症预防。
本研究采用年龄分组、病灶大小分组和穿刺深度分组分析CT引导下经皮肺穿刺活检是否受以上因素影响。结果发现各年龄组诊断敏感度均超过90%,组间比较无统计学差异,P均>0.05;在各病灶大小分组中及各穿刺深度分组中敏感度也均无统计学差异,P均>0.05。提示CT引导下经皮肺穿刺活检的敏感度不受以上因素影响,稳定性高,因此高龄患者只要无严重心肺功能异常,也能完成穿刺。但值得注意的是,本研究中漏诊的患者中以病灶直径<2 cm,>7 cm较多。考虑是病灶太小难以控制进针角度及深度,降低了穿刺准确率;病灶过大则常出现病灶中央坏死、液化组织以及周围炎性浸润,穿刺到炎性组织或坏死组织导致假阴性[15]。
综上所述,CT引导下经皮肺穿刺活检在早期诊断肺癌敏感度高,不受病灶大小、穿刺深度、患者年龄影响,与超声引导下经皮肺穿刺活检早期诊断肺癌有几乎相同的诊断价值,尤其在超声难以诊断的周围型病变中更有优势,对过小的病灶和过大的病灶则需进一步提高进针技术。

