128例抗肿瘤药物不良反应现状分析
李丹
(河南省安阳市肿瘤医院 药剂科,河南 安阳 455000)
化疗是恶性肿瘤的主要治疗方式,具有普遍性和经济性,具有一定效果,但其应用受到抗肿瘤药物不良反应(adverse drug reaction,ADR)的限制[1]。在正常剂量下,抗肿瘤药物ADR依旧不可避免,ADR不仅对患者身心造成损害,也影响化疗效果和预后,如何减少抗肿瘤药物ADR发生率是临床关注要点[2~3]。为减少患者痛苦,预见性防治ADR,指导临床用药,本文选择128例抗肿瘤药ADR患者进行分析研究,现报道如下。
1 资料与方法
1.1 研究方法与观察指标
选择本院2015年6月-2018年6月抗肿瘤药物不良反应患者128例,纳入患者均知情同意本研究,并获院伦理委员会批准。首先收集患者一般资料,包括年龄、性别等,其次再收集患者ADR报告,对其年龄、药物情况,包括服药种类临床常见抗肿瘤药物种类如烷化剂类、抗生素类、激素类及抗代谢类等)、服药方式(静脉注射、静脉滴注及口服等)、剂量(单一用药、联合用药、序贯用药等及每日服药次数、每次服药剂量)等,并对ADR表现如恶心、呕吐、唇周麻木、心电图异常及骨髓抑制等数据进行分类整合,其中ADR关联性评价标准依照《药品不良反应评价判断标准》[4]进行评价,根据用药和ADR发生顺序、停药后ADR情况、再次使用该药物ADR情况、激发试验是否为阳性及是否有文献资料佐证等资料,运用综合分析推理法将药品与ADR的关联性分为肯定有关、很可能有关、可能有关、可能无关及无法评价。
1.2 统计学方法
本文涉及所有数据均采用SPSS 19.0软件分析,对于各种构成比等无序性计数资料均以百分比(%)形式表示,均采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 ADR患者一般情况
128例ADR患者各年龄段分布如表1所示,51~60岁年龄段占总人数比例最多,为32.81%,其次是61~70岁,占据26.69%;性别比例基本符合1∶1。
2.2 ADR患者服药情况
表2显示,128例肿瘤患者涉及不同药物共12种,包括烷化剂类、抗生素类、激素类及抗代谢类等,其中氟尿嘧啶服用频次最高,占18.75%,其次是环磷酰胺(16.41%)、紫杉醇(14.06%);其中91(71.09%)例患者为联合用药,37(28.91%)例仅使用单种药物;ADR发生次数合计179次(联合用药患者ADR情况按照其所服用的每种药物记录),其中17次为严重ADR,表现为剧烈消化道反应,急剧白细胞减少,涉及药物主要为氟尿嘧啶、环磷酰胺、紫杉醇及多西他赛等,162次为一般ADR,有轻微头痛、发热、恶心、呕吐及食欲减退等;所有药物中引起ADR次数最多的药物为氟尿嘧啶,共计引起29次,占总发生次数的16.20%;128例患者给药途径静脉注射、口服及介入分别为117(91.41%)例、7(5.47%)例和4(3.13%)例。
2.3 ADR累及部位及主要表现
128例患者主要累及系统-组织由高到低依次是消化系统74(41.34%)、血液系统27(15.08%)、神经系统25(13.97%),分别表现出食欲减退、腹痛腹泻、骨髓抑制、血液指标异常、麻木及眩晕等对应系统症状。见表3。
2.4 ADR关联性
根据《药品不良反应评价判断标准》判定,128例ADR患者判定为肯定相关、很可能相关、可能相关及可疑的例数分别是37(28.91%)、46(35.94%)、43(33.59%)和2(1.56%)。
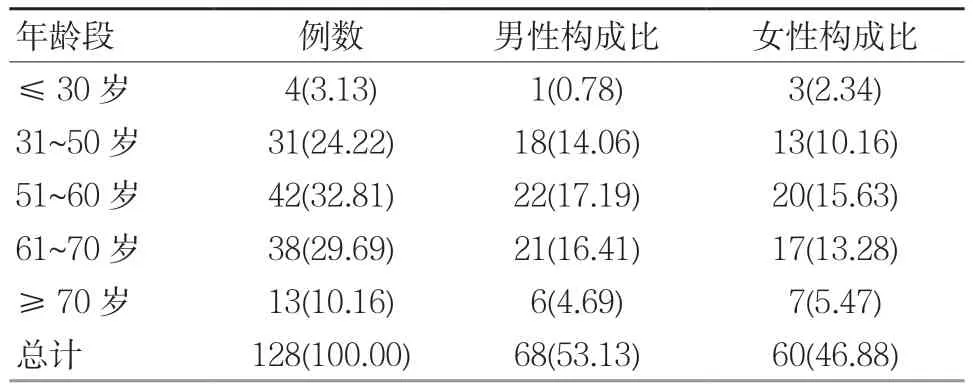
表1 ADR患者一般情况 例(%)

表2 ADR患者药物服用情况 例(%)
3 讨论

表3 ADR累及部位及主要表现 例(%)
3.1 ADR发生群体
本文结果显示,128例研究患者中男女性别比例接近于1∶1,男性患者略多于女性患者,考虑可能与吸烟男性较多有关,尽管男女比例没有显著差异,但在临床上应注意根据男女患者体质不同制订个性化化疗方案,普遍而言女性身体素质逊于男性,器官、组织较为敏感且耐受性较差,提示临床用药可根据患者ADR情况酌情增减、更换药物。此外,流行病学上显示抗肿瘤药物ADR多发、常发于51~60岁患者,其次是61~70岁这一年龄段,说明老年患者可能是ADR的易发人群,这可能与老年患者各方面身体机能退化及肝肾等器官无法对药物进行有效代谢有关,加上肿瘤、化疗对患者的消耗,ADR更易出现。研究发现,50~70 岁这一年龄段是消化系统肿瘤(胃癌)、生殖系统肿瘤(乳腺癌)发生的重要时期[5]。对此,临床治疗中应根据患者年龄,综合考虑其身体素质,给予必要预防措施。
3.2 ADR服药情况
128例患者中服用抗肿瘤药物总计12种,使用次数由多至少依次是氟尿嘧啶(18.75%)、环磷酰胺(16.41%)、紫杉醇(14.06%)、多西他赛(11.72%)。氟尿嘧啶是一类广谱抗肿瘤药物,具有多条药理作用途径,可抑制多种肿瘤细胞的生长、增殖,通常与多西他赛、奥沙利铂等联合治疗,这可以解释为何氟尿嘧啶在128例患者中基数较大,同时也说明联合用药可能是恶性肿瘤的普遍选择,本文可见71.09%的患者为联合用药。氟尿嘧啶有效剂量与中毒剂量之间的差值较小,在有效杀伤肿瘤细胞的同时对正常细胞也有较强毒副作用[6]。本文统计后发现,128例患者共发生ADR次数179次,引起ADR次数最多的药物是氟尿嘧啶,共计引起29(16.20%)次。因此笔者认为,临床恶性肿瘤的治疗为弥补体质较差等原因造成的疗效折扣,提高治疗效果,联合用药是医患双方的共同选择,但多种药物联用可能出现药物相克、药效减低及增加毒副作用等现象,提示临床治疗不仅要关注疗效,也应注意关注各类药物药性、药理、禁忌证以及患者耐受水平等。此外,研究发现,91.41%的患者均为静脉注射给药,口服给药和介入给药仅占少数,与文献[7]称静脉注射为抗肿瘤药物最普遍给药方式一致。抗肿瘤药物普遍具有细胞毒性作用,通过静脉注射可能会发生渗漏,药物渗出血管外进入皮下或组织,造成正常活跃细胞死亡,这或许是ADR产生的直接或间接原因,故抗肿瘤药物应当重视静脉注射。
3.3 ADR累及部位及对应措施
表3显示,本文纳入患者发生抗肿瘤药物ADR主要累及的系统或组织前3位分别是消化系统74(41.34%)、血液系统27(15.08%)、神经系统25(13.97%),分别表现出恶心呕吐、食欲减退、腹痛腹泻,骨髓抑制、血液指标异常,麻木及眩晕等对应系统症状。顺铂是目前致呕吐作用最强的抗肿瘤药物,其对消化系统的伤害主要通过损伤消化道黏膜,导致羟色胺等物质的释放和激活,引起呕吐中枢兴奋;抗肿瘤药物中的某些化学成分对催吐感受区的作用也是消化道不良反应发生的机制之一[8]。血液系统反应则以骨髓抑制为主,骨髓抑制对免疫功能有较大影响,应当重点关注,对于造血系统障碍或免疫低下患者,理当禁用此类药物,从目前抗肿瘤药物应用、研究来看,只有极少数药物未观察到骨髓抑制反应,有强烈致呕作用的顺铂,因其较强的抗癌活性仍在使用[9]。因此,临床用药无法做到禁用此类具有明显ADR抗肿瘤药物,只能在使用时谨慎考虑,实时监测,必要时给予骨髓抑制患者骨髓再生刺激药物、广谱抗菌药。抗肿瘤药物的神经毒性机制尚未完全清晰,猜测可能与药物本身(如铂类)在体内积蓄过多及药物体内代谢产物损伤神经有关[10],提示肿瘤研究不仅要加强用药规范、合理,强调ADR监管,更应加大研发新药力度,研制ADR少甚至没有的抗肿瘤药物或是未来肿瘤研究的主要趋势。
综上所述,抗肿瘤药物多发于年龄较大、联合用药及静脉注射患者,主要累及消化系统,临床治疗可重点关注此类患者,尽可能防治、减少ADR。

