暴发性1型糖尿病1例
1型糖尿病(type 1 diabetes mellitus,T1DM)是一种遗传易感个体在环境因素的触发下,发生的以T淋巴细胞介导的胰岛β细胞破坏引起胰岛素分泌绝对缺乏而导致的代谢性疾病。根据是否有自身免疫因素的参与,美国糖尿病协会和世界卫生组织将其分为自身免疫性T1DM(1A型)和特发性T1DM(1B型)。暴发性1型糖尿病(FT1D)是由日本学者Imagawa等在2000年提出一种以急骤起病(症状<1周)、代谢紊乱严重、胰酶升高并缺乏糖尿病相关抗体为特征的1型糖尿病新亚型。,美国糖尿病学会及世界卫生组织将其暂归为特发性 T1DM的范畴[1]。此类患者需终身使用胰岛素治疗,预后极差[2]。本文报道1例FT1D。
1 病例特点
1.1 简要病史
患者男,25岁。因口渴、多饮、多尿3天,恶心、呕吐、腹泻1天于2013年11月29日17:00入院。患者平素饮用含糖饮料500~1 000 mL/d。入院前3天患者无诱因出现口渴、多饮、多尿。入院前1天进食不洁饮食后出现恶心、呕吐、腹泻,无发热、腹痛,后口服800 mL糖水及1 600 mL可乐,自服头孢类药物。次日因上述症状无缓解入我院急诊,查血常规:白细胞27.65×109/L、中性粒细胞90.9%。血生化:血糖50.5 mmol/L,谷丙转氨酶(ALT)43 U/L,谷草转氨酶(AST)23 U/L,钾(K+)6.28 mmol/L、钠(Na+)129.9 mmol/L,肌酐(Cr)263 μmol/L,尿素(Urea)13.6 mmol/L。动脉血气分析:pH 7.104,氧分压129 mmHg,二氧化碳分压17.3 mmHg,剩余碱(ABE)-24.6 mmol/L,碳酸氢根浓度(HCO3-)5.2 mmol/L,血乳酸3.8 mmol/L。尿常规:尿糖(++++)、尿酮体(+++),,肌钙蛋白、CK-MB同工酶未见异常。血淀粉酶76.73 IU/L。心电图示窦性心动过速。予氯化钠2 000 mL静脉滴注及胰岛素12 U降糖,以“糖尿病酮症酸中毒”收入内分泌科。患者既往体健,无烟酒嗜好,无胰腺炎病史,无糖尿病家族史。体检:T 36.6℃,Bp 129/78 mmHg,P 116次/分,R 19次/分,BMI 23.66 kg/m2。口腔呼出气无烂苹果味,心肺查体无异常。腹平软,上腹部有压痛,无反跳痛及肌紧张。肌力及肌张力正常,病理征(-)。
1.2 主要辅助检查
入院后急查静脉血糖38.86 mmol/L。确诊为糖尿病酮症酸中毒急性胃肠炎急性肾功能不全,立即给予吸氧、大量补液、小剂量人胰岛素静脉泵入降糖、奥美拉唑抑酸、头孢他啶抗感染等治疗。胸部CT示双肺轻度间质性改变,双侧胸膜增厚。腹部CT示胰腺形态、大小、密度正常,胰腺周围未见积液,显示脂肪肝。血、尿淀粉酶动态变化结果,见图1。入院第3天OGTT试验示空腹及餐后0.5 h、1 h、2 h、3 h血糖分别为15.73 mmol/L、21.77 mmol/L、27.87 mmol/L、29.47mmol/L、26.63mmol/L,空腹及餐后0.5 h、1 h、2 h、3 h C肽分别为0.19 ng/mL、0.24 ng/mL、0.25 ng/mL、0.22 ng/mL、0.25 ng/mL,空腹及餐后0.5 h、1 h、2 h、3 h胰岛素分别为 15.03 μU/mL、5.23 μU/mL、4.59 μU/mL、6.81 μU/mL、6.16 μU/mL。糖化血红蛋白(HbA1c)7.1%,谷氨酸脱羧酶抗体(GADAb)、胰岛素自身抗体(IAA)均为阴性,确诊为暴发性1型糖尿病。超敏C反应蛋白9.81 mg/L;甲功示血清游离T3(FT3)3.21 pmol/L(参考值3.5~6.5 pmol/L)、高敏促甲状腺激素(sTSH)0.34 mIU/L(参考值0.51~4.94 mIU/L)。EB病毒壳抗体IgG(+)、EB病毒核心抗体IgG(+),EB病毒壳抗体IgM阴性。血沉18 mm/h。心肌酶谱、泌乳素、生长激素、血脂、抗核抗体(ANA)、抗ENA抗体、抗中性粒细胞胞浆抗体(ANCA)、抗双链DNA、补体、免疫球蛋白、类风湿因子、肿瘤相关抗原未见异常。疱疹病毒抗体、巨细胞病毒抗体、柯萨奇病毒抗体均阴性。UALB/Cr 33.68 mg/g。上腹部超声示脂肪肝(重度)。促肾上腺皮质醇激素、皮质醇、雌激素、睾酮、黄体生成素、促卵泡激素均正常。UALB/Cr 7.98 mg/g。24小时尿蛋白定量及尿微量白蛋白定量分别为62.48 mg、16.93 mg。颈部血管超声及神经传导速度未见异常,眼底未见渗出及出血。
1.3 治疗经过
患者入院前3天使用小剂量胰岛素泵静脉泵入,第4天使用实时动态血糖监测(CGMS:MinMedInc)及便携式胰岛素泵(美敦力722型),根据血糖调整门冬胰岛素用量(图1和表1),住院期间平均血糖(11.0±5.6)mmol/L,每日胰岛素总量(63.4±20.8)U,基础量和三餐前负荷量各占总量的50%。入院第12天空腹血糖5~6 mmol/L,餐后血糖6~9 mmol/L,血糖较前明显好转,遂出院。院外使用门冬胰岛素(早16 U,午12 U,晚12 U)、地特胰岛素(睡前28 U)皮下注射降糖。
2 讨论
2012年日本糖尿病学会提出确诊FTlD标准:(1)高血糖症状出现1周内即发展为DK或DKA(首诊时血或尿酮体升高);(2)首诊时血糖≥16 mmol/L且HbAlc<8.7%;(3)发病时尿C-P<10 μg/d,或FC-P<0.3 ng/mL且刺激后(胰升血糖素或进食)<0.5 ng/mL。本例的临床特点是:(1)病程3 d内出现糖尿病酮症酸中毒且代谢紊乱严重,动脉血pH 7.104,剩余碱-24.6 mmol/L,血钾6.28 mmol/L、血钠129.9 mmol/L、血肌酐263 μmol/L。(2)首诊血糖50.5 mmol/L,而HbA1c 7.1%。(3)胰岛功能极差,入院查空腹及餐后0.5~3 h C肽均<0.5 ng/mL。以上符合暴发性1型糖尿病诊断的要点。此外本例还有以下临床特点:(1)胰岛自身相关抗体阴性。(2)血淀粉酶升高,但胰腺CT及B超检查均无胰腺炎的改变。(3)有恶心、呕吐、腹泻等胃肠道症状。
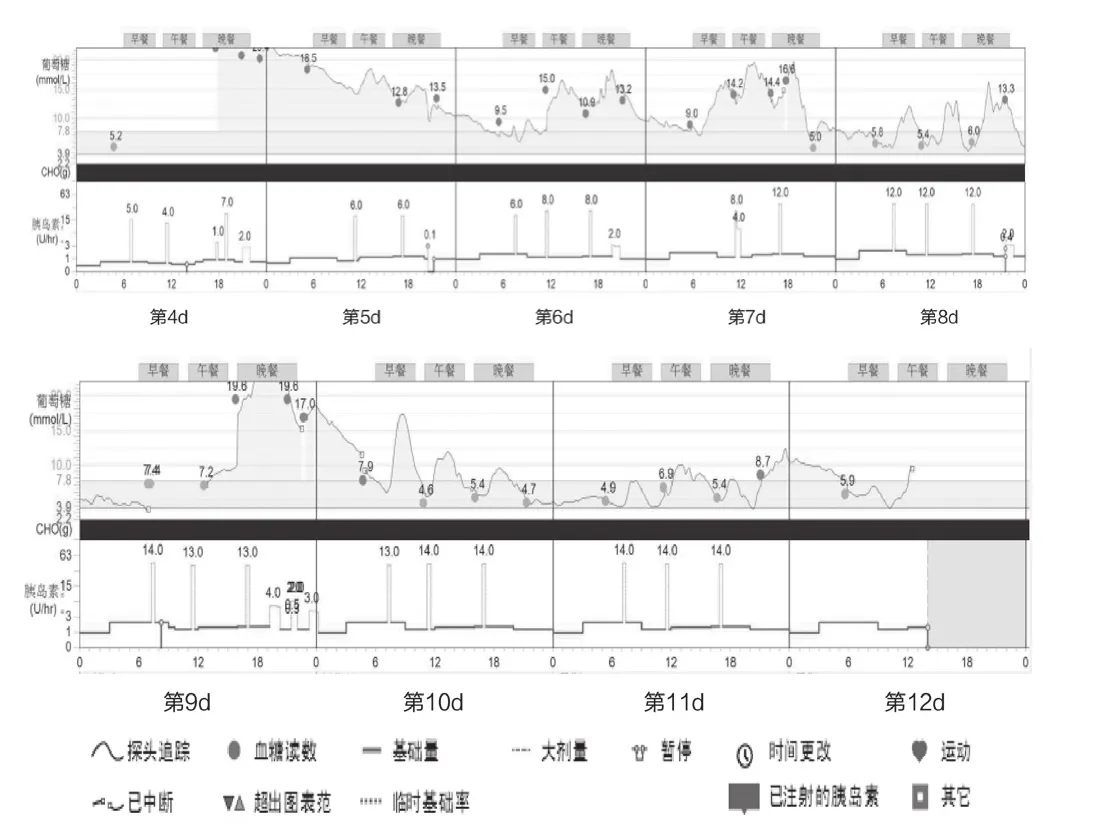
图1 住院第4~11天全天血糖及胰岛素泵皮下注射用量图

表1 1例暴发性1型糖尿病治疗后平均血糖值与胰岛素总量之间的关系
目前已有大量研究证明病毒与暴发性1型糖尿病发病存在相关性,这些病毒包括HHV-6病毒、单纯疱疹病毒、B型流感病毒 、EB病毒 、流行性腮腺炎病毒、科萨奇病毒、甲型病毒肝炎病毒、病毒性心肌炎等[3-8]。人类白细胞抗原(HLA)基因[9]及自身免疫反应[10]与本病相关。本例有进食不洁饮食,有恶心、呕吐、腹泻等胃肠道症状,可能存在病毒感染。
本例有血淀粉酶升高,且伴有恶心、呕吐症状及上腹部压痛,需注意有无合并急性胰腺炎。糖尿病酮症酸中毒时出现血清胰酶升高的机制可能是胰腺外组织分泌淀粉酶;血容量减少,肾小球滤过率下降导致胰酶清除减少;严重的神经调节及代谢异常使胰酶自胰腺滤泡漏出;自身免疫机制致胰腺腺泡损伤,胰酶释放入血。此外,FT1D患者常伴有横纹肌溶解症,应注意观察患者尿液颜色有无变化及是否有肌肉酸痛,同时动态监测血肌酸激酶、肌红蛋白[11]。少数FT1D患者可发生脑水肿[12-13]。
FT1D因起病急骤,代谢紊乱严重,疑诊或确诊后应立即按严重的糖尿病酮症酸中毒处理,给予大量补液、小剂量胰岛素静脉滴注。本例积极补液排酮、小剂量胰岛素降糖后,第3天糖尿病酮症酸中毒纠正。住院第4天使用胰岛素泵持续皮下泵入,门冬胰岛素量由34 U逐渐增至79 U,平均1.1 U/(kg·d),较1A型糖尿病日胰岛素需要量大。图1可见,患者一旦出现胰岛素漏注,血糖迅速上升。在FT1D治疗上,胰岛素泵较胰岛素多次注射更有利于血糖控制。因此对于有条件的患者,使用胰岛素泵控制血糖更为有效。

