3D打印技术制备主动脉弹性血管模型在主动脉疾病中的应用
江启迪 胡何节 方征东 王晓天 孙小杰 葛新宝 程 灿
安徽医科大学附属省立医院血管外科,合肥市 230001
主动脉瘤的发病机制尚不明确,目前的主流观点认为其与炎症反应及巨噬细胞的渗透相关,这些因素引起主动脉壁弹性蛋白的降解,最终导致主动脉壁局部扩张[1]。主动脉瘤的危害主要为动脉瘤破裂引起致死性休克,其中腹主动脉瘤破裂的死亡率可达90%[2]。通常小的胸腹主动脉瘤的瘤体直径平均每年约增长0.32 cm,若瘤体直径大于5.0~6.0 cm,瘤体的破裂概率可达5%~7%,当瘤体直径大于7 cm时,瘤体的五年破裂率可达95%[3]。目前胸腹主动脉瘤的手术治疗可分为传统开放手术及瘤体覆膜支架腔内隔绝术(endovascular aneurysm repair, EVAR),开放手术患者围术期死亡率可达49%,而EVAR术患者围手术期死亡率可降至15.7%[4]。EVAR手术修复有很多潜在的并发症,如支架的移位、术后内漏、支架覆盖重要分支血管等,术前评估显得尤为重要[5]。已经有学者根据患者术前CT血管造影(CT angiography, CTA)图像进行三维建模,运用3D打印技术制备精准的动脉瘤模型,应用于术前评估中,但大多学者都采用刚性材料打印,与正常血管的物理性质不符,其在数据测量、血管解剖结构的表现方面具有一定的优势,但对于体内支架释放后血管形态学改变、支架在血管中服帖情况的评估不太准确。也有学者采用3D打印机打印出了弹性的透明血管模型,但这种材料价格昂贵,且需要用到的打印机同样十分昂贵,高成本严重限制了其在临床上的应用[6]。本文介绍了一种新型的廉价主动脉瘤弹性血管模型建立方法,以期为主动脉疾病患者的精准术前评估提供一种新的工具。
1 资料与方法
1.1 一般资料
选择2018年1月至2019年1月本科室收治的胸主动脉瘤患者及假腔血栓化的主动脉夹层患者15例,排除动脉瘤破裂及严重主动脉粥样硬化使主动脉狭窄>50%者。其中,主动脉夹层6例,胸主动脉瘤9例,男性11例,女性4例,年龄(61±13)岁。患者入院后均完善超声心动图检查,检查前测量其收缩压及舒张压(测量三次取平均值),得出脉压差。检查中测量患者一个心动周期内主动脉弓部的最大直径及最小直径,得出内径变化(多次测量取平均值),最后计算患者胸主动脉弹性系数,弹性系数K=脉压差(mmHg)/直径变化(mm)。
1.2 方法
石蜡模型制作:用石蜡制作11个高15 cm、直径3 cm的圆柱体模型,取出3个,标记为A、B、C;涂抹弹性材料:将A、B、C三个模型分别涂上硅胶硬化剂混合物,配比为推荐配比(硅胶:硬化剂=100∶2),放入模型架上待其自然干燥(约12 h,受气温及硬化剂用量影响,过量硅胶会因重力作用自行流下)。干燥后于B、C模型表面再次涂抹硅胶硬化剂混合物,再次干燥后于C模型表面涂抹第三层硅胶硬化剂混合物。去除填充物:将完全干燥的模型放入约70 ℃热水中,待石蜡软化后去除石蜡,修剪底部硅胶沉积物,得到3个不同厚度的圆柱体模型。测量弹性系数:将模型的一端与压力泵连接,测量每组模型的外直径(测三次取平均值),再分别将压力泵压力打到40 mm Hg、50 mm Hg、60 mm Hg、70 mm Hg、80 mm Hg(1mm Hg=0.133kPa),测量每个模型的外直径(测三次取平均值)。将结果导入SPSS 21.0作线性回归分析,压力为自变量,直径为因变量。结果表明三组数据均符合线性关系,其斜率的倒数定义为模型的弹性系数K。结合相关文献可知B模型弹性系数最接近于人体动脉弹性系数[4]。
1.3 硬化剂用量与硅胶模形弹性系数的关系
建立不同硬化剂比例模型:根据前次实验结果,B模型的弹性系数最接近于人体动脉弹性系数。将其余8个石蜡模型编号为B1-B8,并配制8组不同硬化剂比例的硅胶, 依 次为 100:1.4,100:1.6,100:1.8……100:2.8, 编 号为B1~B8。测量弹性系数:采用与前述相同的方法,每组模型分别用相对应的材料涂抹表面两次,干燥后去除填充物,以相同方法测量其弹性系数。得出函数关系:用SPSS 21.0对硬化剂用量百分比和弹性系数进行相关性分析,得出函数关系。
1.4 制作仿真弹性血管模型并验证
CT图像获取:患者行主动脉多层螺旋CT增强扫描,应用的对比剂是碘海醇注射液,注射流速为3.5~4.0 ml/s,注射总量为90~100 ml,扫描层厚为0.5~1.5 mm,输出图像为DICOM格式。数据处理:将CT原始数据导入Mimics 17.0软件,进行阈值分割,保留动脉部分,再对胸主动脉病变部分进行三维重建,光滑化处理后以STL格式导出数据,接着将数据导入切片软件cura15.0,打印材料选择丙烯腈一苯乙烯一丁二烯共聚物(acrylonitrile butadiene styrene, ABS),打印床温度设置为110 ℃以防止材料翘边,打印精度选择0.1 mm,壁厚1.2 mm,填充率30%,打印速度为默认值。构建支撑结构后生成G-code文件保存于SD卡上,准备打印。3D打印模型:本研究中使用的打印机为Anycubic 4MAX 3D打印机,采用熔融沉积造型技术。打印前在热床上均匀涂一层ABS丙酮溶液,可有效防止翘边,室温应高于25 ℃,以提高打印成功率。打印完成之后去除支撑结构,表面用丙酮蒸汽抛光处理。涂抹弹性材料:计算动脉弹性系数,将K值代入公式,选择最合适的硬化剂比例,将硅胶硬化剂混合物涂抹于打印出的模型表面,共涂抹两层。溶解支撑结构:在通风厨中将模型完全浸泡入丙酮溶液中,待内层ABS塑料溶解软化后(约6 h),在丙酮溶液中反复清洗模型,直至ABS塑料完全溶解,再在流动水中冲洗模型,直至模型完全洗净,表面无ABS塑料附着,烘干后即制备出主动脉弹性半透明模型。验证:截取模型的降主动脉部分,将模型的一端封闭,另一端连接压力泵,将压力泵压力设置为检查前测量出的脉压差,测出模型的内径变化。
1.5 模型在主动脉疾病患者中的应用
通过模型了解主动脉弓形态,并对动脉模型主动脉弓三支分支血管的直径、主动脉弓直径、近端锚定区长度进行测量,与患者CT图像进行对比,评估合适的支架尺寸。再将实验用覆膜支架释放入血管模型中,观察支架释放后模型的形态变化并预测手术中可能出现的问题。
2 结果
2.1 弹性材料最佳层数
A,B,C三组模型的压力和直径变化均符合线性关系(R2≈1),其斜率的倒数即为模型的弹性系数(表2)。结合相关文献可知,涂抹2层弹性材料后,模型的弹性最接近真实血管弹性。
2.2 硬化剂用量与材料弹性系数的关系
每组不同硬化剂用量的模型,其压力与直径变化均符合线性关系(R2≈1)。硬化剂用量 X(1.2<X<2.8)与弹性系数K之间满足三次方程关系(R2=0.990),解析式为K=-3.243X2+2.057X3+16.587(表3,图1)。
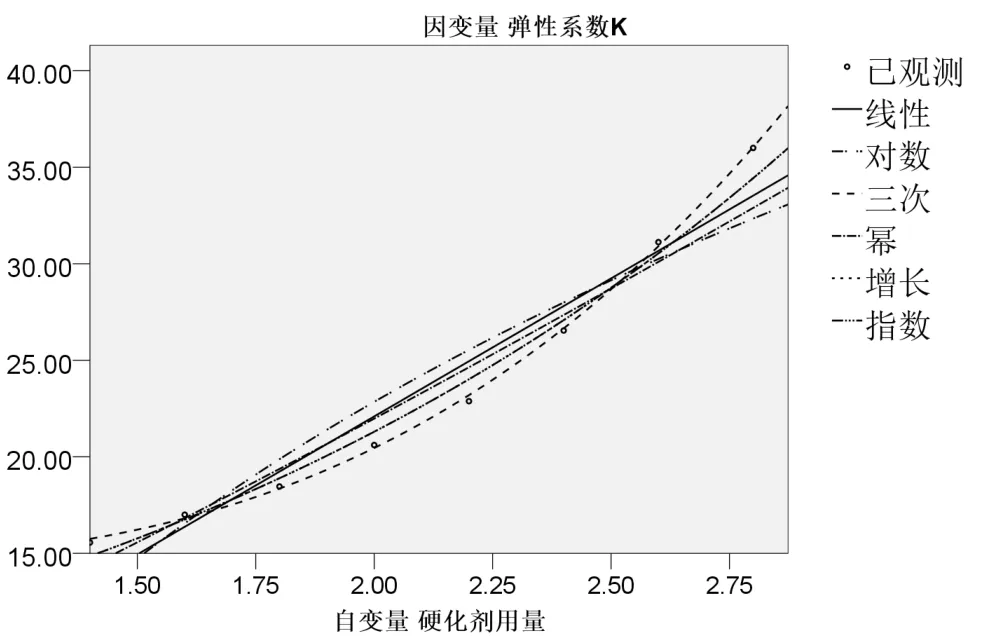
图1 硬化剂用量x值(自变量)与弹性系数k值(因变量)回归分析
2.3 验证弹性模型的效果
对15例患者的动脉弹性系数与对应的模型弹性系数进行统计学分析,两组K值无统计学差异(t=0.294,P=0.773)。
2.4 患者的治疗效果
本次研究的15例患者最终均行主动脉腔内修复术,其中有1例体外预开窗,2例封堵左锁骨下动脉,1例患者术中支架近端内漏,予球囊扩张后内漏消失。手术即刻成功率100%,未发现手术相关的并发症,术后1个月复查均未见明显内漏。
3 讨论
随着技术的发展,血管外科在过去二十年里有了很大的进步。特别是腔内技术的发展,让越来越多的大动脉疾病患者能够以最小的创伤完成手术,极大提高了患者的住院生存率及远期生存率[5,8]。但是腔内手术相较于传统手术,由于涉及手术方案的选择、支架的选取、锚定区的选择,往往需要更精确的术前评估[9]。目前血管外科主流的术前评估方法为术前CTA三维重建,部分医院开始尝试3D可视化、虚拟现实以及术前3D打印血管模型以寻求更加高效准确的术前评估方式[10]。3D打印模型可以使复杂的结构可视化,可用于协助诊断、规划手术方案、指导支架的选择,同时也有助于提高与患者家属的沟通效率[11]。尽管目前已经有较为成熟的CT三维重建技术,但是对于复杂血管病变空间结构的表现,仍需要临床医生充分的空间想象能力,且由于术中查阅的不便,该技术在临床实际中主要用于术前评估,术中对病变的把握仍依赖于二维的DSA造影。
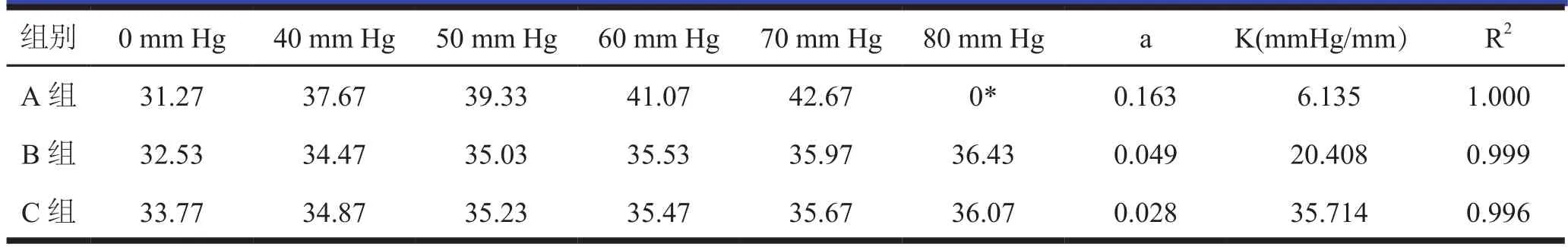
表1 对A、B、C三组数据进行线性回归分析

表2 硬化剂用量与材料弹性系数的函数公式
3D打印技术,也称为快速成型制造或增材制造技术,其概念最早由Hull在1986年提出,他运用计算机数据资料,以光敏树脂为原料,通过逐层增材打印的方式,制造出了精准的三维模型[12]。由于早期3D打印设备比较昂贵,最初仅限于汽车和航空航天工程,随着技术的进步,商业打印机造价逐渐低廉,再加上数据处理软件的普及,3D打印技术开始进入各行各业[13]。2001年,Lermusiaux P等[14]报道了3D打印技术在血管外科领域中的首次应用,他们运用3D打印技术制备了腹主动脉瘤的三维血管模型用于患者的术前评估。这种直观的血管模型相较于三维CT显然更受血管外科医生欢迎,自此,越来越多运用3D打印技术进行血管外科手术术前评估的报道被发表,3D打印技术在血管外科的应用越来越多。
目前国内学者选择的3D打印材料大多为聚乳酸(Polylactic acid, PLA)、ABS工程塑料[15-16]等刚性材料,其优势包括:(1)便于测量动脉瘤的相关数据,如瘤颈长度、各分支距瘤体距离、瘤颈角度等;(2)可以直观地观察病变血管的结构及与周围组织的关系,特别是腹主动脉瘤及腹腔动脉动脉瘤的模型,可以直观地将瘤体部位、瘤体周围血管与瘤体的关系、血管分支的解剖学变异呈现给血管外科医生,协助医生选择合适的手术方案、合适大小的支架;(3)在腹腔动脉动脉瘤患者的手术过程中,血管模型可以协助医生顺利地将导丝旋入远端分支血管,避免反复多角度造影增加手术时间、造影剂用量及X线的暴露时间[15-17]。但刚性模型也有其局限性,它无法模拟支架释放后血管的形态改变,在支架体外预释放中的应用受限。国外已经有学者打印出了具有弹性的血管模型,但是高昂的造价严重限制了其应用于临床,且弹性材料的打印精度可能差于刚性材料。
为了解决刚性模型的不足以及弹性3D打印材料价格昂贵的问题,本研究采用3D打印支撑结构,再用硅胶翻模的方式,在提高精度的同时降低了成本。ABS塑料具有抗冲击强度较高、化学稳定性、电性能良好等优点,被广泛应用于3D打印材料。其耐水、无机盐、碱和酸类,不溶于大部分醇类和烃类溶剂,而容易溶于醛、酮、酯和某些氯代烃中[18]。硅胶是一种化学性质极为稳定的材料,除了强碱和氢氟酸,几乎不与任何溶剂反应。本研究中使用的翻模硅胶在常温下呈粘稠的液态,加入硬化剂后可缓慢固化成富有弹性的固体结构。鉴于硅胶和ABS的这种特性,研究人员以ABS为材料打印出血管模型后,在模型表面涂抹液态硅胶,待硅胶干燥硬化后用丙酮解掉ABS,最终保留硅胶外壳,保留精确的弹性模型。在实际使用中,发现只涂一层硅胶常常会出现最终制作的模型有多处孔洞,可能与ABS支撑结构表面不平滑有关。且即使模型结构完整,在用压力泵加压后仍经常出现模型破裂。在尝试涂两层硅胶后,上述情况发生的机率大大减少。制作过程中,还发现模型的弹性性能与涂抹层数及硬化剂比例有较大的相关性,所以本研究设计了两组试验。在第一组中,研究者选择了相同的硬化剂比例,分别涂抹不同的层数,结果显示只涂抹一层硅胶,模型的强度不够,且弹性系数与人体血管实际的弹性系数相差过大,而三层硅胶使模型显得过于臃肿,部分分支血管无法看清,且模型弹性变差。最终研究者选择了两层硅胶,它兼顾了模型弹性和强度,且与实际血管情况相接近。在第二组实验中,建立了一组硅胶层数为两层,硬化剂用量不同的模型。由于固化时间的差别,每组模型厚度也不一致,随着硬化剂使用量的增加,模型固化速度加快,厚度增加,弹性也相应降低,且添加的硬化剂本身就有让硅胶变硬变脆的特性。在双重因素的影响下,硬化剂用量与模型的弹性系数呈三次函数的关系。得到方程后,只要知道患者大动脉的弹性系数,就可以知道最佳的硬化剂使用量,得到的模型就更加准确。在第三部分验证实验中,由于主动脉弓部解剖结构复杂,不利于测量,且有时会出现模型漏水的情况,最终决定截取模型的降主动脉部分进行验证,最后的结果表明这种模型制作方法是可行的。
本研究15名患者最终均行主动脉腔内修复术,术后即刻成功率为100%。分析弹性模型有着刚性模型无法比拟的优势:(1)更好地服务于体外预开窗:3D打印模型辅助覆膜支架预开窗很多医院已经常规开展,但这些中心大多采用中空的刚性模型。在实际使用中,经常会发现输送系统无法顺利放入刚性模型内部,特别是动脉狭窄或主动脉弓严重扭曲的病例,且由于模型内部不是绝对光滑,可能会损伤支架的外膜,增加内漏风险,改用弹性模型就不存在这种问题。(2)提供更真实的体外实验:弹性模型可以很好地模拟真实的支架释放过程,因为其具有良好的扩张性特征,且解剖形状与患者本人相一致。(3)新技术的测试:在评估新器械或者新技术在人体的适用性方面,弹性模型有着独到的优势。它既不像动物模型那样与人体结构差距过大,也避免了直接应用于人体可能带来的伤害。
3D打印技术作为一个新型的工具,在血管外科中应用前景广阔。本研究介绍了一种新型的弹性动脉模型制作方法,该模型制作方法简单,费用低,旨在为广大临床医生提供一个新的血管实体模型制作方案,以便3D打印技术更好地为血管外科服务。

