高中生物疑难问题集萃
【疑问1】甲基绿和派若宁(吡罗红)染色的具体原理是什么?
Bracher于上个世纪40年代建立了甲绿-派若宁染色以来,一直是对比显示DNA和RNA分布的经典染色方法,广泛应用于教学、科研和临床诊断。
染色原理:甲绿(Methyl green甲基绿)和派若宁属于碱性染料且在水中电离后均为带正电荷的染料,甲绿带有两个正电荷,派若宁则带有一个正电荷。DNA和RNA都有磷酸基和碱基,为两性电解质,有一定的等电点。染色中两种染料通过竞争性作用分别与相应的核酸成分结合。
碱性较强的甲基绿与DNA反应(pH为3.8~4.2)使两个正电荷间的距离与DNA的磷酸基间的距离相当(见图),每个甲基绿分子中两个带正电荷的氮原子分别与DNA分子双链之中每条链的每一螺旋中的一个磷酸根相结合,这就是两者结合的基础[1]。甲基绿与DNA结合关键在于DNA分子的双螺旋空间构型的完整性,只要双螺旋构型略有改变,立即引起甲基绿与DNA的结合能力降低。
碱性较弱的派若宁与RNA结合(pH为4.6~5.2)也正好符合RNA的聚合度范围。也有人提出:甲绿-派若宁染色与DNA和RNA的聚合程度有关。甲绿对聚合程度高的DNA有较强的亲和力,而吡罗红对聚合程度低的RNA有亲和力。
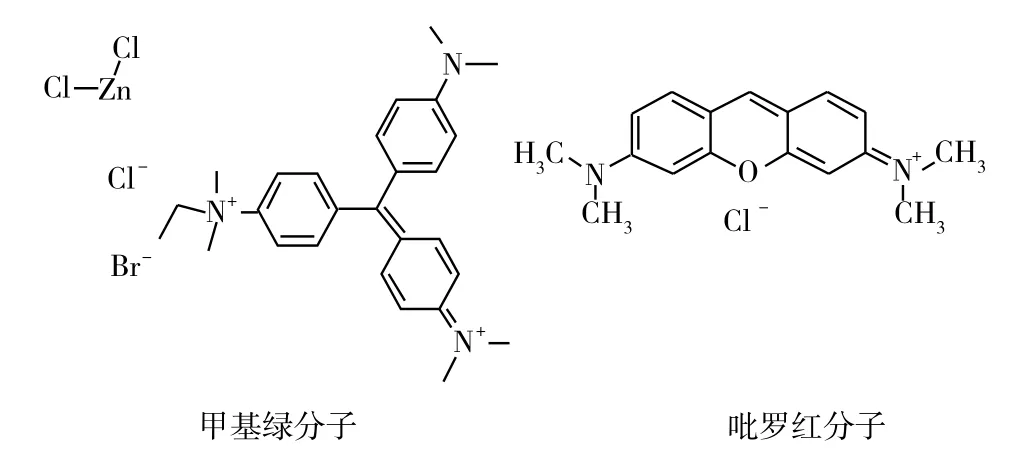
图 甲基绿和派若宁分子结构
【疑问2】甲基绿和吡罗红能不能单独使用以鉴定DNA和RNA呢?
教材中提到的甲基绿和吡罗红混合染色剂指的是A液20 mL(甲基绿和吡罗红水溶液)和B液80mL(醋酸缓冲液,pH=4.8的溶液)配制的混合染色液。教材中同时使用甲基绿和吡罗红混合染色剂的意图是将细胞染色,并可同时显示DNA和RNA在细胞中的分布,从而形成对比达到实验目的。
根据甲基绿和吡罗红染色原理可知,二者可以单独去鉴定、提纯DNA或RNA。若单独使用会分别将他们染成绿色或红色,但是无法显现出DNA和RNA在细胞中的分布情况。
【疑问3】为什么甲基绿和吡罗红混合染色剂为pH=4.8左右?
醋酸和醋酸钠缓冲液的pH约为4.8左右,在此pH条件下能够保持DNA分子的空间结构,稳定甲基绿和吡罗红染色剂的结合能力。若pH偏高或偏低均会对DNA和RNA的结构造成一定的破坏,从而对染色效果有一定的影响。
【疑问4】为何选用浓度为8%的盐酸?
根据人教版教材必修1第26页内容可知,盐酸的作用是加速染色剂进入细胞,同时使染色质中的DNA与蛋白质分离,有利于与染色剂结合。而教材中提出的染色液最佳pH约为4.8左右,盐酸浓度可能为本实验的关键影响因素,如:盐酸浓度过高,或者冲洗装片不彻底等因素均会导致pH低于4.8,从而影响观察的效果。
新疆师范大学生命科学院王佳等人做过相关的探究实验:不同盐酸浓度对细胞核染色效果的影响[2],相关内容见表:
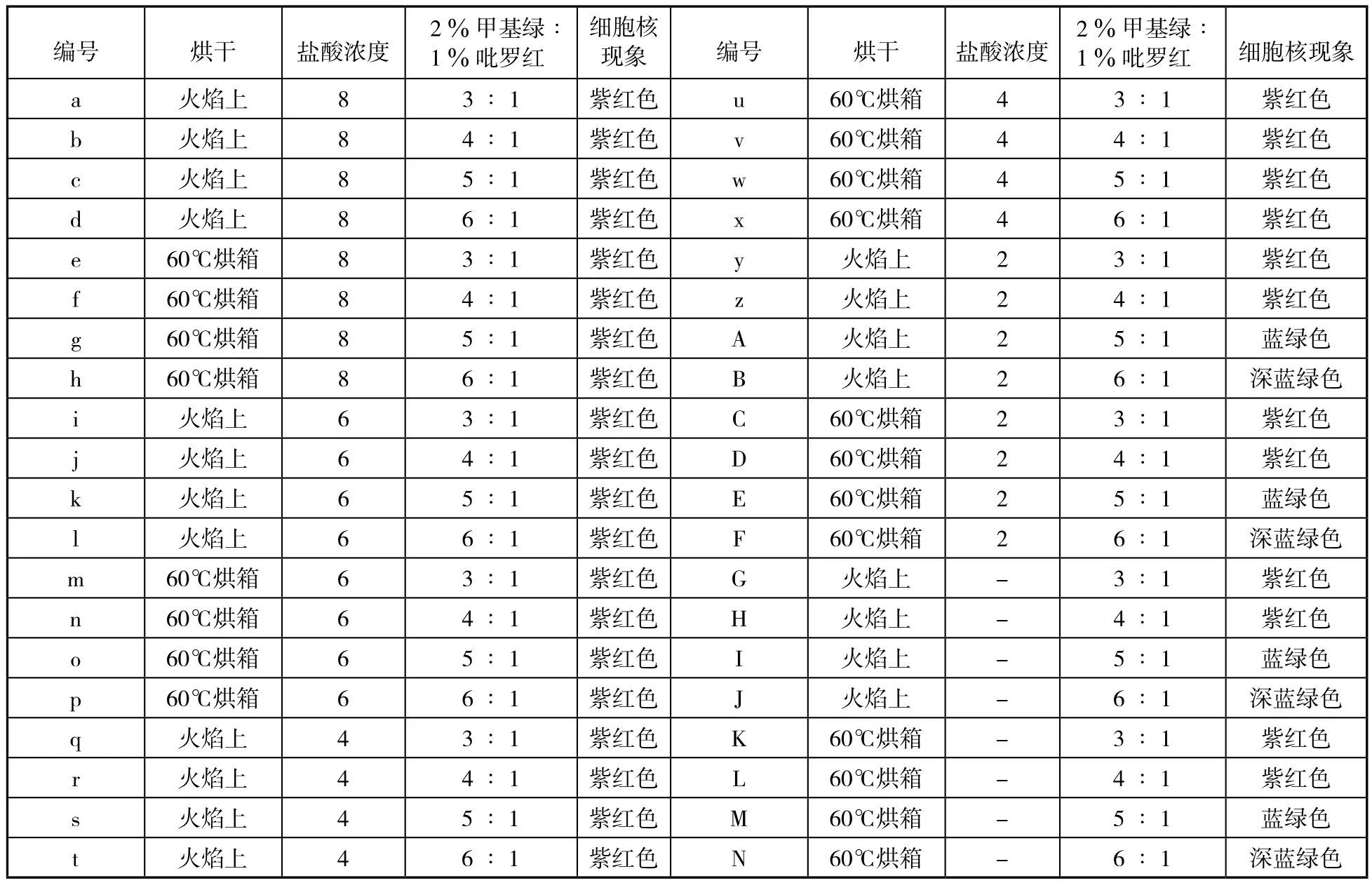
表 不同条件下人的口腔上皮细胞染色现象
通过上述实验结果可以看出,教材提出的8%的盐酸浓度染色效果不是最佳,反而是2%的盐酸浓度染色效果更好,可能的原因是8%的盐酸浓度使pH过低,导致DNA发生酸水解,同时北京第一中学的李鑫也做了此改进实验的探究[3]:在不使用盐酸水解,直接染色的条件下,实验效果也比较理想。

