清胰Ⅱ号汤剂HPLC指纹图谱研究
郑小翠,王 森,欧水平,陈 灵,蔡迎迎,任 丽
(1.遵义医科大学 药学院,贵州 遵义 563099;2.遵义医科大学附属医院 药剂科,贵州 遵义 563099)
急性胰腺炎(acute pancreatities,AP)是临床上常见的急腹症,具有较高的发病率和病死率,20% ~30%发展为重症急性胰腺炎(severe acute pancreatities,SAP)[1]。SAP病情凶险,常伴有全身炎症反应综合征及全身多器官功能不全。清胰Ⅱ号汤由大黄、赤芍、栀子、延胡索、丹皮、木香、厚朴及芒硝等 8 味药组成,具有疏肝利胆、清热泻火、止痛通便的功效,临床常用于治疗AP和SAP,疗效显著[2-3]。现代医学研究表明,清胰复方的作用机制是多方面的,能抑制胰酶释放及其活性,增加肠蠕动;短期内促进肠排空,减轻胃肠压力及腹压;改善胃肠道功能和毛细血管通透性;还可以阻断炎症因子释放,减少炎症因子对患者胰腺等器官的损害;防止细菌移位;清除氧自由基,防止过氧化损伤等[4-6]。
目前,对于清胰Ⅱ号汤剂的质量控制研究多体现在单一有效成分或几个主要有效成分如栀子苷、芍药苷、丹皮酚、大黄素等的HPLC含量测定[7-8],而对1种或几种指标成分的控制对于中药本身多组分、多靶点作用特点而言,不能全面反映中药复方制剂有效成分总体特征及其内在的质量特征,从而不能对其整体质量进行控制。采用指纹图谱方法可以弥补这些缺点,现在指纹图谱技术和研究方法已经相对成熟完善,利用指纹图谱技术来控制中药的质量已经得到了国际的认可[9-11]。因此,为了更有效地、系统地控制清胰Ⅱ号汤剂的质量,本研究采用HPLC建立清胰Ⅱ号汤剂的指纹图谱,对其中的特征性成分进行指认,并将清胰Ⅱ号汤剂的指纹图谱与组方单味药材的指纹谱图进行比对,以获得专属、整体的综合特征信息。
1 材料与方法
1.1 仪器 1260型液相色谱仪,包括DAD检测器(美国Agilent公司);BT125D电子天平(德国Sartorius公司);JA1002电子天平(上海浦春计量仪器有限公司);Exceed-Cd-20 型实验室超纯水机(成都艾科水处理设备有限公司);DL-820D超声仪(上海之信仪器有限公司);TD5A-WS离心机(上海卢湘仪离心机仪器有限公司)。2012版 “中药指纹图谱相似度评价系统”软件。
1.2 试药 大黄素、大黄酸、丹皮酚(购自中国食品药品检定研究院,批号分别为110756-201512、110757-201607、110708-201407 ),芦荟大黄素、大黄酚、大黄素甲醚、栀子苷、芍药苷、延胡索乙素、厚朴酚、和厚朴酚、木香烃内酯、去氢木香烃内酯(购自成都曼思特生物科技有限公司,批号分别为MUST-17030605、MUST-17030603、MUST-17030622、MUST-17020401、MUST-16041901、MUST-17022720、MUST-17031102、MUST-17020205、MUST-16050705、MUST-16041601),9批清胰Ⅱ号汤剂(遵义医科大学附属医院药剂科代煎,依次标记S1~S9)。
大黄(产地四川,批号160301-170401)、赤芍(产地四川,批号160601-170401)、炒栀子(产地四川,批号160301-170401)、丹皮(产地四川,批号160601-170601)、姜厚朴(产地四川,批号(160701-170601)、醋延胡索(产地浙江,批号160801-170701)、木香(产地云南,批号160301-161101)、芒硝(产地青海,批号20160302-20161109)均购自重庆慧远药业有限公司,经遵义医科大学杨建文主任药师鉴定以上中药饮片均合格。甲醇、乙腈为色谱纯,水为蒸馏水,其余试剂均为分析纯。
1.3 方法
1.3.1 色谱条件 Ultimate LP-C18色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱程序:0~10 min,2%~10% A;10~100 min,10%~30% A;100~130 min,30%~55% A;130~150 min,55%~85% A;柱温:30℃;流速:1 mL/min,检测波长:237 nm,进样量10 μL。
1.3.2 对照品溶液的制备 精密称取芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品4.94、4.90、4.83、4.71、5.29 mg,加少量氯仿使之溶解,加甲醇定容至5 mL,精密称取栀子苷、芍药苷、丹皮酚、和厚朴酚、厚朴酚、木香烃内酯、去氢木香烃内酯、延胡索乙素对照品5.03、4.95、5.06 、5.11、5.14、5.15、5.16、5.21 mg,加甲醇溶解分别定容至5 mL,得单个对照品储备液。
分别精密量取上述单个对照品溶液150、150、35、120、100、40、50、230、230、470、90、90、90 μL,加甲醇稀释至5 mL,得栀子苷、芍药苷、丹皮酚、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚、和厚朴酚、厚朴酚、木香烃内酯、去氢木香烃内酯、延胡索乙素的含量分别为94.63、45.56、46.57、6.92、23.53、19.30、7.54、10.58、30.93、30.99、18.41、18.52、18.74 μg/mL的混合对照品溶液。
1.3.3 供试品溶液的制备 取9剂清胰Ⅱ号处方,加适量水煎煮3次,合并煎液,浓缩成2 000 mL,得9批清胰Ⅱ号汤剂[12]。精密量取清胰Ⅱ号汤剂5 mL于50 mL离心管中,加入甲醇25 mL,称定重量,超声处理30 min,放冷,甲醇补足减少的重量,3 500 rpm 离心10 min,取全部上清于蒸发皿中挥干,残渣加甲醇溶解并定容至5 mL ,摇匀,0.22 μm滤膜滤过,即得。
1.3.4 单味药材供试品溶液的制备 按清胰Ⅱ号汤剂制备方法分别制得大黄、赤芍、木香、丹皮、厚朴、栀子、延胡索单味药材提取液。按1.3.3项下方法制备单味药材供试品溶液,0.22 μm微孔滤膜滤过,即得。
1.3.5 样品的测定 取混合对照品溶液、单味药材供试品溶液及9批清胰Ⅱ号汤剂供试品溶液,按1.3.1项下色谱条件,分别进样分析,记录色谱图。
2 结果
2.1 精密度试验 取同一供试品溶液,重复进样 6 次,测得 HPLC 图,以栀子苷成分的保留时间和峰面积为参照,计算各共有峰的相对保留时间和相对峰面积,结果表明各共有峰的相对保留时间RSD为0.10%~0.37%,相对峰面积 RSD为0.51%~9.33%,表明仪器精密度良好。
2.2 重复性试验 制备同一批号供试品溶液 6份,进样测定,结果表明各共有峰的相对保留时间RSD为0.03%~1.63%,相对峰面积 RSD为0.71%~7.95%,表明供试品处理方法重现性良好。
2.3 稳定性试验 同一供试品溶液,分别在 0、3、6、 9、 12、 24、36 h进样测定,结果表明各共有峰的相对保留时间RSD为0.02%~0.84%,相对峰面积 RSD为0.86%~8.34%,表明供试品溶液在36 h内稳定。
2.4 指纹图谱的建立
2.4.1 参照峰的选择 在HPLC图谱中26.173 min的色谱峰的峰面积最大且稳定,经与对照品对照鉴定为栀子苷,故选择其为参照峰 (见图1和图2)。
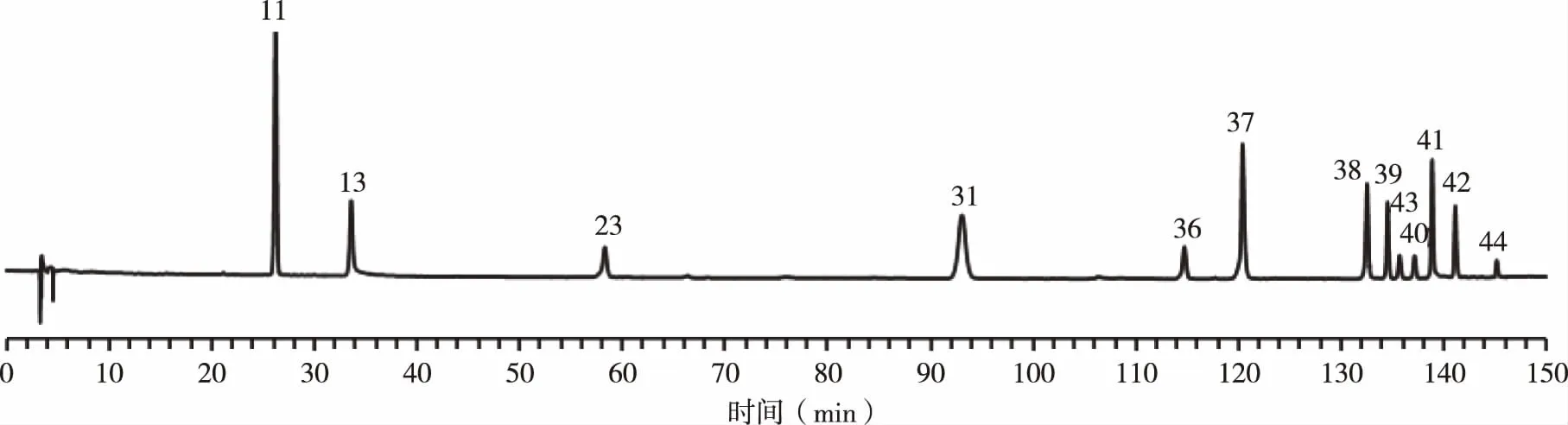
图1 混合对照品色谱图

图2 9批清胰Ⅱ号汤HPLC 特征谱图(S1~ S9)和对照指纹图谱(R)
2.4.2 相似度分析 将9批清胰Ⅱ号汤的HPLC图谱导入“中药指纹图谱相似度评价系统(2012版)”软件,以S1为参照图谱,多点校正后自动匹配,生成对照图谱(R),结果见图2。计算指纹图谱和对照图谱的相似度,结果见表1,可见9批样品相似度均在0.9以上,表明各批样品与对照指纹图谱有良好的相似性。对共有峰进行编号,以11号色谱峰(栀子苷)为参照峰,其保留时间和峰面积为1,计算其他各共有峰的平均相对保留时间和平均相对峰面积,其结果见表2。
表1 9批清胰Ⅱ号汤相似度结果

批号S1S2S3S4S5S6S7S8S9RS11.0000.9930.9471.0001.0000.9960.9990.9980.9240.998S20.9931.0000.9570.9950.9930.9900.9940.9910.9360.997S30.9470.9571.0000.9480.9460.9210.9460.9300.9970.963S41.0000.9950.9481.0001.0000.9960.9990.9980.9260.999S51.0000.9930.9461.0001.0000.9960.9990.9980.9230.998S60.9960.9900.9210.9960.9961.0000.9970.9990.8920.991S70.9990.9940.9460.9990.9990.9971.0000.9990.9220.998S80.9980.9910.9300.9980.9980.9990.9991.0000.9030.994S90.9240.9360.9970.9260.9230.8920.9220.9031.0000.943R0.9980.9970.9630.9990.9980.9910.9980.9940.9431.000
表2共有峰平均相对保留时间和相对峰面积

峰号平均相对保留时间RSD(%)平均相对峰面积RSD(%)峰号平均相对保留时间RSD(%)平均相对峰面积RSD(%)10.362 0.780.13012.97222.174 0.260.01618.4120.477 0.260.0119.24232.230 0.490.02410.0830.533 0.210.03317.59242.318 0.820.01721.7040.565 0.200.03517.99252.451 0.260.02728.4550.586 0.180.0097.12262.665 0.440.00916.1860.598 0.220.0108.94272.867 0.260.00614.8370.609 0.440.01113.53283.197 0.260.03918.4880.681 0.230.0235.76293.233 0.250.01012.8990.791 0.330.04713.00303.316 0.270.04915.28100.808 0.240.05616.63313.560 0.280.04656.98111.001 0.231.0000.00323.667 0.270.0543.71121.140 0.260.2389.46333.774 0.270.00619.81131.281 0.290.8169.57343.877 0.270.01426.84141.485 0.300.01126.89354.249 0.280.00417.13151.675 0.320.01613.63364.389 0.390.01427.32161.711 0.300.04610.93374.609 0.260.03117.33171.799 0.381.49028.10385.070 0.270.00314.43181.915 0.290.04310.63395.146 0.280.01626.48191.947 0.240.0379.70405.245 0.280.00330.90202.042 0.250.0159.19415.310 0.280.03730.20212.117 0.390.03225.48425.3960.280.00623.94
2.4.3 共有峰归属分析 取单味药汤剂和清胰Ⅱ号汤剂供试品溶液进行测定,得色谱图(见图3)。通过保留时间和紫外吸收光谱图比对,结果发现,清胰Ⅱ号汤的共有峰中2、3、4、5、6、7、10、11、15 、19、20、25、26、27、35 号峰来源于栀子,12 号来源于赤芍,共有峰 16、18 、24、28、29、30、33、34、37、38、42 号来源于大黄,23号来源于延胡索,31 号来源于丹皮,36、39、41 号来源于厚朴,40 号来源于木香,1号来源于栀子和赤芍,8、22号来源于栀子和大黄,9号来源于丹皮、木香和厚朴,14号来源于丹皮、大黄和厚朴,13、17、21、32号来源于赤芍和丹皮。经鉴定 11、13、23、31、36、37、38、39、40、41、42号峰分别为栀子苷、芍药苷、延胡索乙素、丹皮酚、芦荟大黄素、大黄酸、大黄素、和厚朴酚、去氢木香烃内酯、厚朴 酚、大黄酚,芒硝对共有峰没有贡献。
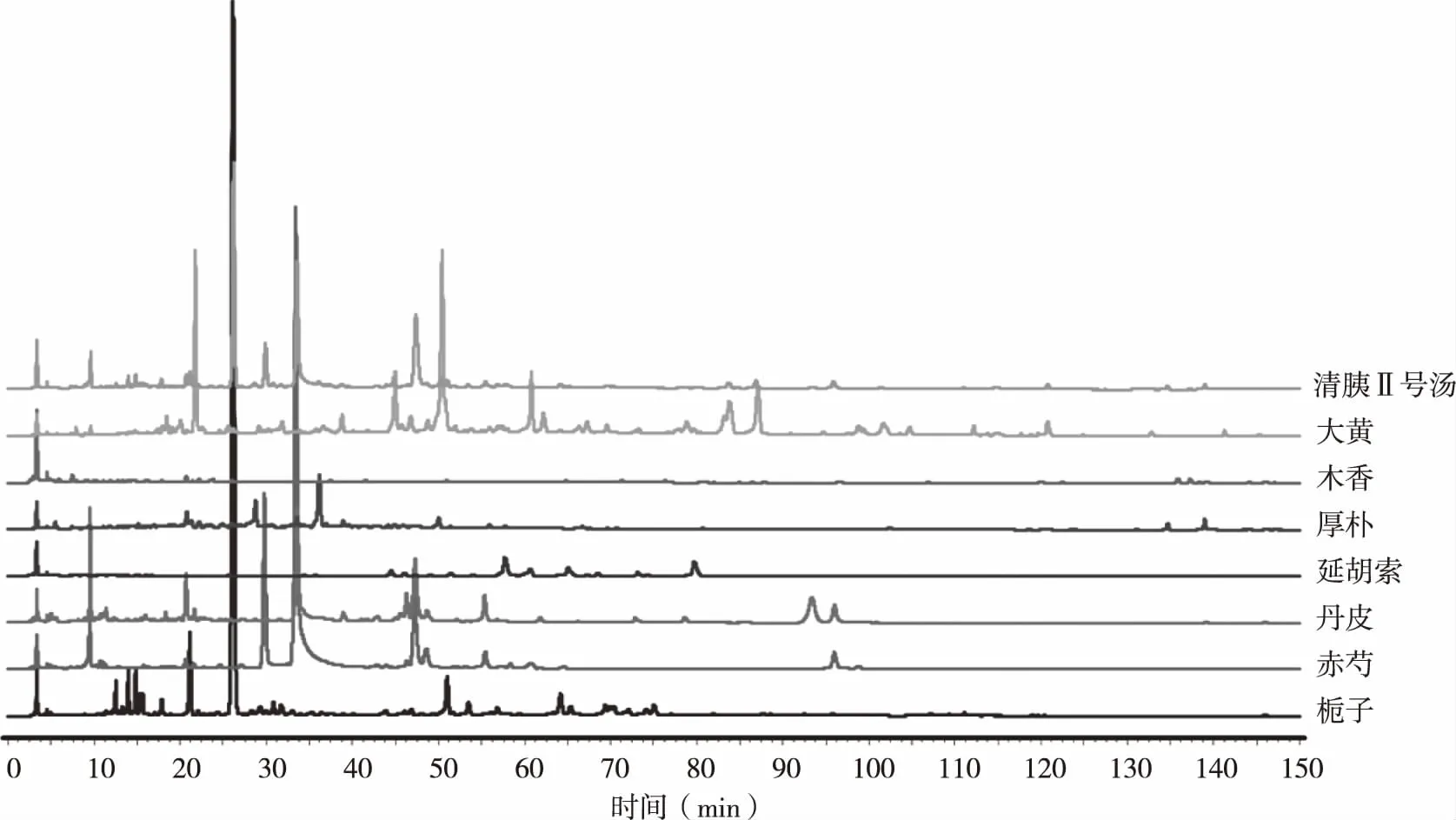
图3 清胰Ⅱ号汤和各单味药材的HPLC图谱
3 讨论
本实验采用 DAD检测器在220~400 nm范围进行全波长扫描,考察了220、230、254、280、300、400 nm 等波长,结果发现,波长大于280 nm后栀子苷无紫外吸收,经比较后237 nm下色谱峰最为丰富,各色谱峰之间分离度良好,强度较大且均匀,基线平稳,因此选择 237 nm 为最佳检测波长。在研究中发现,供式品溶液中的成分在 150 min 之前出峰完全,150 min 之后无色谱峰的出现,因此检测时间定为150 min。
对9批清胰Ⅱ号汤剂 HPLC 图谱进行匹配,标定了42个共有峰,并通过与对照品、单味药汤的保留时间和紫外光谱图比对,对所有共有峰进行了组方药味归属分析,指认了其中11个成分。9批样品在对照品木香烃内酯的出峰位置(43号峰)均未出峰,单味药材在相同位置有出峰。刘俊红等[13]分别考察了60、80、100 ℃加热不同时间对木香水提液中木香烃内酯和去氢木香内酯的影响,结果表明3个温度下两者含量均降低,随着温度的升高,时间的延长,木香烃内酯含量显著降低,而去氢木香内酯略有降低;在同一时间内, 温度变化影响显著,尤其在 100 ℃,加热 1 h后木香烃内酯的含量几乎损失殆尽 。清胰Ⅱ号汤剂为医院制备,单次煎煮需近300 L水,煎煮时间虽相同,相比实验室制备单味药材,单次提取仅100 mL水,水达到沸腾状态所需时间更长,且使用100℃加热浓缩,长时间高温加热使样品汤剂中木香烃内酯损失殆尽,而去氢木香内酯受温度影响较小,所以还能检出。有4批样品在大黄素甲醚的出峰位置(44号峰)未出峰,究其原因,可能是由于不同批次大黄的质量差异造成的;大黄药材中大黄素甲醚的含量本身较其他4种蒽醌类成分低,而大黄-赤芍、大黄-栀子、大黄-木香同煎煮会降低游离型与结合型大黄素甲醚的量[14],导致有的批次大黄素甲醚含量低于检测限;蒽醌类成分不稳定,在煎煮浓缩过程中受温度影响易分解;因此未纳入共有峰中。
相似度评价结果表明,9批样品的指纹图谱相似度较高,相对保留时间 RSD 均在 1% 以内,相对峰面积RSD为3.71%~30.90% ,丹皮酚的相对峰面积RSD 56.98%,这可能由于不同批次药材来源和质量不同,煎煮浓缩过程使用的是敞口锅,温度不易控制,而丹皮酚属挥发油,易挥发,增加丹皮酚损失差异,造成9批样品中丹皮酚相对峰面积差异较大。提示需进一步控制药材的质量及确保煎煮浓缩时间、温度等条件相同。
本实验建立的HPLC方法准确、可靠,对清胰Ⅱ号汤剂中的化学成分进行相关性研究,并对部分色谱峰予以归属。可选择栀子苷、芍药苷、延胡索乙素、丹皮酚、芦荟大黄素、大黄酸、大黄素、和厚朴酚、去氢木香烃内酯、厚朴酚、大黄酚对照品标定的11个共有峰作为清胰Ⅱ号汤剂指纹图谱的质控指标。存在不能定量且分析时间长的不足,已报道文献[7-8]只测定了复方中单个或几个成分,本实验选择11个质控指标更全面,且指纹图谱全峰能全面反应全方成分;可为其质量控制提供一定参考。

