微生物检验质量的影响因素与病原菌耐药性研究
陈惠
(中国医科大学附属盛京医院大连医院 辽宁大连 116600)
1 前言
微生物检验结果影响因素较多,对检验结果影响因素进行详细分析,给予对应质量干预,提高微生物检验操作的效率与质量。选取本院出具的微生物检验报告103例,对检验内容加以分析。
2 资料与方法
2.1 一般资料
选取2017年9月—2018年12月130名受检者的微生物检验报告103例,其中,男53例,女50例,年龄 20~60 岁,平均年龄(43.62±3.98)岁。所选检验报告满足本研究相关条件,符合操作指征[1],病例收集工作通过医学伦理委员审查。
排除标准[2,3]:(1)合并免疫系统、造血系统、恶性肿瘤等严重疾病者;(2)妊娠及哺乳期妇女;(3)治(诊)疗依从性比较高(低)者。
2.2 研究方法
检验方法如下:(1)菌株来源:对本组患者所分离出来的病原菌进行收集,剔除来自同一个患者同一个部位的菌株。(2)细菌培养:严格遵守《全国临床检验操作规程》中相关标准及检验要求。麦康凯、血琼脂、哥伦比亚血琼脂、嗜血杆菌巧克力琼脂等培养基购自国内某梅里埃(上海)生物制品有限公司,菌株鉴定则采用美国BD(DADE BEHRING)公司所提供的细菌鉴定装置 (型号:PhoenixTM-100(MicroScan autoSCAN4))。(3)药敏试验:采用上述细菌鉴定/药敏监测装置,判定所有菌株的药敏试验结果,根据美国临床和实验室标准协会(CLSI)标准折点,对药敏结果进行判断。
2.3 评价指标
统计检验正确及误差情况。总结发生误差的原因,分析微生物检验质量的影响因素。对送检标本的细菌培养结果进行分析,统计每种细菌所占比例,并在典型菌株耐药率占前3位的抗菌药物。
3 结果
3.1 检验结果分析
103例患者中,检验结果准确88例(85.44%),15例患者检验结果出现误差,误差率为14.56%。
3.2 影响因素分析
对检验误差原因进行分析,其中,人员因素导致的误差8例,标本因素4例,操作因素3例,所占比例分别为53.33%、26.67%、20.00%,见表1。

表1 检验误差的原因分析
3.3 细菌培养结果
103例患者送检标本中,共培养出134株病原菌,其中,革兰阴性菌89株,革兰阳性菌40株,真菌5株,所占比例分别为66.42%、29.85%、3.73%,见表2。

表2 细菌培养结果分析
3.4 典型菌株耐药性
革兰氏阴性杆菌以大肠埃希菌为主,耐药性前3位的抗菌药物为哌拉西林(复方新诺明)、头孢呋辛(环丙沙星)、环丙沙星(左氧氟沙星);革兰氏阳性细菌以金黄葡萄球菌为主,其耐药性前3位的抗菌药物为青霉毒、红霉素、克拉霉素,见表3。
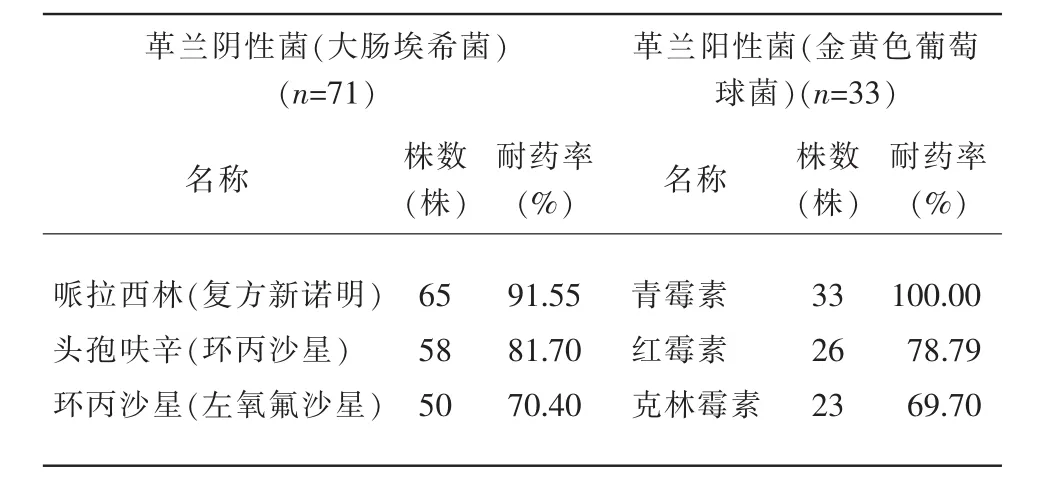
表3 典型菌株耐药性情况
4 讨论
微生物检验是目前诊断感染性疾病的主要方法之一,其检验结果准确,结合检验结果,可为患者治疗及用药提供准确指导。但是由于病原菌种类多,加之微生物检验流程复杂,若不能对多种影响检验结果的因素进行合理控制,则会直接干扰检验结果[4]。通过本研究发现,15例检验结果误差中,人员因素8例,标本因素4例,操作因素3例,提示应不断提高检验人员专业技术水平,加强标本送检的指导。
微生物检验是诊断多种感染性疾病的主要方法,根据细菌水平,为医院诊疗工作提供更多科学指导。要实现良好的检验质量管理,前提在于保证微生物检验检测质量。影响微生物检验质量的因素比较多,因此,应在开展微生物检验时严格把关每个环节,采取必要措施,最大程度保证检验结果的正确性。通过研究发现,出现质量问题的主要原因在于工作人员缺乏高度的责任心,没有深刻意识到工作失误的严重危害。因此,定期对检验人员开展技能考核,合格者方能上岗工作。开展细节管理,要求所有检验人员在积极学习的同时,进一步从细节处着手,不断规范工作行为,降低检验操作失误现象。
标本送检原因,临床医护和患者对标本的送检要求不明确或没在意,没有意识到不合格标本的送检导致的严重错误。据统计,检验结果误差中70%~80%来自实验前、分析前,而且实验前(分析前)误差是仪器、试剂、质控品和标准品等再好也无法弥补的。因此,保证实验前质量对减少实验误差尤为重要,并且非常有必要定期对临床医护人员、患者开展标本送检相关培训。
与此同时,103例送检标本分离出134株病原菌,革兰阴性菌89株,革兰阳性菌40株,真菌5株。其中,革兰阴性菌以大肠埃希菌为主,耐药性前3位的抗菌药物为哌拉西林、头孢呋辛、环丙沙星;革兰阳性菌金黄葡萄球菌为主,其耐药性前3位的抗菌药物为青霉毒、红霉素、克拉霉素,与文献报道结果基本相同。
通过上述分析认为,微生物检验结果影响因素多,结合影响因素,不断完善检验操作流程,可提高检验质量,提供更多、更准确的参考依据,从而降低用药风险。

