动态调强子野优化技术在胸上段食管癌治疗中的应用研究*
张武哲 黄宝添 翟田田 彭 逊*
目前,调强放射治疗(intensity modulated radiation therapy,IMRT)已成为胸上段食管癌的主要治疗手段,其剂量学优势明显,能提高肿瘤控制率,减少危及器官和正常组织损伤,但是实际治疗时间较长可能导致相对生物效应降低,亦增加了治疗中不确定因素的影响[1-4]。容积旋转调强(volume modulated arc therapy,VMAT)是IMRT技术的延伸,利用可变的机架旋转速度、多叶光栅(multi-leaf collimator, MLC)运动速率和动态剂量率来调制强度,高效的实现剂量投递。相对IMRT技术,VMAT能够明显减少机器跳数(monitor units,MUs),缩短治疗时间(treatment time,TT)[5]。但是由于VMAT是全周连续照射,势必导致低剂量照射区域的增多,这对于肺部低剂量受照区域的损伤不容忽视[6-9]。
动态调强(dynamic MLC-IMRT)是在射线照射时多叶准直器叶片处于运动状态,利用多叶准直器相对应的每对叶片在射线照射时在计算机控制下对靶区进行扫描以实现对射野强度的调节。由于节省了叶片运动时间,所以动态调强比静态调强的治疗时间更短,提高了治疗效率。
然而,Eclipse系统在Truebeam直线加速器的动态调强中每个射野的默认子野数目是166个(64~320),理论上,减少每个射野的子野数目即减少了叶片的运动轨迹,应该能缩短治疗时间,但子野数目的减少是否能够满足射野强度的调节,是否会导致计划质量的下降,目前国内外在胸上段食管癌方面尚无相关研究。因此,本研究尝试在保证不降低计划质量的提前下,寻求满足射野调控要求的最少子野数目的治疗计划,以达到尽可能的缩短治疗时间,提高治疗精度,使胸上段食管癌患者获益。
1 资料与方法
1.1 一般资料
选取2017年1-8月汕头大学医学院附属肿瘤医院治疗的30例胸上段食管癌患者,其中男性18例,女性12例;年龄43~68,平均年龄(51±2)岁。所有患者均为首程放射治疗,其中病灶下缘位于胸7和胸6椎体水平者分别为3例和8例,位于胸5、胸4和胸3椎体水平者分别为8例、5例和6例。
1.2 仪器设备
采用Briliance CT Big Bore型大孔径CT(荷兰飞利浦公司)。
1.3 放射治疗定位
患者取仰卧位,双臂自然下垂至身体两侧,头颈肩网罩固定体位。采用大孔径CT机进行定位扫描,层厚及层间距均为5 mm。范围包括整个病灶,其上界至少包括下半颈,下界包括双肺下缘。获取的CT图像通过DICOM 3.0传输到Eclipse(Version 10.0)治疗计划系统。
1.4 靶区定义
大体肿瘤区(gross tumor volume,GTV)包括食管肿瘤病灶和食管旁肿大淋巴结。临床肿瘤区(clinical tumor volume,CTV)包括高危临床肿瘤区CTV1和低危临床肿瘤区CTV2;CTV1轴向在GTV外扩5~10 mm,纵向包括GTV外20 mm食管及食管旁组织,不包括区域淋巴结;CTV2在CTV1基础上加上纵膈淋巴引流1区和2区,以及双侧锁骨上区。计划靶区(planning target volume,PTV)在各CTV基础上三维外扩5 mm生成PTV1(64 Gy)、PTV2(54 Gy);需勾画的危及器官包括双肺、脊髓、脊髓计划区和心脏。脊髓计划区由脊髓三维外扩5 mm生成。
1.5 计划设计
应用TrueBeam直线加速器,X射线照射能量为6 MV,Eclipse系统进行计划设计。动态调强共面5野照射,机架角度为210o、300o、0o、60o以及150o。用95%靶区体积获得100%处方剂量进行归一,PTV1(64)64 Gy/32次,PTV2(54)54 Gy/32次。危及器官剂量限制:脊髓计划区Dmax<45 Gy,脊髓Dmax<40 Gy,肺V20≤25%、V30≤20%;采用剂量体积优化(dose volume optimizer,DVO)算法,最终剂量计算采用各向异性分析算法(anisotropic analytical algorithm,AAA),计算网格为2.5 mm。在射野角度、处方剂量、优化条件等全部不变的情况下,初步制定下列计划。
(1)基底剂量计划(base dose plan,BDP)。
(2)最佳剂量计划(top dose plan,TDP):将BDP的处方分割数改为16次,单次处方剂量不变;复制更改分割数后的BDP,利用优化程序中的base dose plan功能将更改分割数后的BDP引入并关联,进而继续优化,计算最终剂量结果后再将处方分割数重置为32次,单次处方剂量仍保持不变,得到基于基准剂量补偿的TDP。
(3)利用计算叶片运动(leaf motion calculator,LMC)功能,依据得到的TDP的子野数目,将其分为G1组(64个)、G2组(115个)和G3组(166个)3组再行剂量计算。
1.6 评估指标
适型指数(conformity index,CI)为公式1:
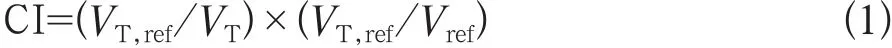
式中参考取值VT为靶区体积,VT,ref为处方剂量等剂量线所包绕的靶区体积,Vref为处方剂量等剂量线所包绕的体积。CI取值在0~1,越接近1表明靶区适型度越好。

剂量均匀性指数(heterogeneity index,HI)为公式2:式中D2近似最高剂量,D98近似最低剂量,D50中位剂量。HI值越小表明其剂量均匀性越好。其他参数:最高剂量(Dmax)、平均剂量(Dmean)、剂量体积参数(Vx)、MU以及TT。
1.7 统计学方法
运用SPSS 19.0软件进行统计学分析,正态分布的数据以(±s)表示,采用配对t检验比较各组参数的差异,以P<0.05为差异有统计学意义。
2 结果
2.1 靶区剂量参数比较
(1)PTV1(64 Gy):G2组与G3组靶区CI比G1组高[CIG1(0.924±0.011)<CIG2(0.925±0.011)<CIG3(0.926±0.011)],HI略低[HIG1(0.053±0.005)>HIG2(0.052±0.005)>HIG3(0.049±0.009)];相对于G1组,G2组的Dmax、Dmean、D2、D50略低,D98略高;G3组的Dmean、D2、D50略低,D98略高。
表1 三组不同子野计划靶区的剂量学参数比较(Gy,±s)
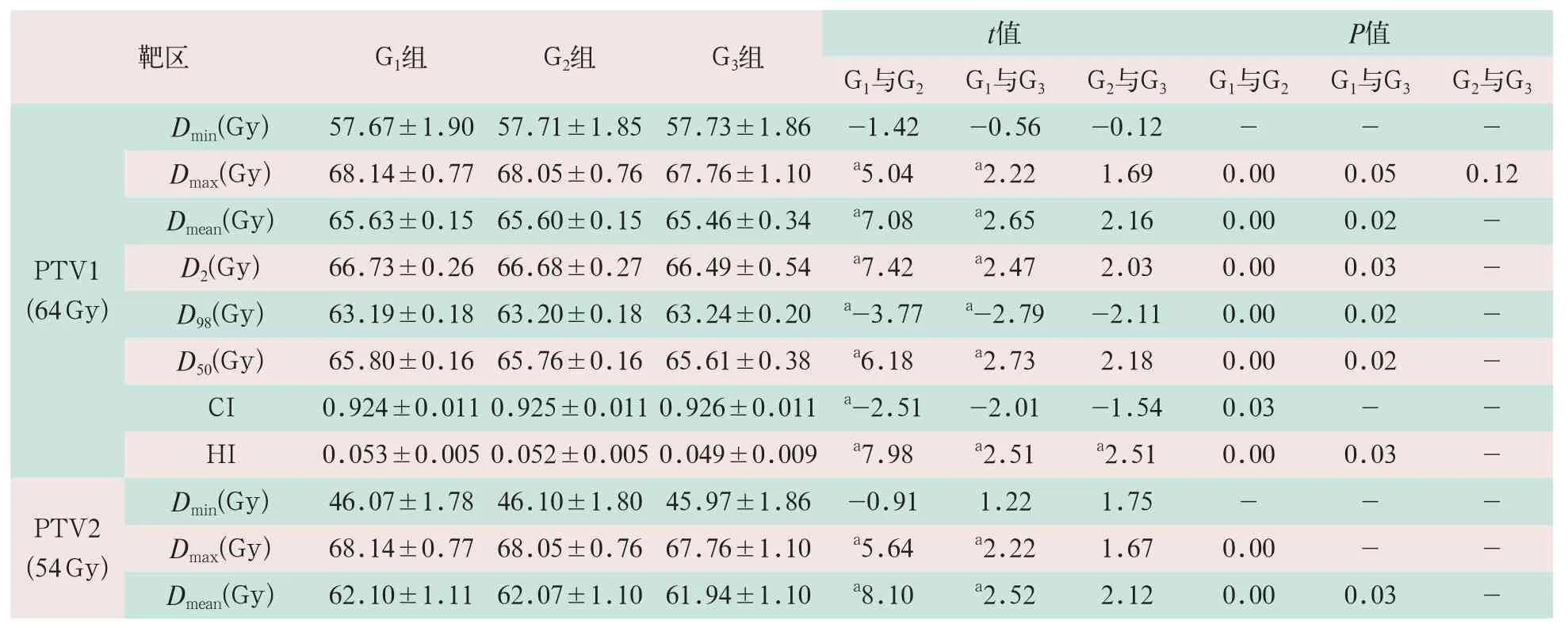
表1 三组不同子野计划靶区的剂量学参数比较(Gy,±s)
注:表中a为与G1组比较,t=-3.77~8.10,P<0.05; b为与G2组比较,t=2.18,P<0.05。
靶区 G1组 G2组 G3组 t值 P值G1与G2 G1与G3 G2与G3 G1与G2 G1与G3 G2与G3 PTV1(64 Gy)PTV2(54 Gy)Dmin(Gy) 57.67±1.9057.71±1.8557.73±1.86 -1.42 -0.56 -0.12 - - -Dmax(Gy) 68.14±0.77 68.05±0.76 67.76±1.10 a5.04 a2.22 1.69 0.00 0.05 0.12 Dmean(Gy) 65.63±0.15 65.60±0.15 65.46±0.34 a7.08 a2.65 2.16 0.00 0.02 -D2(Gy) 66.73±0.26 66.68±0.27 66.49±0.54 a7.42 a2.47 2.03 0.00 0.03 -D98(Gy) 63.19±0.18 63.20±0.18 63.24±0.20 a-3.77 a-2.79 -2.11 0.00 0.02 -D50(Gy) 65.80±0.16 65.76±0.16 65.61±0.38 a6.18 a2.73 2.18 0.00 0.02 -CI 0.924±0.011 0.925±0.011 0.926±0.011 a-2.51 -2.01 -1.54 0.03 - -HI 0.053±0.005 0.052±0.005 0.049±0.009 a7.98 a2.51 a2.51 0.00 0.03 -Dmin(Gy) 46.07±1.7846.10±1.8045.97±1.86 -0.91 1.22 1.75 - - -Dmax(Gy) 68.14±0.77 68.05±0.76 67.76±1.10 a5.64 a2.22 1.67 0.00 - -Dmean(Gy) 62.10±1.11 62.07±1.10 61.94±1.10 a8.10 a2.52 2.12 0.00 0.03 -
表2 三组不同子野计划危及器官的剂量学参数比较(Gy,±s)
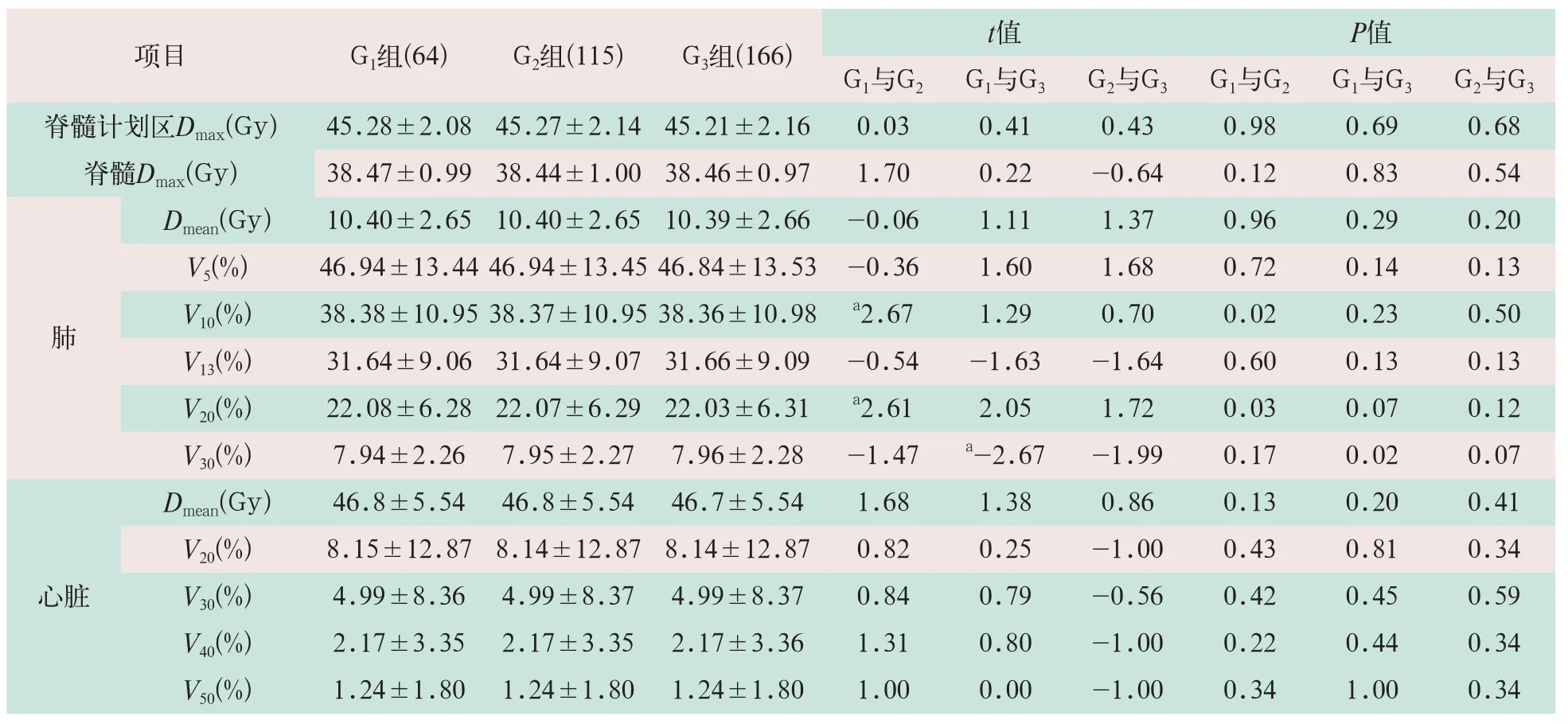
表2 三组不同子野计划危及器官的剂量学参数比较(Gy,±s)
注:与G1组比较,at=-2.67~2.67,P<0.05。
项目 G1组(64) G2组(115) G3组(166) t值 P值G1与G2 G1与G3 G2与G3 G1与G2 G1与G3 G2与G3脊髓计划区Dmax(Gy) 45.28±2.08 45.27±2.14 45.21±2.16 0.03 0.41 0.43 0.98 0.69 0.68脊髓Dmax(Gy) 38.47±0.99 38.44±1.00 38.46±0.97 1.70 0.22 -0.64 0.12 0.83 0.54肺心脏Dmean(Gy) 10.40±2.65 10.40±2.65 10.39±2.66 -0.06 1.11 1.37 0.96 0.29 0.20 V5(%) 46.94±13.44 46.94±13.45 46.84±13.53 -0.36 1.60 1.68 0.72 0.14 0.13 V10(%) 38.38±10.95 38.37±10.95 38.36±10.98 a2.67 1.29 0.70 0.02 0.23 0.50 V13(%) 31.64±9.06 31.64±9.07 31.66±9.09 -0.54 -1.63 -1.64 0.60 0.13 0.13 V20(%) 22.08±6.28 22.07±6.29 22.03±6.31 a2.61 2.05 1.72 0.03 0.07 0.12 V30(%) 7.94±2.26 7.95±2.27 7.96±2.28 -1.47 a-2.67 -1.99 0.17 0.02 0.07 Dmean(Gy) 46.8±5.54 46.8±5.54 46.7±5.54 1.68 1.38 0.86 0.13 0.20 0.41 V20(%) 8.15±12.87 8.14±12.87 8.14±12.87 0.82 0.25 -1.00 0.43 0.81 0.34 V30(%) 4.99±8.36 4.99±8.37 4.99±8.37 0.84 0.79 -0.56 0.42 0.45 0.59 V40(%) 2.17±3.35 2.17±3.35 2.17±3.36 1.31 0.80 -1.00 0.22 0.44 0.34 V50(%) 1.24±1.80 1.24±1.80 1.24±1.80 1.00 0.00 -1.00 0.34 1.00 0.34
(2)PTV2(54 Gy):G2组的Dmin比G3组覆盖更好,G1组除了Dmean略高于G3组之外,其Dmax均高于其他两组。见表1。
2.2 危及器官剂量参数比较
脊髓计划区、脊髓和心脏均在剂量限值之内,且组间差异无统计学意义。G1组的双肺V10、V20高于G2组,差异有统计学意义;V30则比G3组低,差异有统计学意义,见表2。
2.3 其他参数比较
在MU和TT参数中,G2组MU为(652±48),G3组为(670±56),分别较G1组(648±48)增加了0.6%、3.4%,其差异有统计学意义(t=-2.48,t=-3.08;P<0.05)。G2组的TT为(176±13)s,G3组为(184±15)s,分别较G1组(175±13)s增加了0.6%和5.1%,其差异有统计学意义(t=-4.28,t=-4.81,P<0.05)。
3 讨论
放射治疗的主流技术是逆向调强,其主要目标是最大程度提高靶区照射剂量的同时最大限度地保护危及器官,但调强技术的不足之处是治疗时间较长,可能增加患者治疗时移动的可能性,使治疗依从性下降,分次内治疗时间相对的延长,对肿瘤细胞损伤的生物学效应也可能随之下降[10]。子野数目的减少,治疗时间的缩短对于减少移动误差和提高治疗效率有积极意义。
通过30例研究计划可见,3组计划均能满足临床剂量学要求,而本研究结果显示,G2组与G3组的靶区适形度指数虽比G1组略高,但实际数值非常接近,G1组同样高度适形靶区,其均匀性指数略差,亦满足剂量学要求,G2组与G3组的靶区剂量学参数无明显差异。Schultheiss等[11]报道,当脊髓Dmax为45 Gy时,放射性脊髓病发生概率为0.03%,要求最大程度降低脊髓受量以减少脊髓功能受损伤的风险。本研究中3组计划的脊髓Dmax<40 Gy,脊髓计划区Dmax约为45 Gy,很好的保护了脊髓,体现了一定的优势[12]。另有多篇文献[13-14]报道了双肺的V5~V30和MLD与放射性肺炎的发生率相关,并且与其严重程度明显相关,一般认为双肺V20<25%~30%可被接受。本结果中3组计划的双肺V20均<25%,这对预防及降低放射性肺炎的发生率及严重程度更具优势,这与Yin等[15]的研究结果相符。Kumar等[16]的研究表明,急性放射性肺炎主要与V30相关,3组计划均远低于可接受范围(V30<18%~20%且G1组最低)。肺部低剂量大体积照射亦是引起放射性肺炎的重要危险因素,建议V5应限制在65%以内[17-18]。本研究结果显示,3组计划的V5均≤47%,远低于剂量限值,更能有效降低放射性肺炎的发生率。国内外文献报道,心脏受照体积和剂量是心脏损伤的重要因素,3组计划中的心脏平均剂量均≤5 Gy,远低于各项指标,起到了很好的保护作用。G1组与G2组、G3组相比,其最大优势在于减少MU和缩短治疗时间。本研究中G2组、G3组的MU分别较G1组增加了0.6%和3.4%,而TT分别增加了0.6%和5.1%。治疗时间的缩短对图像引导放射治疗的开展具有重要意义。Bewes等[19]报道,治疗时间的缩短,能够增加肿瘤的相对生物效应,利于肿瘤细胞的杀伤。由于在较长时间治疗过程中体位可能产生变化,将导致治疗精度下降,因此缩短治疗时间对精确放射治疗具有显著意义。
本研究中的3组计划均能满足临床剂量学要求,G1组在保证靶区剂量分布情况下,同样能够有效保护脊髓、脊髓计划区和心脏的同时降低部分危及器官的受量,MU减少对降低放射线诱导的继发肿瘤的发生率有重要意义,TT缩短对提高治疗效率和精度具有显著意义的同时亦降低了设备损耗率,患者不适感的减轻增加了治疗依从性[20]。因此,动态调强的子野优化技术在胸上段食管癌具有临床应用价值。

