AU5800型全自动生化仪对脂蛋白相关磷脂酶A2活性的检测性能研究*
吴美玲 刘 斌 高 华 张炳昌 栾 芳*
脂蛋白相关磷脂酶A2(1ipoprotein-associated phospholipase A2,Lp-PLA2)是磷脂酶超家族中的亚型之一,又称为血小板活化因子乙酰水解酶,由血管内膜中的巨噬细胞、T细胞和肥大细胞合成和分泌,血小板活化因子可促进其分泌。Lp-PLA2与脂蛋白颗粒结合的形式存在,与低密度脂蛋白结合的约占80%,其余与高密度脂蛋白和极低密度脂蛋白相结合;Lp-PLA2可水解氧化低密度脂蛋白中的氧化磷脂,生成溶血卵磷脂和氧化游离脂肪酸脂类等促炎物质[1-3]。在动脉粥样硬化患者中,Lp-PLA2水平与低密度脂蛋白胆固醇(low density 1ipoprotein cholesterol,LDL-C)亚组分水平[4-5]呈正相关,是血管特异性的炎症及与斑块稳定性密切相关的新炎症标志物,是冠心病和脑卒中及其他动脉粥样硬化相关疾病的临床预测指标[6-10]。
目前,Lp-PLA2检测多采用酶联免疫或化学发光的方法检测其质量,对Lp-PLA2活性检测的报道少见。AU5800型全自动生化分析仪检测Lp-PLA2活性的优势是可以与其他血脂指标同时检测,方便临床解读化验结果。为此,本研究对AU5800型全自动生化仪检测Lp-PLA2活性的正确度、精密度、线性范围、可报告范围、参考区间和灵敏度进行分析评价。
1 资料与方法
1.1 标本来源
选取2017年7月在健康体检中心体检的20名健康体检者,其中男性9名,女性11名;年龄18岁~59岁,平均年龄(33.55±12.10)岁;排除高血压、高血脂、糖尿病、甲状腺功能异常等疾病。清晨无剧烈运动,空腹采集静脉血标本3 ml,离心后取血清于2 h内在AU5800型全自动生化仪上检测。
1.2 仪器与试剂
BECKMAN AU5800型全自动生化仪(美国贝克曼库尔特公司),Lp-PLA2活性试剂盒(批号Z170501)及配套校准品(重庆中元生物技术有限公司 批号Z170501),原装质控品(低值批号170501、高值批号170502),速率法检测。
1.3 检测方法
1.3.1 正确度验证
依据国家卫生行业标准“临床检验定量测定项目精密度与正确度性能验证”(WS/T492-2016)文件[11]要求,检测Lp-PLA2活性试剂盒配套校准品(校准品可溯源至DRE-XA15590400ME)15次,计算15次连续测定结果的均值。测定值与理论值相比较,与说明书参考值相对偏差≤10%作对照。
1.3.2 精密度验证
(1)批内精密度。依据国家卫生行业标准(WS/T420-2013)和临床实验室标准化协会(clinical and laboratory standards institute,CLSI)EP5-A2文件[12-13]“定量测量方法的精密度性能评价”要求,取Lp-PLA2活性试剂盒配套低值质控品和高值质控品各1份,连续检测20次,计算均数±标准差(M±SD)及变异系数(coefficient of variation,CV)。
(2)批间精密度。依据国家卫生行业标准(WS/T420-2013)和CLSI EP5-A2文件[12-13]要求,取Lp-PLA2活性试剂盒配套低值质控品和高值质控品各1份,连续检测20 d,计算M±SD及CV。
实验室自定义总允许误差(total error allowance,TEa)为20%,批内精密度目标按1/4TEa计算即批内CV≤5%为符合要求,批间精密度目标按1/3 TEa即批间CV≤6.6%为符合要求。
1.3.3 线性范围验证
依据国家卫生行业标准(WS/T420-2013)和CLSIEP6-A文件[12-14]要求,选取接近线性范围上限的高浓度血清标本(H)、低浓度血清标本(L)各一份,按高低比例H、6∶2、4∶4、3∶5及L混匀,测定每份标本分析物浓度3次取平均值作为实测值,以实测值为Y、理论值为X拟合一次线性回归方程,评估Lp-PLA2在10.0~1500.00 IU/L范围内的检测是否呈线性。结果判断:曲线回归系数r2≥0.990。
1.3.4 可报告范围验证
选取浓度在接近线性范围上限的高浓度血清标本,按照1∶2、1∶4、1∶8、1∶16、1∶32、1∶64以及1∶128的比例稀释,每个浓度检测3次,统计均值与理论值比较,以80%≤R≤120%定位可接受范围。
1.3.5 参考区间验证
依据国家卫生行业标准(WS/T402-2012),从医院健康体检中心收集健康人血液标本20份,与说明书提供的参考范围0~659 IU/L进行验证,R≥90%符合要求。
1.3.6 灵敏度分析
Lp-PLA2连续测试6个样本,查看各测吸光度变化量⊿A,通过⊿A=A2-A1,计算样本浓度为检测范围内时,分析灵敏度的变化。⊿A≥0.02 mA/min·L/IU,符合要求。
1.4 统计学方法
采用Graphpad Prism 5软件对数据进行统计学分析和作图。均数采用±s表示,理论值和实测值的线性关系分析通过拟合一次线性回归方程。以P<0.05为差异有统计学意义。
2 结果
2.1 正确度
可溯源至DRE-XA15590400ME的校准品连续测定15次,计算均值为530.4 mg/l,理论值为515.0 mg/l,偏差2.99%,符合要求,见表1。
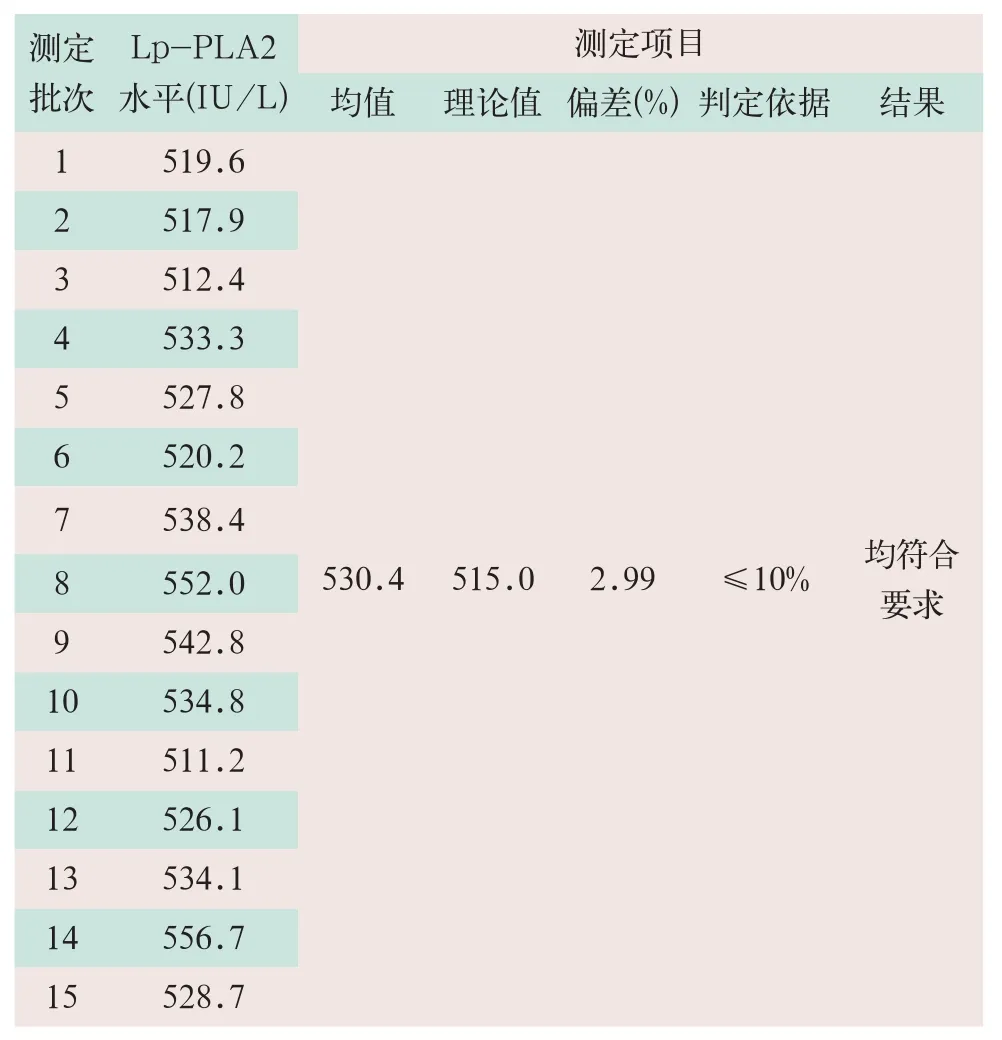
表1 AU5800型全自动生化仪测定Lp-PLA2活性的准确度
2.2 精密度
2.2.1 批内精密度
试剂盒配套低值质控品和高值质控品分别连续检测20次,变异系数CV分别为1.39%和2.67%,均<5%,符合要求,见表2-1、表2-2。
2.2.2 批间精密度
每日测试试剂盒配套低值质控品和高值质控品,连续检测15 d,变异系数CV分别为3.47%和3.00%,均<6.6%,均符合要求,见表3。
2.3 线性范围
以Lp-PLA2活性理论值(不同稀释度)为X轴,实测均值为Y轴,得出回归方程为Y=0.9961X+7.213(r2=0.9997),显示线性良好,线性范围在9.63~1580.87 IU/L内,大于试剂盒说明书规定的10~1500 IU/L,且符合要求,其线性检测情况如图1所示、见表4。
2.4 可报告范围
通过验证,标本按照不同比例稀释后,最大稀释64倍在80%≤R≤120%可接受范围之内,可报告范围为9.63~101175.68 IU/L,见表5。
2.5 参考区间
随机抽取20名健康者的血清进行Lp-PLA2活性测定,验证厂家提供范围0~659 IU/L,90%在范围内为合格。实际侧得范围397.0~711.1 IU/L,95%在厂商给定参考范围之内,符合要求,见表6。
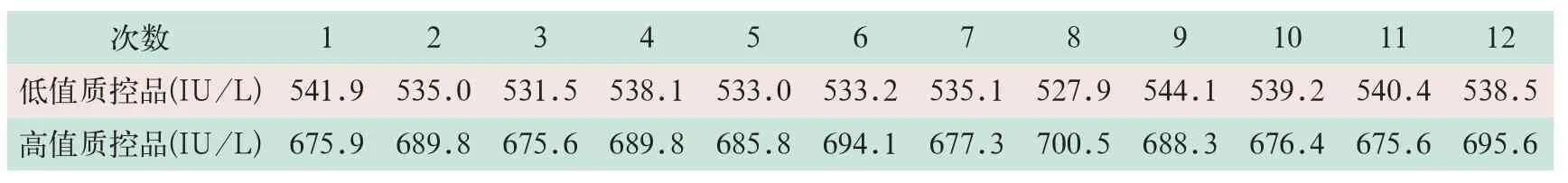
表2-1 AU5800型全自动生化仪测定Lp-PLA2活性的批内精密度(1~12次)
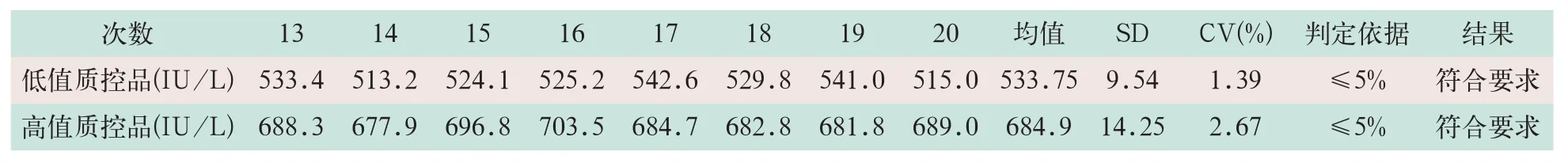
表2-2 AU5800型全自动生化仪测定Lp-PLA2活性的批内精密度(13~20次)
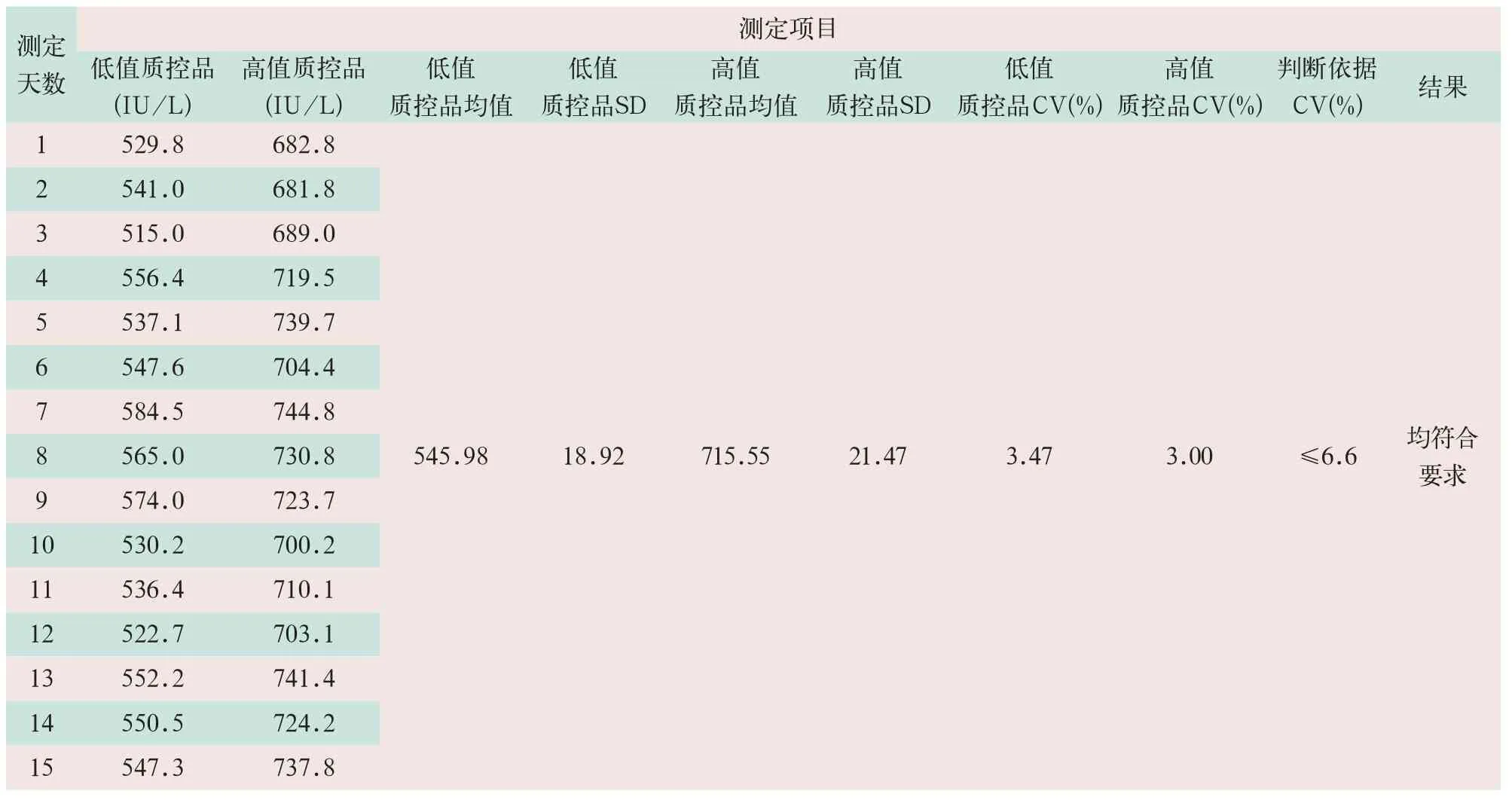
表3 AU5800型全自动生化仪测定Lp-PLA2活性的批间精密度
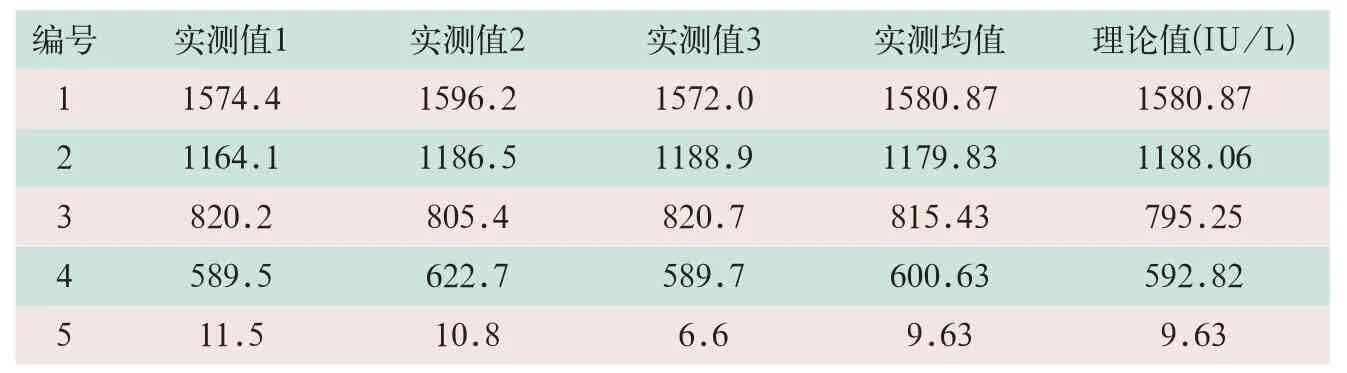
表4 AU5800型全自动生化仪测定Lp-PLA2活性的线性范围验证(IU/L)
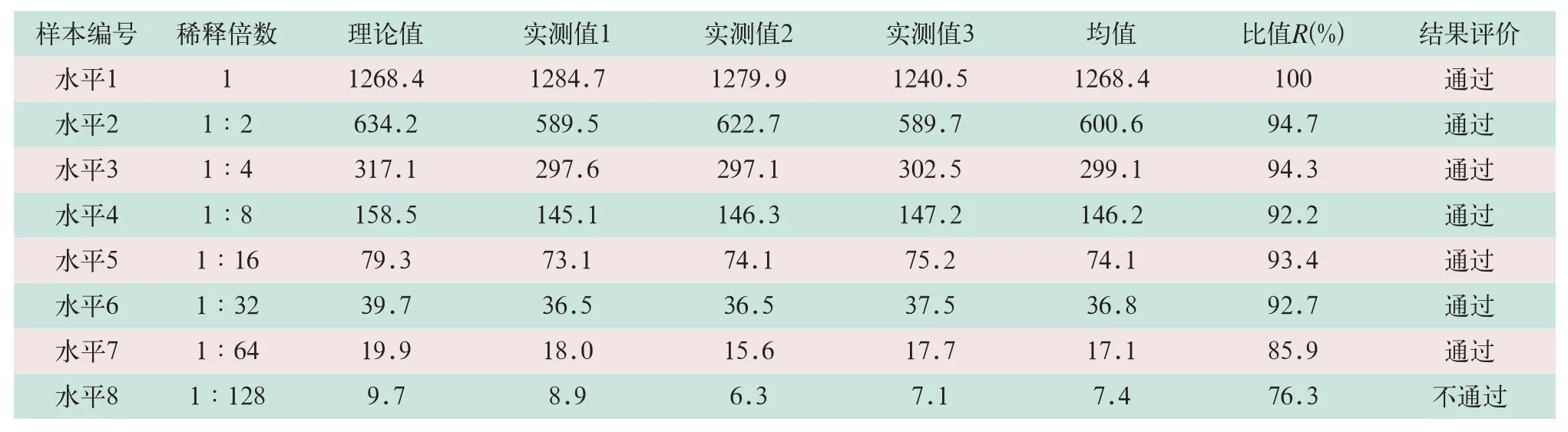
表5 AU5800型全自动生化仪测定Lp-PLA2活性的可报告范围验证(IU/L)
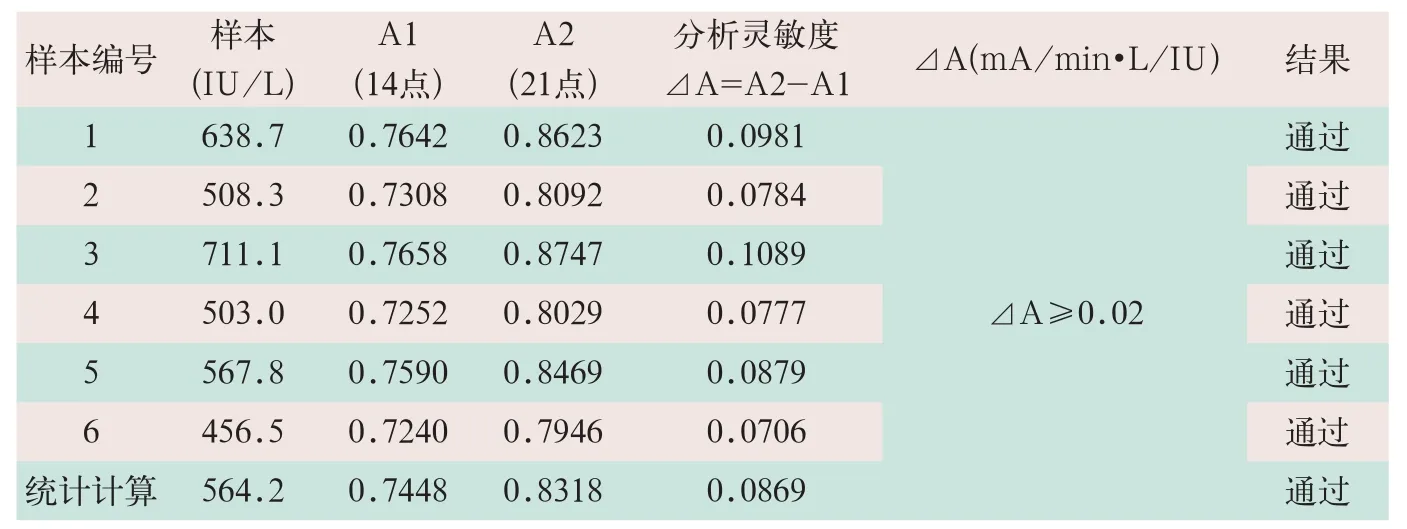
表7 AU5800型全自动生化仪测定Lp-PLA2活性的分析灵敏度验证
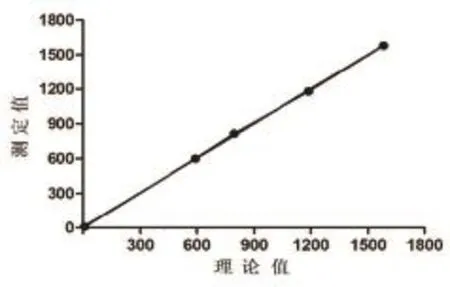
图1 AU5800型全自动生化仪测定Lp-PLA2活性范围验证的线性图
2.6 分析灵敏度
连续测试6个标本进行Lp-PLA2活性测定,实际检测浓度在检测范围内时,试剂吸光度平均变化⊿A=0.0869≥0.02,符合中元生物试剂说明书要求,见表7。
3 讨论
Lp-PLA2是心血管疾病中一种新的炎症标记物,在动脉粥样硬化的发病、进展和斑块破裂中起关键作用,是近几年来心血管领域研究的重点和热点。相对于C反应蛋白、白介素等传统的炎症指标,Lp-PLA2在心血管疾病的诊治中具有特异性高的优势。本研究实验室在AU5800型全自动生化仪引入Lp-PLA2活性检测,与低密度脂蛋白胆固醇、同型半胱氨酸以及小而密低密度脂蛋白胆固醇等血脂指标组合,方便临床对心血管疾病风险的评估。
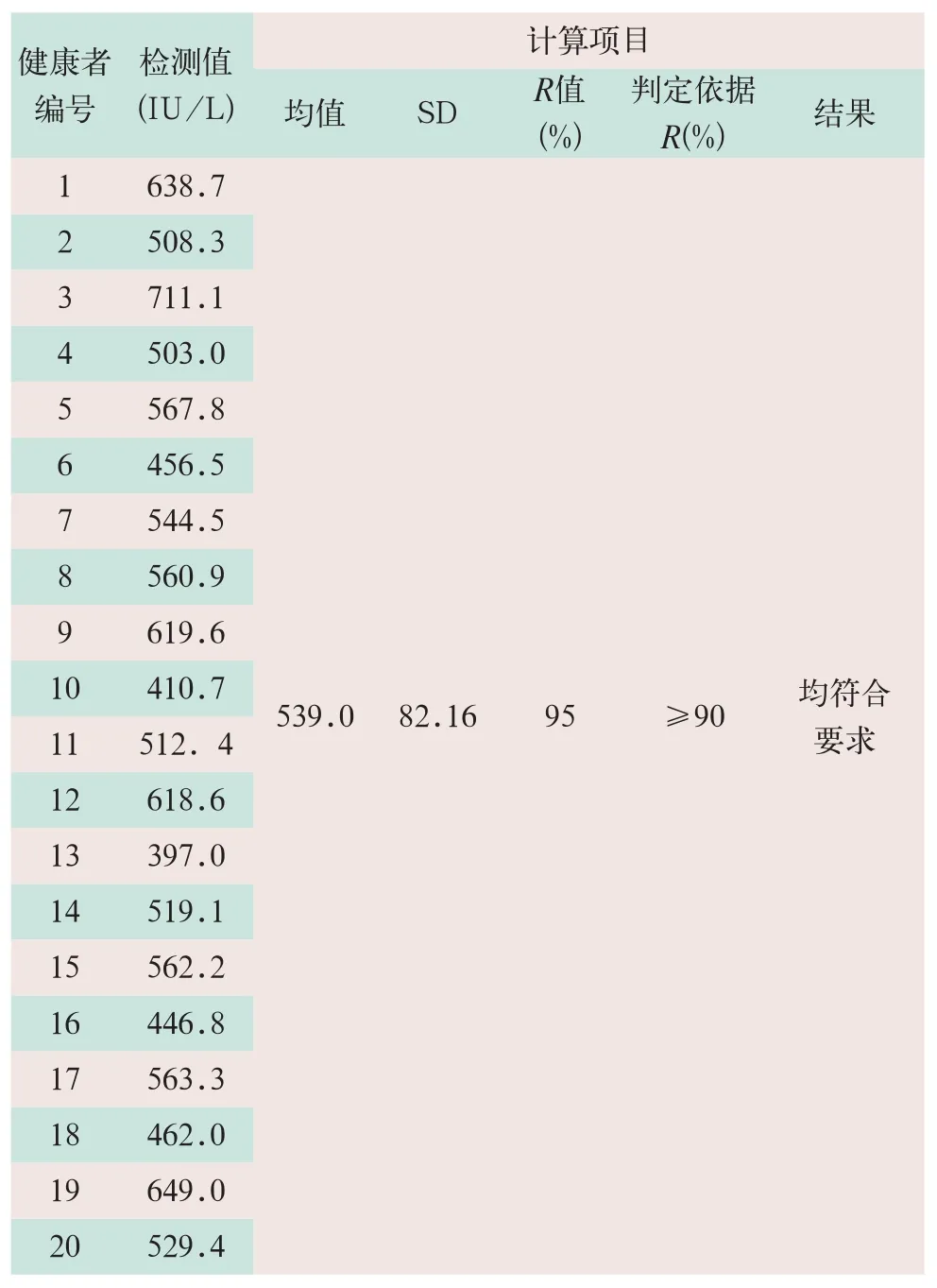
表6 AU5800型全自动生化仪测定Lp-PLA2活性的参考区间验证
本研究依据国家卫生行业标准(WS/T 420-2013、WS/T 492-2016、WS/T 402-2012)以及CLSI EP5和EP6文件的要求,评估了AU5800型全自动生化仪检测Lp-PLA2活性的性能。结果显示,AU5800型全自动生化仪检测Lp-PLA2活性的正确度较高,偏差为2.99%;批内不精密度和批间不精密度均在实验室设置的精密度目标之内;检测线性范围为9.63~1580.87 IU/L,可报告范围为9.63~101175.68 IU/L,满足临床检测需要;正常人群参考区间验证和灵敏度验证均符合要求。
2018年4月,美国《临床化学》杂志报道,传统免疫法检测Lp-PLA2质量时,由于受Lp-PLA2与脂蛋白结合存在形式干扰,导致检测结果偏低,使得Lp-PLA2质量和活性检测结果不一致;串联质谱法(LC-MS/MS)检测Lp-PLA2质量时,可以把Lp-PLA2与脂蛋白完全解离,Lp-PLA2质量和活性检测结果一致[15]。但是,串联质谱法检测Lp-PLA2标本前处理复杂、成本高,因此AU5800型全自动生化仪检测Lp-PLA2活性更能满足于临床需求,LC-MS/MS检测的Lp-PLA2活性与AU5800型全自动生化仪检测的Lp-PLA2活性结果是否一致,尚需进一步研究。
AU5800型全自动生化仪测定Lp-PLA2活性,具有快速简便、准确度高、重复性好等优点,适合临床大批量标本的检测,适用于心内科、神经内科等科室对心脑血管疾病风险评估。

