2018年春季兰州市鸡肉中磺胺类药物残留的检测与分析
杨建红
(甘肃省静宁县畜牧兽医局,甘肃 静宁 743400)
磺胺类药物是具有对氨基苯磺酰胺结构的、人工合成的一类药物的总称,在降低动物发病率和死亡率、促进生长和改善动物产品品质方面具有显著作用[1]。磺胺类药物作为饲料添加剂,被广泛应用于动物饲养中[2]。但这类药物也具有较强的毒副作用,可引起机体过敏、中毒、导致耐药性菌株的产生,还可引发造血系统障碍、溶血性贫血、粒细胞缺乏症、再生障碍性贫血、血小板减少症等疾病。为此,国内外对其残留均有限量要求[3]。
磺胺类药物主要通过动物性食品进入人体,非法使用违禁药物、滥用抗菌药和药物添加剂、不遵守休药期规定是导致动物性食品中药物残留的主要原因,这些原因可导致药物以原形或其代谢产物的形式蓄积在动物的细胞、组织、器官或可食性产品中,造成残留[4]。随着人们生活水平的提高,无残留、优质、安全、绿色食品日益受到消费者的青睐,因而加强兽药残留的监控和检测工作具有重要意义[5]。为了加强兰州市市售鸡肉中磺胺类药物残留的检测、监督,采用ELISA法进行了磺胺类药物残留的检测,以确保市场上流通鸡肉的安全性,保障消费者权益。
1 材料与方法
1.1 材料
1.1.1 仪器 DNM-9602G型微孔板酶标仪(北京普朗新技术有限公司),波长450~630 nm;MTN-2800D型氮气吹干装置(北京八方世纪科技有限公司);SQ2119N型组织搅碎机;MH-2型微型振荡器(海门市其林贝林仪器制造有限公司);XW-80A型漩涡混合器(上海精科实业有限公司生产);3K15型高速冷冻离心机(北京博劢行仪器有限公司),转速不低于4 000 r/min;AB135-S型梅特勒电子天平(上海精科实业有限公司生产),感量为0.000 1 g和0.01 g;优普超纯水制造系统(上海优普实业有限公司);10 ml玻璃试管,2 ml、50 ml聚苯乙烯离心管;微量移液器:单道20~200 μl、100~1 000 μl,多道250 μl;移液枪,排枪;烧杯、量筒(所有玻璃仪器均由天津玻璃仪器厂制造,使用前经过超纯水反复洗涤)。
1.1.2 试剂 乙酸乙酯(分析纯)、正己烷(分析纯)、十二水合磷酸氢二钠(分析纯)、二水合磷酸二氢钠(分析纯)、去离子水。
1.1.3 ELISA试剂盒 本次研究所使用的试剂盒是北京勤邦生物技术有限公司生产的磺胺七合一快速检测试剂盒,批号为E130413E20。试剂盒保存温度为2~8℃,所含组分有:96孔酶标板1板(包被有酶联抗体);标准液6瓶(1 ml/瓶):0 μg/L、2 μg/L、4 μg/L、8 μg/L、16 μg/L、32 μg/L;高浓度标准品:1 mg/L(1 ml/瓶);酶标2抗12 ml;抗体工作液10 ml;底物液A液7 ml;底物液B液7 ml;终止液7 ml;20×浓缩洗涤液50 ml。
1.1.4 溶液配制 盐酸溶液:量取41.5 ml浓盐酸加入到去离子水中定容至500 ml。氢氧化钠溶液:称取20.0 g氢氧化钠加500 ml去离子水溶解混匀。pH=6的磷酸盐缓冲液:称取1.75 g十二水合磷酸氢化钠、10.52 g二水合磷酸二氢钠加500 ml去离子水溶解混匀。复溶工作液:用去离子水将2×浓缩复溶液按1∶1体积比进行稀释,用于样本的复溶,复溶工作液在4℃环境下可保存一个月。洗涤工作液:用去离子水将20×浓缩洗涤液按1∶19体积比进行稀释,用于酶标板的洗涤,洗涤工作液在4℃环境下可保存一个月。
1.2 试验方法
1.2.1 样品采集 2018年2—4月从兰州市肉菜市场及超市中随机抽取40份鸡肉作为检测对象,并编号为1~40号,详见表1。
1.2.2 样品处理 用组织搅碎机均质样本;称取2.0±0.05 g均质物,置于50 ml聚苯乙烯离心管中,加入4 ml pH为6的磷酸盐缓冲液涡动成糊状,再加入6 ml乙酸乙酯,振荡1 min后在室温下(20~25℃),用高速离心机按3 000 r/min以上的速度离心5 min;取3 ml上清液至10 ml干净玻璃试管中,用氮气吹干装置的氮气流吹干;加入1 ml正己烷,用涡旋仪涡动30 s,再加入1 ml复溶工作液涡动10 s,然后在室温下用离心机按3 000 r/min以上的速度离心5 min;除去上层正己烷相,取下层水相50 μl用于分析。
1.2.3 样品测定 将所需试剂从冷藏环境中取出,置于室温平衡30 min以上,每种液体试剂使用之前均需摇匀;取出所需数量的微孔板,将不用的微孔板放入自封袋,保存于2~8℃温度下;洗涤工作液在使用前也需回温;编号:将样本和标准品对应微孔按序编号,每个样本和标准品做2孔平行,并记录标准孔和样品孔所在的位置;加标准品/样本、酶标二抗和抗体工作液:加入标准品/样本50 μl到对应的微孔中,随即加入酶标二抗50 μl/孔,再加入抗体工作液50 μl/孔,轻轻振荡混匀,用盖板膜盖板后置于25℃避光环境中反应30 min;洗板:小心揭开盖板膜,将孔内液体甩干,用洗涤液250 μl/孔洗涤,充分洗涤4~5次,每次间隔10 s,用吸水纸拍干(拍干后未被清除的气泡可用未使用过的枪头戳破);显色:加入底物液A液50 μl/孔,再加底物液B液50 μl/孔,轻轻振荡混匀,用盖板膜盖板后置于25℃避光环境中反应15 min;测定:加入终止液50 μl/孔,轻轻振荡混匀,设定酶标仪于450 nm处(建议用双波长450/630 nm检测,并在5 min内读完数据),测定每孔OD值。
1.2.4 百分吸光率的计算 标准品或样本的百分吸光率等于标准品或样本的吸光度值的平均值(双孔)除以第一个标准品(0标准)的吸光度值,再乘以100%,公式如下:
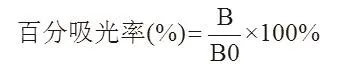

表1 样品采集情况
式中B为标准溶液或样本溶液的平均吸光度值,B0为0 μg/L标准溶液的平均吸光度值。
1.2.5 标准曲线的绘制 以标准品百分吸光率为纵坐标、磺胺类药物标准品浓度(μg/kg)的对数为横坐标,绘制标准曲线图。将样本的百分吸光率代入标准曲线中,从标准曲线上读出样本所对应的浓度,再乘以其对应的稀释倍数即为样本中磺胺类药物的实际浓度。
1.2.6 统计学分析 对两组以上的数据差异显著性分析用方差分析即“F检验”,主要有组内变异和组间变异。组内偏差平方和(SSw)、组间偏差平方和(SSb)除以各自的自由度(组内dfw=n-m,组间dfb=m-1,其中n为样本总数,m为组数),得到其均方MSw和MSb。一种情况是处理没有作用即MSb/MSw≈1;另一种情况是处理确实有作用,组间均方是由于误差与不同处理共同导致的结果,MSb》MSw(远远大于)。MSb/MSw比值构成F分布,F值大于1有显著差异,反之则没有。
1.2.7 判定标准 依据农业部1025号公告-7-2008的规定,鸡肉中磺胺类药物残留限量≤100 μg/kg,超过此限量值则为不合格。
2 结果与分析
2.1 2月份鸡肉中磺胺类药物的残留量
2.1.1 标准曲线的绘制 第一批次试验中标准品的数据与标准应符合的量的偏差在0.4%范围内,平均偏差为0.167%。本次检测存在的误差极小,检测结果(见表2)可用于判定样品中磺胺类药物的实际残留量,所绘制的标准曲线如图1。
2.1.2 鸡肉中磺胺药的残留量 2月份鸡肉的检测结果显示,10份样品中均含有磺胺药残留,检出率为100%,其中检出的最大残留量为18.12 μg/kg,最小残留量为0.783 μg/kg。3号疑似磺胺类药物残留量较高,应再次检测以确定是否过高。其他的检测浓度均在0.783μg/kg以下,在<100 μg/kg的正常范围内,详见表3。
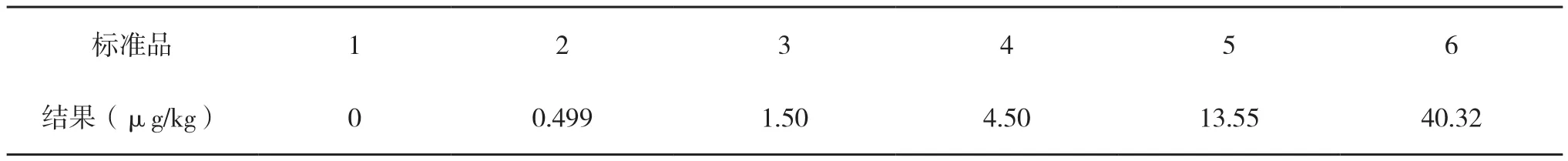
表2 第一批次标准品中磺胺类药物的量
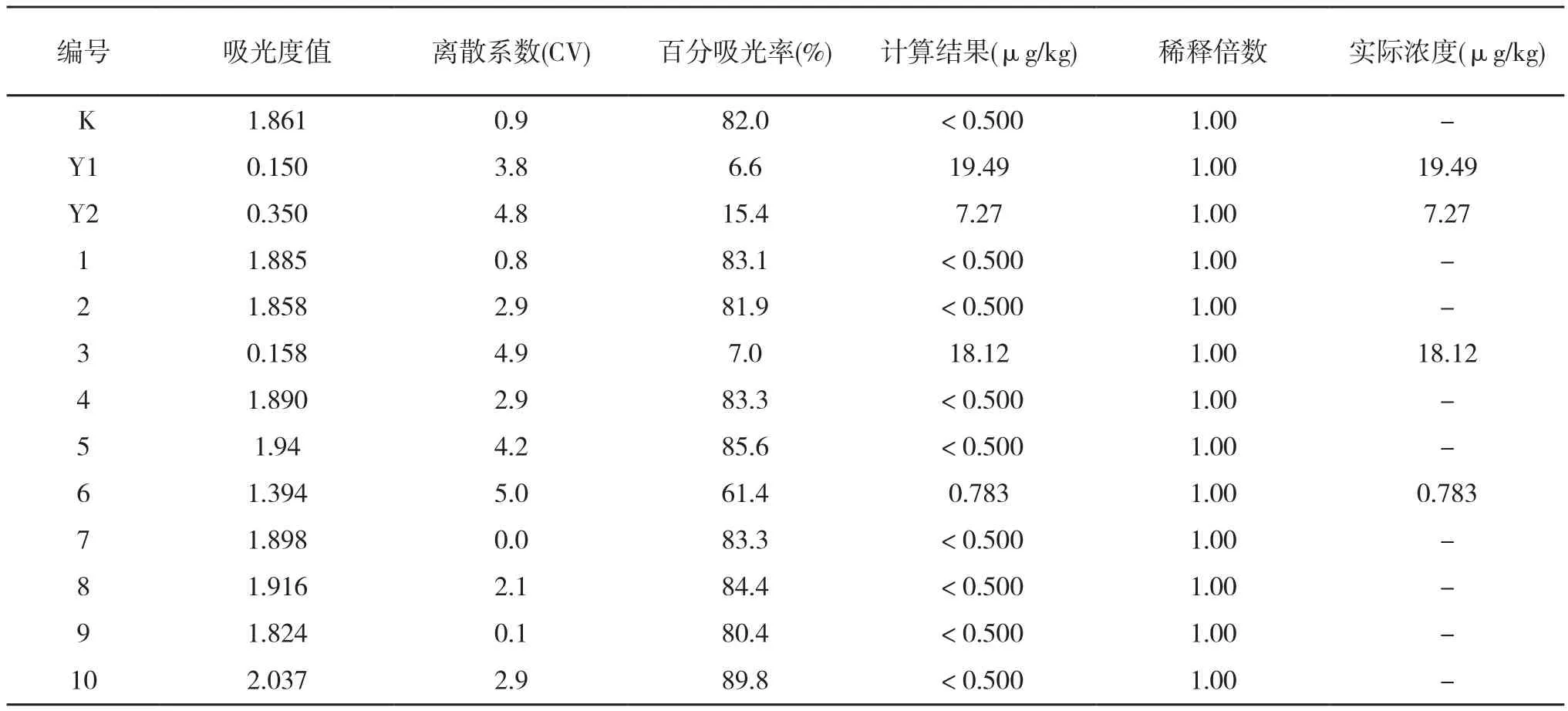
表3 2月份鸡肉中磺胺类药物残留的检出量与百分吸光度值
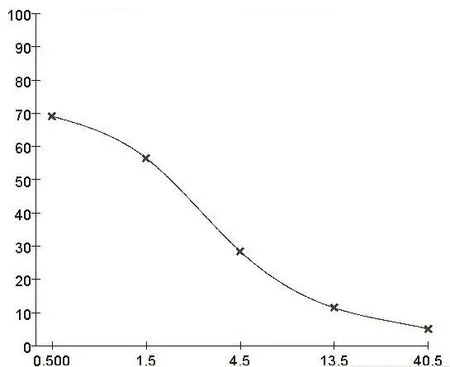
图1 第一次检测磺胺类药的标准曲线
2.2 3月份鸡肉中磺胺类药物的残留量
2.2.1 标准曲线的绘制 第二批次的试验中标准品的数据与标准应该符合的量的偏差在0.5%内,平均偏差为0.233%。说明本次检测存在的误差较小,检测结果(见表4)可以用于判定样品中磺胺类药物的实际残留量,所绘制的标准曲线如图2。

图2 第二次检测磺胺类药物的标准曲线
2.2.2 鸡肉中磺胺类药物的残留量 3月份的检测结果如表5所示,其离散系数小于13,说明该组试验重复性好。10份样品中均含有磺胺类药物,检出率为100%,其中最小残留量<0.500 μg/kg,最大残留量为1.76 μg/kg,均符合农业部对磺胺类药物残留限量的规定。

表4 第二批次标准品中磺胺类药物的量
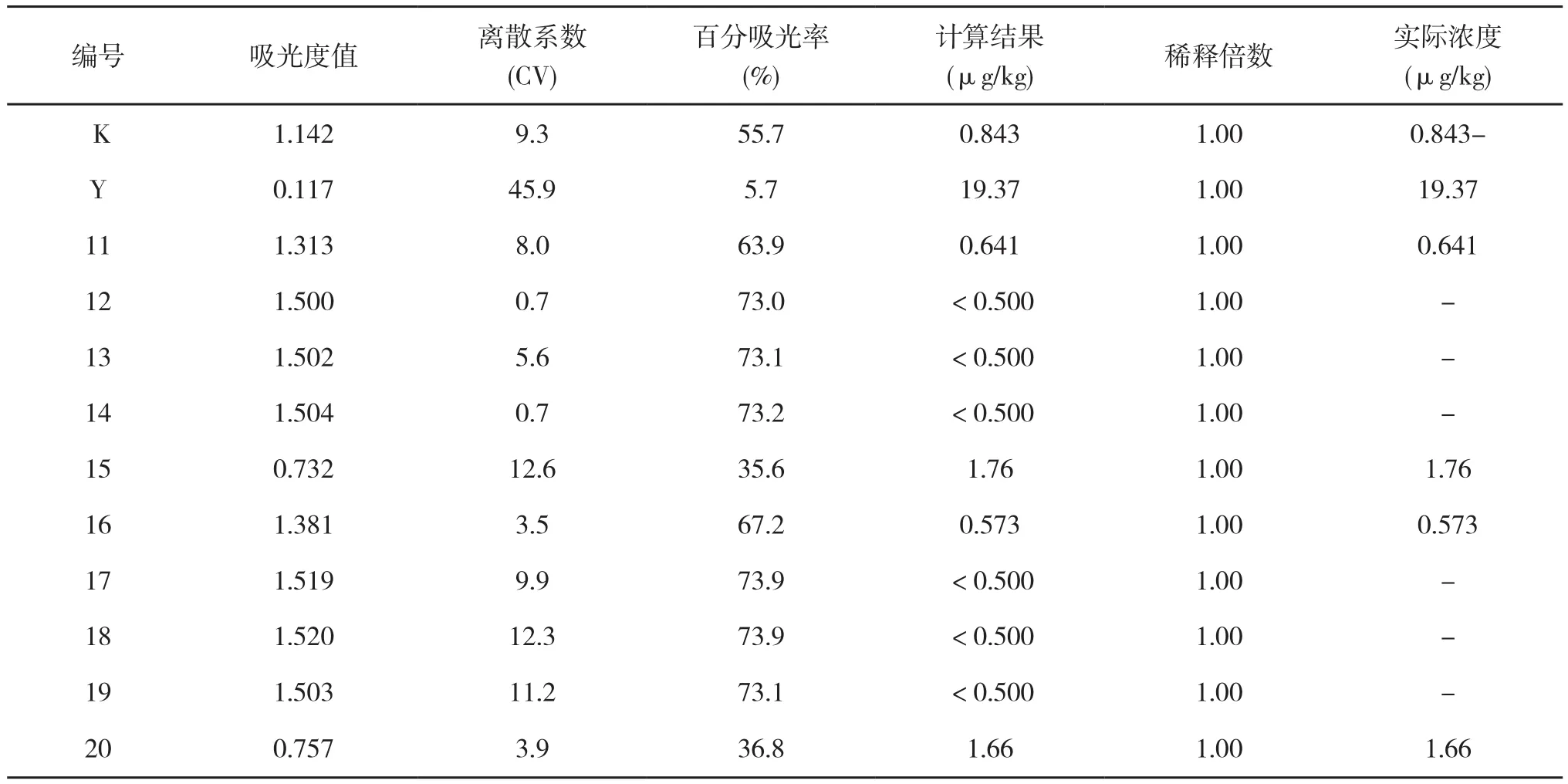
表5 3月份鸡肉中磺胺类药物残留情况
2.3 4月份鸡肉中磺胺药的残留量
2.3.1 标准曲线的绘制 第三批次检测的最大试验偏差为0.7%,说明本次检测的误差在允许范围内,检测结果(见表6)可以用于判定样品中磺胺类药物的实际残留量,所绘制的标准曲线如图3。
2.3.2 鸡肉中磺胺类药物的残留量 4月份的检测结果见表7,20份样品中有19份含有磺胺类药物残留,检出率为95%,磺胺类药物的最大残留量为4.54 μg/kg,均在农业部规定的磺胺类药物残留限量内。

图3 第三次检测磺胺类药物的标准曲线

表6 标准品中磺胺类药物的量
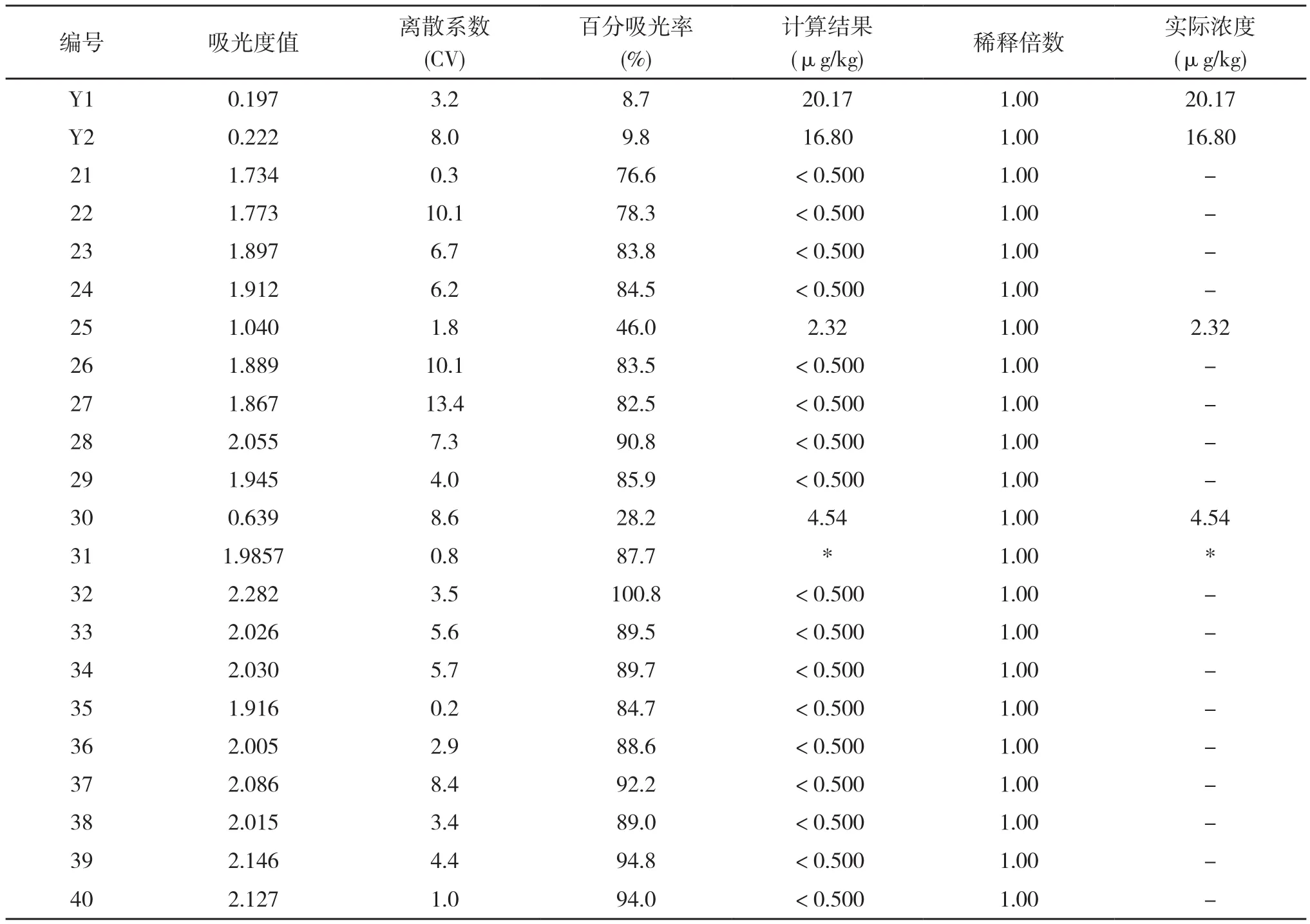
表7 4月份鸡肉中磺胺类药物残留情况
2.4 不同月份鸡肉中磺胺药残留量比较分析
2018年2—4月份兰州市市售鸡肉中磺胺类药物检出率从100%下降到95%,实际检出最小值从2月份的0.783 μg/kg减小为4月份的0 μg/kg,检出平均值从1.89 μg/kg减小为0.34 μg/kg(详见表8、图4)。
统计分析可知2—4月份的检测变异系数分别为0.169、0.664、0.733,试验误差很小。组间方差为0.017、组内方差为0.21,F值为1.496大于1,说明3组试验间有显著差异。3次试验均存在误差,但均有研究意义。
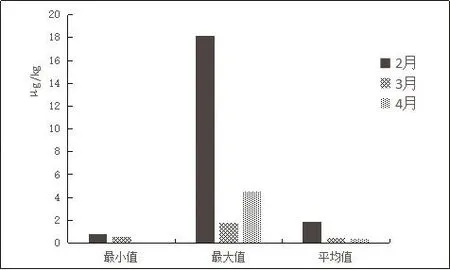
图4 2—4月份鸡肉中磺胺类药物的残留情况
2.5 不同采样地点鸡肉中磺胺类药物残留量比较分析
检测结果显示,2018年2—4月份从超市抽取的鸡肉样品磺胺类药物残留量的检出率为100%,实际检出最小值为0 μg/kg、最大值为1.66 μg/kg、平均值为0.419 μg/kg;从市场抽取的鸡肉样品磺胺类药物残留量的检出率为95%,实际检出最小值为0.641 μg/kg、最大值为18.12 μg/kg、平均值为1.369 μg/kg(详见表9、图5)。
经统计分析可知,市场和超市的检测变异系数分别为0.328、0.195,试验误差很小。市场检验的方差为0.274,超市检验的方差为0.133,F值为2.06大于1,说明市场检验与超市检验间有显著差异。试验存在误差,但具有研究意义。
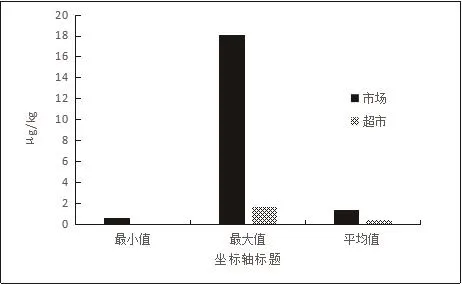
图5 市场与超市中鸡肉检测结果比较
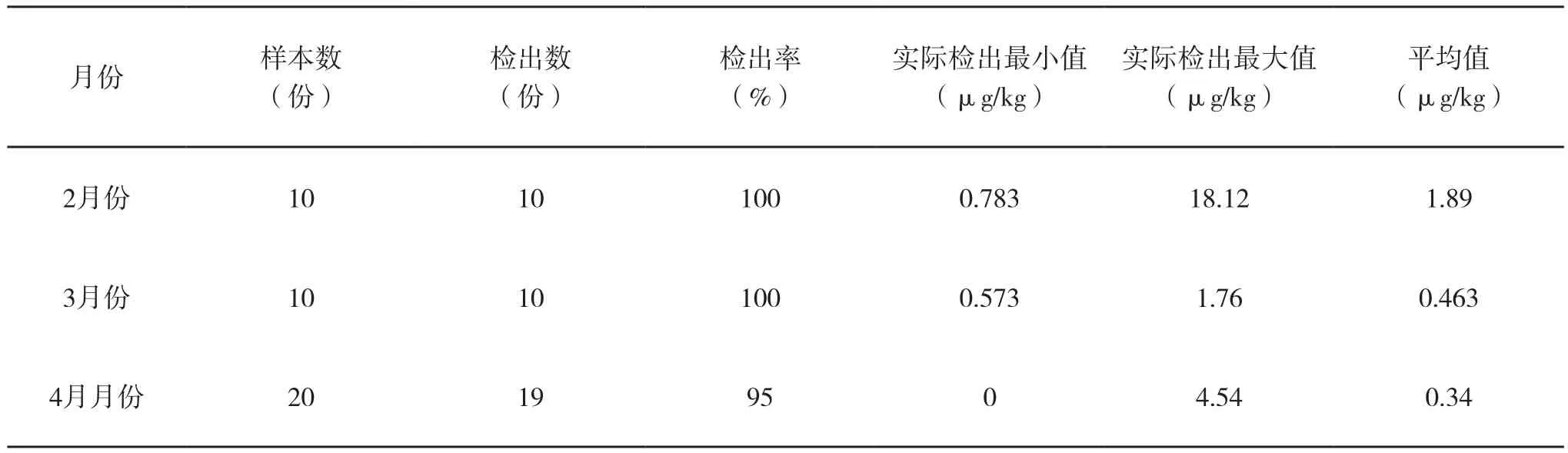
表8 不同月份鸡肉中磺胺类药物残留情况

表9 不同采样地点鸡肉中磺胺类药物残留情况
3 讨论
ELISA检测法既可测抗原,也可测抗体;既可进行定性测定,又可进行定量测定。具有快速、灵敏、操作简单、特异性好、经济、无污染、不需大型仪器设备、技术要求低等优点,适合大批样品的筛选检测,在实际应用中可更方便地检测鸡肉中磺胺类药物的残留是否超标[6]。
为了保证试验结果的准确性,检测前需将所有试剂和所需板条的温度回升至室温(20~25℃),否则会导致所有标准品的OD值偏低[7]。温度太低会减弱甚至抑制抗体抗原反应,导致在正常试验时间内反应还不完全便被加入停止液终止反应,使得最终结果不正确。洗板拍干后应立即进行下一步操作。试剂盒应储存在2~8℃温度下,不能冷冻。标准物质和无色的发色剂对光敏感,应避免直接暴露于光下。在所有恒温孵育过程中,应用盖板膜盖住微孔板,避免光线照射。
试验结果表明:所有样品中磺胺类药物的残留量范围为0~18.13 μg/kg,均符合农业部规定的磺胺类药物的残留限量,合格率为100%。说明兰州市销售的鸡肉中磺胺类药物未超标,消费者可以放心食用。

