磷灰石结构荧光粉Ba10(PO4)6F2∶Ce3+,Tb3+的合成、发光和能量传递
程少文 张 娜 卓宁泽 朱月华 陈永浩
蒋 鹏4 杜文慧4 叶恩淦4 王海波*,3
(1南京工业大学,能源科学与工程学院,南京 211816)
(2轻工业部南京电光源材料科学研究所,南京 210015)
(3南京工业大学,电光源材料研究所,南京 210015)
(4南京工业大学,材料工程与科学学院,南京 210009)
0 引 言
WLED(white light emitting diode)凭借其发光效率高、寿命长、体积小、节能环保等优点[1-2],开启了照明领域的新革命,被誉为21世纪最有价值的新光源。目前,商用WLED主要通过蓝光LED芯片结合钇铝石榴石结构的黄色荧光粉YAG∶Ce3+得到,由于光谱曲线中缺少深红色光谱部分[3],导致获得的白光显色指数 (Color Rendering Index,CRI)较低(CRI<80),与自然光有着显著的差异,降低了其光色品质,限制了其应用范围[4-5]。相比之下,紫外光LED芯片结合三基色(红、绿、蓝)荧光粉可以获得低色温、高显色指数的全光谱WLED,得到了人们的广泛关注[6]。三基色荧光粉不仅在照明领域具有提高CRI和调节色温的作用,在显示领域也占据重要地位,现已广泛应用于场发射显示、阴极射线管显示等领域。因此开发出新型高效的三基色荧光粉在照明和显示方面中都具有重要的现实意义。
磷灰石作为一种重要的荧光粉基质材料,赋予了磷灰石结构荧光粉以高的效率、热稳定性以及化学稳定性[7]。磷灰石结构晶体是一个大家族,主要包括氧磷灰石、卤磷灰以及羟基磷灰石。磷灰石结构晶体具有(A1)2(A2)3(XO4)3Y的化学通式,其中A1和A2 代表二价碱土金属离子 Ca2+、Sr2+、Ba2+等,Y 主要是 F-、Cl-、OH-,XO4表示 PO43+、SiO44+、VO43+等[8]。稀土磷灰石结构荧光粉大部分具有P63/m高对称性的空间群,随着晶体中的阳离子被其他离子取代,磷灰石结构晶体从P63/m高对称性空间群变成相对低对称性的 P6、P63、P3 和 P21/m 空间群[9-10]。 近年来,磷灰石结构荧光粉屡见报道。Zhu等[11]通过高温固相法合成的具有磷灰石结构的绿色荧光粉Sr4La2Ca4(PO4)6O2∶Ce3+,有较好的热稳定性,发光强度是商用绿 色 荧 光 粉 LMS520B(化 学 式(Sr,Ba)2SiO4∶Eu2+)的78.6%。Que等[12]采用高温固相法合成了具有磷灰石结构青色荧光粉Ca10(SiO4)3(SO4)3F2∶Eu2+,空间群P63/m,对荧光粉的热猝灭机理给出了深刻的见解。除了单掺的磷灰石结构荧光粉外,共掺Tb3+而发绿光的荧光粉 Sr3.5Y6.5O2(PO4)1.5(SiO4)4.5∶Eu2+,Tb3+、Ca2Ba3(PO4)3Cl∶0.015Ce3+,0.02Tb3+和 Ca5(PO4)3F∶0.10Eu3+,0.06Tb3+等[13-15],共掺 Mn2+而发红光的荧光粉 Ca9Mg(PO4)6F2∶Eu2+,Mn2+、La9.33(SiO4)6O2∶Eu2+,Mn2+等[16-17],以及三掺杂磷灰石结构白光荧光粉 Ca4Y6(SiO4)6O∶Ce3+,Mn2+,Tb3+,Mg2Y8(SiO4)6O2∶Ce3+,Mn2+,Tb3+等[18-19]均已见 诸 报道。一般单掺杂Ce3+/Eu2+的方法不容易获取磷灰石结构绿色荧光粉,通过共掺Tb3+能量传递的方法则有不少的研究。Ce3+/Eu2+与Tb3+共掺杂,极大地提高Tb3+的发光强度,比如被广泛应用的绿色LaPO4∶Ce3+,Tb3+荧光粉[20-21]。 因此,在磷灰石结构的 Ba10(PO4)6F2晶体中,通过共掺杂稀土离子之间的有效能量传递来实现绿光发射。
本文采用高温固相法合成了一系列具有磷灰石结构的荧光粉 Ba10-x-y(PO4)6F2∶x Ce3+,y Tb3+(x=0,0.005,0.015,0.03,0.045,0.06,0.075,0.09,0.11,0.13;y=0,0.04,0.12,0.20,0.28,0.36,0.44,0.52)。 讨论了晶体结构以及Ce3+和Tb3+间能量传递过程和机理。结果表明,这种具有磷灰石结构且可实现绿光发射的荧光粉能够被紫外光有效激发,作为一种重要的基色荧光粉,在照明和显示领域具有潜在的应用。
1 实验部分
1.1 样品制备
采用高温固相法合成了系列Ce3+单掺杂和Ce3+,Tb3+共掺杂的荧光粉 Ba10-x(PO4)6F2:x Ce3+(x=0,0.005,0.015,0.03,0.045,0.06,0.075,0.09,0.11,0.13)和 Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+(y=0,0.04,0.12,0.20,0.28,0.36,0.44,0.52)。 按照化学计量比,称取 BaCO3(AR),(NH4)2HPO4(AR),NH4F(AR)(以上药品购自国药集团化学试剂有限公司)和稀土氧化物CeO2(99.99%),Tb4O7(99.99%)(稀土原料购自济宁天亿新材料有限公司)。将称取好的原料在玛瑙研钵中充分研磨,将混合均匀的原料转移到刚玉坩埚中,在还原气氛下,1 100℃烧结3 h,冷却到室温,研磨过筛,即得到荧光粉 Ba10-x-y(PO4)6F2∶x Ce3+,y Tb3+样品。
1.2 样品测试
合成样品的相纯度和结构采用SmartLab型高分辨衍射系统(Rigaku,Japan)进行X射线衍射分析。用Cu靶Kα辐射,λ=0.154 06 nm,工作电流和电压分别是 200 mA 和 45 kV, 扫描范围 2θ=5°~90°,扫描速度为 20°·min-1,扫描步长是 0.02°。 样品的颗粒形貌采用JSM-6510型扫描电子显微镜观察分析,工作电压为15 kV。光致发光特性采用RF-6000荧光光谱仪(Shimadzu corporation,Japan)进行测试,氙弧灯作为激发光源。
2 结果与讨论
2.1 X射线衍射分析和晶体结构
图1为不同掺杂浓度和不同掺杂离子的荧光粉 Ba10(PO4)6F2∶Ce3+,Tb3+的 XRD 图,样品的所有衍射峰与标准卡片(PDF No.71-1316)具有较好的匹配性,说明Ce3+和Tb3+已经成功进入了主晶格当中,取代了晶格中Ba2+的位置,而不是生成杂相。图1(b)表明衍射峰随着Ce3+/Tb3+掺杂量的增加而向高2θ值偏移,这是由于半径较小的Ce3+/Tb3+取代半径较大的Ba2+导致的,因此进一步说明Ce3+和Tb3+成功进入Ba2+的位置。
表1总结了Ba10(PO4)6F2的晶胞参数。制备的未掺杂Ba10(PO4)6F2样品的XRD数据经Jade5.0精修后[22],将 精修得到的晶胞 参数 与 White 等[23]报 道 的理论晶胞参数对比后发现,最大偏差只有0.233%,与理论结果吻合的很好。
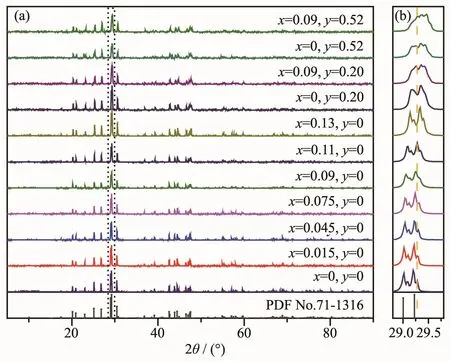
图 1 样品 Ba10-x-y(PO4)6F2∶x Ce3+,y Tb3+的 XRD 图 (a)和28.8°~29.8°局部放大图 (b)Fig.1 XRD patterns of Ba10-x-y(PO4)6F2∶x Ce3+,y Tb3+(a)andmagnified patternsin the region of 28.8°~29.8°(b)

表1 Ba10(PO4)6F2的晶胞参数Table 1 Crystal parameters of Ba10(PO4)6F2
Ba10(PO4)6F2的单位晶胞和Ba1、Ba2的配位环境如图2所示,根据晶体结构的CIF数据信息[24],其中包含4f和6h两种不同的阳离子格位以及3种不同的配位O原子,P与4个O配位形成PO4四面体结构,F-离子占据晶格的六重轴中心,形成自由通道离子。图2为2种阳离子Ba1和Ba2的配位环境,其中Ba1占据C3点对称的4f格位,具有9个O原子与之配位,形成三帽三棱柱的十四面体结构。Ba2占据Cs点对称的6h格位,具有6个O和2个F原子与之配位,形成双帽三棱柱的十一面体结构。它们分别与PO4四面体共用边和角相互连接在一起。根据不同配位环境阳离子半径大小的差异,更小离子半径的 Ce3+(RCN=8=0.114 3 nm;RCN=9=0.119 6 nm)和Tb3+(RCN=8=0.104 0 nm;RCN=9=0.109 5 nm)倾向于取代6h格位的大半径Ba2+离子(RCN=8=0.142 nm;RCN=9=0.147 nm)形成了置换固溶体[25],其中 CN=8 和 CN=9分别代表配位数为8和9。

图2 沿c轴方向Ba10(PO4)6F2的晶胞的结构图(a)和 Ba1(b)、Ba2(c)的配位环境Fig.2 Crystal structure of Ba10(PO4)6F2 along the c-axis direction(a)and the coordination environment of Ba1(b)and Ba2(c)
2.2 扫描电镜(SEM)分析
图 3所示为合成的 Ba9.39(PO4)6F2∶0.09Ce3+,0.52Tb3+荧光粉的SEM照片,从照片中可以看出样品颗粒表面比较光滑,并呈现不规则形貌,颗粒尺寸在2~5μm之间。
2.3 荧光光谱分析
为了获得最佳的Ce3+掺杂量,合成出系列不同掺杂浓度的荧光粉 Ba10-x(PO4)6F2∶x Ce3+。 图 4(a,b)展现了Ba10-x(PO4)6F2∶x Ce3+的发射光谱和相对强度。在295 nm波长紫外光激发下,随着Ce3+掺杂量的增加,发射光谱强度依次递增,当x=0.09时,发射峰达到最大值,再继续增加Ce3+掺杂量,开始出现浓度猝灭现象,发射峰强度随之而下降。

图 4 Ba10-x(PO4)6F2∶x Ce3+的发射光谱(λex=295 nm)(a)和Ce3+的发射强度与Ce3+掺杂浓度的关系 (b)Fig.4 PL spectra of Ba10-x(PO4)6F2∶x Ce3+(λex=295 nm)(a)and emission intensity dependence on doping concentration of Ce3+(b)
图 5(a)是 Ba9.91(PO4)6F2∶0.09Ce3+荧光粉的激发光谱和发射光谱。监测波长为335和358 nm时,得到激发光谱为240~330 nm的宽带。2条激发光谱除强度略有差异外,激发光谱的形状和峰值均相同,其中激发光谱在270和295 nm具有激发峰,归属于Ce3+的4f→5d跃迁吸收。在270和295 nm紫外光激发下,得到的发射光谱具有几乎完全相同的强度,并且没有出现红移或蓝移。发射光谱具有335和358 nm两个峰,归属于Ce3+的5d→4f(2F5/2,2F7/2)跃迁发射。基态4f电子组态的2F5/2和2F7/2两个能级由于自旋轨道偶合,两者相差2 000 cm-1,而335 nm(29 851 cm-1)和358 nm(27 933 cm-1)两个峰相差1 918 cm-1,十分接近 2 000 cm-1,这就证明晶体中的Ce3+仅占据一种阳离子格位,再根据不同配位环境的阳离子半径差异,因此可以得出发射峰是来自于Ce3+取代基质中6h格位上的Ba2+离子产生的。此外,Ba9.91(PO4)6F2∶0.09Ce3+荧光粉在 295 和 313 nm 紫外光激发下,发射光谱也呈现相同的形状。Ba9.48(PO4)6F2∶0.52Tb3+荧光粉的激发光谱和发射光谱如图5(b)所示,在261 nm波长光激发下,得到了Tb3+特征发射谱,包括来自5D4→7FJ(J=6,5,4,3)跃迁发射的487、542、581和620 nm的发射峰以及来自高能级5D3→7FJ(J=6,5,4,3) 跃迁发射的 379、412、434和455 nm的发射峰[26]。监测542 nm波长处最强发射峰,得到Tb3+的激发光谱。Ba9.48(PO4)6F2∶0.52Tb3+的激发和发射均来自宇称禁戒的4f→4f层内跃迁,激发光谱和发射光谱强度都十分的弱,在313 nm紫外光激发下,发射强度表现得更弱。Ce3+→Tb3+的能量传递可以显著提高Tb3+的发光强度,图5(c)是Ce3+、Tb3+共掺杂荧光粉的发射光谱和激发光谱,不难发现,监测Ce3+的358 nm波长发射峰和监测Tb3+的542 nm波长发射峰,得到的激发光谱在250~350 nm范围内除了强度有差异外,两者趋势十分相似,这就暗示着在Ba9.39(PO4)6F2∶0.09Ce3+,0.52Tb3+中存在 Ce3+→Tb3+的能量传递。 激发光谱在313 nm处具有最强的激发峰,在313 nm紫外光激发下,542 nm处绿光发射达到最强。

图 5 Ba9.91(PO4)6F2∶0.09Ce3+(a)、Ba9.48(PO4)6F2∶0.52Tb3+(b)和 Ba9.39(PO4)6F2∶0.09Ce3+,0.52Tb3+(c)的激发光谱和发射光谱Fig.5 PLE and PL spectra of Ba9.91(PO4)6F2∶0.09Ce3+(a),Ba9.48(PO4)6F2:0.52Tb3+(b)and Ba9.39(PO4)6F2∶0.09Ce3+,0.52Tb3+(c)phosphors
为了进一步证明能量传递的发生,图6展示了Ba9.91(PO4)6F2∶0.09Ce3+的 发 射 光 谱 和 Ba9.8(PO4)6F2∶0.20Tb3+的激发光谱,红色区域是两者重叠部分。Ba9.8(PO4)6F2∶0.2Tb3+的激发光谱呈现出许多尖锐的吸收峰,由于4f→4f层内跃迁是绝对禁阻的,激发强度都十分的弱,因此Ba9.8(PO4)6F2∶0.20Tb3+很难被有效激发。 但是 Ba10(PO4)6F2∶Ce3+,Tb3+却可以很容易被313 nm波长紫外光激发发射出Tb3+的542 nm的绿光,绿光强度相对单掺Tb3+的强度有非常大的提高,这归功于 Ce3+→Tb3+的能量传递[27-29]。
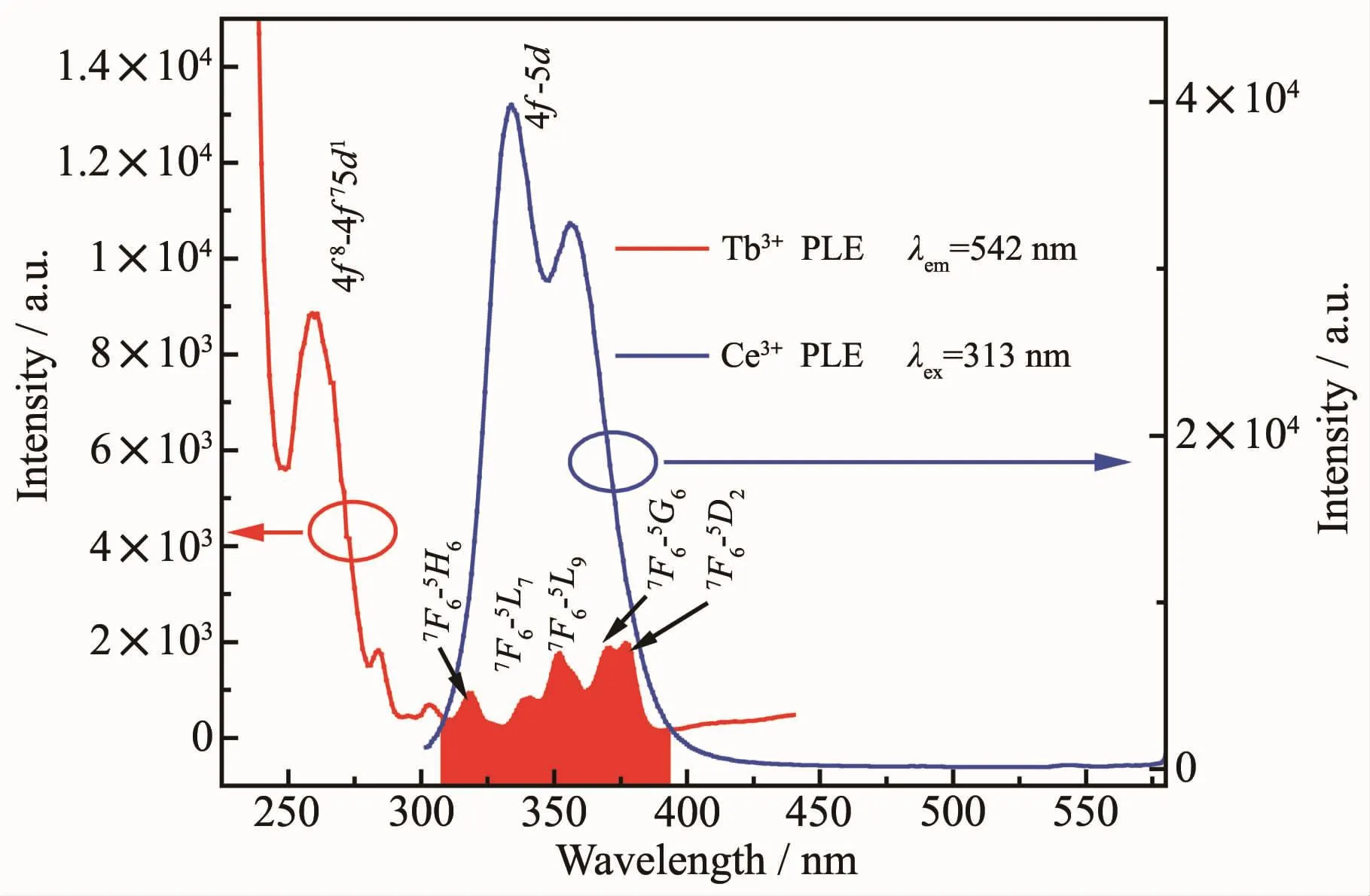
图 6 Ba9.91(PO4)6F2∶0.09Ce3+和 Ba9.8(PO4)6F2∶0.20Tb3+的发射和激发光谱重叠图Fig.6 Overlap plot of emission spectrum of Ba9.91(PO4)6F2∶0.09Ce3+and the excitation spectrum of Ba9.8(PO4)6F2∶0.20Tb3+
由于Ce3+→Tb3+能量传递过程的存在,因此选择在Ba9.91(PO4)6F2∶0.09Ce3+的基础上掺杂不同量的Tb3+。Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+(y=0,0.04,0.12,0.20,0.28,0.36,0.44,0.52)在 313 nm 波长紫外光激发下,发射光谱如图7(a)。随着共掺杂Tb3+浓度的增加,Ce3+的发射强度依次递减,Tb3+的窄带发射谱不断增强,这也证实了Ce3+和Tb3+之间能量传递的事实。图7(b)更为直观地表达了Ce3+发射强度递减趋势。Ce3+→Tb3+的能量传递效率ηT可以通过公式(1)计算[30]:

公式(1)中,τS和τS0分别表示敏化剂Ce3+在不掺杂和掺杂Tb3+时的荧光寿命,IS和IS0分别代表敏化剂Ce3+在不掺杂和掺杂Tb3+时的发光强度,IS/IS0可以近似取代 τS/τS0[31-32]。 随着 Tb3+掺杂量的依次递增,Ce3+发射强度单调降低,当Tb3+的掺杂量达到0.52时,根据公式ηT=1-IS/IS0,能量传递效率达到了0.6,这也说明,Ce3+和Tb3+之间可以产生有效的能量传递。
能量传递机理是研究荧光粉中稀土离子间进行能量传递过程的一个重要内容,能量传递的临界距离RCe-Tb有必要首先进行计算。临界距离指的是激发态的敏化剂离子通过自身的辐射跃迁回到基态的几率PCe与通过能量传递的方式传递给被敏化对象的几率PCe-Tb相等时对应的距离。根据Dexter和Schulman的理论结果,临界距离RCe-Tb可以通过公式(2)计算得到[33-34]。
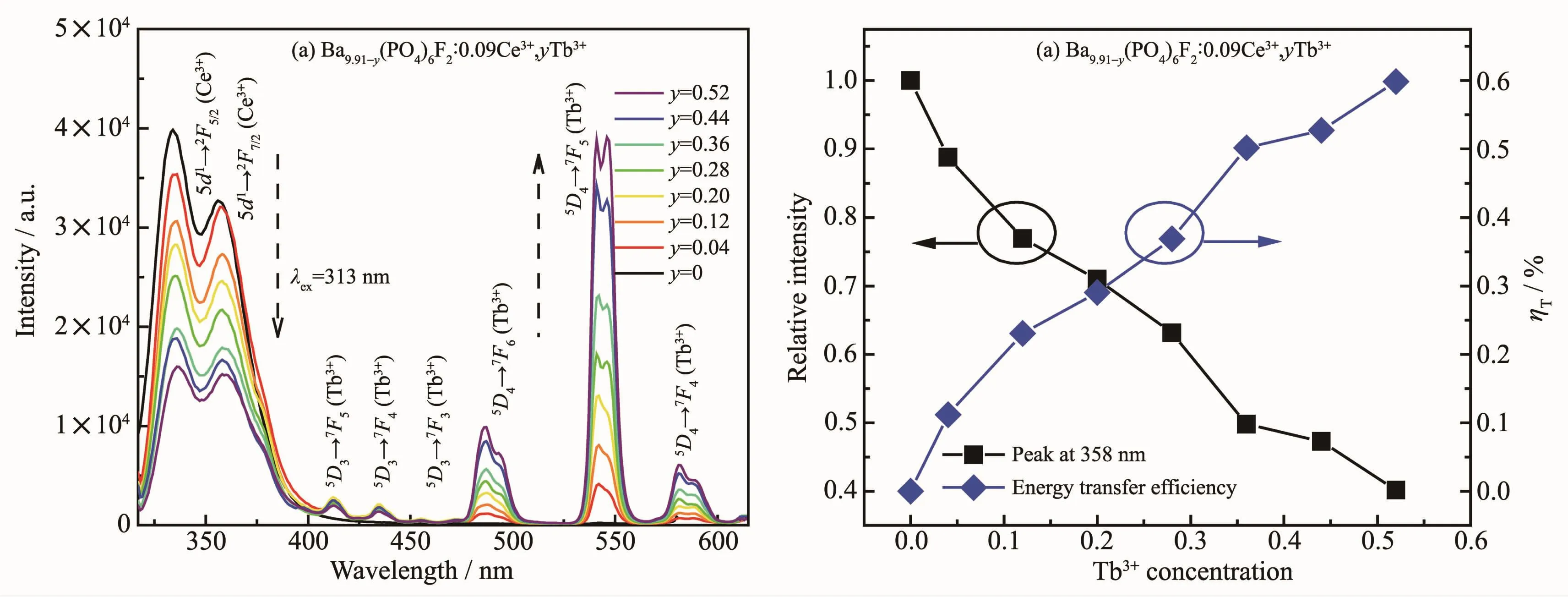
图7 不同Tb3+掺杂量荧光粉Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+的发射光谱 (a);Ce3+的发射强度和能量传递效率与Tb3+掺杂量的关系(b)Fig.7 PL spectra of Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+phosphors with various Tb3+contents(a);Dependence of Ce3+emission intensity and energy transfer efficiency on Tb3+concentration(b)

其中V是单位晶胞的体积;xc是临界浓度,指的是当被敏化剂浓度为某一值,敏化剂的发光强度降低为没有被敏化对象时发光强度的一半时的被敏化剂的浓度与敏化剂的浓度的总和 (可通过图7得到)。N为单位晶胞中可以被稀土离子取代的阳离子的总数,N=Z×6。 对于 Ba10(PO4)6F2晶体,V=0.690 4 nm3,N=6,xc=0.45。 通过公式(2)得到 RCe-Tb=0.79 nm,临界距离RCe-Tb>0.5 nm,因此交换相互作用传递能量的概率低于多偶极交互作用能量传递的概率。
根据Dexter提出的多偶极交互作用能量传递公式以及Reisfeld的近似理论,公式(3)可以用于推导多偶极交互作用能量传递机理[35-37]。

其中IS0是不掺杂Tb3+时,Ce3+的发光强度;IS是掺杂Tb3+时,Ce3+的发光强度;CCe+Tb是 Tb3+和 Ce3+掺杂浓度之和。不同的n值意味着不同的多偶极交互作用机理。当n取6、8、10时,能量传递机理分别是偶极-偶极、偶极-四极、四极-四极交互作用[38]。 如图 8所示,对IS0/IS-CCe+Tbn/3作图,比较线性拟合度R2,发现n=6线性拟合结果最好,因此,可以得出Ce3+→Tb3+能量传递机理为偶极-偶极交互作用。
图 9 为荧光粉 Ba10(PO4)3F∶Ce3+,Tb3+的激发、发射和能量传递过程。Ce3+具有4f和5d两个能级,4f能级可以劈裂成跨度为2 000 cm-1的2F5/2和2F7/2两个能级,5d能级可以劈裂成2~5个能级,最大可以相隔15 000 cm-1。在紫外光激发下,处于4f能级的基态电子被激发,跃迁到5d能级,然后激发态电子以非辐射方式驰豫到5d的最低激发态能级,位于5d激发态能级的电子一部分以辐射发光的形式跃迁回4f基态,一部分以能量传递的方式将能量传递到Tb3+的激发态5D3和5D4,其中部分5D3能级通过交叉驰豫(cross relaxation)方式,驰豫到5D4能级,然后5D3和5D4再跃迁回Tb3+的不同基态,得到系列Tb3+的特征发射峰。交叉驰豫发生在2个Tb3+离子之间,其能级跃迁过程如下:
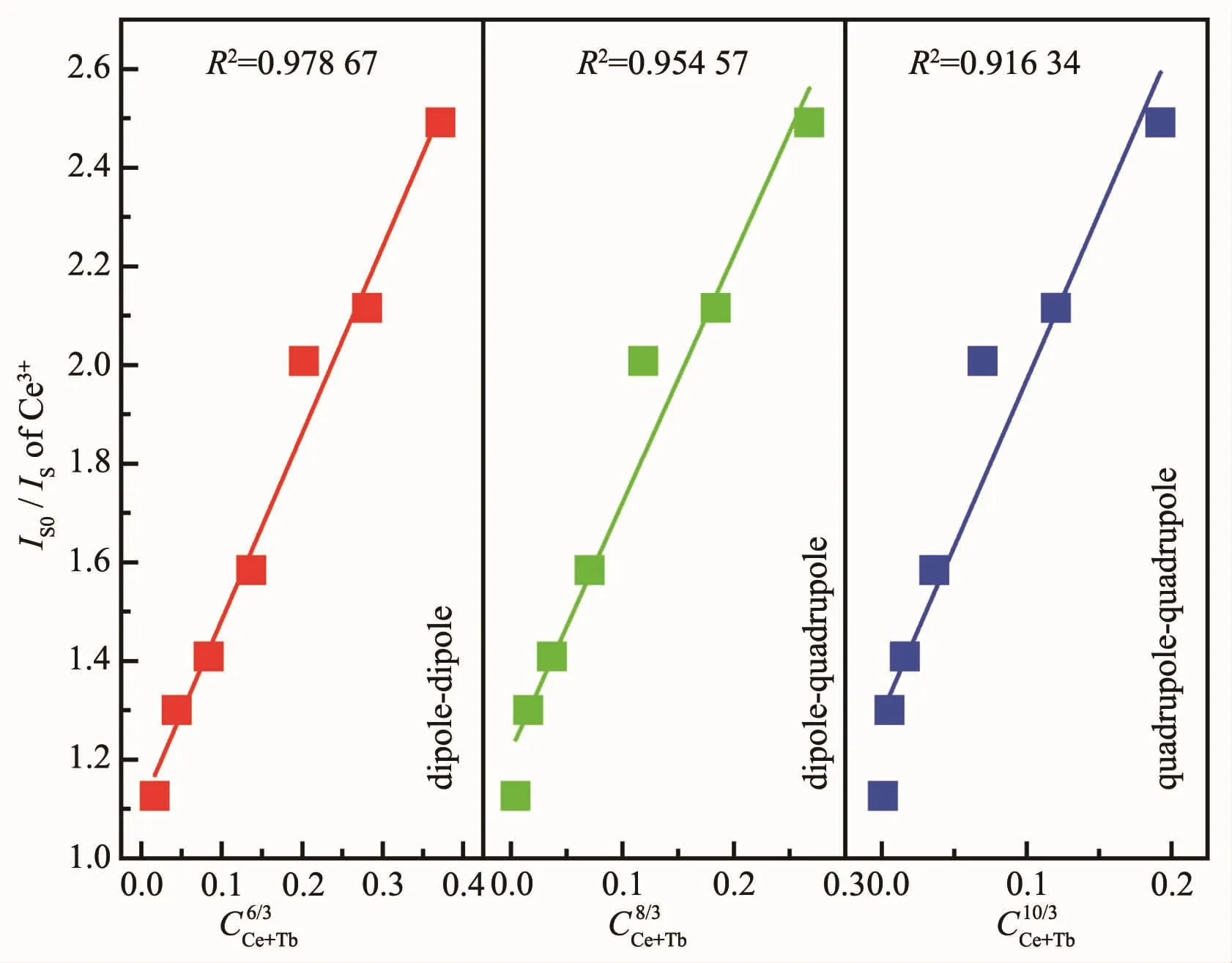
图 8 Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+(y=0,0.04,0.12,0.20,0.28,0.36,0.44,0.52)荧光粉中 Ce3+的 I S0/I S 与C Ce+Tb6/3,C Ce+Tb8/3和C Ce+Tb10/3的关系曲线Fig.8 Dependence I S0/I S of Ce3+on C Ce+Tb6/3,C Ce+Tb8/3 and C Ce+Tb10/3 in Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+(y=0,0.04,0.12,0.20,0.28,0.36,0.44,0.52)phosphors


图9 Ba10(PO4)6F2∶Ce3+,Tb3+荧光粉的电子跃迁和能量传递机理的能级图Fig.9 Energy-level diagram showing the electronic transition and energy transfer mechanism of Ba10(PO4)6F2∶Ce3+,Tb3+phosphors
交叉驰豫只有部分激发能参与传递,激发态的Tb3+离子发生5D3→5D4的跃迁,将5D3-5D4之间能量传递给基态Tb3+离子,基态Tb3+离子发生5F6→5F0的跃迁。由于交叉驰豫过程发生在2个离子之间,因此它与稀土离子掺杂浓度有关,只有当浓度较高时,交叉驰豫才会占据主导地位。不难发现,交叉驰豫的发生可以抑制高能级(5D3)跃迁发射过程,对于提高低能级(5D4)跃迁的绿光发射具有积极作用[39]。这也是图7中在487、542、581 nm处的发射不断增强,而在412、434和455 nm处的发射却没有增加的原因。
2.4 Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+的 CIE 色度图
在313 nm紫外光激发下,通过对发射光谱进行计算,得到 Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+(0≤y≤0.52)的 CIE(Commission International de L′Eclairage,CIE)色度图(图10),对应色坐标如表2。图中Tc表示颜色温度,即色温。
随着Tb3+掺杂量的不断增加,发光颜色逐渐由蓝色区域(0.149 4,0.045 1)过渡到绿色区域(0.280 1,0.585 3)。由于能量传递,导致了发光颜色和色坐标的变化,能够为紫外光激发的WLED提供绿色光谱部分,在显示方面也具有潜在的应用。
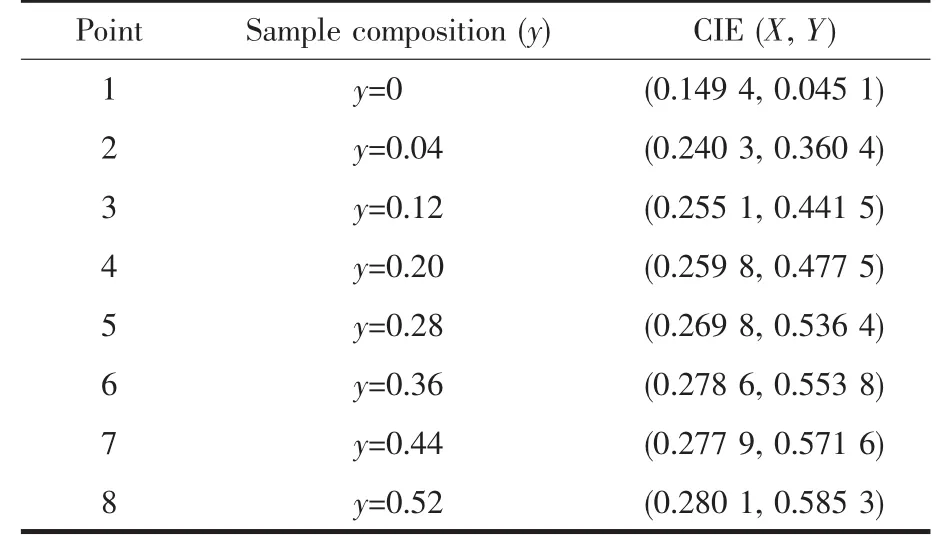
表 2 Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+样品的 CIE 色坐标Table 2 CIE chromaticity coordinates for Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+samples

图 10 Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+荧光粉在 313 nm激发下色度坐标图Fig.10 CIEchromaticity diagram of the Ba9.91-y(PO4)6F2∶0.09Ce3+,y Tb3+phosphors under 313 nm excitation
3 结 论
利用高温固相法合成了一系列具有磷灰石结构的新型荧光粉 Ba10(PO4)6F2∶Ce3+,Tb3+。XRD 和 SEM 分析表明,样品不含杂相,样品颗粒呈不规则形貌,尺寸在 2~5 μm 之间。 荧光粉 Ba10-x(PO4)6F2∶x Ce3+的最佳Ce3+掺杂量为0.09,发射峰335 nm(29 851 cm-1)和358 nm(27 933 cm-1)是Ce3+取代了基质中6h格位上的Ba2+产生的。 单掺 Tb3+的荧光粉 Ba10-y(PO4)6F2∶y Tb3+不能被有效激发。Ce3+和Tb3+共掺杂荧光粉Ba10(PO4)6F2∶Ce3+,Tb3+,由于存在 Ce3+→Tb3+的能量传递,Ce3+的发光强度随着Tb3+掺杂量的增加而单调降低。根据样品的光谱特性,Ce3+掺杂量为0.09,Tb3+掺杂量为0.52时,能量传递效率可以达到60%。能量传递机理是偶极-偶极相互作用。CIE色度图分析发现,随着Tb3+掺杂量的增加,发射光谱色坐标逐渐从蓝色区(0.149 4,0.045 1)过渡到绿色区(0.280 1,0.585 3),绿光色纯度不断提高。作为紫外光激发的基色荧光粉,在显示和照明领域具有潜在的应用。

