煤自燃程序降温特性参数的实验研究
王晓东
(陕西陕煤彬长矿业有限公司,陕西咸阳 712000)
0 引言
煤炭是我国的主要能源,在我国一次能源生产和消费结构中占70%左右[1],煤炭在我国能源结构中的这种主体地位未来几十年不会改变。但我国煤炭开采的自然条件相对较差,各种灾害时有发生,严重影响了安全生产,煤层自燃灾害就是其中之一。
近年来,我国广泛采用综采放顶煤开采技术和瓦斯抽放技术,造成采空区遗留残煤多、漏风严重,使得煤自然发火频繁。我国国有重点煤矿每年因自燃火灾而封闭的工作面超过100个[2],大量的煤炭因火区而冻结,合理的开拓部署和开采顺序常被打乱,为矿井带来巨大的经济损失和重大的事故隐患。
煤自燃不仅烧毁大量的煤炭资源,造成巨大的资源损失和环境污染,而且产生有毒有害气体,严重危及井下人员的生命安全。当前国内外对煤自燃特性的研究大多集中于升温阶段,如王长安[3]研究了煤在低氧气体积分数条件下的煤燃烧特性,金永飞[4]等对煤自燃高温贫氧氧化燃烧特性参数进行了试验研究,郑学召[5]等研究了水分含量对煤自燃发火特性参数的影响,邓军[6]等对不同变质程度煤二次氧化自燃的微观特性进行了研究,秦荣宏[7]等研究了地温和湿度对采空区特厚遗煤自燃影响规律,马砺[8]等研究了粒度对煤自燃极限参数的影响,鲜少有对降温过程中煤自燃过程特性的研究。文中通过程序升温和降温实验,研究煤自燃耗氧速率、含氧气体及含氢气体的变化规律,在一定程度上可以对煤矿现场实施煤自燃灭火有重要的理论依据和指导意义。
1 实验装置及实验条件
采用XK系列煤自燃程序升温实验系统,模拟分析煤自燃的升温和降温过程。实验主要有气路、控温箱和气样采集分析3部分组成,如图1所示。
选用黄陵二号煤矿煤样,其煤种为弱粘煤,煤样的工业分析数据见表1。将原煤破碎成:0~0.9 mm、0.9~3 mm、3~5 mm、5~7 mm 和7~10 mm 的5种粒径,取5种粒径煤样各200 g,组成1 000 g混合煤样。实验条件见表2。

图1 煤自燃程序升温实验示意图

表1 煤样的工业分析和元素分析

表2 实验条件
2 实验结果及分析
2.1 耗氧速率分析
在程序升温和程序降温的实验中,O2体积分数变化曲线如图2所示。耗氧速率与煤温变化曲线,如图3所示。
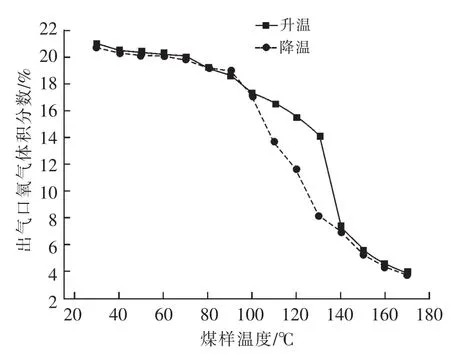
图2 出气口氧气体积分数曲线
由图2、3可知:100℃之前,升温和降温的耗氧速率基本一致;100~140℃之间,程序升温出气口氧气体积分数大于程序降温出气口氧气体积分数,降温过程耗氧速率大于升温过程耗氧速率;140℃之后,降温过程耗氧速率略大于升温过程耗氧速率,变化趋势相似。
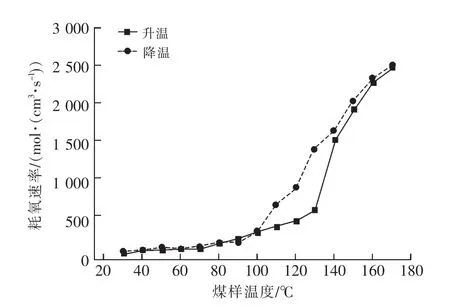
图3 耗氧速率曲线
70℃之前,煤的耗氧速率特别缓慢;70~90℃之间,耗氧速率逐渐增加;90℃以后耗氧速率迅速增加,氧气体积分数迅速减小;150℃后,氧气体积分数降至5%以下,煤氧复合反应维持在较高的耗氧量状态,且耗氧量继续增加,导致耗氧速率呈缓慢上升趋势,氧气体积分数缓慢降低。这说明在煤体温度较高时,煤氧复合反应在贫氧条件下可继续进行。
2.2 含氧气体产生规律分析
CO产生规律:在程序升温和程序降温实验过程中,随煤温的增加CO产生量的变化曲线,如图4所示。

图4 CO产生量随煤温变化曲线
由图4可知,降温过程中,随温度的降低CO产生量整体呈下降趋势;90℃之前,下降趋势较缓;60℃之前,下降趋势近似水平。说明温度小于60℃时,煤氧复合反应几乎不再进行。30~60℃之间,升温和降温过程CO产生量基本相同,但主要来源不同。升温过程CO主要是成煤过程中吸附或游离于煤结构表面和空隙内的CO脱附产生。降温过程CO主要是高温段煤氧反应生成的CO吸附或游离于煤结构表面,然后逐渐解析脱附产生。60~170℃之间,降温过程CO产生量大于升温过程CO产生量,此温度区间范围内CO主要是由煤氧复合反应生成。150℃之后,降温过程和升温过程CO产生量之差逐渐减小。
CO2产生规律:在程序升温和程序降温实验过程中,随煤温的增加CO2产生量的变化曲线,如图5所示。
由图5可知,降温过程中,CO2产生量整体呈下降趋势;80℃之前,CO2产生量随煤温的降低而减小的趋势变缓;降温过程CO2产生量大于升温过程CO2产生量。因为经过燃烧的煤,其结构发生变化,分子间空隙增大有利于氧气流动,再次氧化时氧与煤分子接触更加充分,氧化还原反应更强烈。
2.3 含氢气体产生规律分析
含氢气体 CH4、C2H6、C2H4产生量随煤温变化曲线如图6、图7和图8所示。
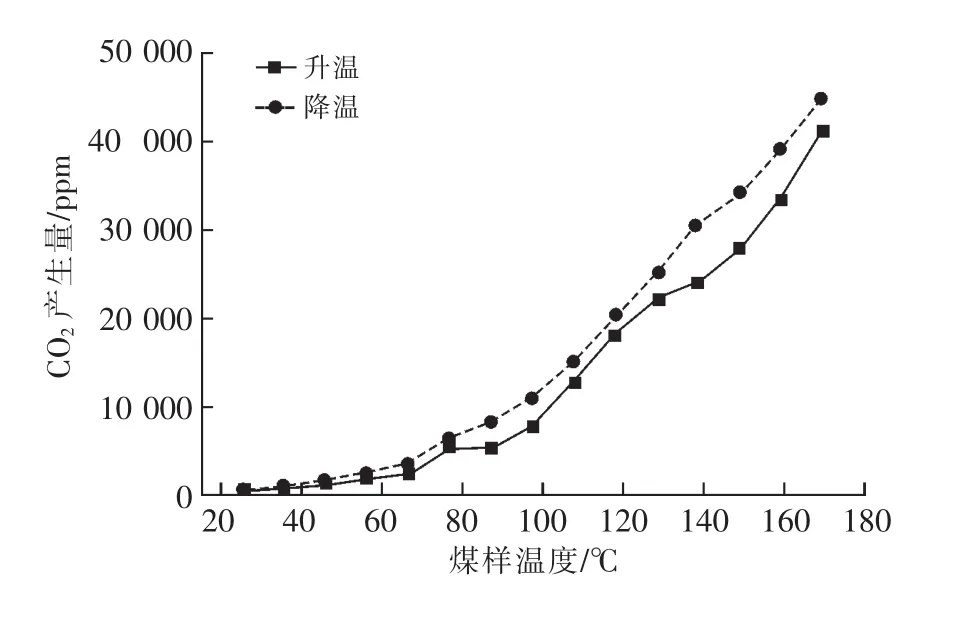
图5 CO2产生量随煤温变化曲线

图6 CH4产生量随煤温变化曲线
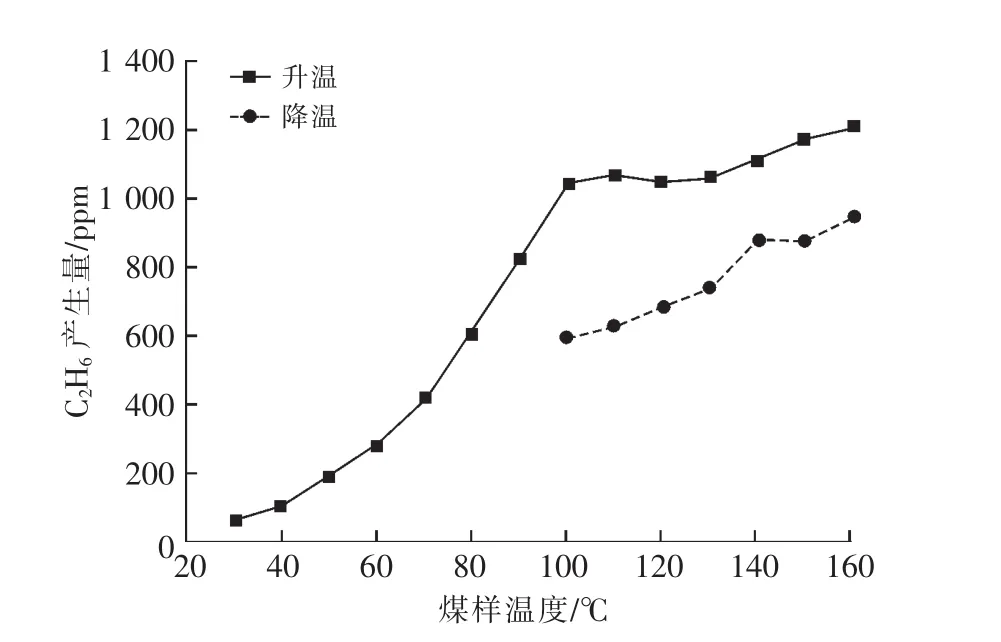
图7 C2H6产生量随煤温变化曲线
由图6可看出:程序降温阶段,CH4产生量随温度的降低而逐渐减少;120~90℃之间,CH4减小速率较缓慢;90℃以后不再产生CH4。降温阶段CH4产生量大于升温阶段CH4产生量。降温过程中CH4是由煤氧化热解产生的。升温过程中低温阶段(30~90℃),CH4来源于煤中CH4的脱附解析,之后随温度的升高,煤结构发生热解反应,煤分子中的侧链(甲基侧链、脂肪侧链)和桥键等裂解断裂生成CH4[9-11]。因为升温过程中产生的侧链和桥键还没有完全热解为CH4,紧接着降温过程又有新的侧链和桥键产生。所以相同煤温时,降温过程中CH4产生量大于升温过程中CH4产生量。在90℃附近时,煤温不足以提供侧链和桥键热解所需的能量,故不再产生CH4。
由图7可以看出:降温过程中,C2H6产生量随煤温的降低而减小;煤温降到100℃之后,不再产生C2H6;相同温度,降温时C2H6的产生量小于升温时C2H6的产生量;煤体本身吸附一定量的C2H6;160℃是C2H6产生量的一个突变拐点,与文献[12]研究结果一致。
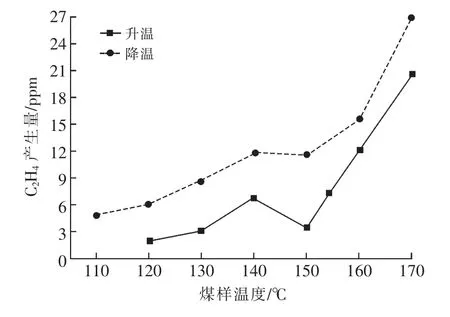
图8 C2H4产生量随煤温变化曲线
由图8可看出:降温过程中,C2H4产生规律与C2H6产生规律相似,这是因为两种气体产生机理相同,均为煤结构中游离相脂肪烃上自由基裂解和苯环上脂肪烃侧链断裂生成[13],因此也解释了降温时C2H6产生量低于升温过程,而C2H4则相反。升温时C2H4出现温度为120℃,而降温时C2H4消失温度为110℃,可能是因为自燃后煤的微观结构发生变化,使C2H4的生成较容易。
3 结论
(1)煤样在降温过程中,各种气体产物产生量均随温度的降低而减小。
(2)含氢气体出现和消失时对应的温度不同。
(3)煤自燃降温和升温过程均呈现出明显的非线性特征,但降温与升温阶段并不重合,即煤自燃的降温过程和升温过程具有非对称性,这种现象称之为“滞后”效应。

