威灵仙中的三萜皂苷类成分及其抗关节炎作用机制的研究进展
郑佳逸,辛贵忠,刘丽芳
(中国药科大学,天然药物活性组分与药效国家重点实验室,江苏 南京 210009)
威灵仙为毛茛科铁线莲属植物威灵仙ClematischinensisOsbeck)、棉团铁线莲(ClematishexapetalaPall.)或东北铁线莲(ClematismanshuricaRupr.)的干燥根和根茎[1],具有祛风除湿、止痛通络等功效。其单方和复方制剂在临床上都有广泛的应用,主要可用于风湿痹痛、肢体麻木,筋脉挛急、屈伸不利等症状,具有抗菌消炎、止痛解痉、抗肿瘤、降血压、抗动脉粥样硬化及心肌梗死等药理活性[2-4]。威灵仙所含化学成分比较复杂,主要包括三萜皂苷类[5-6]、黄酮及多元酚类[7-8]、内酯和生物碱类[9-10],此外还有一些多糖类成分[11-12]、挥发性成分[13-14]、以及原白头翁素[15]和白头翁素[16]等。其中,三萜皂苷已被证实是威灵仙药材的主要活性成分,亦是威灵仙药材质量控制的关键指标。因此,本文将介绍我国药典收载的不同来源威灵仙药材中三萜皂苷类成分的分布情况,同时对其治疗关节炎的作用机制进行概述,为科学利用威灵仙药材、开展威灵仙药材的成分分析、并对三种威灵仙药材进行基原和真伪鉴别提供依据。
1 皂苷类化学成分的研究
国内众多学者对《中国药典》收载的三种不同来源威灵仙中的三萜皂苷类成分进行了一系列分离纯化研究,从威灵仙中分离得到40余种三萜皂苷类成分,从东北铁线莲中分离得到17种三萜皂苷类成分,但是关于棉团铁线莲中三萜皂苷类成分的报道较少,仅找到了7种并且这7种都是与其他两种所共有的成分(表1)。此外,从威灵仙和东北铁线莲中分离得到的三萜皂苷类成分在种类及含量上均有所不同[2, 17],表明三种基原威灵仙药材中的三萜皂苷类成分存在着一定的差异。
从化学结构上看,根据苷元类型大致可将威灵仙中的三萜皂苷分为四类,包括齐缴果酸型(oleanolic:Ole)、常春藤皂苷元(hederagenin:Hed)、表常春藤皂苷元(epihederagenin:Epi)和丝石竹苷元(gypsogenin:Gyp)。大部分的威灵仙三萜皂苷苷元为Ole和Hed型,少数为Epi和Gyp型[3, 18]。这四类皂苷元的基本骨架都为齐墩果烷型,只是在C-23和/或C-24位取代的基团有所差别。Hed型、Epi型和Gpy型皂苷元的取代方式分别为C-23处连有—OH,C—24处连有—OH和C—23处连有—C=O。而Ole型皂苷元的C-23和C-24仅连有—CH3(图1)。
威灵仙三萜皂苷类成分侧链糖的取代种类多样,其中大部分在C-3和C-28位均有糖链取代,少数只在C-3或C-28位取代单糖链。此外,有一些皂苷还有异阿魏酰基(Isoferuloyl, IF),对甲氧基桂皮酰基(P-methoxy cinnamyl, MC)和3,4-二甲氧基桂皮酰基(3,4-dimethoxy cinnamyl, DMC)取代在C-28位的糖链上,且这几种基团常连接在位于糖链近末端的葡萄糖基团上[24-25]。糖链中结合的糖主要包括有鼠李糖(Rha)、核糖(Rib)、葡萄糖(Glc)、阿拉伯糖(Ara)、半乳糖(Gal)和木糖(Xyl)[3,24-25](图2,表1)。
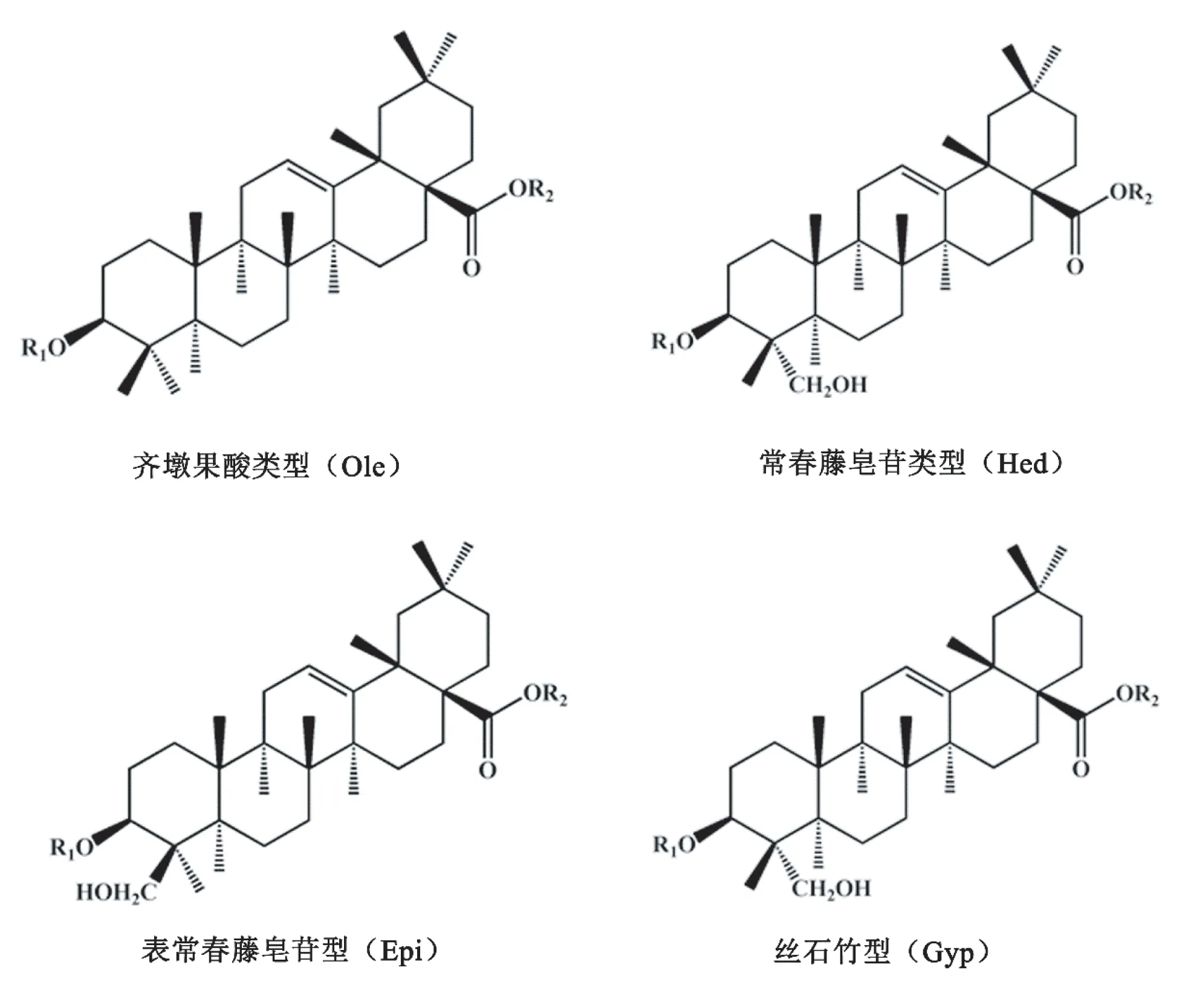
图1 威灵仙三萜皂苷四种苷元结构式

表1 三种威灵仙所含三萜皂苷类成分

续表1

续表1
注:A:具有单个糖链的皂苷;B:具有两个糖链但不包含特殊取代基的皂苷;C:具有特殊取代基的双糖链皂苷。W:威灵仙ClematischinensisOsbeck.;D:东北铁线莲ClematismanshuricaRupr.;M:棉团铁线莲ClematishexapetalaPall.
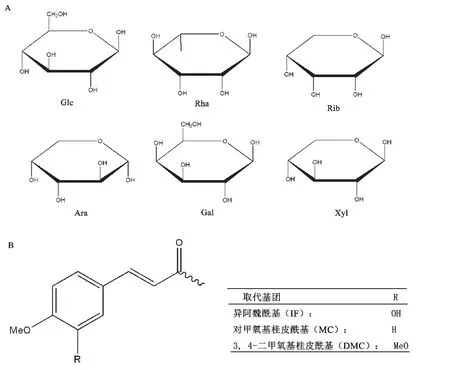
图2 威灵仙三萜皂苷糖链(A)和取代基(B)结构
2 威灵仙皂苷类成分治疗关节炎的机制研究
2.1 抗类风湿关节炎(RA)的作用机制研究
尽管威灵仙治疗关节炎已有数千年的临床应用基础,但其作用机制尚不明确,三萜皂苷类成分作为其发挥药效的活性物质,国内外众多学者对其抗关节炎的药理作用机制进行了一系列的探索研究。
2.1.1 抑制细胞因子信号转导通路的激活
大量研究表明RA疾病的发生发展与多种细胞因子的表达密切相关,如一系列白细胞介素(IL-3、IL-6、IL-1β)、肿瘤坏死因子α(tumor necrosis factor-α, TNF-α)和一些干扰素(IFN-γ)等[33-35]。而与JAK激酶家族受体相关的酪氨酸激酶已被证实参与RA的过程,一旦被激活,JAKs便会募集并激活STATs,当STAT被激活后会诱导细胞因子的转录[36]。在RA中,STAT的激活与滑膜炎症,滑膜成纤维细胞(FLSs)的存活都密切相关[37]。邓龙飞[38]等发现灌胃给予威灵仙总皂苷可有效缓解佐剂性关节炎(AA)的足趾肿胀和体重的减轻,并且可以有效改变滑膜组织炎细胞浸润和组织增生。并且分别从转录水平和蛋白水平检测了滑膜细胞中JAK2、信号转导子和转录激活子STAT3的mRNA水平、磷酸化JAK2(p-JAK2)和磷酸化STAT3(p-STAT3)的蛋白表达水平,得到的实验结果提示威灵仙总皂苷可能通过抑制JAK2/STAT3信号通路的激活来达到抗炎作用。在细胞内众多的信号通路中,磷酸肌醇3-激酶/蛋白激酶B(phosphoinositide 3-kinase/protein kinase B,PI3K/Akt)对于细胞因子网络的诱导和放大发挥着重要作用[39]。Akt作为PI3K的下游,一旦被激活可以发挥抑制细胞凋亡的作用[40]。已有研究表明PI3K/AKT信号通路的激活会促进滑膜增生和TNF-α的分泌[41-42]。基于此,Wang等[43]研究了从威灵仙提取的三萜皂苷AR-6对胶原诱导的关节炎(CIA)大鼠体内PI3K/AKT信号通路的干预作用。病理切片显示AR-6有效的缓解关节炎滑膜增生和炎性细胞浸润。根据滑膜组织免疫组化的结果发现,相比于模型组AR-6可以减少TNF-α的产生,并且抑制PI3K和磷酸化Akt的表达。以上研究结果表明AR-6发挥抗类风湿关节炎活性的机制与PI3K/Akt信号通路相关。相似的,NF-κB作为RA中研究最多的转录通路,主要调节促炎因子的水平和抗凋亡相关通路[43],因此也被广泛的应用于治疗RA的药物机制[44-46]。研究发现与CIA模型组大鼠相比,AR-6给药组大鼠的血清中TNF-α、IL-1β水平均有所下降,同时NF-κB p65的表达明显受到抑制。而AR-6处理的大鼠滑膜组织中TNF-α、COX-2和p65的表达都有所降低。提示AR-6对于CIA大鼠具有潜在的抗炎作用,并且这种作用机制可能与NF-κB信号通路受到抑制相关[47]。
2.1.2 抑制氧化应激
细胞因子的大量产生可以通过上调ROS的释放进而引发氧化应激,反过来又可以再调节转录因子的表达, 因此细胞内异常的氧化还原状态将会诱发促炎因子的产生[48-49]。有研究报道在TNF-α刺激的人脐静脉内皮细胞中,从东北铁线莲中提取出的灵仙新苷(C-AR)可以降低TNF-α诱导的 VCAM-1和ICAM-1的转录和表达。同时发现了C-AR还可以抑制p65的转位和IκBα的磷酸化水平。此外,C-AR对TNF-α刺激的细胞内降低的O2和H2O2水平都有回调, 并可以降低NOX4和NADPH氧化酶的活性。但值得一提的是,C-AR并没有表现出直接的清除活性氧的能力。这些实验结果说明AR可以通过调节依赖于NF-κB信号通路的NADPH氧化酶的活性来降低VCAM-1和ICAM-1的表达[50]。
2.1.3 免疫抑制作用
RA疾病发生过程中的另一特点是机体免疫紊乱,因此免疫疗法也在逐渐进入大众视线并有望得到较好的临床效果[51]。在关节炎自身免疫的发生发展过程中Treg和Th17亚基呈现一种相反的免疫调节作用,故调节Treg和Th17亚基的平衡对于治疗关节炎是非常重要的[52-53]。目前已有研究证明C-AR在小肠部位有较好的膜透过性,可以通过被动扩散进入肠粘膜[54]。基于此,Xiong[55]等人推测C-AR治疗RA的机制可能与调节肠粘膜免疫系统相关。利用AA大鼠模型进行实验发现,C-AR的免疫抑制作用主要是通过上调 PPS 淋巴细胞中CD4(+)CD25(+)Foxp3(+)Treg细胞的百分比,并诱导ConA-来激活PPs淋巴细胞产生抑炎的细胞因子(IL-10),同时下调IL-17A和TNF-α的水平;此外,C-AR还具有抑制Th17细胞表型的活性,从而调节Treg细胞和Th17的比例失衡,最终达到调节关节炎中的免疫反应的作用。
2.1.4 抑制纤维化
除了炎症反应、免疫反应和氧化应激,有研究提出滑膜组织纤维化也是RA发病过程中一个重要事件,而纤维原细胞的激活和细胞外基质重塑是纤维化发生的主要诱因[56-57]。Li[58]等人最近详细探讨了C-AR抑制RA滑膜组织纤维化的作用机制,揭示了关节炎炎症反应和纤维化之间的关系。研究结果表明,缺氧条件下琥珀酸堆积会上调缺氧诱导因子(HIF-1α)的表达,进而诱导NLRP3炎症小体的激活,最终加剧CIA大鼠滑膜组织的炎症反应和纤维化。而C-AR可以通过减轻滑膜缺氧降低琥珀酸的堆积,从而抑制NLRP3炎症小体的激活来达到抑制炎症和纤维化的作用。
2.1.5 抑制NO的产生
NO是RA发生发展过程中的另一个促炎因子[59-60]。目前已有研究在RA患者体内检测到过高的NO浓度,并证实了其与RA炎症反应的联系[60-61]。Sun等[62]分别利用AA大鼠、腹腔巨噬细胞和TNF-α刺激的滑膜细胞考察了AR-6的体内体外抗炎活性及机制。结果证明AR-6可以抑制体内体外IL-1β和IL-6这些促炎因子的分泌。值得一提的是,AR-6对AA大鼠血清中iNOS水平有抑制作用,并且在腹腔巨噬细胞和TNF-α刺激的滑膜细胞中AR-6可以减少 NO的产生。
2.2 抗骨关节炎(OA)作用机制研究
OA是一种慢性的关节退行性疾病,以关节软骨侵蚀为特点[63]。尽管目前OA的发病机理和病因尚不明确,但是可以确定的是炎症因子引起的软骨损伤是其发病的关键原因之一[64-65]。因此,威灵仙三萜皂苷治疗OA的作用机制研究主要围绕软骨保护展开。①抑制软骨破坏相关酶的表达:Hsieh等[66]提取了人原代软骨细胞,利用LPS刺激后,发现威灵仙中的丙酮部位的皂苷提取物(CC6)通过抑制COX-2的表达可以发挥前列腺素E2(PGE2)和基质金属蛋白酶(MMP)抑制作用,提示CC6可以通过抑制软骨破坏相关酶的表达来发挥软骨保护作用。②抗凋亡和线粒体损伤:Wu等[67]利用硝普钠刺激兔原代软骨细胞释放NO,并用不同浓度的威灵仙总皂苷提取物处理24h后,检测了细胞的核形态、细胞凋亡率、线粒体功能和caspase-3的活性。结果显示,威灵仙皂苷提取物可以防止硝普钠诱发的软骨细胞凋亡。此外,硝普钠导致的细胞线粒体膜势能的去极化和caspase-3的激活都能被威灵仙皂苷提取物阻断。基于以上结果可以推测,威灵仙皂苷保护关节软骨细胞的机制可能与抑制线粒体损伤和激活caspase-3发挥的抗凋亡作用相关。③防止细胞外基质降解:Wu等[68]在另外一项研究中通过给关节腔内注射谷氨酸钠碘乙酸(MIA)建立大鼠骨OA模型,发现威灵仙总皂苷提取物可以抑制MIA引起的软骨损伤和蛋白聚糖(PG)降解,而阳性药双氯芬酸仅呈现出微弱的缓解作用。这说明威灵仙皂苷提取物可以通过防止细胞外基质降解和软骨细胞损伤起到保护关节软骨的作用。
3 威灵仙皂苷类成分体内代谢研究
威灵仙作为传统中药,通常以口服用药为主,进入机体后易受到胃肠道的影响,如酸碱度、肠道菌群及各种酶类的影响。威灵仙主要活性成分为总皂苷,当其在机体内发生代谢转化后,生物利用度会明显降低。总皂苷进入生物系统后,在肠道一系列酶的作用下(包括β葡糖苷酶和酯酶)[69-70],发生I相代谢反应水解脱去葡萄糖、鼠李糖等糖基,形成不同种类的总皂苷代谢产物,故其代谢产物也可能是药效成分[71]。此前已有文献表明人参皂苷Rb1的代谢产物Compound K比起原型有更强的生物活性[72-73]。研究威灵仙总皂苷在生物体内的药物代谢变化,揭示原型成分与代谢成分之间的代谢关系、转化规律,对威灵仙的药效及作用机制研究将起到重要意义。
4 结 语
本文首先对药典收载的三种基原威灵仙中的三萜皂苷类成分的分布进行了综述,一共总结出56中三萜皂苷类成分,其中有45种存在于威灵仙中,17种存在于东北铁线莲中,还有7种存在于棉团铁线莲中。其中,属于威灵仙特有的三萜皂苷有32种,属于东北铁线莲特有的三萜皂苷有11种。此外,并没有找到棉团铁线莲种特有的三萜皂苷。因此,对这三种基原威灵仙的三萜皂苷类成分进行更系统的化学成分分离和结构鉴定依然是非常有必要的。
三萜皂苷作为威灵仙发挥抗关节炎活性的主要成分,其具体的作用机制尚不明确,传统的研究机制主要集中于软骨保护和抑制细胞因子的转导,近几年研究发现的抑制氧化应激、抑制纤维化和免疫调节等作用机制为其临床应用提供了新的依据。此外,针对威灵仙皂苷的体内代谢行为研究发现其生物利用度极低,进而限制了其新药开发的进程。因此,针对其体内代谢产物的研究或进行结构修饰对更好的发挥其药效具有很大的意义。

