医学科技颠覆性技术展望
李永洁 ,杨俊涛 ,杜建
(1. 中国医学科学院医学信息研究所,北京 100005;2. 中国医学科学院,北京 100005)
一、前言
随着医学与现代信息技术、材料科技等技术的深度交叉融合,极大地促进了医学科技的发展,基因组学、合成生物学、组织工程与干细胞技术等现代医学技术成果越来越快地应用于临床,正在使疾病诊断和治疗模式发生革命性的变化。党的“十八大”以来,我国卫生与健康事业取得巨大成就,在基础研究、疾病防控、新药创制等医学与健康科技领域取得了一系列创新成果,科技创新对卫生与健康事业发展的支撑作用逐步显现[1]。医学科技创新是推进健康中国、科技强国建设的核心动力。
一般认为,颠覆性技术是指在性能或功能上有重大突破,可能是全新技术,或是基于现有技术的跨学科、跨领域的创新型应用。颠覆性技术会使一个或多个相关行业发生翻天覆地的变化,使社会生产结构、人们的生活发生重大的变化。医学领域内的颠覆性技术自有其内涵特征,是指基于医学生物领域的新原理、新发现,交叉融合现有多领域(医学、信息、互联网)的先进技术,能够从根本上打破原有模式、改变原有技术路线并对原有技术体系和应用系统产生颠覆性效果的技术。医学领域内的颠覆性技术不仅将极大地影响人类健康寿命、思维方式和生活方式,还将助推生物医药、医疗器械产业成为国家战略性新兴产业。
每一次医药卫生领域科学技术的重大突破,或引发形成新理论,或建立新方法,或变革诊疗手段。当前,新的科技革命正在孕育之中,医学科技不断发展,催生出了转化医学、系统医学、精准医学、个体化医疗、智慧医疗等一系列新的医学思想和理念,不断出现的创新成果成为疾病防治和健康管理不可或缺的重要支撑。
二、医学科技颠覆性技术发展态势
以人工智能及生物大数据、基因组学新技术、合成生物技术、基因编辑(CRISPR/Cas9,clustered regulatory interspaced short palindromic repeats/CRISPR-associated protein 9)、肿瘤免疫治疗等技术为核心的技术突破,推动了以生命科学为支撑的医学科技发生深刻改革。
(一)肿瘤免疫治疗
随着对肿瘤微环境和肿瘤逃逸机制的深入了解,调动机体免疫系统去抵御肿瘤逐渐成为一种新的研究方向。免疫检查点抑制及免疫检查点阻断和免疫细胞疗法在肿瘤界中炙手可热。目前,国外已上市的PD-1/PD-L1抑制剂、CTLA-4单克隆抗体注射液等五种新药均属此类,覆盖肿瘤类型多达十余种[2]。2018年10月公布的诺贝尔生理学或医学奖授予了美国和日本的免疫学家,以表彰他们在癌症疗法以及免疫负调控的抑制领域所做出的贡献。
2017年是肿瘤免疫治疗快速发展、成熟的关键年,美国食品及药品监督管理局(FDA)批准了两种靶向CD19的嵌合抗原受体细胞(CAR-T)疗法,是肿瘤学的又一里程碑。CAR-T主要原理是,从患者体内分离获取的T淋巴细胞,利用基因工程技术进行基因修饰使其识别CD19,再将扩增好的CAR-T细胞回输到病人体内。使用这种方法治疗顽固性B细胞恶性肿瘤的患者已经表现出卓越的临床疗效。
Clinical Trials网站数据显示,截至2018年9月30日,美国关于CAR-T疗法的临床试验数量为243项,中国相关临床试验数量为195项(东亚地区为205项),其试验数量远高于亚洲的其他国家(日本6项)和欧盟国家(98项)。药智数据库数据显示,目前,国内生物医药公司有逾19款CAR-T产品向中国国家食品药品监督管理总局药品审评中心申报临床应用。
(二)基因编辑技术
基因编辑技术能够对基因组及其转录产物进行定点修饰或者修改,高效精确的基因工程技术对于发展基因治疗和核酸诊断、建立细胞和动物疾病模型具有极为重要的价值,为生物学研究及医学治疗领域带来革命性的变化。CRISPR/Cas9技术出现后,更是引起了世界广泛的关注,曾两次荣登《Science》“年度十大科学突破”。
目前,首批CRISPR/Cas9基因编辑临床试验已经在美国、中国和欧洲开展起来。早在2016年10月,中国科学家启动了利用CRISPR基因编辑技术的人体临床试验,这项由四川大学主导的I期临床试验针对的是晚期非小细胞肺癌患者。2018年1月,美国宾夕法尼亚大学公示其要开展的I期临床试验——在黑色素瘤等患者体外使用CRISPR技术编辑T细胞中的几个关键基因,包括程序性死亡受体-1(PD-1),试验目标是确定注射的安全剂量,并评估制造基因修饰T细胞的操作可行性。
近年来,在全球已有的四例胚胎编辑实验中,中国科学家均有参与。世界首例以及第二例利用基因编辑进行胚胎编辑实验都是由中国学者团队主导进行。2015年,中山大学黄军就教授团队[3]利用CRISPR/Cas9技术,将胚胎中地中海贫血症的相关基因敲除。2016年,广州医科大学范勇团队[4]利用CRISPR/Cas9技术对人类受精卵进行基因编辑,以抵制艾滋病病毒感染。2017年,《Nature》公布了美国首例基因编辑人类胚胎的研究[5],该项研究来自于俄勒冈健康与科学大学,研究者中同样有中国科学家的身影。其利用CRISPR/Cas9技术在人类早期胚胎中修复与心肌肥大相关的突变基因,并且评估了CRISPR技术的安全性。基因编辑技术具有极其重大的科研和实用价值,同时也具有潜在的风险和伦理方面的争议,各方妥善解决基因编辑技术相关的医学伦理难题任重道远。
(三)医学人工智能
基于大量数据产生的人工智能算法为医疗服务提供了快捷、优化的途径,人工智能在医疗领域的应用带来的不仅是技术革新,还是医疗服务模式的转变[6]。医疗人工智能的率先崛起,与医疗资源严重短缺、分布失衡的现状有关。解决医疗资源的供给不足,将成为人工智能渗入医疗的根本性动因。医学人工智能应用在医疗健康领域应用于以下各个场景:虚拟助理、医学影像、药物挖掘、营养学、医院管理、健康管理、精神疾病、可穿戴设备、风险管理、病理学和临床诊疗活动等。
《2017人工智能赋能医疗产业研究报告》显示[7],截至2017年8月,中国医疗人工智能公司共131家;国内在医疗人工智能布局的企业主要有阿里巴巴网络技术有限公司、腾讯计算机系统有限公司、百度有限公司、科大讯飞有限公司、华大基因有限公司;海外主要有IBM公司、Google公司、苹果公司、微软公司、亚马逊公司等。我国人工智能相关协同创新政策的引导也催生了中国医学科学院-科大讯飞医学人工智能研究中心、华西-希氏医学人工智能研发中心、浙江大学睿医人工智能研究中心等“产学研”联合的研究中心的建立。2018年4月,首款完全自主人工智能诊断系统诊断设备(IDx-DR)获得美国FDA批准,可以在无专业医生参与的情况下,通过查看视网膜照片对糖尿病性视网膜病变进行诊断。IDx-DR类人工智能产品的批准通过,可以使普通人更方便自主地完成常规诊断,同时极大地节约了社会成本,至此,人工智能诊断爆炸时代已然来临。这同样也是人工智能应用的一大里程碑式成绩。
(四)合成生物学技术
以基因组设计合成为标志的合成生物学是继“DNA双螺旋发现”和“人类基因组测序计划”之后,被众多学者认为可引发第三次生物技术革命的技术。合成生物学的核心思想是在系统生物学的基础上,借鉴工程学思想和现代生物学技术方法来设计和构建新的生物元件、网络和体系,最终人工重构新型的生命体。
在生物医学领域,合成生物学在基因工程、体内外诊断、开发新疫苗,乃至人工合成真核生物方面都有潜力产生重大医疗突破。现今,合成生物学在抗癌药物筛选、设计肿瘤免疫治疗以及特异性结合肿瘤细胞工程菌(工程化微生物)方面都取得了显著进展。科学家也使用合成生物学为自身免疫疾病、代谢性疾病、传染病等提供新的治疗策略。另外,合成生物学也已经被用来生产复杂的小分子或者新蛋白药物,如抗疟疾药物的前体或者疫苗。
2010年,美国科学家创建了世界上首个“人造生命”——原核生物支原体,引发世界的关注。2017年,《Science》报道了合成酵母基因组计划中另外5条染色体的合成,其中4条以中国学者元英进团队、杨焕明团队和戴俊彪团队为主完成。正值人们期待着人工合成的真核细胞问世时,2018年中国科学院研究团队[8]与国内多家单位合作,在国际上首次人工创建了自然界中不存在的简约化的生命——仅含单条染色体的真核细胞,取得了合成生物学领域上具有里程碑意义的重大突破。
(五)干细胞与转化医学
干细胞作为一类具有自我复制更新的多潜能细胞,在一定条件下,可以分化为多种功能细胞,能够修复和更新人体受损细胞和器官。组织工程技术、诱导性多能干细胞(iPS)技术、肿瘤干细胞的癌症治疗和干细胞相关基因疗法等基于“修复”和“替代”的新型疾病治疗理念,也将使疾病治疗模式发生革命性的变化[9]。
日本政府将再生医疗等尖端医疗技术作为“新经济成长战略”的重要支柱,致力于在2030年实现干细胞再生医疗的普及。2018年3月,欧盟批准了干细胞疗法Alo fisel用于成人非活动性/轻度活动性腔内克罗恩病患者复杂性肛周瘘的治疗,这是欧盟批准的首个异体干细胞疗法。近年来,我国《“十三五”国家战略性新兴产业发展规划》《“十三五”生物技术创新专项规划》《“十三五”卫生与健康科技创新专项规划》等政策法规依次出台,明确提出发展干细胞产业。2018年,“干细胞及转化研究”重点专项拟立项30个项目,共计获得中央财政经费5.85亿元,其中包括干细胞制剂、细胞器、分离设备、培养设备等。国家在政策及资金上提供支持,对干细胞技术的发展和临床应用起到了引导作用。
三、医学科技发展方向展望
在接下来的十几年中,医学领域将通过多项技术突破而产生颠覆性变革(见图1)。随着技术体系的进步,肿瘤免疫细胞疗法将用于更多的肿瘤类型,多肽和病毒作为治疗性疫苗将获得更多的进步,成本的降低和安全性的提高,最终结果就是改善预后,惠及更多的癌症患者。基因组学的发展将催生个性化医疗,有望治疗癌症、心血管疾病、阿尔茨海默氏症和其他个体遗传疾病。未来基因编辑和基因驱动技术将改变传染病传播源的特征,有望控制和阻断传染病传播。合成生物学技术将推动新型疫苗(包括治疗性疫苗)的研发和产业化,且助力开发快速、灵敏的诊断试剂和体外诊断系统。人工器官将从自身干细胞样本中培养器官进行移植,大大缩短匹配移植器官的等待时间和宿主排斥的风险。假肢可直接连接到神经系统,并将结合基于生物的传感器,提供接近正常的触觉。医学人工智能和生物医学工程的进步将促使假肢完全模仿自然肢体的能力。纳米机器人将能够进行药物传递及操作微创手术[10]。
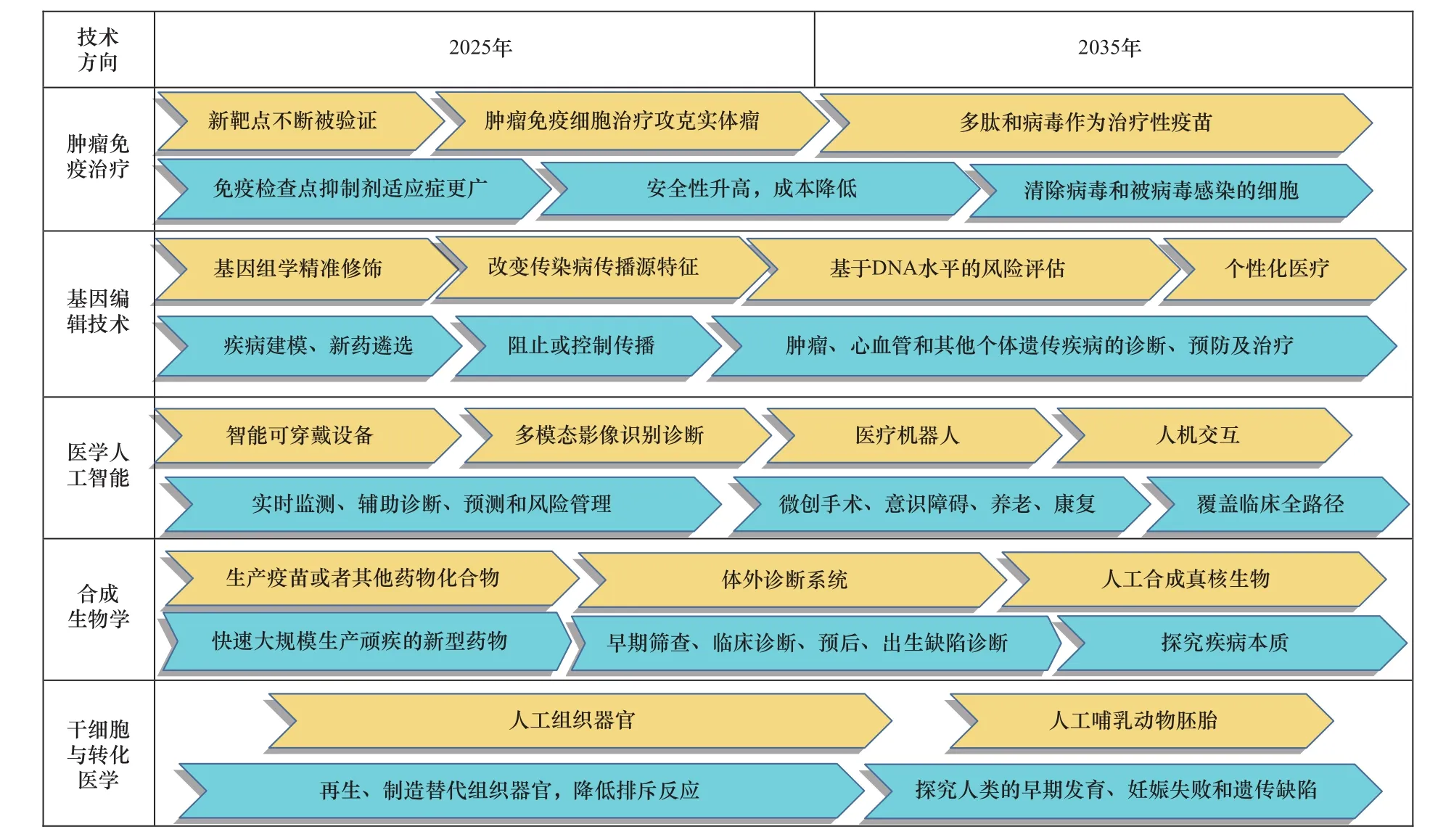
图1 未来医学科技可能的发展方向及应用
四、政策建议
(一)重视医学基础研究投入,鼓励原始技术创新
基础科学是生产力发展的源头,是技术转移和产品创新的基石,而原始创新是运用基本学科和基础知识独立开发一种全新的技术,并将其应用到实际生产的过程,是催生颠覆性技术的动力与源泉。基础科研的交叉融合与创新发展是颠覆性技术的培养皿,信息、生命、材料等基础研究的交叉融合有助于催生新技术[11]。因此,对这些基础科学研究提前布局人、财、物资源,为新技术的研发获得长期发展并有所突破,有助于下一阶段颠覆性技术的培育和产出。
(二)优化医学科技战略顶层设计,重点布局技术交叉融合领域
医学的进步与科技创新和前沿多学科交叉融合息息相关。医学科技的发展也体现了医工结合,医理结合,医学和生命科学结合,医学与光学、电子、材料、信息等技术的结合。医学科技是一个综合平台,多种前沿科学在这个平台上能够进行交叉融合,医学同时也可以作为一个出口,承接多种前沿技术的转化和应用。优先布局并重点支持与生命科学、大数据、纳米技术、人工智能等前沿技术和交叉融合的医学技术研究,将有望产生具有颠覆性效果的技术成果。
(三)完善政策及监管体系,约束技术风险
技术发展必然同时附带各种“副作用”,基因编辑技术促使可遗传的基因修饰成了可能。若不规范使用在基因组水平上改变遗传性状的操作技术,不仅将带来巨大的社会和伦理问题,也可能会涉及潜在的军事安全和威胁。医学科技相关的治理和监管问题不容忽视,应尽快推动制定相关的实验安全技术导则。针对基因编辑、人工智能、合成生物学、干细胞技术的安全性建立健全的和规范的技术指南和国家层面的安全法规以及监管体系,建立从宏观政策到法律法规和标准规范的全面管理体系,从研究与应用两方面加强对技术的监管。

