非布司他对伴高尿酸血症的老年慢性心力衰竭患者心功能的影响
张倩 杨星林
250062 济南大学 山东省医学科学院医学与生命科学学院(张倩);272011 济宁,山东省医学科学院附属济宁市第一人民医院心内科(杨星林)
心力衰竭是各种基础性心脏病发生、发展的终末阶段,其发生机制与炎症、内皮细胞功能失调、氧化应激等多种因素密切相关,病死率和致残率极高。流行病学调查显示,慢性心力衰竭(chronic heart failure,CHF)的发病率约0.9%,但病死率可高达40%,尤以老年人居多[1]。而高尿酸血症(hyperuricemia,HUA)是一种由于人体内嘌呤代谢异常导致尿酸产生过多或尿酸排泄障碍而引起的代谢性疾病。国内外大量临床研究表明,CHF与尿酸水平密切相关,尿酸作为CHF患者预后的独立预测指标,可预测CHF患者的死亡及生存率[2-3]。由于血清尿酸水平与CHF及其他心血管疾病密切相关,研究者们试图通过干预血清尿酸水平改善心功能,寻找针对伴HUA的CHF患者更加有效的治疗方法。本研究通过对合并HUA的老年CHF患者在基础抗心力衰竭治疗药物上加用非布司他,观察尿酸变化对老年CHF患者心功能的影响,从而评价非布司他在CHF患者中的临床应用价值。
1 对象和方法
1.1 研究对象
本研究为随机对照临床研究。选取2016年10月至2017年8月于济宁市第一人民医院心内科住院的合并HUA的老年CHF患者150例,其中男性72例,女性78例,年龄62~78岁,平均(66.2±4.6)岁。包括不稳定型心绞痛71例,陈旧性心肌梗死26例,扩张型心肌病11例,风湿性心脏病13例,高血压29例。入选标准:(1)年龄≥60岁;(2)符合纽约心脏病协会(New York Heart Association,NYHA)心功能分级Ⅱ~Ⅳ级,合并心脏收缩功能不全,超声心动提示心脏扩大、左心室射血分数(left ventricular ejection fraction,LVEF)<50%;(3)入院后正常嘌呤饮食状态下,非同日检测两次空腹血清尿酸浓度,男性>7.0 mg/dl(420 μmol/L),女性>6.0 mg/dl(>360 μmol/L)。排除标准:(1)合并肺部感染、肺源性心脏病;(2)急性心肌梗死、先天性心脏病引起的心力衰竭;(3)恶性肿瘤;(4)合并自身免疫性疾病或严重的肝肾功能不全;(5)痛风及既往服用其他影响尿酸的药物;(6)合并甲状腺疾病、糖尿病、红细胞增多症及慢性溶血症;(7)有其他大型外科手术治疗史;(8)对非布司他过敏。本研究经济宁市第一人民医院伦理委员会批准(伦理批号:2016-03-03),所有受试者均签署知情同意书。
1.2 分组及治疗方法
采用计算机简单随机化分组方法将受试对象分为非布司他组(治疗组)和常规治疗组(对照组),每组各75例。根据2016年欧洲心脏病协会制定的成人慢性心力衰竭诊断及治疗指南,两组患者在低嘌呤饮食状态下均给予地高辛、利尿剂、血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂、β受体阻滞剂和醛固酮受体拮抗剂,部分冠心病患者使用他汀类药物。
治疗组在常规治疗的基础上给予非布司他40 mg/d(商品名:优立通,国药准字:H20130058,江苏万邦生化医药集团有限责任公司生产),观察血清尿酸浓度,2周后若血清尿酸仍未达标者(血清尿酸最低控制目标为<360 μmol/L),非布司他加量至80 mg/d,并以此剂量维持至试验结束终止,治疗时间为6个月。
观察期间如患者出现急性痛风发作、肝肾功能异常(血肌酐>133 μmol/L,谷丙转氨酶/谷草转氨酶>2倍正常上限)、胃肠道反应(严重恶心、呕吐、腹泻等不耐受情况)、血常规异常(白细胞<4.0×109/L或血红蛋白<100 g/L或血小板<100×109/L)、过敏(皮肤大面积皮疹、伴随严重瘙痒)、心血管不良事件(窦性停搏、恶性室性心律失常、急性充血性心力衰竭、急性血栓形成)等不良反应需终止试验。
1.3 观察指标
受试者于治疗期间每月月初过夜空腹至少12 h抽取静脉血2~3 ml,采用罗氏Cobas 8000全自动生化分析仪,测定患者血清尿酸、肌酐、N末端B型利钠肽原(N-terminal pro-brain natriuretic peptide,NT-proBNP)水平;并同时检测肝功能、血糖、血脂、血常规、尿常规和大便常规。使用Aloka SSD4000型彩色多普勒超声诊断仪测定治疗前后左室收缩末期内径(left ventricular end systolic diameter,LVESD)、左室舒张末期内径(left ventricular end diastolic diameter,LVEDD),并计算LVEF,同步记录心电图;测量受试者6 min步行的最远距离(6 min walk distance,6MWD)。
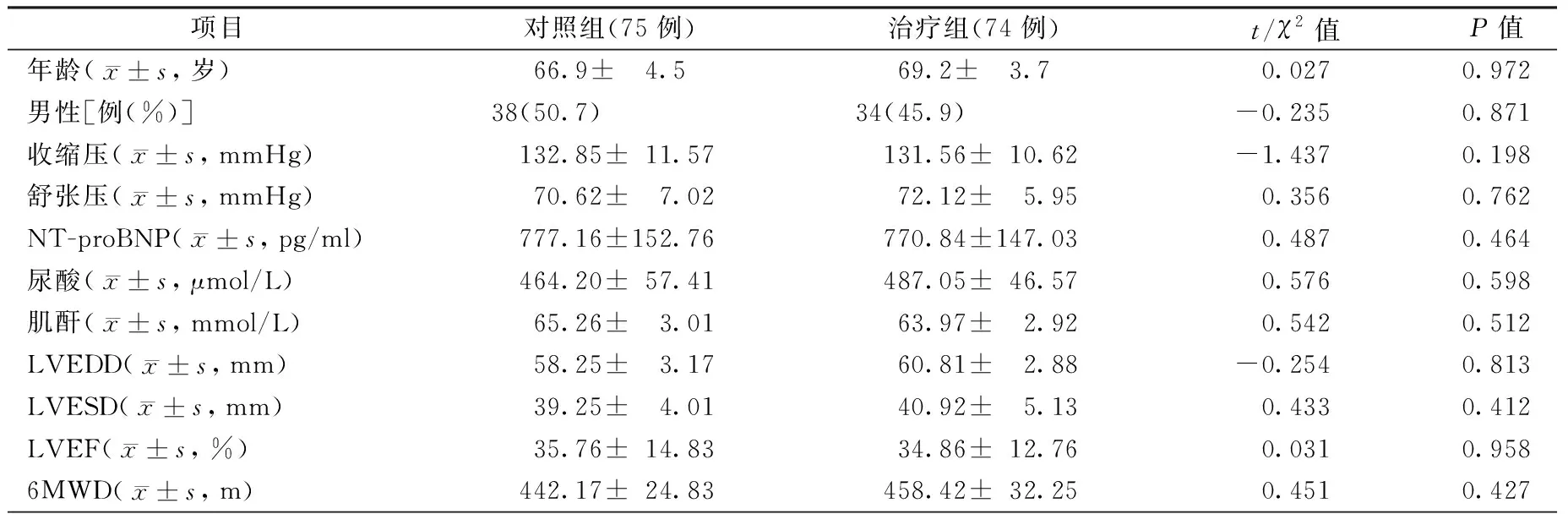
表1 两组基线资料比较
注:两组患者在治疗前均给予低嘌呤饮食,规律服用降压、降糖药物,观察期间其他药物依据病情进行相应合理调整,但基本治疗保持相对稳定。观察期间治疗组因过敏反应终止试验1例
1.4 统计学方法
2 结果
2.1 基线资料比较
观察期间治疗组因严重过敏反应终止试验1例。两组年龄、性别、血压、肌酐、尿酸、LVESD、LVEDD、LVEF、6MWD等基线资料比较,差异均无统计学意义(均为P>0.05),具有可比性,见表1。
2.2 非布司他降尿酸的疗效分析
对照组经常规治疗后血清尿酸水平缓慢下降,但仍维持在一个较高水平;而治疗组加用非布司他治疗后血清尿酸水平较基线时明显降低,根据受试者的敏感性调整非布司他的剂量,使尿酸降低水平显著而平稳。治疗6个月后,治疗组血清尿酸浓度为(325.36±37.57)μmol/L,对照组为(421.14±50.21)μmol/L,两组比较差异有统计学意义(t=4.236 2,P=0.001 2),见表2。
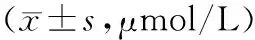
表2 两组治疗随访期间血清尿酸水平变化
2.3 非布司他的耐受性及安全性分析
治疗期间,治疗组74例患者中共出现48例次不良事件,其中非布司他40 mg/d时出现25例次,80 mg/d时出现23例次,常见不良反应包括肝肾功能异常、血常规异常、过敏反应、胃肠道反应和高脂血症,且发生几率随着用药剂量的增大而上升,但本研究中上述不良反应均相对轻微,大多数患者可耐受并继续接受治疗,仅有1例因严重过敏反应而终止治疗,见表3。两组患者均未出现急性痛风发作及心血管不良反应。
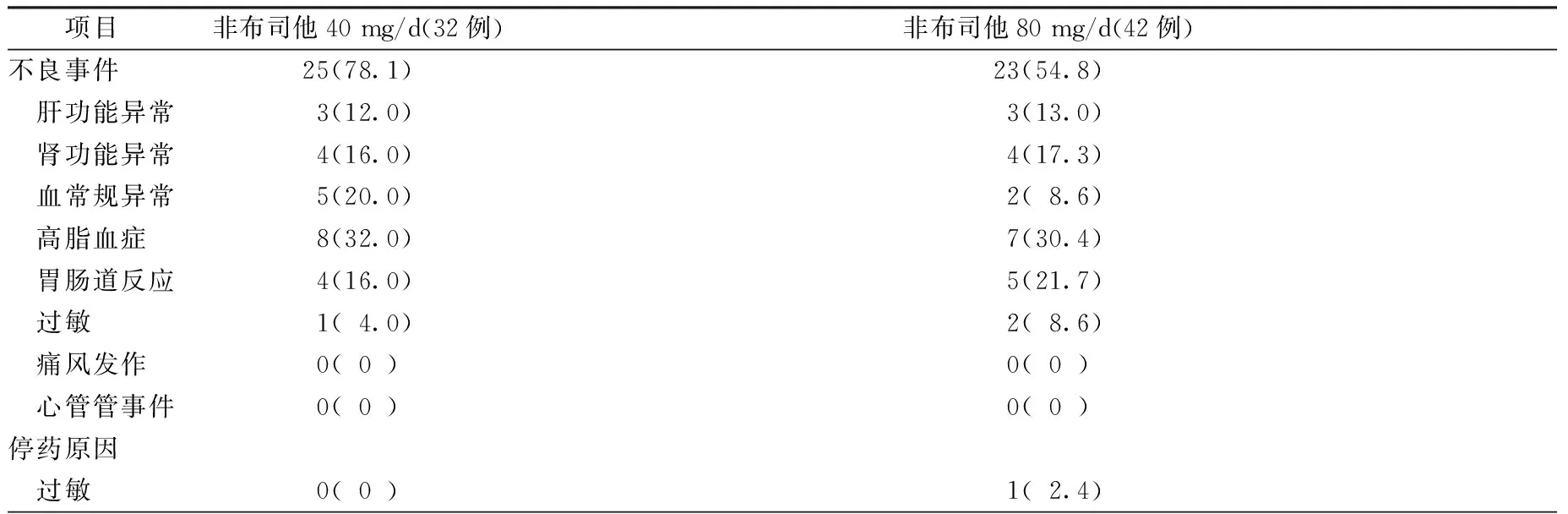
表3 治疗组中不良事件及停药原因[例(%)]
2.4 两组观察指标及心功能变化
治疗6个月后,两组患者血清尿酸、NT-proBNP、LVESD和LVEDD均呈下降趋势,治疗组下降更明显(P<0.05);而LVEF、6MWD均呈升高趋势,且治疗组上升幅度更显著(P<0.05),见表4。
3 讨论
国内外研究均已证实,HUA是CHF患者发病及死亡的独立危险因素,与其发生、发展和预后均密切相关。HUA加重CHF患者病情的作用机制包括:(1)血清尿酸的升高可直接损伤血管内皮细胞,导致血管平滑肌细胞增殖、心脏泵血功能下降、血小板聚集、细胞凋亡及局部炎症反应,进而促进CHF的发生和发展[4];(2)血清尿酸在血管平滑肌细胞增殖过程中可直接激活炎症免疫通路,产生炎症介质,引起心室肥大。相关研究表明,血清尿酸同时作用于肾素-血管紧张素-醛固酮系统[5-6],导致血管紧张素Ⅱ的产生,促进细胞增殖及活性氧生成,将进一步促进心室重构;(3)血清尿酸可影响心血管系统中一氧化氮的产生,使其生物利用度呈现下降趋势,导致血管内皮细胞的功能障碍,促进平滑肌细胞增殖。CHF患者体内嘌呤产生增多,尿酸合成增多,而硝酸甘油等药物扩张冠状动脉的同时,也扩张外周动静脉血管,加重通气/血流比例失调及低氧血症,使肾血流减少、尿酸排泄减少,最终致体内SUA堆积,加快了心力衰竭的进展,增加了老年人的住院率及病死率。
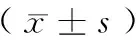
表4 两组治疗后观察指标变化
本研究显示,合并HUA的老年CHF患者随着尿酸水平降低,心功能分级、左室功能相关指标及运动耐量均明显提高;NT-proBNP水平明显降低,提示干预血清尿酸可有效改善CHF患者的心功能。常用降尿酸药物主要针对:(1)抑制尿酸生成:其中以别嘌呤醇为代表,主要是通过抑制黄嘌呤氧化酶的活性,减少活性氧和尿酸的产生,一般用于痛风的急性发作,但因其具有肝肾损害和过敏的不良反应限制了临床应用[7];(2)促进尿酸排泄:苯溴马隆为其代表药物,主要通过作用于近端肾小管的尿酸盐转运体,抑制肾小管对尿酸的再次重吸收而促进尿酸的排泄[8-9],使血尿酸水平降低,但也具有一定的肝肾毒性。
非布司他可选择性抑制黄嘌呤氧化酶,是一种新型的非嘌呤类药物,2009年经美国FDA批准上市,被证实可有效抑制尿酸合成、降低血清尿酸浓度[8-9],显著优于其他降尿酸药物,如:(1)对于合并轻中度肝肾功能不全的患者,非布司他不影响药物动力学参数[10-11],故不需要调整用药剂量;(2)口服吸收完全,生物利用度可高达85%,可通过胆汁和肾脏两种途径排泄;(3)在常规剂量下,非布司他不影响其他酶的活性,不参与嘌呤和嘧啶的合成与代谢[12-13]。
本研究结果显示,非布司他的不良反应相对较少,绝大多数患者可耐受轻微的不良反应并可继续接受治疗。研究过程中受试患者均未出现心血管不良事件,但鉴于近期FDA对非布司他的心血管安全性进行了警示,我们考虑到本试验入选病例数相对较少,观察、随访时间较短,下一步我们拟对非布司他在CHF患者的长期疗效及远期预后展开进一步研究,并加强患者的病情观察与监测。
利益冲突:无

