Car-T治疗B细胞淋巴瘤疗效研究的Meta分析
张锡友*,李丹丹*,陈峰,2△,宋清坤,钟晓松
淋巴瘤是一组起源于淋巴结和淋巴组织的恶性肿瘤,其中以弥漫性大B细胞淋巴瘤(diffuse large B-cell lymphoma,DLBCL)最为常见。据报道2016年美国DLBCL新增27 650例,约占B细胞淋巴瘤的26%,其次较为常见的依次为滤泡性淋巴瘤(follicular lymphoma,FL)、边缘区淋巴瘤(marginal zone lymphoma,MZL)和套细胞淋巴瘤(mantle cell lymphoma,MCL),约占B细胞淋巴瘤的13%、7%和3%[1]。对于复发/难治性B细胞淋巴瘤患者,常规治疗方案难以奏效。近年来,肿瘤免疫治疗在血液肿瘤的治疗中取得了巨大进展,特别是嵌合抗原受体T细胞(chimeric antigen receptor T-cell,Car-T)技术在B细胞淋巴瘤中的突破,为复发/难治性B细胞淋巴瘤患者带来了新的希望。CD19的表达几乎贯穿于整个B细胞发育的过程,因此CD19成为Car-T治疗B细胞淋巴瘤的理想靶点,靶向CD19的Car-T治疗是临床上应用最广、研究最全面的治疗方案[2]。除 CD19 外,CD20[3]、CD22[4]、κ 轻链[5]、ROR1[6]也是具有一定潜力的靶点。本研究通过荟萃分析的方法,探讨影响Car-T治疗B细胞淋巴瘤疗效的相关因素,旨在为更加合理、高效地应用Car-T提供理论依据。
1 资料与方法
1.1 文献检索 全面检索Pubmed数据库和The Cochrane library数据库的英文文献,检索日期从建库至2018年1月止,采用主题词和自由词结合的检索方法,使用的检索字符串包括 :(1) Lymphoma、Lymphomas、Lymphoma、Malignant、Lymphomas、 Malignant、 MalignantLymphoma、 Malignant Lymphomas。(2)CAR、CAR-T、CAR-T Cell、CAR-T Cells、Chimeric Antigen Receptor、Chimeric Antigen Receptor T-Cell、Chimeric Antigen Receptor T-Cells、Chimeric Antigen Receptor-modified T-Cell、Chimeric Antigen Receptormodified T-Cells、Chimeric Antigen Receptor-transduced TCell、Chimeric Antigen Receptor-transduced T-Cells。并且对检索出的文献的参考文献进行二次检索,保证全面获取数据。
1.2 文献纳入标准 (1)国内外公开发表的关于Car-T治疗B细胞淋巴瘤的研究。(2)研究对象为B细胞淋巴瘤患者。(3)完整提供或部分提供年龄、病理类型、目标抗原、共刺激分子、预处理方案等Meta分析必要的信息。(4)提供患者经Car-T治疗后的疗效评价。(5)文献语言限定为英文。
1.3 文献排除标准 (1)所有不符合纳入标准的文献。(2)原始数据不完整,或前后不一致。(3)重复发表的研究。(4)完全没有提供诸如年龄、性别、临床分期等Meta分析必要信息的文献,或没有提供患者经Car-T治疗后的疗效评价的文献。(5)综述、个案报道和动物实验。(6)低质量文献或严重偏倚的文献。
1.4 数据提取 由2名研究员根据文献的纳入标准和排除标准筛选所需的文献,对符合要求的文献进行质量评价并从中提取数据,包含文献作者、出版时间、患者年龄、病理类型、目标抗原、共刺激分子、预处理方案等信息,整理数据并汇总。
1.5 结局指标 反应率(response rate)为完全缓解(complete remission,CR)和部分缓解(partial remission,PR)患者占总患者数的百分比。
1.6 统计学方法 所有的数据处理均使用Stata 12.0软件完成。按照患者的年龄、病理类型、目标抗原、共刺激分子、预处理方案等因素的不同进行亚组分析,采用Meta分析汇总反应率。异质性分析使用I2检验和Q检验两种方法,当I2<50%,且Q检验P>0.1时,可认为不存在异质性,采用固定效应模型进行分析,反之则存在异质性,选用随机效应模型进行合并分析[16]。分别采取随机效应模型和固定效应模型对各因素进行合并,进行敏感性分析,若两项结果间未见明显差异,提示结果稳定。分别应用Begg法和Egger法检测文献的发表偏倚,Begg法P>0.05,Egger法P>0.05,提示无发表偏倚。
2 结果
2.1 文献的基本特征 初步检索出文献248篇,根据纳入标准和排除标准,最终纳入11篇文献,均为高质量研究,文献筛选流程图,见图1。所有入选文献情况见表1。

Fig.1 Process of literature screening图1 文献筛选流程图
2.2 Meta分析结果
2.2.1 总反应率 11 个研究[3,5,7-15]均记录了 Car-T治疗B细胞淋巴瘤的疗效,文献之间存在异质性(I2=45.0%,P=0.052),采用随机效应模型,结果显示,总反应率75%(95%CI:0.67~0.84),进一步证实Car-T对B细胞淋巴瘤具有相当的疗效,见图2。

Tab.1 Basic characteristics of the literature表1 纳入文献的基本特征
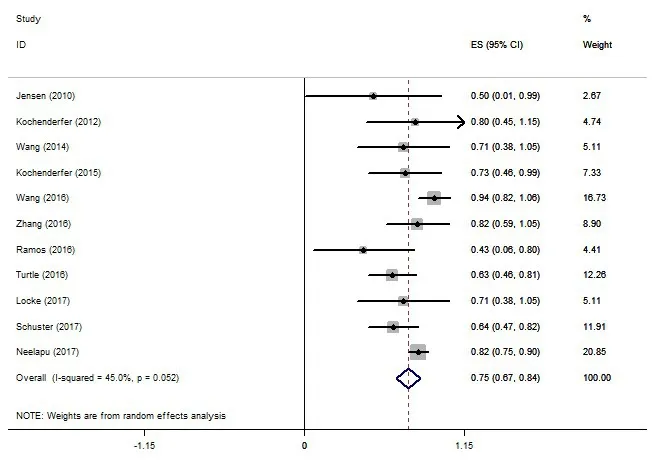
Fig.2 Meta-analysis of the total response rate图2 总反应率的Meta分析结果(随机效应模型)
2.2.2 亚组分析
2.2.2.1 基于年龄的亚组分析结果 将B细胞淋巴瘤患者分为低龄组(<65岁)和高龄组(≥65岁)两个组别,进行亚组分析。8个研究记录了年龄与Car-T治疗B细胞淋巴瘤疗效的相关性,低龄组7篇文献[5,7-8,10-11,13,15]之间不存在异质性(I2=0,P=0.652),高龄组3篇文献[9,13,15]之间亦不存在异质性(I2=14.2%,P=0.312),均采用固定效应模型分析,结果显示,低龄组反应率80%(95%CI:0.73~0.87),高龄组反应率88%(95%CI:0.78~0.98),提示高龄患者对Car-T治疗具有较高的反应率,见图3。

Fig.3 Subgroup analysis based on age(fixed effects model)图3 基于年龄的亚组分析结果(固定效应模型)
2.2.2.2 基于病理类型的亚组分析结果 将B细胞淋巴瘤患者分为DLBCL组(病理类型为DLBCL)和非DLBCL组(病理类型不是DLBCL)两个组别,进行亚组分析。9个研究记录了病理类型与Car-T治疗B细胞淋巴瘤疗效的相关性,DLBCL组7篇文献[8-11,13-15]之间不存在异质性(I2=21.7%,P=0.264),非DLBCL组6篇文献[5,7,9,11,14-15]之间亦不存在异质性(I2=0,P=0.890),均采用固定效应模型,结果显示,DLBCL组反应率81%(95%CI:0.74~0.87),非DLBCL组反应率79%(95%CI:0.68~0.89),提示DLBCL患者对Car-T治疗具有较高的反应率,见图4。

Fig.4 Subgroup analysis based on pathological type(fixed effects model)图4 基于病理类型的亚组分析结果(固定效应模型)
2.2.2.3 基于目标抗原的亚组分析结果 将B细胞淋巴瘤患者分为CD19组(目标抗原为CD19)和非CD19组(目标抗原不是CD19)两个组别,进行亚组分析。10个研究记录了目标抗原与Car-T治疗B细胞淋巴瘤疗效的相关性,非CD19组3篇文献[5,8,11]之间不存在异质性(I2=36.1%,P=0.209),但是CD19组7篇文献[7,9-10,12-15]之间存在异质性(I2=52.4%,P=0.050),采用随机效应模型,结果显示,CD19组反应率77%(95%CI:0.68~0.87),非CD19组反应率69%(95%CI:0.47~0.91),提示目标抗原CD19的Car-T具有较高的反应率,见图5。

Fig.5 Subgroup analysis based on target antigen图5 基于目标抗原的亚组分析结果(随机效应模型)
2.2.2.4 基于共刺激分子的亚组分析结果 将B细胞淋巴瘤患者分为CD28组(Car-T中以CD28作为共刺激分子)和非CD28组(Car-T中含其他共刺激分子,或者没有共刺激分子)两个组别,进行亚组分析。11个研究记录了共刺激分子与Car-T治疗B细胞淋巴瘤疗效的相关性,CD28组6篇文献[5,7,9,13-15]之间不存在异质性(I2=31.8%,P=0.197),非CD28组5篇文献[3,8,10-12]之间亦不存在异质性(I2=4.2%,P=0.383),均采用固定效应模型,结果显示,CD28组反应率 78%(95%CI:0.71~0.84),非 CD28组反应率73%(95%CI:0.62~0.84),提示以CD28作为共刺激分子的Car-T具有较高的反应率,见图6。

Fig.6 Subgroup analysis based on costimulatory molecule(fixed effects model)图6 基于共刺激分子的亚组分析结果(固定效应模型)
2.2.2.5 基于预处理方案的亚组分析结果 将B细胞淋巴瘤患者分为Cy/Flu组(应用环磷酰胺+氟达拉滨预处理方案)和非Cy/Flu组(应用其他预处理方案,或者没有预处理方案)两个组别,进行亚组分析。11个研究记录了预处理方案与Car-T治疗B细胞淋巴瘤疗效的相关性,非Cy/Flu组6篇文献[3,5,8,10-12]之间不存在异质性(I2=66.8%,P=0.010),但是Cy/Flu组6篇文献[7,9,12-15]之间存在异质性(I2=0.0%,P=0.534),采用随机效应模型,结果显示,Cy/Flu组反应率78%(95%CI:0.72~0.84),非 Cy/Flu 组 反 应 率 69%(95%CI:0.50~0.88),提示以选用Cy/Flu作为预处理方案的Car-T具有较高的反应率,见图7。上述6组Meta分析结果汇总见表2。

Fig.7 Subgroup analysis based on conditioning chemotherapy图7 基于预处理方案的亚组分析结果(随机效应模型)

Tab.2 Summary of Meta-analysis表2 Meta分析结果汇总
2.3 敏感性分析 采取随机效应模型和固定效应模型对各因素分别进行合并,见表3,其中除非Cy/Flu组的两项结果间略有差异以外,其余Meta分析中两项结果间未见明显差异,提示合并结果基本稳定。

Tab.3 Analysis of the sensitivity表3 敏感性分析结果
2.4 发表偏倚 分别应用Begg法和Egger法检测文献的发表偏倚,见表2,结果示各个影响因素的Meta分析结果经Begg法检验P≥0.05;总反应率、非DLBCL组以及非Cy/Flu的Meta分析结果中,Egger法P<0.05,其余Meta分析中Egger法P>0.05,表明上述3组Meta分析可能存在发表偏倚,其余Meta分析无发表偏倚存在。
3 讨论
本荟萃分析结果显示,Car-T治疗B细胞淋巴瘤的总反应率为75%,进一步证实Car-T对B细胞淋巴瘤具有相当的疗效。在亚组分析中,年龄在65岁以上、病理类型为DLBCL、目标抗原为CD19、共刺激分子为CD28以及预处理方案为Cy/Flu(环磷酰胺+氟达拉滨)的Car-T治疗均有较高的反应率。但是,本研究存在一定的局限性:(1)由于Car-T是一种新兴治疗手段,开展时间较短,缺乏大规模的样本数据,进行Meta分析的样本量过少。(2)目前尚未出现关于Car-T疗效的随机对照试验(randomized controlled trial,RCT),多数文献为病例数较少的临床前研究,研究中分组的随机性较小,无法保证变量的控制。(3)荟萃分析依赖原始文献的数据,笔者参照原始文献分组标准的制定本研究的分组标准,这一环节可能造成汇总结果与实际情况之间存在偏差。(4)可能存在未公开发表的阴性结果文章。(5)本文仅进行Car-T治疗B细胞淋巴瘤的有效性评价,未进行安全性评价。
针对B细胞淋巴瘤多种靶点的Car-T,不少国家和地区的医疗机构已进行了大量的临床试验,同时目前有更多的临床试验仍在进行中。在已有报道的治疗B细胞淋巴瘤的临床试验中Car-T表现出显著的疗效,尤其对于复发/难治性B细胞淋巴瘤患者。但是,在临床应用过程中,Car-T的安全性有待进一步研究:从短期来看,Car-T治疗过程中存在不良反应,包括细胞因子释放综合征[17]、肿瘤溶解综合征以及脱靶效应[18]等。从长期来看,目前尚鲜有证据证明病毒载体是否会给机体带来有害的插入性突变。笔者将持续追踪Car-T的最新研究进展,在未来大样本数据的支持下,更加深入研究Car-T的有效性,同时完善Car-T治疗的安全性评价,为更加合理地应用Car-T提供理论依据。

