经皮椎体成形术与经皮椎体后凸成形术治疗老年轻中度骨质疏松性胸腰椎压缩性骨折的临床比较研究
朱 斌,贺 元,李怀伟,阿 海,关炳瑜,李永娟
骨质疏松患者其骨质量下降、骨微细结构被破坏,表现为骨强度降低、脆性增加,发生骨折的风险增大,骨折是骨质疏松最常见和最严重的并发症[1-2]。由于骨质疏松以老年人最为常见,而骨质疏松性骨折又以胸腰椎压缩性骨折居多,因而老年骨质疏松性胸腰椎压缩性骨折(OTCF)颇受关注。经皮椎体成形术(PVP)和经皮椎体后凸成形术(PKP)是治疗OTCF的两种常用微创术式,其中PVP虽被证实为治疗OTCF的有效方式,但治疗过程中常发生骨水泥渗漏,易造成严重并发症[3-4],而PKP能否在取得同样效果的前提下减少并发症的发生率仍存在较大的争议[5]。近年来虽有较多的学者致力于PVP与PKP治疗OTCF的研究,但关于两种治疗方式治疗OTCF的系统性对照研究较少。本文以老年轻中度OTCF患者为研究对象,比较PVP与PKP两种术式的治疗效果及安全性,为临床提供参考。
临床资料
1 一般资料
2012年1月—2017年1月笔者医院收治老年OTCF患者76例,根据手术方式分为PVP组(41例)和PKP组(35例)。PVP组:男性25例,女性16例;年龄60~80岁,平均67.84岁;骨折部位:T116例、T1222例、L18例、L23例、L32例;单一椎体骨折38例,L1+L2骨折3例。PVP组:男性20例,女性15例;年龄60~81岁,平均67.21岁;骨折部位:T115例、T1219例、L17例、L22例、L32例;单一椎体骨折32例,L1+L2骨折3例。两组患者的一般资料比较差异无统计学意义(P>0.05)。患者均表示配合本研究并签署知情同意书,研究经医院伦理委员会审核批准。
纳入标准:(1)明确诊断为OTCF[6]:①有明确的外伤史;②X线、CT等影像学检查有一定程度的压缩,椎体后壁完整;③外观有后突畸形,胸腰局部肿痛、压痛及叩击痛,腰部活动不利;(2)经MRI检查为新鲜骨折(骨折时间<3周);(3)骨折严重程度为中轻度(根据Genant半定量法进行分级,骨折椎体高度减少<40%,无合并脊髓及神经损伤);(4)年龄>60岁;(5)身体状况能够耐受手术治疗。
排除标准:(1)合并严重内科疾病及患有椎体骨髓炎;(2)因任何原因影响疗效评价;(3)对所用药品器械有过敏反应;(4)无法纠正凝血机制障碍和出血倾向;(5)非骨质疏松性急性创伤性骨折。
2 治疗方法
所有患者入院后卧床休息、止痛等对症处理,常规查体、实验室检查及X线、CT、MRI等影像学检查,常规禁食、禁水、备皮等,专业医师对患者进行手术耐受力评估,对精神紧张的患者可适当给予镇痛催眠药物。
两组均取仰卧位,在局部麻醉下采用单侧入路术式;常规铺巾消毒后在C型臂X线机透视下定位伤锥锥弓根皮肤为进针点,沿定位点置入穿刺针,透视下确定穿刺针位于伤椎体椎弓根内,在椎体前1/3处后拔出穿刺针芯后插入导针并退出穿刺针,然后进一步操作。
PVP组:C型臂X线机透视确保穿刺位置良好后,于椎体前1/3处缓慢向椎体内注入拉丝期的骨水泥(意大利Tecres S.P.A公司生产),待骨水泥硬化后退出工作套管。
PKP组:采用与PVP组相同的方法建立工作通道,于椎体后1/3处插入工作套管,经工作套管置入骨钻,透视确保骨钻至椎体前臂2~3cm处,取出骨钻并植入球囊,注入碘海醇造影剂,待球囊扩张良好(压力在20~40bar)、椎体高度复位满意后退出球囊,透视引导下逐渐推入拉丝期骨水泥(意大利Tecres S.P.A公司生产),待骨水泥硬化后退出工作套管。抽出造影剂后扩张压缩的椎体,拔出球囊后注入骨水泥。
两组患者术后采取同样的处理方案,即术后仰卧2h,常规心电监护12h,预防性使用抗生素2d,术后第2天开始常规下地活动,严格预防感染、血肿等不良反应的发生;患者出院后继续常规治疗骨质疏松。所有患者术后至少随访12个月,每3个月患者回院复查一次,随访内容包括观察骨水泥情况、脊髓神经损伤情况及有无感染、血肿、疼痛等一般情况,同时评估两组的治疗效果。
3 观察指标
手术情况:记录两组手术时间、骨水泥注入量、住院时间。疗效指标:记录两组术前、术后3d,术后3、6及12个月VAS和活动能力,记录两组术前、术后3d及术后6个月的Cobb’s角[7]和椎体前缘高度[8]。VAS评分总分0~10分,0分为无痛,10分为剧烈疼痛。活动能力总分1~4分,活动无明显困难1分,活动需要辅助2分,坐立不能行走3分,只能卧床4分。安全性评价:记录两组住院及随访期间并发症的发生情况。
4 统计学分析
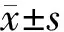
结 果
1 两组手术情况比较
PKP组手术时间、住院时间长于PVP组,骨水泥注入量多于PVP组,组间比较差异有统计学意义(P<0.05)。见表1。
2 两组伤锥椎体改善情况比较
术前Cobb’s角、椎体前缘高度PVP组与PKP组组间比较差异无统计学意义(P>0.05)。与术前比较,两组术后3d、术后6个月的Cobb’s角显著减小(P<0.05),但组间比较差异无统计学意义(P>0.05);两组术后3d、术后6个月椎体前缘高度显著增加,且PKP组高于PVP组,组间比较差异有统计学意义(P<0.05)。见表2。
3 两组手术前后VAS评分比较
PKP组术后3d的VAS评分高于PVP组,组间比较差异有统计学意义(P<0.05);其余各观察时间的VAS评分PKP组与PVP组比较差异均无统计学意义(P>0.05);两组术后各观察时间的VAS评分均低于术前,组内与术前比较差异均有统计学意义(P<0.05)。见表3。
4 两组手术前后活动能力评分比较
PVP组各观察时间点的活动能力评分与PKP组比较,差异均无统计学意义(P>0.05);两组术后各观察时间点的活动能力评分均低于术前,组内与术前比较,差异均有统计学意义(P<0.05)。见表4。
5 两组并发症发生率比较
PKP组发生骨水泥渗漏1例,慢性疼痛3例,邻近椎体压缩性骨折2例,并发症发生率17.14%(6/35);PVP组发生骨水泥渗漏5例,神经根疼痛1例,慢性疼痛2例,并发症发生率19.51%(8/41)。两组并发症发生率比较差异无统计学意义(χ2=0.873,P=0.462)。
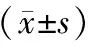
表1 两组手术情况比较
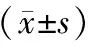
表2 两组Cobb’s角、椎体前缘高度改善情况比较
组内与术前比较:*P<0.05
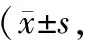
表3 两组手术前后VAS评分比较分)
组内与术前比较:*P<0.05
表4 两组手术前后活动能力评分比较分)
组内与术前比较:*P<0.05
讨 论
OTCF患者主要以老年人为易发群体,目前临床上治疗OTCF的方法较多,如卧床休息、佩戴支具和药物镇痛等非手术治疗,传统手术治疗(钉棒内固定)和微创手术治疗(PVP和PKP)[9],临床上一般不建议采用非手术治疗。钉棒内固定是治疗OTCF的传统术式,该术式虽能缓解患者的疼痛,取得一定的疗效,但手术创伤较大、费用较高,且常发生内固定植入物松动而导致手术失败[10],因而其并不是治疗OTCF最理想的术式。随着微创技术的发展,椎体成形术(PVP和PKP)普遍应用于OTCF的临床治疗,与传统术式比较具有手术时间短、创伤小、并发症少、术后恢复快等优点,被认为是目前治疗OTCF最有效的术式[11]。然而,随着PVP和PKP在临床上的广泛应用,关于二者孰优孰劣的争议也越来越大,而目前学界关于两种术式的系统性对比研究较少。
本研究中,较PKP而言,PVP具有手术时间短、术后恢复较快、骨水泥用量较少等优点,其原因主要是因为PVP操作简便,体位复位后可直接进行骨水泥高压注射,而PKP需依赖球囊扩张作用,这与既往研究具有一致性[12]。从椎体恢复情况方面看,两组术前Cobb’s角、椎体前缘高度比较差异不明显,术后3d、术后6个月PVP组Cobb’s角与PKP组比较差异不明显,术后3d、术后6个月与术前比较,两组Cobb’s角显著减小,椎体前缘高度显著增加,PKP组术后3d、术后6个月椎体前缘高度显著高于PVP组。这说明对老年轻中度OTCF患者的临床治疗,PVP和PKP两种术式治疗OTCF均能获得良好的Cobb’s角恢复效果,且二者的效果相当,但PKP组椎体前缘高度恢复优于PVP组。其原因可能是因为PKP通过球囊扩张作用,可直接机械地达到恢复椎体高度的作用,而PVP通过体位复位直接高压注射骨水泥,骨水泥可较好地分散到骨折微小裂隙中,对Cobb’s角恢复效果理想,对椎体前缘高度恢复也有一定的作用,但椎体前缘高度恢复效果不如PKP。然而有研究表明[13],OTCF患者的临床治疗中,椎体高度过度恢复会加大再次骨折的风险。从疼痛缓解效果方面看,PKP组术后3d的VAS评分高于PVP组;两组术后各观察时间的VAS评分与术前比较显著降低。这说明,两种术式均可显著缓解OTCF患者的疼痛,其原因是OTCF患者的疼痛发于椎体的微小骨折,在椎体机械应力或椎体内炎症反应变化时疼痛程度增加,而注入骨水泥可加骨折裂痕,减少与负载相关的机械应力,从而减轻疼痛,两种术式均可以发挥这种效果[14];而PKP术后3d的VAS评分高于PVP,可能是PKP操作造成。从术后椎体功能恢复方面,PVP组各观察时间点的活动能力评分与PKP组比较差异不明显;两组术后各观察时间点的活动能力评分与术前比较显著降低。表明两种术式均可获得良好的椎体功能恢复,其原因可能是因为两者均能获得较理想的椎体恢复,缓解疼痛,这与既往研究[15-16]基本一致。从安全性方面看,两组并发症总发生率比较差异不明显,表明两种术式治疗老年轻中度OTCF的安全性相当;需要指出的是,PVP组发生骨水泥渗漏5例,而PKP组仅1例,但PKP组发生邻近椎体压缩性骨折2例,其原因可能是PKP椎体复位过程中势必造成空腔,空腔周边疏松骨质被压缩后有利于防止骨水泥渗漏,但亦可能引起骨小梁断裂。
本研究从手术一般情况、椎体恢复情况、疼痛缓解情况、椎体功能恢复情况及安全性等方面比较了PVP与PKP治疗老年轻中度OTCF患者的优劣,表明两种术式各有优劣,但研究中样本量较小,有待大样本量的研究进一步证实。另外,本研究中排除了陈旧性骨折患者,对于这两种术式治疗陈旧性OTCF的效果比较尚需开展专题探讨。
- 创伤外科杂志的其它文章
- 保留旋前方肌多轴锁定钢板治疗C1、C2型桡骨远端骨折Treatment of C1-type and C2-type fractures of the distal radius by open reduction and numelock II polyaxial system fixation with pronator quadratus reserved
- 解剖型锁定钢板对粉碎性Pilon骨折疗效的影响Effect of anatomic locking plate on the curative effect of comminuted Pilon fracture
- 胸腔镜辅助镍钛记忆合金肋骨接骨板内固定术治疗多发肋骨骨折临床疗效研究
- 股骨头骨折合并同侧髋臼骨折的手术疗效分析
- 玉米剥皮机致手部复杂损伤的临床治疗分析
- 内外侧联合入路合并早期支具固定治疗复杂肘关节脱位的临床疗效

