高碱煤自身灰捕捉碱金属特性的实验与量化
王要克,杜梅芳,刘欢欢,李明强
(1. 上海理工大学 理学院,上海 200093;2. 上海理工大学 环境与建筑学院,上海 200093)
新疆准东地区是全国煤炭储量占比极大的地区之一[1],但其工业燃煤中富含Na,K,Ca等碱性金属元素,其中总体Na2O含量都在2%以上,部分矿区甚至高达10%,远大于常规动力用煤1%[2]以内的要求,属于高碱煤煤种。与常规动力用煤相比,该煤种燃用过程中,随着锅炉温度升高,煤中高岭石、伊利石、云母岩等黏土矿物质分解生成莫来石、偏高岭石、石英等耐熔矿物。这些耐熔矿物在高温条件下易与含碱性金属的矿物反应生成钠长石、钾云母、钙长石等低熔融矿物,进而反应生成低温共熔体,致使该煤种在高温锅炉条件下极易发生沾污、结渣[3-5]。为此,该地区大部分煤电锅炉设备无法长期稳定使用,极大增加了电站的运行成本。
目前,缓解准东煤沾污结渣现象的传统方法是向燃煤中加入配煤添加剂,例如高岭土等沾污性弱的煤种[6-8],但添加剂的成本也在一定程度上限制了电厂的有效运营。研究发现高碱煤自身灰能够捕捉煤中的碱金属元素,由于自身灰来源方便,这有可能会是解决燃用高碱煤结渣、沾污问题的有效技术途径之一。近年来,量子化学的发展为研究物质的微观结构提供了一种高效的手段,利用第一性原理计算固体的电子结构、热力学性质等微观性质已经成为越来越热门的研究领域之一[9-11]。本文模拟自身灰捕捉碱金属进行实验,探究自身灰对碱金属的捕捉特性,并基于第一性原理,量化探究高碱煤含Na复盐长石类矿物质钠长石的理化性质,进而为解决准东高碱煤种锅炉内沾污、结渣问题提供理论指导。
1 实验与理论
1.1 实 验
实验选用大南湖二矿煤作为研究对象,大南湖二矿煤的分析数据如表 1所示。由表1可知,大南湖二矿煤煤灰中含有较高的碱性氧化物CaO(25.48%)和Na2O(5.19%),而作为酸性氧化物的 Al2O3(5.05%)和 TiO2(0.7%)含量偏低,因此在高温锅炉条件下,会生成较多的低熔融矿物,使得该煤样具有较低的熔融温度,进而导致锅炉沾污结渣[12-13]。

表1 大南湖二矿样煤数据分析Tab.1 Data analysis of the properties of coal and ash samples
实验首先将粒径小于75 μm的实验煤样按照《煤灰成分分析方法》GB/T 1574–1995的规定进行815 ℃标准制灰。然后,将样煤(2.7548g)放置于小坩埚底部,其上层均匀覆盖一层自身灰(2.0023g)。同时取另外一小坩埚放入等质量的自身灰样,作为对比灰样。接下来将盖好坩埚盖的两坩埚同时放入 YFX5/16Q-YC型号高温多功能箱式电阻炉900 ℃马弗炉恒温区加热(15~20 min左右)至反应完全。取出坩埚放入干冰容器中低温冷却,待冷却后分别提取灰样、煤样、对比灰样。重复试验在1 000 ,1 100 ,1 200 ℃条件取样。最后对取样样品依次通过X射线衍射(X-RayDiffraction,XRD )以及电感耦合等离子光谱发生仪(inductive coupled plasma emission spectrometer,ICP)进行了分析。
1.2 理论与计算
采用基于第一性原理(first-principles)的超软赝势(ultrasoft pseudo-potential)[14]平面波法,将离子势用赝势替代,用平面波基组展开电子波函数,结构优化采用BFGS算法[15],密度泛函总能计算则是在Perdew等提出的广义梯度近似(GGA)[16]下进行。利用Materials Studio软件包中CASTEP[17]模块,对含Na复盐长石类矿物质钠长石进行量子化学优化计算。为了保证计算精度,总能量精度为1.0×10-5eV/atom,能量截断值为370.0 eV,周期性边界条件选取物质的晶体原胞,采用Monkhost-Pack方法布里渊区抽样,K点网格尺寸设置为3×3×2。
2 结果与讨论
2.1 自身灰对不同元素的捕捉效果
根据ICP数据分析结果,由反应后灰中某种元素含量减去对比灰样中该元素含量,得到该元素反应前后绝对变化量,再用该绝对变化量除以原煤样该元素总含量,得到自身灰对该种元素的捕捉效率。以900 ℃煤灰反应实验数据为例,自身灰对高碱煤中常见元素的捕捉效率如图1所示。
由图1可知,实验反应过程中,Na,Mg,K,Cr,Al,S,Ca等元素从煤样中迁移到自身灰样中,被自身灰捕捉,不同元素的捕捉效率不同,其中Na元素捕捉率高达45.15%。这说明原煤样与自身灰接触反应过程中,不同的元素有不同的行为特性,煤样中大量的Na透过反应界面迁移到灰样中,被自身灰固定。目前的研究表明,高碱煤中Na的含量过高是造成锅炉沾污问题的关键因素[18]。区别于传统方法向煤中加入添加剂[19],尝试利用自身灰捕捉煤中碱金属来缓解高碱煤,特别是高钠煤沾污结渣问题,具有十分重要的意义。

图1 自身灰对不同元素的捕捉效率Fig.1 Capture efficiency of the own ash on different elements
2.2 Na元素的迁移特性
反应过程中,煤灰中矿物组成随温度变化出现较大的差异。通过XRD分析,图2为实验灰样中一些主要矿物质组分随温度的变化规律。图中:Q代表石英quartz;Alb代表钠长石albite;N代表霞石nepheline;A代表硬石膏anhydrite;An代表钙长石 anorthite;H代表赤铁矿hematite;Ru代表金红石rutile。XRD谱图是X射线衍射仪以2θ的角度扫描整个衍射区域,2θ为角度变化,作为X射线衍射谱的横坐标。

图2 不同温度下实验灰样XRD谱图Fig.2 XRD patterns of samples at different temperatures
如图2所示,以典型元素Na为例,分析实验反应过程中矿物质迁移特性。对比815 ℃标准灰样XRD图像,在900~1 200 ℃条件下,含Na元素矿物质衍射峰出现了明显的变化。温度为900~1 000 ℃时,含Na元素的主要矿物质霞石和钠长石衍射峰都出现了增长,这是由于灰样与煤样接触时,Na元素通过反应层从煤样中进入灰样被灰样捕捉,游离到灰样中硫酸盐晶系或者硅铝酸盐体系中,形成无水芒硝、霞石、钠长石等[20-22]。温度为1 100 ℃时,由于温度接近钠长石的熔点,钠长石中的Na将会被释放出来,最终以熔点较高的霞石形式滞留灰样中。当温度进一步升高至1 200 ℃时,灰样主要以无定型的熔融态存在,只有石英及微量的霞石被检测到。
2.3 钠长石的量化计算
根据以上结果,霞石和钠长石是煤灰捕捉过程中含量变化较为突出的含Na元素的碱金属矿物质,在实际锅炉条件下,这两种矿物质易与其他矿物质结合形成低温共融体,这是造成沾污、结渣的主要原因[23-24]。研究煤灰矿物质的理化性质,从微观层面上认识煤灰矿物质特性,能够对矿物质的宏观特性作出解释和预测[25],进而可以给工业实践及改善研究提供理论上的指导。下面以钠长石为例,量化探究其微观层面的一些理化性质。
钠长石的分子式为NaAlSi3O8,其晶格属三斜晶系,空间群C1,晶胞参数a=0.814 nm,b=1.279 nm,c=0.716 nm,α=94.19 °,β=116.34 °,γ=87.39 °。钠长石优化后的结构如图3所示,由[Al—O4]四面体和[Si—O4]四面体相互连接,构成一个由4个四面体围成的四方环组成的链。链与链之间相互连接,同一链中相邻的两个水平环彼此扭曲了一定角度形成空穴,Na+占据在空穴的间隙中。由于四方环链特殊的不对称结构,钠长石化学性质不太稳定,容易在外界条件下与其他矿物质发生反应。
钠长石的总态密度如图4所示,费米能级(图中虚线部分,能量E=0)位于左侧态密度范围内,且左侧峰值较高,右侧距离费米能级较远的为导带,且峰值较低,这表明了钠长石更倾向于和亲电体系(电子接受体)反应。当有外来离子作用于钠长石时,带正电的离子更容易进入钠长石晶格进行相变重组。
钠长石的电荷密度和电荷差分密度如图5所示,由电荷密度分布可以看出钠长石晶格体系电荷主要分布于[Si—O4]四面体与Na离子周围,这两者电荷相互作用,维持体系结构的稳定。由电荷差分密度则更明显看出氧原子带有较多的电荷,能量较高,因此当与亲电体系反应时,氧原子上的电子更容易发生转移参与化学反应。
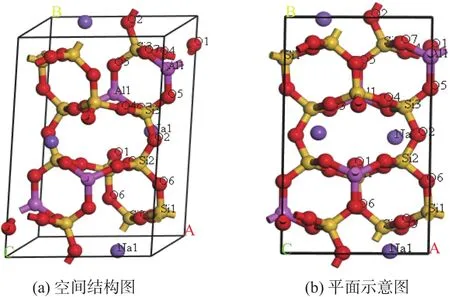
图3 钠长石结构图Fig.3 Structure of albite
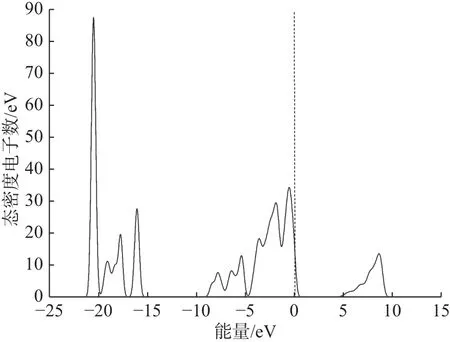
图4 钠长石总态密度图Fig.4 Density of states of albite

图5 钠长石电荷密度图和差分密度图Fig.5 Electron density and electron density difference of albite
图6 (见下页)给出了钠长石的最高能量占据轨道(HOMO)与最低空轨道(LUMO)分子轨道。图中大块的区域表示电子云的密集分布,表明不同原子轨道电子的贡献情况。参照钠长石晶体结构图3,从HOMO图中可以看出,大量的电子云(波函数的平方)几乎全部密集在氧原子周围,可知钠长石的最高占据轨道几乎是由氧原子电子轨道的2p轨道组成。因此,当钠长石体系与其他体系发生作用时,HOMO氧原子上的电子容易发生转移而参与其他体系成键,电子将从钠长石体系中的氧原子转移到其他亲电系。从图6中钠长石体系的LUMO轨道可以看出,少量电子云存在氧原子和Al原子周围,可知钠长石的LUMO主要由晶格内的部分Al原子轨道和几乎全部氧原子的2p轨道组成,而Si原子对轨道的贡献较低。

图6 钠长石的最高占据轨道与最低空余轨道Fig.6 HOMO and LUMO of albite
根据表2可以看出,钠长石结构中所有Al—O键的键长明显大于Si—O键的键长,所以Si—O键化学键更加稳定,当有离子作用于钠长石时,Al—O键要比Si—O键可能先发生断裂现象。另外,[Al/Si—O4]四面体组成的小四方环中,两个[Al—O4]四面体中的Al—O键键长分别相等,[Si—O4]四面体中的Si—O键长度也几乎相等,说明两个[Al—O4]四面体大小相等,环中其他[Si—O4]四面体也相等。但[Al—O4]四面体明显大于[Si—O4]四面体,该处的反应活性比较高。

表2 钠长石几何优化后部分键长数据Tab.2 Part of bond length data of the albite cell
3 结 论
a. 试验中,高碱煤自身灰对于样煤中不同金属元素都有一定程度的捕捉,其中对Na的捕捉效率达到了45.15%,这表明利用自身灰来解决高碱煤,特别是高钠煤沾污问题是一条十分理想的途径。
b. 自身灰捕捉的Na元素主要赋存于霞石、钠长石等矿物质中,而霞石、长石类钠盐是造成锅炉沾污问题的关键因素。不同温度条件下,Na元素的迁移特性不同,适当的温度条件对于高碱煤Na元素迁移具有一定的控制效果。
c. 经过量化计算,钠长石是一种化学反应活性较为活泼的高碱煤矿物质,其结构不稳定,易与亲电体系发生反应进行晶格重组,当带正电的离子作用于钠长石时,HOMO上的氧原子更容易转移电子参与体系反应成键。

