P-Gemox方案与P-GDP方案治疗NK/T细胞淋巴瘤的疗效比较
王杰松 杨 瑜 何鸿鸣 林剑扬 郑艳彬 吴 晖 陈道光 陈 英 陈宁斌 邹思平 陈秀容 王 畅
作为非霍奇金淋巴瘤的特殊类型,结外NK/T细胞淋巴瘤主要分布于亚洲及部分南美地区,具有明显的种族及地区特异性。世界卫生组织(World Health Organization,WHO)于2001年将本病划为淋巴造血组织肿瘤新分类中的独立类型,与EB病毒感染有明确相关性。虽然结外NK/T细胞淋巴瘤较为罕见,发病率低,但我国近年来检出率呈增高趋势,2012年的一项大宗调查显示国内发病率为6%[1]。本病常侵犯鼻腔、鼻咽、鼻窦、喉咽、喉头,恶性程度高,复发率、死亡率高[2]。早期结外NK/T细胞淋巴瘤对放疗较敏感,但对蒽环类为主的传统化疗不敏感,对多种化疗药物耐药,晚期预后极差[3]。美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南中推荐培门冬酶联合Gemox方案(即P-Gemox方案)治疗,由于其临床疗效、安全性较为可观,已成为NK/T细胞淋巴瘤的一线治疗方案。然而,由于本病发病率较低,难以进行大型随机临床对照试验,临床仍缺乏大规模前瞻性研究证实哪种方案更有效,目前本病的化疗方案选择仍有争议,至今未形成标准的治疗模式[4-5]。为此,本研究回顾性对比分析培门冬酶联合Gemox方案与培门冬酶联合GDP方案的临床疗效,以期为结外NK/T细胞淋巴瘤的临床治疗提供一定参考。
1 资料与方法
1.1 一般资料 回顾性分析2015年2月至2017年10月福建省肿瘤医院淋巴瘤头颈部肿瘤内科收治的73例结外NK/T细胞淋巴瘤患者的临床资料,其中35例接受培门冬酶联合Gemox方案化疗(A组),38例接受培门冬酶联合GDP方案化疗(B组)。纳入标准:①年龄≥15岁;②经淋巴结或鼻咽部肿物活检、组织病理学检查及免疫组织化学染色确诊,NK/T细胞抗原表达(无B细胞抗原表达),伴或不伴邻近器官或结构受侵;③初治患者;④预估生存期≥3个月;⑤血常规,肝、肾功能,心电图或心脏彩超检查结果正常;⑥未合并第二肿瘤;⑦临床各项资料完善。排除标准:①无法明确诊断;②无法耐受相关化疗或存在化疗禁忌;③已接受局部放疗或手术治疗;④已接受过其他形式的化疗、放疗或其他肿瘤内科相关治疗;⑤严重的心、肺、脑、肝、肾等重要脏器功能不全;⑥治疗依从性差。两组患者性别、年龄、病变部位、结外浸润和骨髓浸润、Ann Arbor国际分期[6]等基线资料差异均无统计学意义(P>0.05),详见表1。
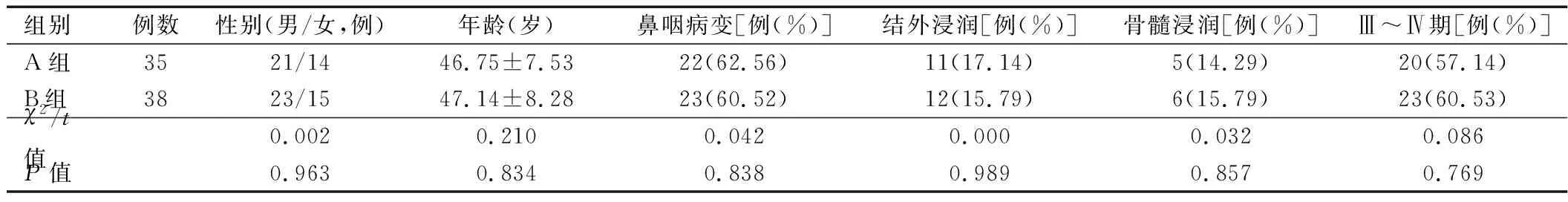
表1 两组患者临床基线资料比较[例(%)]
注:A组接受培门冬酶联合Gemox方案化疗,B组接受培门冬酶联合GDP方案化疗
1.2 治疗方法 早期(Ann Arbor国际分期I~Ⅱ期)患者采用放化疗结合,即先诱导化疗2 周期后开始放疗,放疗(剂量56 Gy)结束后继续完成剩余化疗,晚期(Ⅲ~Ⅳ期)患者以全身化疗为主,所有患者化疗均为3周1次,早期患者化疗疗程为6周期,晚期为8周期。A组:第1天肌内注射培门冬酶(江苏恒瑞医药股份有限公司,国药准字H20090015)2 500 IU/m2;第2天静脉滴入奥沙利铂(杭州中美华东制药有限公司,国药准字H20113457)130 mg/m2+5%葡萄糖500 mL;第1、8天静脉滴入吉西他滨(齐鲁制药有限公司,国药准字H20113285)1 000 mg/m2+生理盐水100 mL。B组:第1天肌内注射培门冬酶2 500 IU/m2;第1、8天30 min内静脉滴注吉西他滨1 000 mg/m2;第1~3天每天静脉滴注顺铂(齐鲁制药有限公司,国药准字H20073652)20~25 mg/m2;第1~4天静脉滴注地塞米松(江苏华阳制药有限公司,国药准字H32020818)40 mg。化疗期间所有患者均常规给予止吐药、胃黏膜保护、护肝、营养心肌等对症干预。
1.3 疗效评价 化疗4个周期后进行血常规、电解质、肝肾功能等生化检查及CT、PET-CT等影像检查。参考实体瘤客观疗效评价标准1.1版[7]评价化疗近期疗效,分为完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、病情稳定(stability of the disease,SD)及疾病进展(disease progression,PD),总有效率(total effective rate,RR)=(CR例数+PR例数)/总例数×100%。
1.4 安全性评估 参照肿瘤化疗药物新的不良反应评价系统-CTCAE v3.0[8]将胃肠道反应、白细胞减少、肝功能异常等药物不良反应情况分为1~5级。
2 结果
2.1 近期疗效比较 A组CR 18例、PR 10例、SD 5例、PD 2例,RR为77.14%;B组CR 21例、PR 8例、SD 6例、PD 3例,RR为76.32%,近期疗效比较差异无统计学意义(χ2=0.145,P=0.704)。
2.2 不同病变特征近期疗效比较 B组非鼻咽病变患者RR为66.67%,与A组的76.92%接近,差异无统计学意义(χ2=0.359,P=0.549);B组发生结外或骨髓浸润的患者RR为94.44%略高于A组的75.00%,Ⅲ~Ⅳ期的患者RR为86.96%略高于A组的70.00%,差异均无统计学意义(χ2=2.553、1.859,P=0.110、0.173)。详见表2~4。
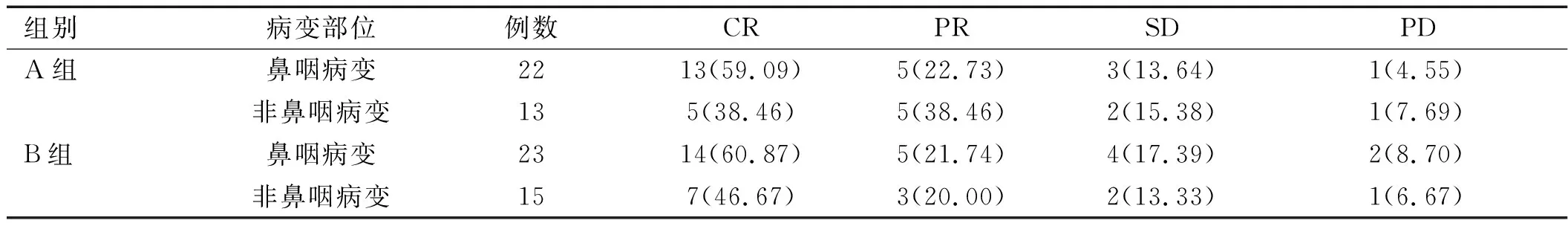
表2 两组不同病变部位患者近期疗效比较[例(%)]
注:A组接受培门冬酶联合Gemox方案化疗,B组接受培门冬酶联合GDP方案化疗;CR为完全缓解,PR为部分缓解,SD为病情稳定,PD为疾病进展
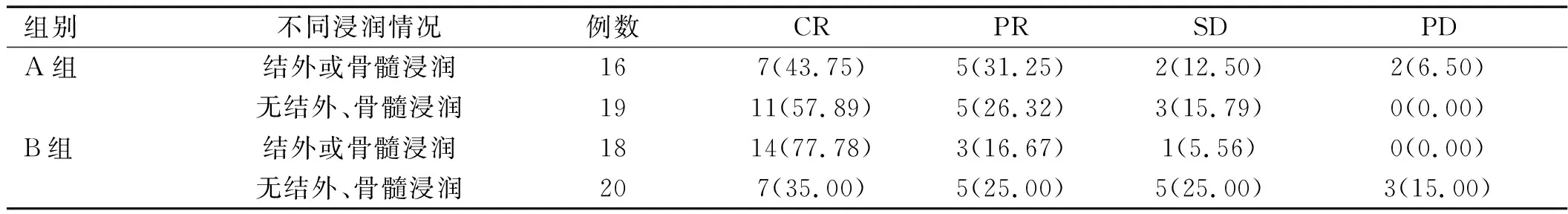
表3 两组不同浸润情况患者近期疗效比较[例(%)]
注:A组接受培门冬酶联合Gemox方案化疗,B组接受培门冬酶联合GDP方案化疗;CR为完全缓解,PR为部分缓解,SD为病情稳定,PD为疾病进展
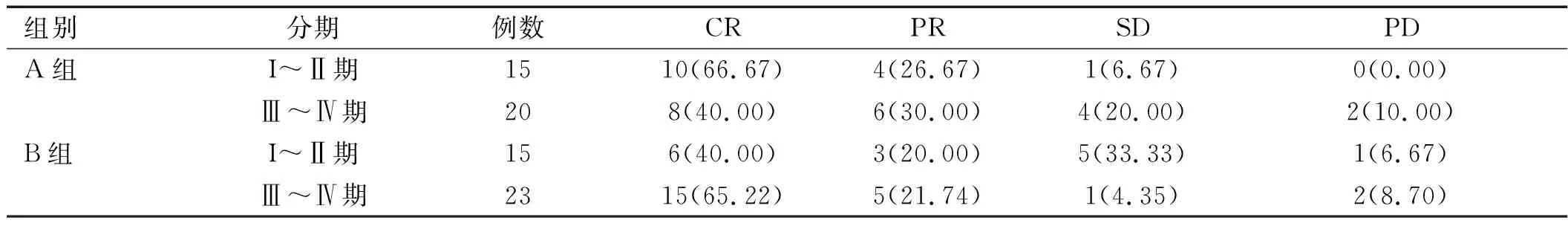
表4 两组不同分期患者近期疗效比较[例(%)]
注:A组接受培门冬酶联合Gemox方案化疗,B组接受培门冬酶联合GDP方案化疗;CR为完全缓解,PR为部分缓解,SD为病情稳定,PD为疾病进展
2.3 化疗安全性比较 两组患者化疗期间不良反应以胃肠道反应(恶心、呕吐、腹泻)为主,其中B组胃肠道反应发生率为28.95%,略高于A组的17.14%,但差异无统计学意义(χ2=1.421,P=0.233);A组、B组总不良反应率分别为37.14%、50.00%,差异无统计学意义(χ2=1.223,P=0.268);不良反应对症干预后均能耐受,未出现因严重不良反应而中断治疗者。详见表5。
注:A组接受培门冬酶联合Gemox方案化疗,B组接受培门冬酶联合GDP方案化疗;胃肠道反应包括恶心、呕吐、腹泻等,骨髓抑制包括白细胞减少、血红蛋白降低及血小板减少等,肝功能异常包括肝脾肿大、疲乏无力等
3 讨论
结外NK/T细胞淋巴瘤占全部非霍奇金淋巴瘤的5%~15%,以鼻、面部中线部位的病变为特征,主要发于鼻腔,也可发于韦氏环,并侵及鼻咽、扁桃体、口咽和舌根等部位,病变可引起面部广泛毁损及形成溃疡[9]。患者临床症状不典型,主要有鼻塞、流涕、鼻衄、吞咽困难,可伴发热等。结外NK/T细胞淋巴瘤患者的病情进展过程不均一,部分患者可经过放化疗实现治愈,而部分患者即使接受针对性化疗和/或放疗,病情控制仍较差,可出现早期局部或系统性复发,如发展皮肤、肝脏、胃肠道及睾丸等处的转移,呈现高度恶性的生物学特征。但临床一致认为尽早采取积极的综合治疗是提高临床疗效及延长生存期的必要手段[10-11]。虽然相关报道[12]已证实,结外NK/T细胞淋巴瘤患者患者对放疗敏感,但单纯放疗的初治患者复发率较高。故放化疗联合治疗仍是本病的推荐疗法。
以往传统的化疗方案多为CHOP(环磷酰胺+表柔比星+长春新碱+泼尼松),随着临床治疗经验的积累,该方案治疗结外NK/T细胞淋巴瘤的局限逐渐凸显,主要表现为受P-糖蛋白高表达的影响,NK/T细胞淋巴瘤对此化疗方案不敏感,存在多药耐药[13]。随着临床新方案的多项研究开展,含L-天门冬酰胺酶类方案治疗逐渐引起临床的广泛关注,被证实在包括晚期、复发或难治性NK/T细胞淋巴瘤患者中可取得可观的疗效[14]。尤其是作为L-天门冬酰胺酶的长效制剂,培门冬酶具有较低的免疫原性,无需皮试,使用更方便。培门冬酶联合Gemox方案被认为是治疗结外NK/T细胞淋巴瘤的一线方案,并列入NCCN指南,很大部分的原因与培门冬酶的作用机制有关:淋巴瘤细胞需依赖宿主供给合成生长所必要的氨基酸门冬酰胺,培门冬酶能使门冬酰胺水解,使肿瘤细胞所需的门冬酰胺维持缺乏状态,从而起到抑制生长的作用;且这种机制不受P-糖蛋白限制[15]。培门冬酶为新型门冬酰胺酶制剂,主要用于急性淋巴细胞白血病患者一线治疗,与奥沙利铂、吉西他滨发挥协同作用,能够抑制DNA、RNA及蛋白质的合成发挥抗肿瘤作用,不仅可获得较好的近期治疗疗效,且从远期疗效来看,被证实可改善NK/T细胞淋巴瘤患者的生存结局[16]。尽管如此,由于缺乏大宗前瞻性报道,对培门冬酶联合Gemox方案的治疗效果仍存在一定质疑,且对部分患者的治疗效果仍存在个体化差异。因此,探索新的安全、有效治疗结外NK/T细胞淋巴瘤的方法仍然重要。
本院在结合临床治疗经验及相关文献报道[17-18]的基础上对培门冬酶联合Gemox方案进行改良,即培门冬酶联合GDP方案。结果提示培门冬酶联合GDP方案治疗NK/T细胞淋巴瘤可取得与NCCN指南推荐的培门冬酶联合Gemox方案接近的近期疗效(RR:77.14%比76.32%),与左文丽等[19]的观点具有一致性,由此可认为培门冬酶联合GDP方案治疗NK/T细胞淋巴瘤具有可行性。进一步分析发现,培门冬酶联合GDP方案治疗发生结外或骨髓浸润的患者RR略高于培门冬酶联合Gemox方案(94.44%比75.00%),Ⅲ~Ⅳ期的患者RR亦略高(86.96%比70.00%),二者差异不明显可能与样本量较少有关,但仍可提示改良化疗方案在发生结外或骨髓浸润和晚期患者中有一定优势,可能与GDP方案对肿瘤细胞的抑制作用更强或地塞米松的溶淋巴作用突出及部分晚期患者对此方案药物更敏感有关,但其具体机制需进一步深入探究。安全性方面,2种方案不良反应以胃肠道反应为主,对症干预后均能耐受,提示培门冬酶联合GDP方案安全性可接受,值得关注的是其胃肠道反应发生率、总不良反应率略高于培门冬酶联合Gemox方案,还需引起关注,建议在应用此方案过程中可采取措施预防或减轻不良反应尤其是胃肠道反应。总之,与培门冬酶联合Gemox方案相比,培门冬酶联合GDP方案治疗NK/T细胞淋巴瘤同样可取得满意的近期临床疗效,鉴于本研究患者多数仍在随访中,改良方案对预后的影响仍需后期补充论证。

