后腹腔镜单层面肾上腺肿瘤切除术的临床研究(附53例报告)
马亚南 王志新 丁友鹏 魏鑫 侯毅 孔祥波
1吉林大学中日联谊医院泌尿外科 130000 长春
肾上腺解剖位置较深,位于腹膜后上方,与较多重要器官以及腹腔大血管毗邻,解剖关系复杂,开放手术难度大,风险高。自从Gagner等[1]于1992年首次报道通过腹腔镜的术式治疗肾上腺肿瘤以来,腹腔镜肾上腺切除术逐渐被泌尿外科医生接受。张旭等[2]提出后腹腔肾上腺解剖理论,为腹腔镜肾上腺手术后腹腔入路奠定了基础,并使之成为了腹腔镜肾上腺肿瘤手术标准入路。随着近年来后腹腔镜技术发展,越来越多的泌尿外科医生更倾向于选择经后腹腔镜入路进行肾上腺肿瘤的切除,与传统后腹腔镜肾上腺三层面分离方法相比,我们通过采取单层面分离方法游离肾上腺肿瘤,即仅分离肾内上方的肾周脂肪囊与肾周筋膜前层之间的相对无血管区,同样可以达到同样的治疗目的。为进一步探讨单层面后腹腔镜治疗肾上腺肿瘤的价值,现回顾性分析2016年10月~2017年12月于我科采用该术式治疗肾上腺疾病的患者临床资料,报告如下。
1 资料与方法
1.1临床资料
选取行后腹腔镜单层面肾上腺切除术患者共53例,其中男21例,女32例,年龄28~63岁。左侧35例,右侧18例;腹部CT示肿瘤直径为0.6~4.2 cm,平均2.4 cm(图1A)。实验室检查包括血尿皮质醇、醛固酮、儿茶酚胺以及电解质等。其中血游离皮质醇升高37例[(874±289)nmol/L],24 h尿游离皮质醇升高12例[(273±47)nmol/24 h];血浆醛固酮升高10例[(0.904±0.078)nmol/L],血浆肾上腺素升高3例[(802±142)pmol/L]。根据术前血浆激素及离子水平,结合部分小剂量地塞米松抑制试验,术前定性诊断:功能性肾上腺肿瘤50例(其中可疑库欣综合征28例),无功能腺瘤3例。据术前检查控制血压、血糖,纠正电解质紊乱,怀疑嗜铬细胞瘤的患者口服酚苄明,必要时加用β受体阻滞剂,术前3 d行扩容准备。
1.2手术方法
所有患者均于全麻成功后实施手术,患者取健侧卧位,垫腋卷、升高腰桥,腰部常规无菌消毒、铺无菌巾单。于腋后线与肋缘下交点切开约2 cm,逐层钝性分离至腹膜后间隙,利用球囊扩张器扩张腹膜后腔隙,分别建立三处操作通道:肋缘下腋后线交点、肋缘下腋前线交点、髂前上嵴上方2横指,分别置入一个5 mm Trocar及两个10 mm Trocar。设置气腹压力1.596 kPa(12 mm Hg),流量20 L/min,直视下游离腹膜外脂肪,钝锐性结合分离并清除上至膈肌、下至髂窝之间的脂肪组织,辨认侧椎筋膜、腹膜返折、肾筋膜、腰大肌,使用超声刀纵行切开肾筋膜进入肾周脂肪囊(图1B),于肾脏内上方肾周脂肪囊与前层肾筋膜之间相对无血管区作为分离层面,于肾脏内侧上方分离至肾上腺区,充分暴露肾上腺组织(图1C),提起肾上腺边缘脂肪组织,于肾上腺外缘靠近肾上极处超声刀离断肾上腺与肾上极,并逐渐向下分离至中央静脉,充分游离中央静脉;提起肾上腺上动脉条带区逐步暴露肾上腺背侧并用超声刀离断,完整切除肾上腺肿瘤及一部分肾上腺组织(图1D)。局部确切止血。清点器械纱布无误,无活动性出血,切除的肿瘤送检病理,肾上腺区留置胶质引流管一枚,缝合皮肤切口,结束手术。
2 结果
本组53例手术均成功实施,中途未改变手术方式,手术时间21~57 min,平均36 min;术中出血量15~40 ml,平均25 ml,术后病理诊断:肾上腺皮质腺瘤38例,肾上腺皮质结节样增生9例,嗜铬细胞瘤3例,肾上腺囊肿1例,髓脂肪瘤2例。术中腹膜损伤1例,未发生其他并发症,术后视引流量留置引流管2~3 d,术后第2天拔除导尿管,平均住院6~9 d。随访3个月,术中及术后均未发生皮下气肿、切口愈合不良等严重并发症,临床症状明显缓解或完全消失。
3 讨论
近年来,随着腹腔镜微创技术及器械发展与应用,肾上腺肿瘤的治疗已经发生了里程碑式的变化,经腹腔镜下肿瘤的切除已经成为肾上腺肿瘤治疗的金标准[3],其中最常用的入路为经后腹腔途径,此路径分离肾上腺较为直接, 但较经腹入路手术难度大[2]。
后腹腔镜肾上腺切除术主要在肾脏与肾上腺周围的间隙进行操作,肾上腺上动脉、下动脉以及中动脉主要位于肾上腺的内侧。张旭[4]通过对后腹腔解剖关系的研究,证明了在肾上腺的外侧面、前后面以及底面与肾上极相邻的区域存在相对无血管区,肾上腺各动脉较多且细小,一般可采用超声刀直接凝切,在相对无血管层面内进行肾上腺肿瘤的分离,解剖层次清楚,对周围脏器的损伤小,术中出血少,术野清晰,提高了手术安全性。但对于腹膜后脂肪组织少、体形瘦削的患者,传统三层面法过多游离肾上腺周围组织可能存在肾下垂的风险,体形肥胖患者由于腹膜后脂肪较多,三层面游离法存在手术时间长,操作困难等问题。唐炎权等[5]认为双平面改良暴露法在开展初期容易损伤后腹膜,影响操作空间,需要对后腹腔解剖标记有一定的熟悉。席俊华等[6]通过对后腹腔镜三层面和两层面法肾上腺肿瘤切除术对比,认为充分游离肾脏内上方脂肪囊与前层Gerota筋膜之间的相对无血管间隙,可以快速找到肾上腺肿瘤。付亚军等[7]通过开放手术与后腹腔镜术式治疗肾上腺肿瘤的对比,证实后腹腔镜术式治疗肾上腺肿瘤具有操作较简便、手术时间短、术中出血少、微创及术后恢复快等优势。
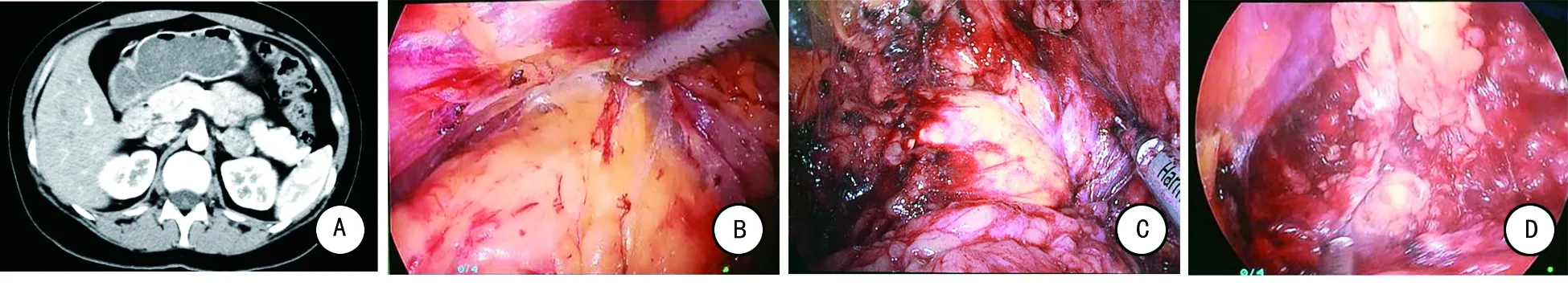
A:术前肾上腺CT资料;B:钝锐性结合分离脂肪组织;C:暴露肾上腺肿瘤;D:完整切除肾上腺。
图1后腹腔镜单层面肾上腺肿瘤切除术资料图
术者术中操作一定要在视野中进行,应熟悉肾上腺解剖,如果出现周围脏器损伤以及其他严重并发症时应及时中转开放手术[8]。Walz等[9]认为肾上腺肿瘤部分切除术如果能确切切除肾上腺肿瘤及肿瘤周围部分肾上腺组织,同样可以达到治疗肿瘤的目的。何竑超等[10]采用距肾上腺肿瘤边缘5 mm切除等方法完整切除肾上腺肿瘤,最大程度地保留了肾上腺功能,并提出手术关键在于准确辨认肿瘤与周围肾上腺组织的界限。
由此,通过对术前CT中对肾上腺肿瘤与周围脏器空间位置结构的比较分析,我们在传统后腹腔镜三层面肾上腺解剖基础上采取仅单纯分离肾内上方肾周脂肪囊与前层肾周筋膜之间的相对无血管区,暴露肾上腺组织从而达到切除肾上腺肿瘤的目的,省略了对另外两个层面的游离。该手术入路减少手术对肾脏周围结构的过多游离,能有效地避免肾脏损伤及肾下垂等风险。根据目前我们的经验,建议选取中等偏瘦,肾上腺肿瘤大小主要为小于4 cm的患者实施手术。现阶段我们尚缺乏对巨大肾上腺肿瘤切除的研究。后腹腔镜下肾上腺切除术常见的术中并发症有动静脉损伤、周围脏器损伤(如肾脏、胰腺等)、胸膜及腹膜损伤。对于直径大于6 cm的肾上腺肿瘤需要术前评估其恶性病变的潜在风险,巨大肾上腺肿瘤切除术中存在与周围脏器黏连的风险、且由于肿瘤组织血运比较丰富,从而易造成术中周围脏器损伤和大出血,甚至造成肿瘤残留,以至肿瘤复发[11]。Agrusa等[12]通过对14例平均直径为8.2 cm的巨大肾上腺肿瘤切除方式的研究,认为经腹腔入路的腹腔镜下手术更具安全性。
总之,后腹腔镜单层面肾上腺肿瘤切除术具有缩短手术时间,减少术中出血量,对周围脏器副损伤少的优点,值得临床应用,但对术者对肾上腺解剖的熟悉程度以及腹腔镜技术操作要求更高。此外,由于该研究病例数量少、随访时间较短以及单层面治疗巨大肾上腺肿瘤经验较少,研究结论还有待更大规模随机对照研究证实。