关于岩矿中稀有和稀散元素的化学分析
许 军 军
(山西省地质勘查局二一三地质队,山西 临汾 041000)
0 引言
我国幅员辽阔,矿产资源储量丰富,分布范围广,种类品种多,并且富含大量的稀有金属元素,这些稀有金属元素因其特殊性能,在原子能工业、电气工业、化学工业等具有重要的价值功能,因此需要加强对稀有金属的分析与开采,对于我国社会经济发展具有重要的意义。然而大部分稀有金属元素多分布于岩矿资源中,并且这些岩矿所在地大多地处偏远,且地形地势复杂,对于稀有金属元素勘察和分析带来了很大的挑战,需要不断进行稀有金属的测定方法创新,才能提升稀有金属元素勘察和分析效率。因此有必要对岩矿中稀有金属元素化学分析方法进行分析,使其准确度变得更高,期望为岩矿勘探的实践工作提供一些小小的帮助。
1 矿区地质状况
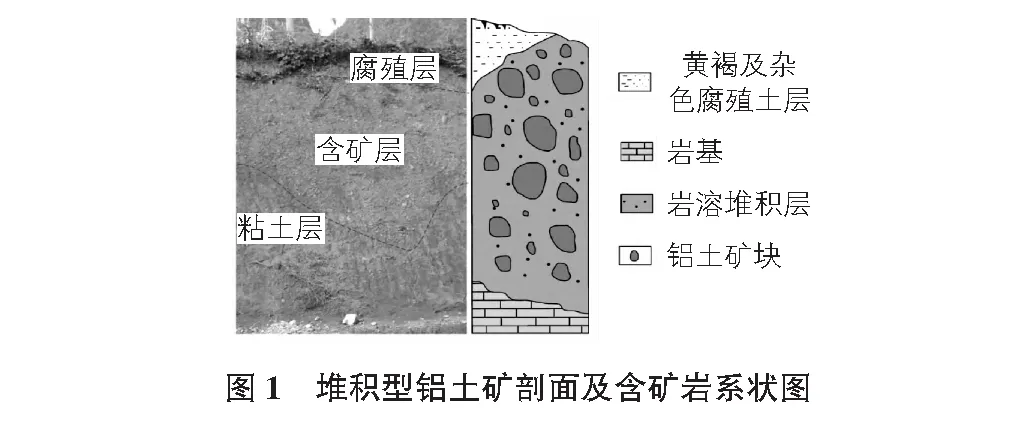
以某地区铝土矿为例,该区域基底主要为上寒武,盖层为盆系至中三叠统,不同时期下构造运动对该区域铝土矿产生了非常大的影响,并逐渐形成了一系列褶皱和断裂构造,该构造方向以北西向为主,并且这些构造非常发育,与铝土矿矿床的分布具有密切的联系。在二叠统茅口组的古风化壳内,存储着大量沉积型铝土矿,在垂向上方向,伴生有粘土层、黄铁矿层和煤层,大多是沿着褶皱的两翼进行产出,部分直接假整合于茅口阶灰岩之上,产状与基底大致相同,在厚度方面,由于基底起伏不定,因此厚度也随之变化,呈不均匀状。该区域的铝土矿层风化面颜色主要以灰黑色、深灰色为主,产出多为层状,下部结构为碎屑状,上部矿石质量较好,一水硬铝石为主要矿物,其次为三水铝石,伴生有黄铁矿、粘土矿物等硅质矿物,角砾状矿石分布在底部。岩溶作用的主要产物便是堆积型铝土矿,该矿矿岩系主要赋存于上泥盆统融县组至下岩溶洼地、谷地中,岩溶洼地、谷地的基底主要为二叠统茅口组碳酸盐岩,厚度范围为3 m~15 m,自下而上分层,可分为3层,其中第一层位于底部,是粘土层,颜色主要为紫红色,土质主要为粘土,局部含少量铝土矿、褐铁矿碎屑,且其磨圆度较好,并沿着基岩呈喀斯特凹陷进行分布;第二层位于中部,是堆积铝土矿层,颜色主要为土红色,土质主要组成部分包括铝土矿碎块、碎屑及粘土,含少量褐铁矿碎屑,磨圆度较差;第三层位于上部,是粘土层,颜色主要为红色或黄褐色,土质为砂质粘土,并含有少量的铝土矿,岩石碎屑,顶部为腐殖层。具体如图1所示。
经过对该区域进行土样采集,经检测发现该铝土矿富含稀有及稀散元素,主要包含Ga,Se,Cd,Te,Li,Be,Hf,Nb等。文章对其中的Li元素含量进行了化学分析。
2 岩矿中稀有金属的化学分析——以堆积型铝土矿为例
2.1 分离Li元素
针对含有Li元素的岩矿而言,要想进行对其的含量测定,首要工作即是先将Li元素从岩矿中进行分离。通过将岩矿中的Li元素进行预分离,从而以免在对其进行化学分析过程中,遭受到其他因素的影响。当大多数的金属氯化物处在相同的有机溶剂中时,其溶解度也是不相同的,其中氯化锂溶解度通常非常大,因此可以利用溶解度不同这一原理,进行Li元素的有效分离。例如在戊醇中,氯化锂的溶解度为6.5 g/100 mL,而堆积型铝土矿石中其他金属氯化物的溶解度都低于氯化锂的溶解度(例如Se2Cl2溶解度为0.008 g/100 mL),因此可以借助不同元素的溶解度差成功将Li分离出来。
2.2 测定方法
目前针对Li元素的主要测定方法是四氧硫酸锂称重法,即将锂元素经过一系列复杂转变,进一步转化四氧硫酸锂,最后通过测定四氧硫酸锂重量来对Li元素含量进行确定。具体原理如下,首先使用碳酸钙分解铝矿体样中的氯化铵,在去除钙元素后,得到大量的金属氯化物(碱金属)的混合体,然后对这一混合体进行蒸发处理,去除掉其中的无水丙酮,然后在其中加入盐酸和硫酸的溶剂,从而将氯化锂转化为四氧硫酸锂,最后通过称取四氧硫酸锂的重量,来测定Li元素含量。在使用该方法时,需要很多试剂及化学药品进行辅助,主要有盐酸和硫酸混合液(1∶1)、碳酸钙、氯化铵、草酸铵饱和溶液、氢氧化铵、碳酸铵饱和氢氧化钙饱和溶液。
2.3 具体化学分析步骤
先进行铝矿土岩石样本选取,一般重量为0.5 g,并称取相同重量的氯化铵,随后利用研缸,将二者进行研磨处理,直至研磨为细末状为止,然后再加入5 g碳酸钙,并混合均匀。在完成以上处理后,将混合细末放置在镍坩埚里,注意镍坩埚底部应铺有一层碳酸钙,然后将镍坩埚放在带有细孔的石棉板之上并进行低温加热,加热时间为10 min,10 min后进行高温加热,直至温度升至900 ℃左右,加热应持续一段时间,约为1 h。在完成加热后,等待坩埚稍稍冷却,需加入些许热水,并进行镍坩埚的壁的清洗,然后将烧结块混合热水一并移入到烧杯里,烧杯容量为200 mL。若发现烧结块质地较硬,不易在烧杯内进行压碎,那么可以先将其移放至研缸中,在研缸中将其磨成粉末,然后进行加水处理,加水总量控制在50 mL左右,接着进行加热煮沸,一般时间控制15 min为宜。随后将煮沸完成的液体过滤到另外一个烧杯中,为确保完全倾泻干净,需要将剩余的残渣水按照此步骤重复操作两次以上,并用饱和氢氧化钙饱和溶液进行洗涤处理。在处理完成后,可以利用蒸发方式,使得液体容量维持在100 mL,然后分别加入氯化铵(0.5 g)、浓氢氧化铵(2 mL)、饱和碳酸铵溶液沉淀钙(25 mL),并加热混合液体,待煮沸至5 min后进行过滤处理,然后利用热水进行沉淀处理,至少五次,并用蒸发皿进行滤液的采集,待液体蒸干后,进行灼烧处理,灼烧温度为500 ℃~600 ℃,目的是将铵盐进行去除。待器皿冷却后,用适量(10 mL左右)热水对器皿进行吹洗处理。添加盐酸、硫酸混合液(1∶1)2 mL,并蒸发至干,此时剩余的混合氯化物便是四氧硫酸锂。然后通过利用小棒,将其研磨成粉末状,随后加入无水丙酮25 mL与1滴浓盐酸,以免形成难溶于水的氢氧化锂,并对液体进行充分搅拌,待静止沉淀后,通过利用垂熔玻璃斗丙酮润湿了的滤纸进行滤液的收集,放置于器皿(已经提前进行了重量测试),然后利用丙酮,对沉淀进行洗涤处理,至少三次以上。
若发现在岩矿样本中,钾和钠元素含量较多,可以采取以下措施处理,首先将沉淀在少量水中进行溶解,然后进行蒸干处理,接着将剩余的残渣进行研磨处理,待研成粉末状后再用丙酮进行重复处理。之后再将混合滤液进行蒸发处理,将残渣中有机物质进行去除。等到冷却以后,加入硫酸润湿氯化物,再继续蒸发操作,并对其进行加热处理,将过量的硫酸进行去除,灼烧1 min以后,直至盐类熔融,待冷却后,即可对四氧硫酸锂进行计重处理。
3 结语
随着地质勘探工作不断发展,相应的矿物质针对稀有方法的化学分析技术也在不断的进行应用,进一步提升了化学分析工作的准确性及快捷性,有效提升了针对稀有及稀散元素化学分析工作的水平与质量,对于我国矿物质开发及经济水平提升具有重要的意义。

