西达本胺治疗外周T细胞淋巴瘤中国专家共识(2018年版)
外周T细胞淋巴瘤(peripheral T−cell lymphoma,PTCL)又称成熟T细胞淋巴瘤,是一组高度异质性来源于成熟T细胞的恶性增殖性疾病。由于NK细胞的免疫表型及功能与T细胞相似,因此常将NK细胞淋巴瘤和成熟T细胞淋巴瘤归为一类,即成熟NK细胞和T细胞淋巴瘤。
1 外周T细胞淋巴瘤概述
1.1 流行病学
PTCL的发病率具有明显的地域差异。在中国PTCL发病率约占非霍奇金淋巴瘤(non−Hodgkin's lymphoma,NHL)的25%~30%[1−3],显著高于欧美国家的 10%~15%[4−5]。根据 2017 年世界卫生组织(WHO)造血与淋巴组织肿瘤的分类标准,PTCL包括外周T细胞淋巴瘤,非特指型(PTCL not otherwise specified,PTCL−NOS)、血管免疫母细胞性T细胞淋巴瘤(angioimmunoblastic T−cell lymphoma,AITL)、结外NK/T细胞淋巴瘤,鼻型(NK/T cell lymphoma,NKT⁃CL)、ALK阳性间变性大细胞淋巴瘤(anaplastic large cell lymphoma,ALK−positive,ALK+ALCL)、ALK阴性间变性大细胞淋巴瘤(anaplastic large cell lymphoma,ALK−negative,ALK−ALCL)、蕈样肉芽肿(mycosis fun⁃goides,MF)、Sézary综合征(Sezary's syndrome,SS)等病理亚型(详见附录)[6−7]。
1.2 治疗现状
初治PTCL最常用的一线治疗方案为CHOP(环磷酰胺+多柔比星+长春新碱+泼尼松)和CHOP样方案。然而除ALK+ALCL外,上述方案对其他病理亚型的治疗疗效均较差,5年生存率仅为30%[5,8]。虽然自体造血干细胞移植可能改善部分患者的长期预后,但多数患者由于疾病状态或体能情况等原因无法接受造血干细胞移植。对于复发或难治性PTCL,2018年美国国立综合癌症网络(NCCN)治疗指南建议适用干细胞移植的患者,首先推荐参加临床试验。此外优选的治疗包括优选单药:即美国食品药品监督管理局(FDA)近年批准的普拉曲沙(pralatrexate)、罗米地辛(romidepsin)、贝利司他(belinostat)和brentux⁃imab vedotin(仅针对系统性ALCL及CD30+PTCL)新药[9];优选联合化疗方案:包括DHAP(顺铂+阿糖胞苷+地塞米松)、ESHAP(依托泊苷+甲基强的松龙+顺铂+阿糖胞苷)、GDP(吉西他滨+地塞米松+顺铂)、Ge⁃mox(吉西他滨+奥沙利铂)和ICE(异环磷酰胺+卡铂+依托泊苷)。不适用造血干细胞移植的患者,首先推荐参加临床试验。PTCL的传统二线化疗方案疗效并不显著,尤其是对蒽环类耐药的患者。对于结外NK/T细胞淋巴瘤,近年来研究已证实含左旋门冬酰胺酶/培门冬酶(PEG−Asp)的联合化疗方案具有较好的临床疗效[10−12]。其中,PEG−Asp联合Gemox方案(P−Ge⁃mox)对初治或复发难治性NK/T细胞淋巴瘤均显示出较好的疗效[13]。另外,放疗也是治疗的重要组成部分。
总之,传统化疗方案对于PTCL的治疗并不理想,随着临床研究的不断深入,组蛋白去乙酰化酶(histone deacetylase,HDAC)抑制剂作为一种新型抗肿瘤药物,已在PTCL治疗中取得显著成果。目前国家食品药品监督管理总局(CFDA)仅批准上市了新型HDAC抑制剂西达本胺(chidamide,爱谱沙®)。
2 西达本胺
2.1 化学结构及作用机制
西达本胺是苯酰胺类HDAC亚型选择性抑制剂。其化学名称和结构式如下:

化学结构式:
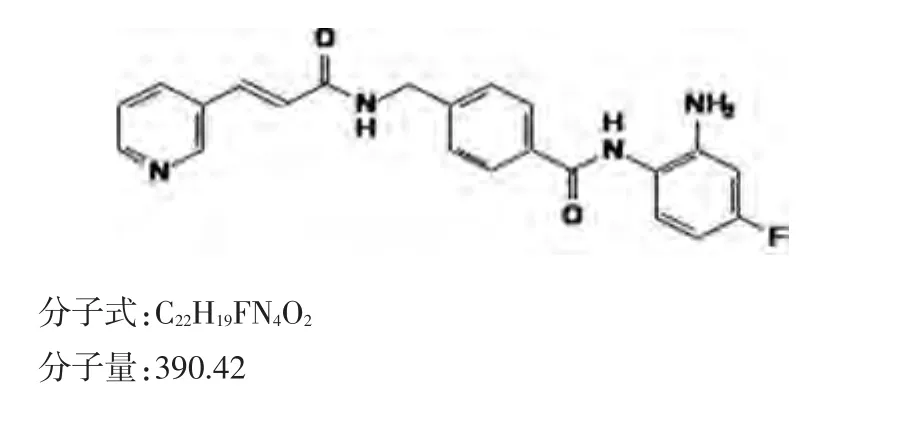
西达本胺主要针对第Ⅰ类HDAC中的1、2、3亚型和第Ⅱb类的10亚型,具有对肿瘤异常表观遗传功能的调控作用。其通过抑制相关HDAC亚型以增加染色质组蛋白的乙酰化水平来引发染色质重塑,并由此产生针对多条信号转导通路基因表达的改变(即表观遗传改变),进而抑制肿瘤细胞周期,诱导肿瘤细胞凋亡,同时对机体细胞免疫具有整体调节活性、诱导且增强自然杀伤细胞(natural killer cell,NK)和抗原特异性细胞毒T细胞(cytotoxic T cells,CTL)介导的肿瘤杀伤作用[14−17]。西达本胺通过表观遗传调控机制,具有诱导肿瘤干细胞分化、逆转肿瘤细胞的上皮间充质转化(epithelial mesenchymal transition,EMT)等功能,进而在恢复耐药肿瘤细胞对药物的敏感性和抑制肿瘤转移、复发等方面发挥潜在作用[18−19]。
2.2 针对PTCL的主要研究成果
2.2.1 关键性临床Ⅱ期试验 在关键性临床Ⅱ期试验(注册性临床试验)中,共入组83例复发或难治性PTCL患者,全部接受30 mg/次、2次/周的西达本胺片治疗,直至疾病进展或出现不可耐受的不良反应为止。主要疗效指标为客观缓解率(objective response rate,ORR)。79例患者进行疗效评价,结果显示,ORR为28%,中位无进展生存期(median progression−free survival,mPFS)和总生存期(overall survival,OS)分别为2.1个月和21.4个月,3个月的持续缓解率为24%。最常见的3~4级不良反应为血小板减少(22%)、白细胞减少(13%)和中性粒细胞减少(10%)[20−21]。
2.2.2 联合方案和单药优化方案的探索性研究
1)针对复发或难治性PTCL的研究:在一项西达本胺联合PCT(泼尼松+环磷酰胺+沙利度胺)方案治疗复发或难治性PTCL的临床研究中(NCT 02879526),探索阶段共纳入12例患者,ORR为75%,完全缓解(complete response,CR)率为42%。中位随访时间为13(3~18)个月,其中疾病进展2例,死亡3例。最常见的3~4级不良反应为中性粒细胞减少(22%),血小板减少(16%)和血红蛋白减少(20%)[22]。该方案疗效显著,安全性较好,特别适用于肿瘤负荷不高的老年、不耐受或不接受化疗的患者。另外,还有多项联合方案治疗复发或难治性PTCL的临床试验正在开展,如西达本胺联合MEPC(泼尼松+环磷酰胺+依托泊苷+甲氨蝶呤,NCT03321890)、西达本胺联合ICE(异环磷酰胺+卡铂+依托泊苷,NCT02856997)以及西达本胺联合PET(泼尼松+依托泊苷+沙利度胺,NCT03273452)治疗AITL的临床试验等。在单药应用方面,一项考察单药不同用法、用量的临床试验(NCT02878278)结果显示,10mgqd和30mgbiw两种用药模式均有效,NK/T细胞淋巴瘤的ORR为66.7%、CR率为44.4%;PTCL的ORR为50%、临床获益率为50%。未检测到EB病毒(Epstein−Barr virus,EBV)再激活,证实外周血WBC H3乙酰化水平与其疗效相关[23−26]。
2)针对初治PTCL的研究:目前正在开展多项临床试验,包括西达本胺联合方案对初治PTCL(NCT02753543)和早期鼻腔NK/T细胞淋巴瘤(ChiC⁃TR−IIR−15007350)的疗效与安全性。
3)自体造血干细胞移植(autologous stem cell transplantation,ASCT)预处理方案的研究:在西达本胺增强ASCT预处理化疗疗效的临床试验中,预处理方案采用CGB(克拉屈滨+吉西他滨+白消安)联合西达本胺,入组20例PTCL患者,植活率为100%,移植相关死亡率为0。中位随访时间为10.3(3~26.5)个月,无事件生存(event−free survival,EFS)率为73.7%,OS率为78.8%[27]。
4)疗效相关的分子标志物探索研究:组蛋白甲基化(KMT2D)和乙酰化相关(EP300、CREBBP)基因突变与PTCL−NOS患者化疗耐药相关,提示西达本胺对具有上述突变的患者可能有效[28]。
2.2.3 临床研究 西达本胺治疗PTCL的研究数据得到定期总结分析。截至2016年8月,研究共纳入接受西达本胺治疗的703例复发或难治性PTCL患者,中位年龄为55岁,男女比为64%∶36%,ECOG≥2分的患者占40%,Ⅲ~Ⅳ期占91%。其中接受单药治疗462例,联合其他治疗241例。疗效分析显示,接受西达本胺单药治疗的患者ORR为47%,其中最为多见病理亚型的单药ORR分别为PTCL−NOS(45%)、AITL(58%)、NK/T细胞淋巴瘤(28%)和ALK−ALCL(46%)。对于中高危患者,联合治疗较单药疗效优势明显,其中国际预后指数(IPI)[29]评分2~3分患者的联合治疗对比单药治疗的ORR为62.3%vs.47.1%(P<0.01);IPI评分4~5分患者的联合治疗对比单药治疗的ORR为54.9%vs.35.9%(P<0.05)。不良反应多为1~2级。单药最常见3~4级不良反应为血小板减少(11.0%)、中性粒细胞减少(9.7%)和血红蛋白减少(6.1%)。联合治疗最常见3~4级不良反应为血小板减少(27.4%)、中性粒细胞减少(25.3%)、血红蛋白减少(13.3%)和乏力(10.8%);联合治疗未发生不可预期的不良反应。近期研究显示,各种联合方案的ORR分别为西达本胺联合ICE(69%)、Gemox(67%)、GDP(65%)、DICE(80%)、DA−EPOCH(61%)、PET(75%),沙利度胺(73%)和来那度胺(64%)[30−31]。
2.3 药代动力学
T细胞淋巴瘤患者口服30 mg西达本胺片后,体内达峰时间(Tmax)出现在2~6 h,血浆药物峰浓度(Cmax)在50~150 ng/mL,药时曲线下面积(AUC0−t)平均为300~1 000 ng×h/mL,终末消除半衰期(t1/2_z)平均约为17 h。服药8次后稳态AUC0~t值较单次给药后存在一定的累积,但未观察到连续服药后体内暴露量增加与其安全性存在关联。服药剂量相同时,男性患者在单位体表面积/体质量下的药物平均暴露量约为女性患者的80%。T细胞淋巴瘤患者在服用标准餐30 h后,口服西达本胺片30 mg,平均血浆暴露量为空腹服用相同剂量患者的2.3倍。提示餐后服药可能有助于减轻部分患者因药物对胃肠道刺激所引起的潜在消化道不良反应。因此推荐餐后30 min服药。
3 西达本胺治疗PTCL的建议
3.1 单药治疗
3.1.1 复发或难治性患者 根据IPI评分为低危(IPI为0~1分)的患者,建议西达本胺单药治疗。采用西达本胺标准用药方法,即成人推荐服药30 mg/次,2次/周,两次服药间隔≥3天(如周一和周四、周二和周五、周三和周六等),餐后30 min服药。若疾病未进展或未出现不可耐受的不良反应,建议持续服药。
3.1.2 不可耐受或不适合常规化疗的患者 采用西达本胺标准用药方法(同本文3.1.1);必要时可根据患者年龄和体能状况酌情减量。
3.1.3 已获得疾病缓解或移植后患者维持治疗 成人推荐服药20 mg/次,2次/周,2次服药间隔≥3天(如周一和周四、周二和周五、周三和周六等),餐后30 min服用。连续服药,持续时间为6~12个月。
3.2 联合治疗
3.2.1 联合二线化疗方案治疗复发或难治性PTCL 根据IPI评分为中、高危(IPI为2~5分)的患者,如肿瘤负荷较大,肿瘤生长偏侵袭性,建议西达本胺联合常用二线化疗方案。联合西达本胺起始剂量为20 mg/次,2次/周,连续服药或服药2~3周停药1周。推荐方案为西达本胺联合ICE方案:西达本胺20 mg/次,2次/周,服药2周停药1周,即d1、4、8、11,其中ICE方案为异环磷酰胺1.2 g/m2,d1~4,静脉输注4 h(美司钠0.4 g,用异环磷酰胺时0、4、8 h,d1~4,静脉注射);卡铂AUC=4,d2,静脉注射;依托泊苷65 mg/m2,d1~4,静脉注射。上述联合方案21 d为1个周期,最多行6个周期。必要时预防性应用重组人粒细胞集落刺激因子(recombinant human granulocyte−colony stimulat⁃ing factor,rhG−CSF)。西达本胺联合Gemox方案:西达本胺20 mg/次,2次/周,服药2周停药1周,即d1、4、8、11。Gemox方案:吉西他滨1 000 mg/m2,d1、d8;奥沙利铂100 mg/m2,d1。上述联合方案21 d为1个周期,最多行6个周期。
西达本胺联合GDP方案:西达本胺20 mg/次,2 次/周,服药2周停药1周,即d1、4、8、11,其中GDP方案为吉西他滨 1 000 mg/m2,d1、d8;顺铂25 mg/m2,d1~4;地塞米松40 mg/次,d1~4。上述联合方案21 d为1个周期,最多行6个周期。西达本胺联合DICE方案:西达本胺20 mg/次,2次/周,持续服药,即d1、4、8、11、15、18,其中DICE方案为地塞米松10 mg/次,d1~4,静脉注射;异环磷酰胺(IFO)1 g/m2,d1~4,静脉注射4 h(美司钠0.4 g、用异环磷酰胺时0、4、8、12 h、d1~4、静脉注射);顺铂25 mg/m2,d1~4,静脉注射;依托泊苷60 mg/m2,d1~4,静脉注射。上述联合方案21 d为1个周期,最多行6个周期。
西达本胺联合DA−EPOCH方案:西达本胺20mg/次,2次/周,持续服药,即d1、4、8、11、15、18,其中DA−EPOCH方案为环磷酰胺750 mg/m2,d6;多柔比星10 mg/m2,d1~4;长春新碱0.4 mg/m2,d1~4;依托泊苷50 mg/m2,d1~4;泼尼松100 mg/次,d1~5。上述联合方案21 d为1个周期,最多行6个周期。
针对复发或难治性NK/T细胞淋巴瘤患者,建议西达本胺联合改良Gemox或P−Gemox方案。推荐方案如下:西达本胺联合改良Gemox方案:西达本胺服药20mg/次,2次/周,持续服药;吉西他滨800~1000mg/m2,d1、d8;奥沙利铂 80~130 mg/m2,d1,上述联合方案21 d为1个周期,最多行6~8个周期。西达本胺联合P−Gemox方案:西达本胺20 mg/次,2次/周,持续服药;吉西他滨800~1 000 mg/m2,d1、8;奥沙利铂130 mg/m2,d1;培门冬酶2 500 IU/m2,d2,上述联合方案21 d为1个周期,最多行6~8个周期。
3.2.2 联合节拍化疗或其他单药治疗复发或难治性PTCL 中、高危(IPI为2~5分)的患者,如肿瘤负荷较小,肿瘤生长偏惰性,建议西达本胺联合节拍化疗方案或来那度胺/沙利度胺。联合时西达本胺起始剂量为30 mg/次,2次/周,连续服药。推荐方案为西达本胺联合PCT(泼尼松+环磷酰胺+沙利度胺)方案:西达本胺30 mg/次,2次/周,持续服药;泼尼松20 mg/d,早餐后服用;环磷酰胺50 mg/d,午餐后服用;沙利度胺100 mg/d,睡前服用。28 d为1个周期。西达本胺联合MEPC(泼尼松+环磷酰胺+依托泊苷+甲氨蝶呤)方案:西达本胺30 mg/次,2次/周,持续服药;泼尼松20 mg/d,早餐后服用;环磷酰胺50 mg/d,午餐后服用;依托泊苷50 mg/d,晚餐后服用;甲氨蝶呤10 mg/d,1次/周,早餐后服用。28 d为1个周期。西达本胺联合PET(泼尼松+依托泊苷+沙利度胺)方案治疗AITL:西达本胺30 mg,2次/周,持续服药;泼尼松100 mg/次,d1~5,早餐后服用;依托泊苷100 mg/次,d1~5,午餐后服用;沙利度胺100 mg/次,d1~14,睡前服用。21 d为1个周期。西达本胺联合沙利度胺:西达本胺30mg/次,2次/周,持续服药;沙利度胺200mg/次,1次/d,睡前服用。28 d为1个周期。西达本胺联合来那度胺:西达本胺30 mg/次,2次/周,持续服药;来那度胺5~25 mg/d,连续服药21 d,28 d为1个周期。可服用阿司匹林预防深部静脉血栓。
3.2.3 作为ASCT预处理方案 PTCL的ASCT预处理方案为西达本胺联合CGB(克拉屈滨+吉西他滨+白消安):西达本胺30mg/次,d−7、−4、0、+3,共服药4次。克拉屈滨6 mg/m2d−6~−2;吉西他滨2 500 mg/m2,d−6、−2;白消安3.2 mg/kg,d−6~−3。
4 不良反应处理和注意事项
4.1 不良反应处理
4.1.1 单药治疗的不良反应处理 西达本胺主要引起血液学不良反应,表现为血小板、白细胞/中性粒细胞和血红蛋白减少。非血液学不良反应为乏力和消化道症状。
血常规监测:服药期间应根据临床诊治需要定期检测血常规(通常1~2次/周)。相关指标满足下述条件可用药:中性粒细胞绝对值≥1.5×109/L,血小板≥75×109/L,血红蛋白≥9.0 g/dL。如患者因肿瘤细胞浸润骨髓导致血常规相关指标不合格,可在严密监控下酌情服用西达本胺。
血液学不良反应的处理和剂量调整:3、4级中性粒细胞减少或缺乏症或出现3级中性粒细胞减少伴体温高于38.5℃时,应暂停用药,并根据临床实践指南应用G−CSF或其他支持治疗,定期检测血常规(隔天1次或至少2次/周),待中性粒细胞绝对值恢复至≥1.5×109/L,并经连续2次检查确认,可继续服用。恢复用药的剂量由临床医师根据骨髓功能判断,决定采用原剂量或降低剂量至20 mg/次。3、4级血小板减少、血红蛋白减少时,暂停用药,并根据临床实践指南应用血细胞生长因子,如白介素11(IL−11)或促血小板生成素(TPO)、红细胞生成素(EPO)和其他支持治疗,定期检测血常规,待血小板恢复至≥75×109/L,血红蛋白≥9.0 g/dL,并经连续2次检查确认,可继续服用。恢复用药的剂量由临床医师根据骨髓功能判断,决定采用原剂量或降低剂量至20 mg/次。对于出血风险较高的患者,预防治疗后血小板减少或保证治疗能够按照预定计划进行,可参考《肿瘤化疗所致血小板减少症诊疗中国专家共识(2014年版)》,给予预防性应用TPO和(或)IL−11治疗。
非血液学不良反应的处理和剂量调整:3级非血液学不良反应,应暂停用药并给予对症治疗。临床上可根据具体不良反应情况,定期进行相关项目的检测,待不良反应缓解至≤1级时可恢复用药,但剂量应降低至20 mg/次。如降低剂量后再次发生≥3级不良反应,应停止服用。服药过程中若出现4级非血液学不良反应,应停止服用。
4.1.2 联合治疗的不良反应处理 西达本胺联合化疗方案治疗时,如出现血液学不良反应,应根据患者的具体情况以及西达本胺和所联合化疗药物的特点,对西达本胺及化疗药物与该不良反应的相关性进行分析,以确定是否调整西达本胺或化疗药物的剂量。如需调整西达本胺剂量则依据西达本胺单药治疗的剂量调整原则进行,如需调整化疗药物剂量则依据医疗实践常规进行。如出现非血液学不良反应,需综合具体情况对各药物与不良反应的相关性进行判断,从而调整药物剂量。
4.2 注意事项
4.2.1 疲乏 出现疲乏,在排除内分泌功能、肝肾功能、心脏功能和电解质紊乱等原因后,在西达本胺减量的同时可给予低剂量泼尼松15 mg/次,1次/d,持续服用或与西达本胺服用周期一致。
4.2.2 消化道症状 推荐餐后30 min服药。在临床试验中观察到,餐后服药平均血药浓度高于空腹服药,有助于缓解部分患者因药物对胃肠道刺激所引起的潜在不适症状。消化道症状明显者,推荐酌情给予对症治疗。
世界卫生组织(WHO)外周T细胞淋巴瘤病理亚型(2017年版)
·外周T细胞淋巴瘤−非特指型(PTCL−NOS)
·血管免疫母细胞性T细胞淋巴瘤(AITL)
·结外NK/T细胞淋巴瘤,鼻型(ENKTL)
·ALK阳性间变性大细胞淋巴瘤(ALK+ALCL)
·ALK阴性间变性大细胞淋巴瘤(ALK−ALCL)
·蕈样肉芽肿(MF)
·Sézary综合征(SS)
·肠病相关T细胞淋巴瘤
·肝脾T细胞淋巴瘤
·皮下脂膜炎样T细胞淋巴瘤
·T细胞型大颗粒淋巴细胞白血病
·慢性NK细胞淋巴增殖性疾病
·侵袭性NK细胞白血病
·成人T细胞淋巴瘤/白血病
·原发性皮肤CD30+T细胞淋巴组织增生性疾病(淋巴瘤样丘疹病、原发性皮肤间变性大细胞淋巴瘤)
·原发性皮肤γδT细胞淋巴瘤
·原发性皮肤侵袭性亲表皮CD8阳性细胞毒性T细胞淋巴瘤
·原发性皮肤肢端CD8+T细胞淋巴瘤
·原发性皮肤CD4+小/中型T细胞淋巴组织增生性疾病
·滤泡T细胞淋巴瘤
·结内外周T细胞淋巴瘤,呈TFH表型
·乳房植入物相关的间变性大细胞淋巴瘤
·儿童系统性EBV+T细胞淋巴瘤
·种痘样水疱病样淋巴组织增生性疾病
·单形性向表皮肠道T细胞淋巴瘤
·胃肠道惰性T细胞淋巴组织增生性疾病
专家组成员
组长
马 军 哈尔滨血液病肿瘤研究所
委员
白 海 兰州军区总医院
白 鸥 吉林大学白求恩第一医院
蔡 真 浙江大学医学院附属第一医院
曹军宁 复旦大学附属肿瘤医院
岑 洪 广西医科大学附属肿瘤医院
陈协群 空军军医大学西京医院
丁凯阳 安徽省肿瘤医院
冯继锋 江苏省肿瘤医院
高玉环 河北医科大学第四医院
高子芬 北京大学第三医院
郭 晔 上海同济大学附属东方医院
洪小南 复旦大学附属肿瘤医院
侯 健 上海交通大学医学院附属仁济医院
侯 明 山东大学齐鲁医院
胡建达 福建医科大学附属协和医院
胡 豫 华中科技大学同济医学院附属协和医院
黄慧强 中山大学肿瘤防治中心
贾永前 四川大学华西医院
江 明 新疆医科大学第一附属医院
金 洁 浙江大学医学院附属第一医院
克晓燕 北京大学第三医院
李文瑜 广东省人民医院
李小秋 复旦大学附属肿瘤医院
李志铭 中山大学肿瘤防治中心
林桐榆 中山大学肿瘤防治中心
刘代红 中国人民解放军总医院(301医院)
刘丽宏 河北医科大学第四医院
刘 林 重庆医科大学附属第一医院
刘 澎 复旦大学附属中山医院
刘启发 南方医科大学附属南方医院
刘 霆 四川大学华西医院
刘卫平 四川大学华西医院
罗建民 河北医科大学第二医院
牛 挺 四川大学华西医院
钱文斌 浙江大学医学院附属第一医院
邱录贵 中国医学科学院血液病医院
沈建箴 福建医科大学附属协和医院
双跃荣 江西省肿瘤医院
宋永平 河南省肿瘤医院
宋玉琴 北京大学肿瘤医院
苏 航 中国人民解放军第307医院
苏丽萍 山西省肿瘤医院
谭 获 广州医科大学附属第一医院
王华庆 天津市人民医院
王季石 贵州医科大学附属医院
王鲁群 山东大学齐鲁医院
王全顺 中国人民解放军总医院(301医院)
王 欣 山东省立医院
吴德沛 苏州大学附属第一医院
伍 钢 华中科技大学同济医学院附属协和医院
徐 卫 江苏省人民医院
薛宏伟 青岛大学附属医院
杨海燕 浙江省肿瘤医院
杨建民 海军军医大学附属长海医院
杨顺娥 新疆医科大学附属肿瘤医院
杨 瑜 福建省肿瘤医院
张会来 天津医科大学肿瘤医院
张明智 郑州大学第一附属医院
张清媛 哈尔滨医科大学附属肿瘤医院
张 薇 北京协和医院
张 曦 陆军军医大学第二附属医院
张永红 首都医科大学附属北京儿童医院
赵洪国 青岛大学附属医院
赵维莅 上海交通大学医学院附属瑞金医院
周道斌 北京协和医院
周 辉 湖南省肿瘤医院
周剑峰 华中科技大学同济医学院附属同济医院
朱雄增 复旦大学附属肿瘤医院
邹立群 四川大学华西医院
执笔人
马 军 哈尔滨血液病肿瘤研究所
沈志祥 上海交通大学医学院附属瑞金医院
朱 军 北京大学肿瘤医院
石远凯 中国医学科学院肿瘤医院
姜文奇 中山大学肿瘤防治中心
李建勇 江苏省人民医院

