超微血流成像技术在颈动脉易损斑块诊断中的应用价值
谢 霞,白志勇,刘 悦,张华斌
清华大学附属北京清华长庚医院超声科 清华大学临床医学院,北京 102218
脑卒中是严重危害人类健康和生命安全的常见难治性疾病。颈动脉粥样硬化是引起脑血管疾病的主要原因,同时也是短暂性缺血发作和脑梗死的病理基础[1]。新生血管可促使斑块快速进展、诱发斑块内出血和斑块破裂、血栓及碎块向远处脱落而造成缺血性脑卒中,目前被认为是易损斑块的高危因素[2]。超声造影(contrast-enhanced ultrasound,CEUS)已经成功应用于斑块内新生血管的检测,斑块内造影剂微气泡的显示标志着新生血管的形成,而且,颈动脉斑块内新生血管形成的造影增强超声成像与手术标本的半定量组织学评分之间具有很好的相关性[3- 4]。超微血流显像(superb micro-vascular imaging,SMI)是一种多普勒成像技术,可显示管径≤100 μm,流速≤0.1 cm/s的血管,且无运动伪像。国外已应用于甲状腺、乳腺、肝脏、肾脏及关节炎等疾病的检测及诊断,未见关于颈动脉斑块的研究[5- 7]。本研究对纳入斑块依次行常规超声检查、SMI检查及CEUS检查,探讨SMI技术在显示颈动脉斑块及斑块内新生血管中的应用价值。
对象和方法
对象选取2015年3月至2017年9月本院常规超声发现颈动脉低回声或低回声为主混合回声斑块患者69例(共计108个斑块),且斑块厚度≥2.5 mm,长度≥10 mm。其中男53例、女16例,年龄42~87岁,平均(68.1±8.8)岁。所有斑块依次行常规超声检查、SMI检查及超声造影检查。
方法采用东芝Aplio500彩色超声诊断仪,线阵探头,频率7.5 MHz,内置SMI及CEUS软件。检查时,受检者取仰卧位,头略向后,颈部放松偏向检查对侧。并由专人采集记录患者的基本情况,包括年龄、性别、高血压史、高血脂史、糖尿病史、吸烟史、冠心病史及既往脑梗病史、现病史。
常规超声检查:对双侧颈总动脉、颈内动脉及颈外动脉行横切、纵切扫查,记录目标斑块位置、厚度、长度。使用频谱多普勒成像技术记录斑块所在处残余管腔流速,使用SMI观察斑块有无溃疡。
SMI检查:对常规超声发现的目标斑块进行扫查,选择灰阶模式超微血流成像,标尺设置选择1.2~1.5 cm/s,横断面扫查时,自斑块近心端向远心端扫查直至斑块消失,纵断面扫查时,观察斑块基底部、顶部、近心端及远心端肩部有无血流信号。记录动态及静态图像用于分析。
CEUS检查:设置颈动脉超声造影参数。采用第2代超声造影剂SonoVueTM(Bracco,意大利),主要成分为六氟化硫(SF6)微泡。使用前生理盐水5 ml溶解造影剂冻干粉,振荡混匀后抽取1.2 ml/次,采用团注法经肘正中静脉注射,紧接着5 ml生理盐水快速注入,必要时重复进行。团注造影剂同时计时并观察目标斑块内有无微气泡灌注,记录动态图像,同一患者不同斑块造影间隔大于10 min。
诊断标准
狭窄纳入标准:采用2003年美国放射年会超声会议公布标准,收缩期峰值流速(peak systolic velocity,PSV)狭窄段>125 cm/s或PSV狭窄段/PSV狭窄远段>2.5。
溃疡斑块诊断标准:斑块表面不规则,可见凹陷,其深度>1 mm,SMI可见凹陷内血流充盈。
CEUS评分标准:0分,斑块内无微气泡灌注;1分,微气泡局限在斑块肩部和/或外膜的一侧,呈点状增强(小于4个);2分,斑块内可见大量微气泡灌注,呈点状或线状增强[8]。
SMI的评分标准:参照CEUS评分标准。0分,斑块内无血流信号;1分,斑块一侧可见少量点状或短线状血流信号(小于4个);2分,斑块内可见弥漫分布的线状或树枝状血流信号。
SMI及CEUS均采用单盲法由2名有经验的超声医师进行联合评价。
观察指标在同一解剖断面、同一深度值,观察SMI对斑块内有无新生血管及新生血管部位、形态的显示是否与CEUS呈现良好的一致性。观察SMI与CEUS对颈动脉溃疡斑块的显示是否存在差异。SMI显示斑块内有无新生血管与斑块是否造成管腔狭窄的关系。
统计学处理采用SPSS 20.0统计软件进行数据分析,计量资料以均数±标准差表示,组间变量采用χ2检验,P<0.05为差异有统计学意义。计算Kappa统计量,评价SMI与CEUS评分结果的一致性,Kappa值在0.40~0.75为中、高度一致,Kappa值≥0.75为具有极好的一致性。
结 果
一般资料69例患者斑块厚度2.6~8.0 mm,平均(4.09±1.04) mm,长度10.7~43.0 mm,平均(19.92±6.91) mm,其中伴高血压51例(73.9%)、高血脂47例(68.1%)、高血糖21例(30.4%)、吸烟史(烟龄>10年)31例(44.9%)、冠心病史18例(26.1%)、既往脑梗史30例(43.5%)。患者一般资料比较见表1。
超声表现108处颈动脉粥样硬化斑块,其中低回声斑块59个(54.6%)、低回声为主混合回声斑块49个(45.4%)。SMI较常规超声能清楚显示斑块的位置及轮廓(图1A),以及斑块表面小裂隙(图1B)。SMI显示2处(1.9%)斑块表面小裂隙,常规超声均未能显示。SMI显示斑块内新生血管75个,CEUS显示斑块内新生血管76个,90处斑块SMI与CEUS显示结果一致,两种评分结果高度一致(Kappa值=0.748)(表2)。在同一解剖断面、同一深度值,评分为1分(图2A、2B)及2分(图3A、3B),SMI与CEUS对斑块内新生血管部位、形态的显示有着极高的相似性。
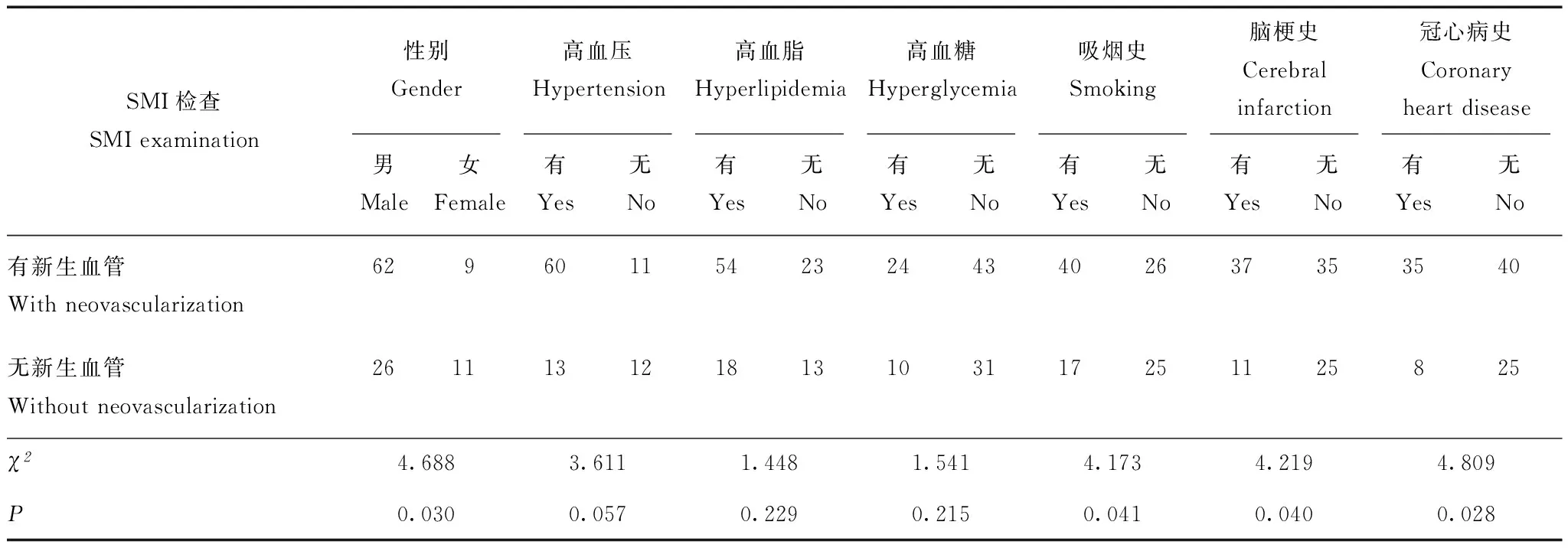
表 1 有无新生血管患者一般资料比较(n=108,n)Table 1 Comparison of general characteristics between patients with and without neovascularization(n=108,n)
SMI:超微血流成像技术
SMI:superb micro-vascular imaging
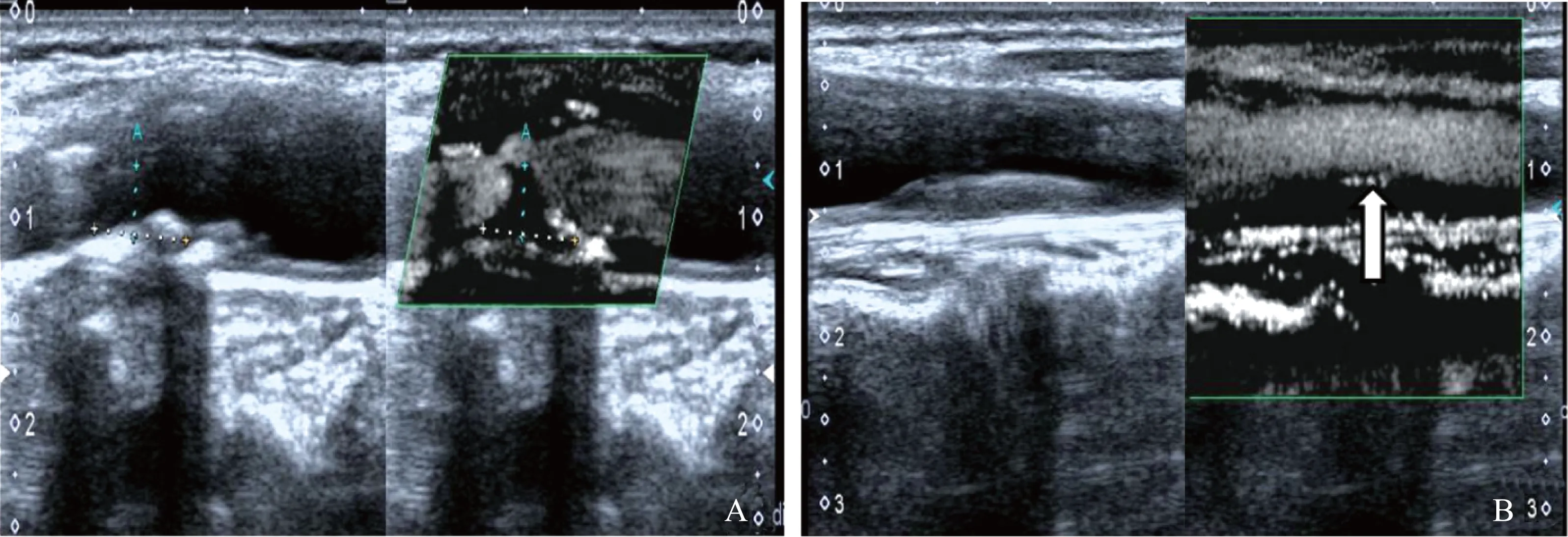
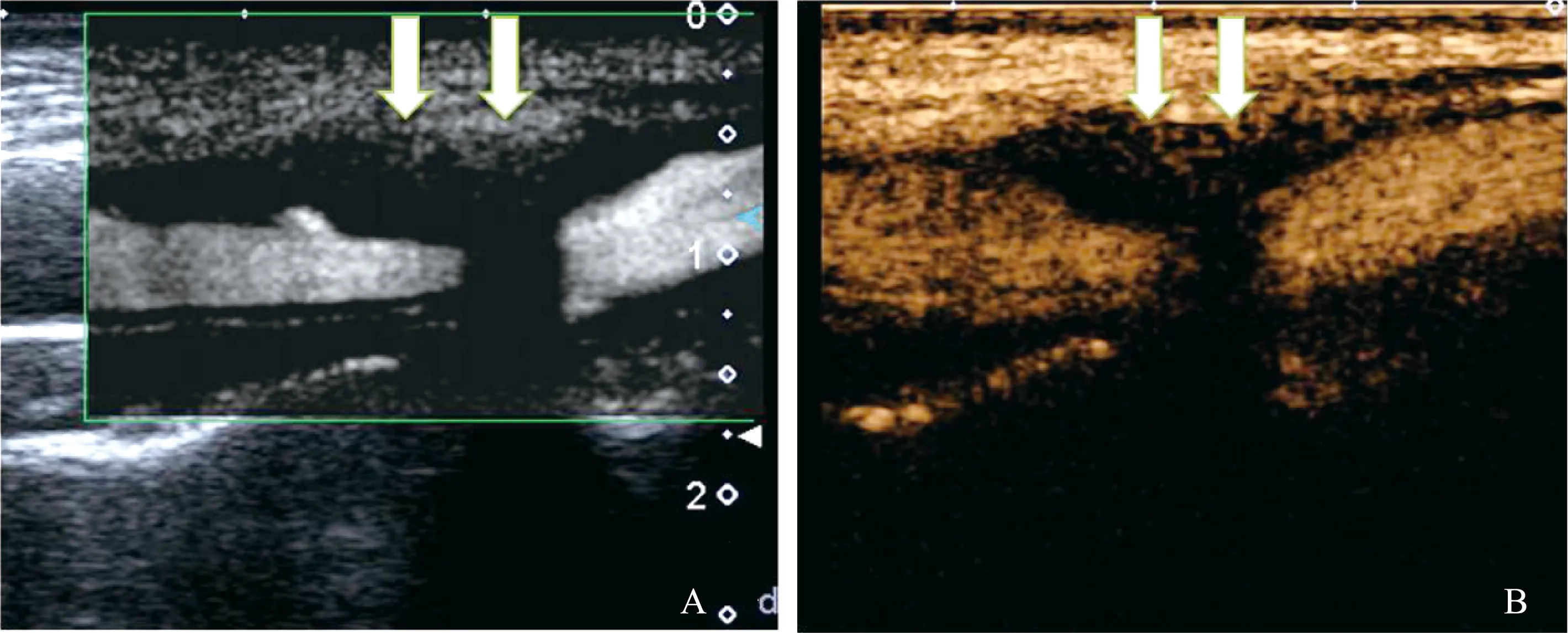
A.左图为常规超声模式,右图为SMI模式,虚线为斑块长度与厚度;B.左图为常规超声模式,右图为SMI模式,白色箭头所示为斑块表面小裂隙(白色亮点)
A.left picture represents conventional ultrasound image,right picture represents SMI image,and the dotted line is the length and thickness of the plaque;B.left picture represents conventional ultrasound image,right picture represents SMI image,and white arrows show small fissures on the surface of the plaque (white lightspots)
图1常规超声与SMI对照图
Fig1Comparison between conventional ultrasound findings and SMI findings
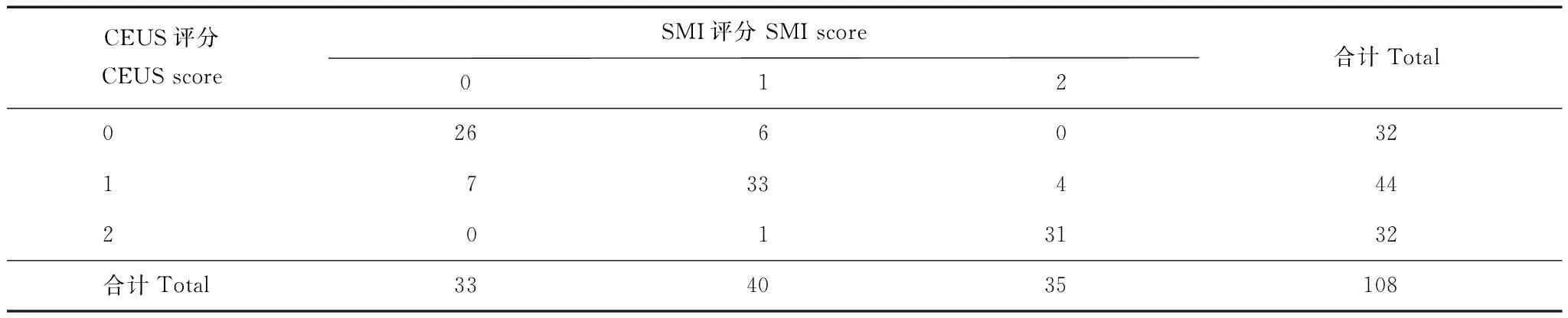
表 2 SMI与CEUS评分的一致性(n=108,n)Table 2 The scoring consistency between SMI and CEUS (n=108,n)
CEUS:超声造影
CEUS:contrast-enhanced ultrasound
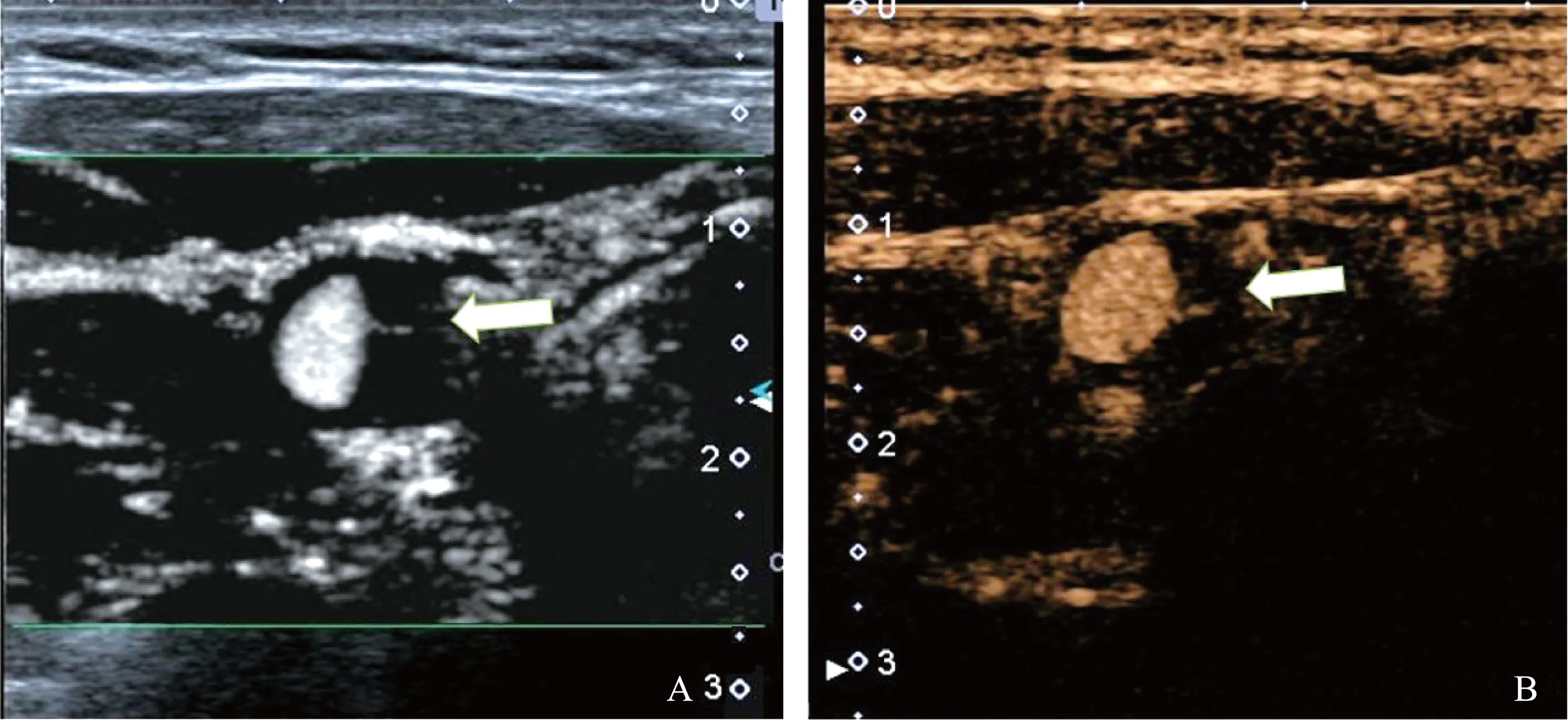
A. SMI模式下斑块内细线样新生血管(白色箭头);B. CEUS模式下斑块内细线样新生血管(白色箭头)
A. the thin line-like neovascularization (white arrow) in the plaque (under SMI);B.the thin line-like neovascularization (white arrow) in the plaque (under CEUS)
图2SMI及CEUS显示斑块内少量新生血管
Fig2A small number of neovascularization inside the plaque(under SMI and CEUS)
A.SMI模式下斑块内较多条棒状新生血管(白色箭头);B.CEUS模式下斑块内较多条棒状新生血管(白色箭头)
A.a relatively large number of bar-shaped neovascularization (white arrow) in the plaque (under SMI);B.a relatively large number of bar-shaped neovascularization (white arrow) in the plaque (under CEUS)
图3SMI及CEUS显示斑块内大量新生血管
Fig3A large number of the plaque neovascularization showed by SMI and CEUS
SMI与CUES结果比较108处颈动脉粥样硬化斑块,SMI检查结果显示溃疡斑6处,同样,CUES检查结果显示溃疡斑6处,两种检查结果完全一致。SMI及CEUS显示所有溃疡斑块内均可见新生血管形成(1分及2分)。55个斑块造成颈动脉局部管腔狭窄,其中SMI检查出有新生血管的斑块37处、无新生血管的斑块18处;53个斑块未造成颈动脉局部管腔狭窄,其中SMI检查出有新生血管的斑块39处、无新生血管的斑块14处,SMI显示斑块内有无新生血管与斑块是否造成管腔狭窄无关,差异无统计学意义(χ2=0.561,P>0.05)。
讨 论
颈动脉粥样硬化斑块与脑血管事件有着密切的联系,据统计,约30%的脑卒中是动脉粥样硬化所致[9]。狭窄程度通常被认为是一种选择治疗方案的参数,很多研究表明动脉狭窄只是动脉粥样硬化疾病进展的间接因素,而直接因素是斑块的结构和组成成份,其预示着未来缺血性脑血管事件的发生和发展。那些容易破裂、脱落并引起远端栓塞的不稳定斑块,称之为易损斑块。易损斑块的形态学特征包含以下几个特点:斑块表面不规则或溃疡形成;纤维帽较薄或出现裂隙、斑块内出血、斑块内富含脂质及炎性活跃成分、斑块内新生血管形成[10]。斑块内出血的主要原因是血管的破裂。颈动脉斑块内新生血管来源于外膜滋养血管的芽生或非芽生,是由简单的内皮细胞围成的管道,周围缺乏结缔组织及基底细胞膜的支撑,血管脆性大,容易破裂出血。斑块内新生血管在斑块启动、进展及破裂中扮演着中心角色,是斑块不稳定及卒中风险的一个预测因子[11]。组织病理学证据显示,与相对稳定斑块相比,斑块内新生血管的存在和密度分布与斑块破裂有着密切的联系,且新生血管常位于斑块纤维帽裂隙区、脂质富集区、炎性活跃区等部位[12]。那些低回声斑块或低回声为主混合回声斑块比强回声斑块能增加脑卒中的风险,回声越低,其内部炎症反应越活跃,新生血管越多[13],因此,本研究选择前两种回声的斑块。
超声造影技术可明显增加血管壁、血管腔内部结构和周边组织显示的敏感性,可更准确反应和诊断血管壁及血管腔内病变。目前能敏感评估动脉粥样硬化斑块内新生血管的方法是颈动脉斑块超声造影检查,有学者将CEUS检测斑块内新生血管作为诊断易损斑块的可靠证据[14- 16]。但由于造影剂费用昂贵,且为有创伤检查,并有造影剂过敏的风险,受到一定的限制。因此,需要探索一种简便易行、无创伤性、花费低廉的超声检查方法。
SMI是显示组织内低速血流的新技术,应用新的自适应算法来临别并移除组织杂乱运动信号,通过消减背景组织信息以提高极低速血流显示的敏感性。其操作简单便捷,无需造影剂注射,真正做到实时无创检查。本研究108处斑块中,SMI较常规超声可以清楚显示斑块的位置及轮廓,尤其是斑块表面的微小裂隙,对于一些溃疡斑块,也更能清晰显示破溃的范围。本研究SMI对斑块内新生血管形态及分布情况与CEUS高度一致。SMI对于显示颈动脉溃疡斑块的研究,目前国内外报道均较少。虽然本研究中病例数较小,但仍能提示SMI对于溃疡斑块的检出有一定的应用价值。颈动脉狭窄程度与缺血性脑梗死的发病明显相关,其准确判断是预防与治疗脑梗死的关键[17]。本研究显示SMI检出斑块内有无新生血管与斑块是否造成狭窄无关(P>0.05),提醒临床医师对于那些没有造成管腔狭窄的低回声斑块,也不要轻易忽视,其性质在脑卒中的发病机制中也发挥着重要的作用,建议临床医师及早进行干预。
本研究纳入患者中,男性(53例)明显多于女性(16例),且男性患者斑块内新生血管明显多于女性患者(P<0.05),提示男性是易损斑块的危险因素之一,与文献报道一致,Wendorff等[18]研究结果显示斑块形态在不同年龄、不同性别的患者中不同,其中男性患者的炎症程度以及新生血管形成更明显,在这些男性患者中,有吸烟史、既往脑梗死病史、冠心病史患者中斑块内新生血管明显多于不吸烟者、无脑梗死既往史、无冠心病史(P<0.05)。因此,以上这些因素应该被纳入易损斑块的预测危险因素,与刘雨等[19]报道基本一致。临床对既往有心脑血管疾病的患者应该密切观察、积极给予干预治疗,对于有吸烟史的患者,应劝导其积极戒烟。本研究发现高血压、高血脂及高血糖患者斑块内新生血管与对照组比较差异无统计学意义,并不能说明“三高”就不是易损斑块的高危因素,分析其原因可能由于样本量较少不能全面反应。
综上,本研究显示SMI作为一种简单、方便、易操作的实时无创超声检查技术,能清楚显示颈动脉斑块轮廓、形态及斑块内新生血管,可评估斑块的易损性,是继超声造影检查之后的一种新的无创检测技术。

