基于均匀和正交试验设计的胶束电动毛细管色谱法同时测定消毒剂和抗抑菌产品中3种核苷类抗病毒药物
王 萍, 李梦琦, 赵丽媛, 杨 屹, 丁晓静*
(1. 北京市疾病预防控制中心, 北京 100013; 2. 北京市预防医学研究中心, 北京 100013; 3. 北京化工大学理学院, 北京 100029)
近50%抗病毒药物均为核苷类药物,如更昔洛韦、阿昔洛韦和喷昔洛韦等。这类药物在临床上是治疗艾滋病、疱疹、肝炎等病毒性疾病的首选,1%(质量分数)喷昔洛韦和3%~5%(质量分数)阿昔洛韦还因对带状疱疹和生殖疱疹有一定的治疗效果而常用于皮肤科外用药膏中[1]。这些药物多数对宿主细胞有一定的毒性,口服难以吸收,多为外用[2]。因此原卫生部发布的《消毒产品生产企业卫生规范》(2009年版)以及《消毒产品卫生安全评价》均禁止在消毒产品中添加此类药物,并在全国开展整治消毒产品违法宣传疗效和添加药物的专项行动,但由于目前没有相应配套的消毒剂和抗抑菌产品中更昔洛韦、阿昔洛韦和喷昔洛韦这3种最为常见的外用核苷类抗病毒药物的检测方法,因而无法实现对消毒剂和抗抑菌产品的有效监管。因此,迫切需要建立同时分析这3种抗病毒药物的方法,以维护消费者的健康和经济利益。
目前抗病毒药物的分析方法主要有紫外分光光度法[3]、高效液相色谱(HPLC)法[3-7]、毛细管电泳(CE)法[8-12]和液相色谱-质谱联用(LC-MS)法[13-16]。其中,HPLC和LC-MS主要用于药品和血浆等的分析。LC-MS所用仪器昂贵,测定成本较高,而HPLC需消耗大量的有机溶剂。CE则具有分离效率高、无需有机溶剂和运行成本低等优点,在水溶性差的抗病毒药物分析中有一定优势。Saleh等[8]以60 mmol/L硼砂+40 mmol/L SDS为分离缓冲液(pH 9.25),对人体血浆中的更昔洛韦进行了测定,但在这个条件下阿昔洛韦和更昔洛韦两峰重叠,不能分开,不能实现阿昔洛韦与更昔洛韦的同时测定。Yeh等[9]用30 mmol/L Tris+140 mmol/L SDS(pH 8.0)作为分离缓冲溶液,不需要进行样品前处理,直接进样就能对生物样本(血浆和脑脊液)中的阿昔洛韦进行测定。Vo等[10]以90 mmol/L硼酸+175 mmol/L SDS+100 mmol/L羟丙基-β-环糊精+0.2%(质量体积分数)NaCl(pH 8.8)为分离缓冲溶液,以大体积进样(进样时间100 s),进行了血浆中阿昔洛韦的高灵敏检测。梁改玲等[11]以30 mmol/L硼砂(pH 9.6)为分离缓冲液,实现了复方阿昔洛韦滴眼液中阿昔洛韦含量的测定。Neubert等[12]采用20 mmol硼砂+10 mmol/L SDS+5 mmol/L十二烷基三甲基溴化铵溶液作为分离缓冲溶液,着重研究了如何从亲水或者亲脂的药品配方中将阿昔洛韦和溴夫定分离开并能快速检出这两种药物的方法。但是,文献所报道的CE方法主要是分析药品和生物样品中3种常用外用抗病毒药物中的某一种,也没有在消毒剂和抗抑菌产品中的分析方法,因此有必要建立消毒剂和抗抑菌产品中3种常用外用抗病毒药物的CE分析方法。
鉴于影响CE分离分析的因素多,各因素之间的交互作用较强,采用通常的单因子优化方法所获得的最佳分离条件实际上可能并不是最佳的条件。为找到最佳的分析条件,往往要做很多试验。因此,运用统计学方法探寻各种影响因素之间的相互关系并尽可能以最少试验次数得到最佳分离条件的方法已应用于CE最佳分离条件的优化[17-20]。黄志东[17]和吴惠芳等[18]使用均匀试验设计,付小帅等[19]和郭雯雯等[20]使用正交试验设计对影响CE分离的多种影响因素进行了考察,并最终确定了最佳分离条件。本研究结合均匀设计及正交设计各自的特点,分别使用3因素7水平的均匀设计及4因素4水平的正交设计,较为全面、系统和科学地对分离条件进行优化,建立了同时分析3种抗病毒药物的胶束电动毛细管色谱(MEKC)新方法,并对喷剂、洗剂、膏状和乳状等不同剂型的复方化学消毒剂或抗抑菌产品进行测定,同时对乳膏型及凝胶型药品也进行了测定,获得了满意结果。
1 实验部分
1.1 仪器与试剂
P/ACE MDQ型毛细管电泳仪配备二极管阵列检测器(美国Beckman公司); Millipore Milli-Elix/RiOs型超纯水器(美国Millipore公司);涡旋振荡器(英国Bibby Sterilin有限公司); F-50A酸度计(北京屹源电子仪器科技公司); Universal 32型高速离心机(德国Hettich公司);未涂层熔融石英毛细管柱(河北永年瑞沣色谱器件有限公司)。
氢氧化钠(NaOH,分析纯,北京化学试剂公司);无水磷酸二氢钠(NaH2PO4,分析纯,国药集团化学试剂有限公司);SDS(分析纯,美国Sigma公司);十水合四硼酸钠(Na2B4O7·10H2O,分析纯,国药集团化学试剂有限公司)。
标准品:更昔洛韦(纯度>97%,加拿大Toronto Research Chemicals公司);阿昔洛韦(纯度>99.8%,中国食品药品检定研究院);喷昔洛韦(纯度>98.0%,日本东京化成工业株式会社)。
样品:在淘宝网购买了带有“卫消证字”,包装或说明书中标识有抑菌、除癣、止痒、保持菌群平衡等作用的喷剂、洗剂、膏状和乳状等不同剂型的复方化学消毒剂共6件。还从北京当地药房购买了1件更昔洛韦眼用凝胶(标识质量分数为0.15%)、1件阿昔洛韦凝胶(标识质量分数为1%)及1件喷昔洛韦乳膏(标识质量分数为1%)。
1.2 分离缓冲溶液及样品提取液
分离缓冲溶液为10 mmol/L硼砂+25 mmol/L磷酸二氢钠(pH 7.41)+140 mmol/L SDS。样品提取液为用超纯水稀释10倍的分离缓冲溶液。
1.3 标准溶液的配制
分别准确称取10 mg(精确到0.000 1 g)更昔洛韦、阿西洛韦、喷昔洛韦,分别用样品提取液定容至10 mL,配制成1 000 mg/L的标准储备液。分别移取适当体积的上述储备液,用样品提取液稀释成质量浓度分别为2、20和40 mg/L的混合标准溶液。
1.4 样品前处理
称取1.0 g样品,置于10 mL具塞离心管(比色管)中,加样品提取液至10 mL,涡旋1 min混匀。如果是液体样品,可直接进样,如果是乳膏样品,还应再超声提取10 min,离心后取上清液进样。
1.5 电泳条件
未涂层熔融石英毛细管(30.2 cm×50 μm,有效长度为20 cm)。分离电压为10 kV;进样时间为4 s;检测波长为250 nm;操作温度为25 ℃。
新装毛细管在使用前分别用1 mol/L NaOH冲洗20 min,超纯水冲洗5 min,分离缓冲液冲洗5 min。每次进样前依次用1 mol/L NaOH冲洗1.5 min,超纯水冲洗1.5 min,分离缓冲液冲洗1.5 min,以保证迁移时间和校正峰面积的重现性。
1.6 数据统计与处理
使用SPSS 19.0进行数据统计与处理
2 结果与讨论
2.1 检测波长的选择
梁改玲等[11]用CE测定复方阿昔洛韦滴眼液中阿昔洛韦的含量时,选择240 nm为检测波长。本研究对更昔洛韦、阿西洛韦和喷昔洛韦在CE分离缓冲溶液中的紫外吸收光谱进行扫描,发现最大吸收波长均在250 nm左右,因此选择250 nm为检测波长。
2.2 分离缓冲体系的优化
2.2.1分离缓冲体系的选择
在大城市想找份工作立稳脚跟是很难的,想不到在小城市生存竞争也这么激烈。一个薪水低得不能再低的职位,竟然有十多名大学生去抢,更不要说稍微像样的工作了。我从一家招聘英语教师的辅导培训学校摔门而出,因为他们一个月仅开1200块钱工资加一点菲薄的课时费,这么低的待遇还要任课老师双休日去公共场所拉生源。我想象自己站在少年文化宫门前像出台的婊子拉客那样,腆着脸拉小学生们来参加培训,简直无法忍受。薪水再低我都忍了,准备先干着再说,唯有这拉生源的条件成为压垮骆驼的最后一根稻草,让我摔门而去。
由于阿昔洛韦的pKa1=2.52, pKa2=9.35,参照Saleh等[8]的报道采用硼砂-SDS作为分离缓冲体系。Saleh等[8]调节pH使用的是NaOH和HCl,而为了得到较宽pH缓冲范围,本文选用磷酸二氢钠来调节pH,这样做可以保证使用均匀试验设计和正交试验设计时,万一pH无法落在硼砂缓冲体系的范围内,还可落在磷酸盐的缓冲范围内,因硼砂和磷酸缓冲体系的缓冲范围分别为pH 8.24~10.24和pH 6.20~8.20,在这两个pH范围内,缓冲液均有较强的缓冲能力,可获得良好的迁移时间重现性。另外,在缓冲体系中加入SDS,除了可以增加分离度外,还可以增加高pH条件下各抗病毒药物的溶解性[12]。
2.2.2分离缓冲体系中各影响因素浓度的优化
有文献[17,18]用均匀试验设计及逐步回归的统计方法找到了影响CE分离主要因素之间的关系。受此启发,本文选取较长的管长(70 cm×50 μm)、适宜的电压(26 kV)及进样时间(15 s)进行均匀试验设计。参考使用硼砂体系分离抗病毒药物的文献[8,11,12]以及以往试验的经验,在较大范围内选定7个浓度水平的SDS、磷酸二氢钠和硼砂,按74均匀设计表进行试验(见表1),以期找到分离体系中SDS、磷酸二氢钠和硼砂与分离度之间的关系。试验结果见表1。
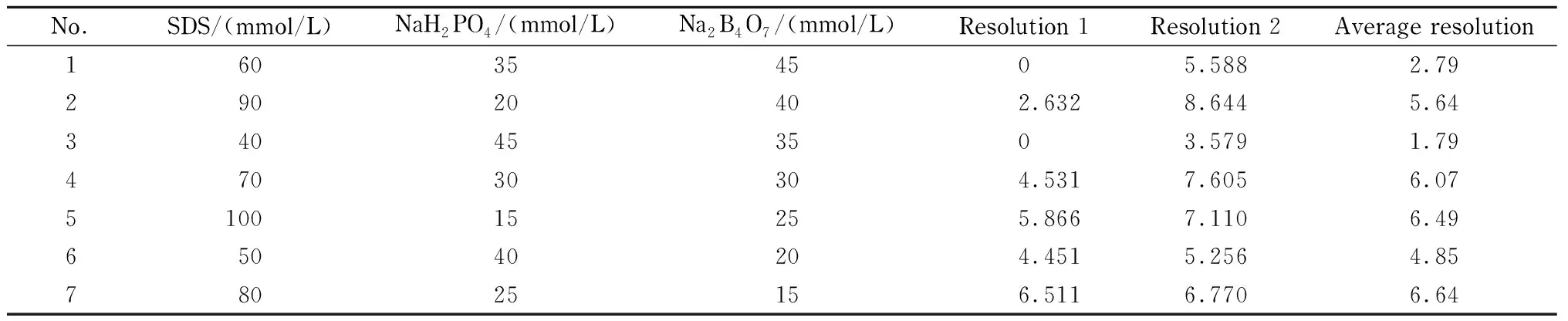
表 1 均匀试验设计因素与水平及分离度结果
Resolution 1 is the resolution between the first peak and the second peak. Resolution 2 is the resolution between the second peak and the third peak.
由表1可见,使用高浓度SDS时,各峰间的分离度要明显好于使用低浓度时的分离度。但磷酸二氢钠和硼砂的浓度对分离度的影响很难从表1中得出结论。将平均分离度作为因变量,将SDS浓度、磷酸二氢钠浓度、硼砂浓度以及它们之间的交互作用(即SDS与磷酸二氢钠浓度乘积、磷酸二氢钠与硼砂浓度乘积和SDS与硼砂浓度乘积)作为自变量,用SPSS 19.0软件进行线性逐步回归分析。其主要判据是:方程的F值(总回归方程线性假设检验值)大于F(0.05)(显著水平为0.05时的F值),且方程各项系数的t(每个自变量偏回归系数假设检验值)值大于t(0.05)(显著水平为0.05时的t值)[17,18]。满足这两个条件的逐步回归分析得到A=8.192-0.004B,A为平均分离度,B为磷酸二氢钠和硼砂的浓度乘积。方程的F值为41.090,P值为0.001;常数和磷酸二氢钠与硼砂浓度乘积的t值分别为14.23和6.41,P值为分别为0.000 03和0.001;相关系数r为0.944。结果表明,在选定的范围内,磷酸二氢钠和硼砂的乘积与平均分离度呈线性关系,且此乘积越小,平均分离度越大。要想得到满意的分离度,SDS应取最大浓度,且磷酸二氢钠和硼砂应尽量取其乘积最小的浓度。
正交试验设计是处理多因素试验的一种科学的试验方法,它利用“正交表”,合理安排试验,若再对正交试验结果进行简单的统计分析,则可得到目标最优值的实验条件[19,20]。依据上述试验结果,将SDS的浓度加大,分别取80(水平1)、100(水平2)、120(水平3)和140 (水平4)mmol/L共4个浓度水平;减小磷酸二氢钠和硼砂的浓度,但是因为需要考虑溶液的缓冲能力,因此分别选取10(水平1)、15(水平2)、20(水平3)和25(水平4)mmol/L这4个浓度。参照文献[21],用SPSS 19.0进行4因素(SDS、磷酸二氢钠、硼砂及空白列)4水平正交试验设计并进行方差分析以,便最终确定SDS、磷酸二氢钠和硼砂的浓度。正交试验设计及结果见表2,方差分析结果见表3,极差分析结果见表4。
从表3可知,SDS、磷酸二氢钠和硼砂的Sig.(显著性差异)均小于0.05,表明3个因素对平均分离度均有影响;3个因素的F值大小的次序依次为SDS>磷酸二氢钠>硼砂,也就意味着影响平均分离度的大小次序为SDS>磷酸二氢钠>硼砂。
正交试验设计的极差分析表中,极差最大的即为对分离度影响最大的因素,在4个试验水平中均值最大的即为最佳实验条件。从表4可见,极差最大的是SDS,然后依次为磷酸二氢钠和硼砂。极差分析表与方差分析表得出相同的结论,即对分离度影响最大的是SDS,最小的是硼砂。从表4中得出的最佳试验条件为:SDS取水平4的浓度即140 mmol/L;磷酸二氢钠取水平4的浓度即25 mmol/L;硼砂取水平1的浓度即10 mmol/L。因为各峰之间的分离度较大,为了节省时间,将毛细管缩短至30.2 cm,并降低电压至10 kV,进样时间缩短至4 s,按照前面选取的最佳缓冲条件,同样得到了令人满意的结果(见图1a)。
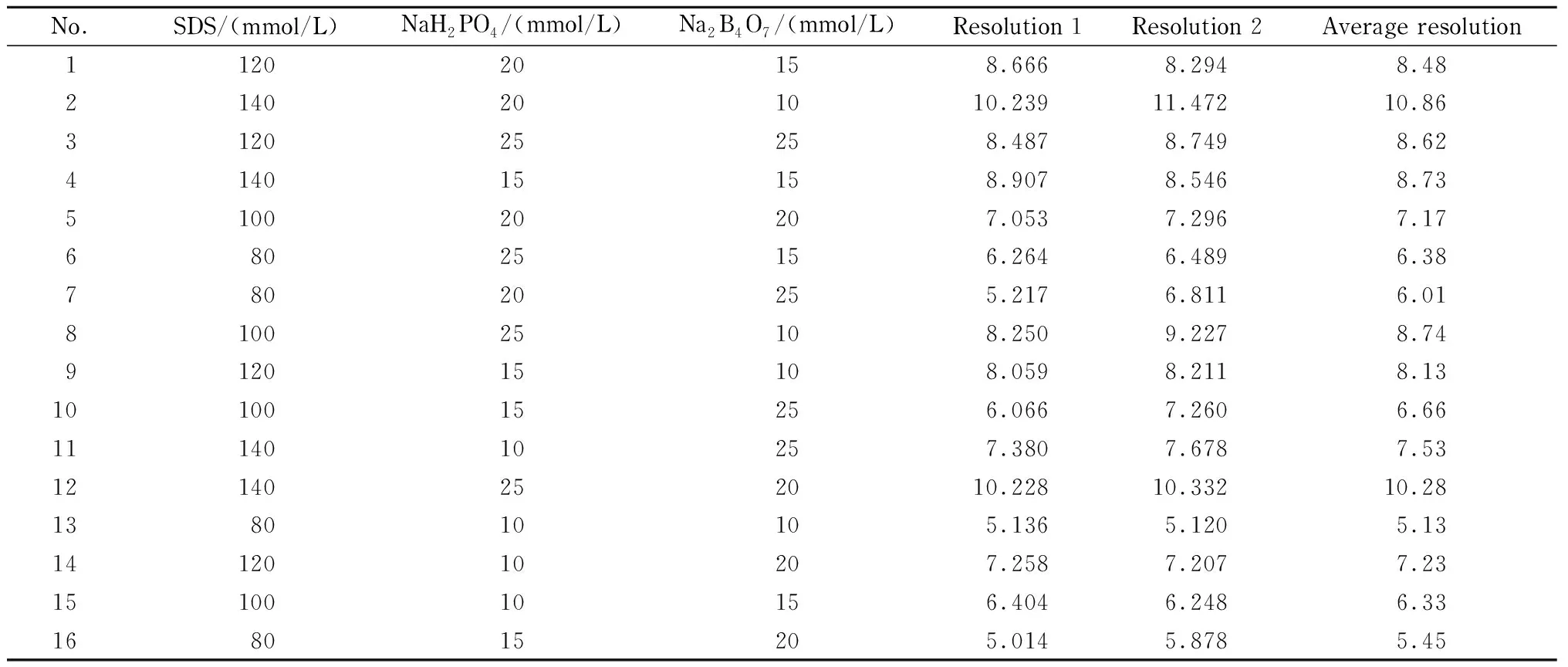
表 2 正交试验设计的因素和水平及分离度结果
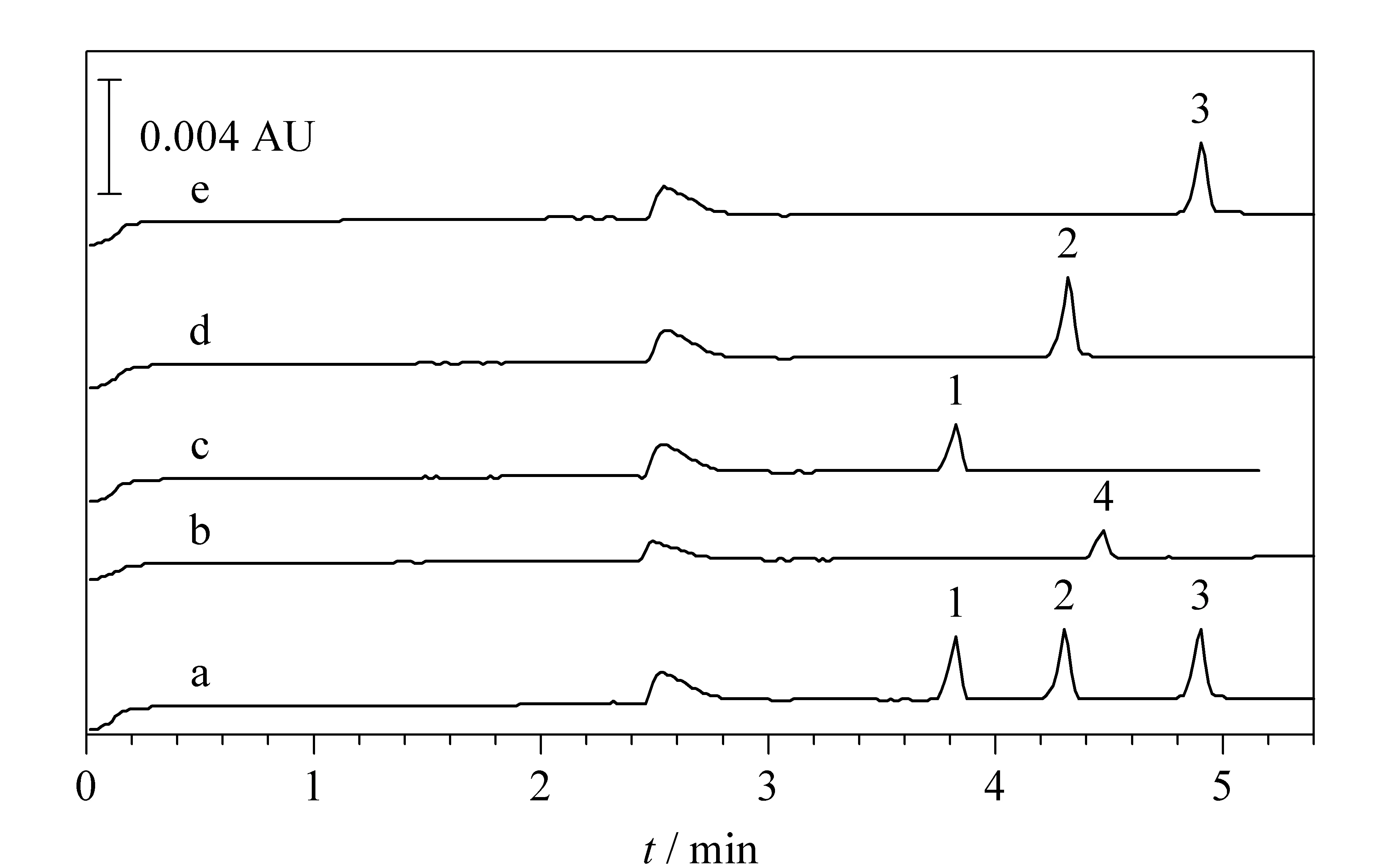
图 1 最佳条件下3种混合标准溶液、药品样品及 抑菌样品的电泳图Fig. 1 Electropherograms of the three kinds of antiviral drug mixed standard, a pharmaceuticals sample and a bacteriostatic sample under the optimal conditions a. 20 mg/L mixed standard solution (ganciclovir, acyclovir, and penciclovir); b. the bacteriostatic sample; c. ganciclovir ophthalmic gel; d. acyclovir gel; e. penciclovir cream. Peak Nos.: 1. ganciclovir (3.879 min); 2. acyclovir (4.279 min); 3. penciclovir (4.867 min); 4. unknown peak.
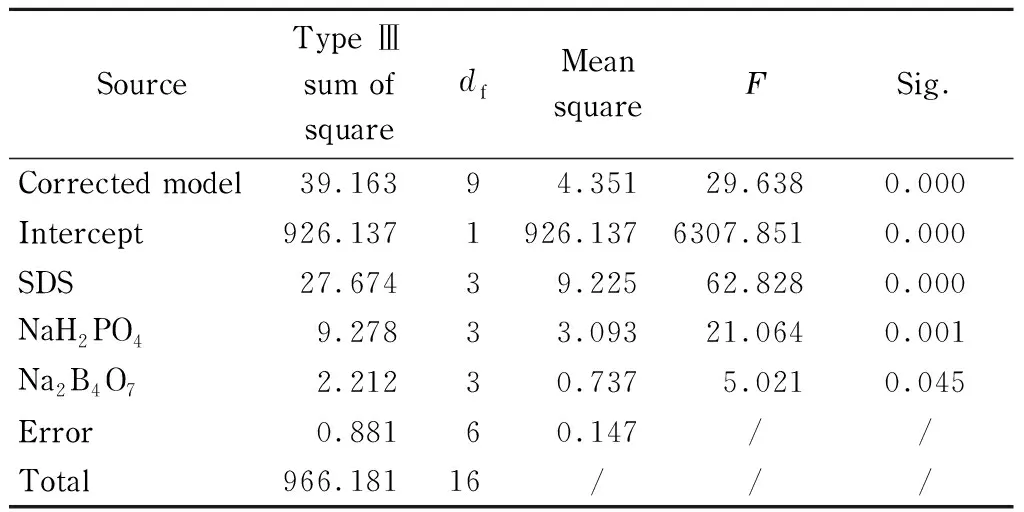
SourceType Ⅲsum of squaredfMean squareFSig.Corrected model39.16394.35129.6380.000Intercept926.1371926.1376307.8510.000SDS27.67439.22562.8280.000NaH2PO49.27833.09321.0640.001Na2B4O72.21230.7375.0210.045Error0.88160.147//Total966.18116///
df: degrees of freedom;F: statistic value for analysis of variance; Sig.: significance; /: not calculated.
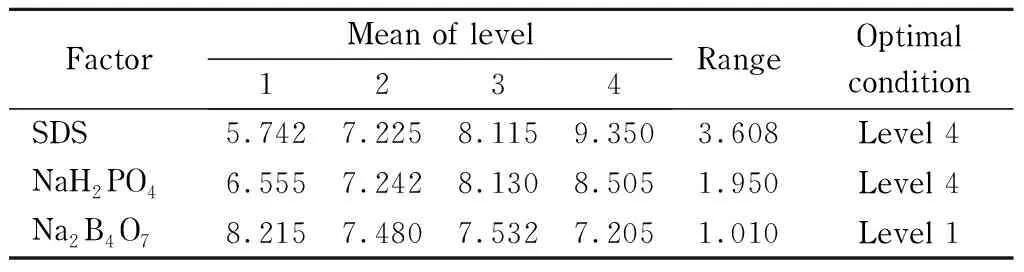
表 4 正交试验设计的极差分析
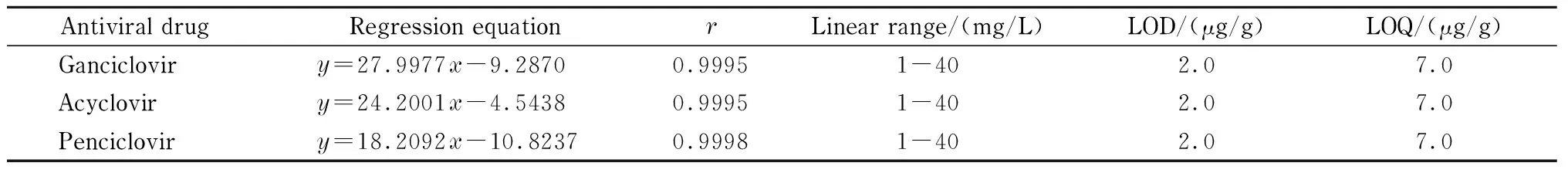
表 5 3种抗病毒药物的回归方程、相关系数、线性范围、检出限及定量限
y: corrected peak area;x: mass concentration, mg/L.
在选定的最佳条件下,以各抗病毒药物的质量浓度(x, mg/L)为横坐标,校正峰面积(y)为纵坐标,绘制校准曲线。检出限以噪声的3倍计算。3种抗病毒药物的校准曲线的回归方程、相关系数(r)、线性范围、检出限(LOD)及取1 g样品时的定量限(LOQ)见表5。
2.2.4精密度与准确度
往不含3种抗病毒药物的液体样品、膏状样品及乳状样品中分别加入低(2 mg/L)、中(20 mg/L)和高(40 mg/L)浓度的混合标准溶液。在最佳电泳条件下进行测定。3种物态样品加标回收率与相对标准偏差结果见表6。更昔洛韦的回收率为88.8%~102.7%;阿昔洛韦的回收率为85.4%~101.0%;喷昔洛韦的回收率为85.5%~104.1%; 3种抗病毒药物的低、中和高浓度加标的相对标准偏差均<8%。
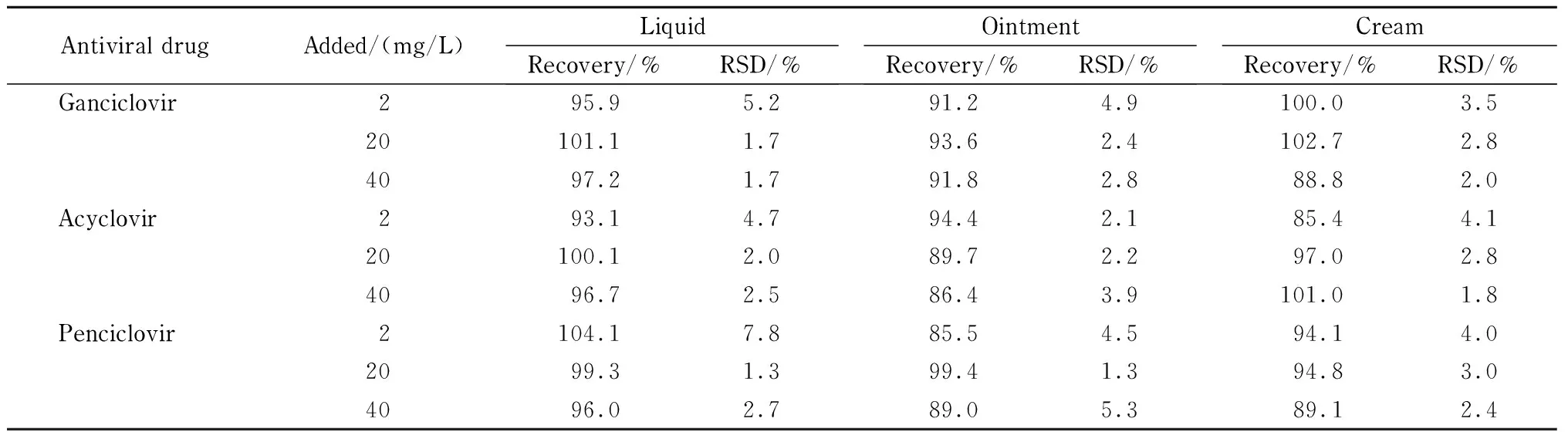
表 6 加标回收率与相对标准偏差结果(n=6)
2.2.5样品测定
用上述方法对6件不同剂型的复方化学消毒剂与抗抑菌产品样品进行测定,均未检出抗病毒药物,其中某抑菌产品的色谱图见图1b。同样用上述方法对购买的更昔洛韦眼用凝胶(标识质量分数为0.15%)、阿昔洛韦凝胶(标识质量分数为1%)及喷昔洛韦乳膏(标识质量分数为1%)进行测定,测得更昔洛韦质量分数为0.15%(见图1c)、阿昔洛韦质量分数为1.10%(见图1d)以及喷昔洛韦质量分数为0.97%(见图1e)。测定结果与标识一致。
3 结论
本文用均匀和正交试验设计对MEKC法的分离条件进行优化,最大限度地实现了3种抗病毒药物在短时间内的有效分离,操作简单,消耗试剂少,成本低,不使用有机溶剂。而且方法的精密度及准确度能够满足消毒剂与抗抑菌产品中抗病毒药物的日常分析需要。

