Th17细胞的研究进展
温小云
【摘要】辅助性T细胞(CD4+)通常分为Th1型和Th2型,Th1细胞产生IFN-γ和IL-2,通过活化巨噬细胞清除胞内病原微生物并介导迟发型变态反应;Th2细胞产生IL-4、IL-5和IL-13,清除细胞外病原微生物并参与变态反应。近年来,在类风湿关节炎、实验性自身免疫性脑脊髓炎等自身免疫病研究中发现一种特殊产生白介素17(IL-17)的辅助性T细胞亚群,该型CD4+T细胞同传统Th1和Th2细胞具有明显不同的特征。此亚群细胞产生IL-17,IL-6和TNF-α而不产生IFN-γ和IL-4,被称为Th17细胞亚群ul该细胞是由天然T细胞前体分化而来,具有独立的分化和发育调节机制,并特异性地产生IL-17效应因子,在自身免疫性疾病和感染性疾病中发挥重要调节作用。
【关键词】Th17细胞;IL-17;CD4+T细胞;免疫调节
1 Th17细胞与IL-17的生物学特性
Th17细胞作为一种效应性CD4+T细胞,其最主要的特征就是分泌IL-17。IL-17与受体结合后,通过活化MAP激酶和NW-κB发挥其生物学活性。IL-17的主要生物学功能是促进炎性反应,与类风湿性关节炎、哮喘、多发性硬化症、银屑病和移植排斥反应密切相关。IL-17還可以刺激上皮细胞、内皮细胞或成纤维细胞产生IL-6、急性反应蛋白、粒一巨细胞刺激因子(G-CSF)和前列腺素E2等表达。因此,适应免疫系统可以通过IL-17和固有免疫系统相联系并促进炎症反应过程。但同大多数炎症因子相似,在体内不同疾病环境中,IL-17也可能发挥不同的免疫调节效应。
2 Th17细胞的诱导产生和分化及其影响因素
Th17细胞是一种新型的CD4+效应性T细胞,如何诱导Th17细胞产生和分化并维持其存活呢?目前大量研究集中于IL-23。研究者认为,虽然IL-23不是Th17分化必需因子,但它是Th17重要存活因子。小鼠缺乏IL-23几乎没有Th17细胞的扩展和存活。同时,IL-23还可以诱导Th17发育并促进IL-17等炎症因子及IL-6、IL-8和TNF等炎症因子分泌为主的慢性炎症发生。因此,IL-23诱导Th17发育在自身免疫性疾病中具有重要调节作用,但目前对IL-23与Th17细胞之间的确切调控机制仍不清楚。
如上所述,虽然IL-23可以维持Th17细胞的正常存活与发展,但IL-23并不参与Th17细胞的早期分化。那么什么因素诱导Th17细胞的分化呢?研究表明CD4+D25+Treg细胞能够抑制T细胞产生IFN-γ和IL-2却明显增加IL-17的产生。提示TGF-β在诱导初始T细胞分化为Th17细胞中起着重要辅助作用除了TGF-β外细胞因子IL-6也起着十分关键的作用。将CD4℃D25'T细胞、未致敏的T细胞和树突状细胞共培养,在IL-6存在时未致敏的T细胞可以有效分化为Th17细胞,且具有TGF-β1依赖性。此外也有研究发现:孤独受体(Orphan nuclearrecep tor,RORγt)是控制Th17细胞分化的转录因子。当小鼠缺乏RORγt后,Th17细胞数量也相应减少。
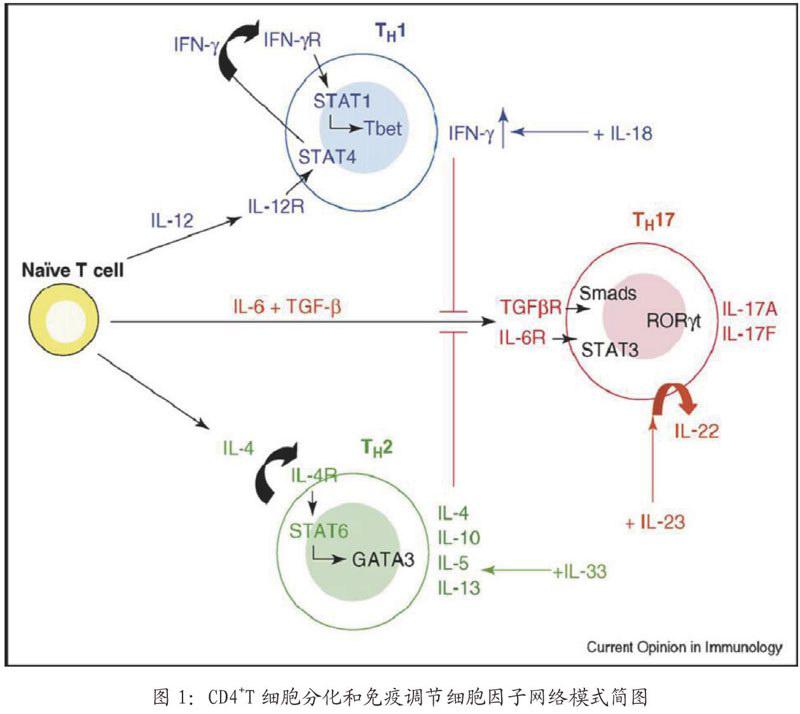
除此之外,研究者还发现,在原代培养中加入IFN-γ或者IL-4可以明显抑制Th17发育分化(图1)。另外,在培养体系中加入外源性IFN-γ或IL-4,也可以阻断IFN-γ缺陷的CD4+T细胞分泌IL-17。这表明,Th1和Th2细胞可有效抑制Th17细胞发育。这也提示,Th-17细胞发育途径明显不同于Th1和Th2细胞,再次说明Th17细胞可能是不同于Th1和Th2细胞的一种CD4+T细胞的新亚型。
3 Th17细胞与调节性T(Treg)细胞之间的关系
在诱导Treg细胞和Th17细胞分化的过程中,TGF-β细胞因子起着十分重要的作用。在TGF-β单独作用下,活化的初始CD4+T细胞分化为Foxp3+Treg细胞;而在TGF-β和IL-6共同作用下,活化的初始CD4+T细胞分化为Th17细胞而不分化为Foxp3+Treg细胞。从而可以看出:IL-6抑制了Foxp3+Treg细胞的分化。同样地,在诱导的过程中加入抗IL-6中和性抗体去除IL-6的作用后,将促进Foxp3+Treg细胞的分化。在IL-6缺陷小鼠模型中获得了同样的结果。
4 Th17细胞与疾病之间的关系
目前研究表明,Th17细胞可能通过其主要效应因子IL-17在炎症和自身免疫性疾病中发挥重要作用大量研究表明,IL-17与类风湿性关节炎、哮喘、狼疮和同种异体移植排斥反应等明显相关。同时,对IL-17缺失小鼠研究显示,其在接触性迟发性和气道性过敏反应中也起到明显的调控作用。在IL-17缺失小鼠给予IL-17R拮抗剂,可以明显对关节炎样疾病具有抗性。
此外,IL-17可以介导中性粒细胞迁移,处于固有免疫和适应性免疫反应的交接面。研究显示,IL-17是通过诱导粒细胞集落刺激因子和IL-8诱导中性粒细胞集聚而IL-17受体缺失小鼠由于粒细胞集落刺激因子和肺巨噬细胞炎症蛋白2大量减少,明显损伤其抗微生物感染能力。
虽然未见文献报道Th17细胞产生的IL-17或IL-17的受体与肿瘤的发生存在直接的关系,但是有证据表明IL-17在肿瘤形成过程中可能起着十分重要的作用。动物肿瘤模型研究己证明IL-17可以促进肿瘤血管的发生,并且促进子宫颈癌在无胸腺的裸鼠中形成。这种现象提示:IL-17有一定的促进肿瘤发生的作用。然而,也有报道认为IL-17通过免疫系统介导的肿瘤排斥作用而抑制肿瘤的发生。Benchetrit等将造血系统肿瘤细胞、肥大细胞瘤P815和浆细胞瘤7558L接种给小鼠后,发现IL-17可以抑制这些肿瘤的生长。由此可见:IL-17与其它细胞因子类似,具有多效性,依据肿瘤的种类和模型的不同对肿瘤的生长可起到促进或抑制的作用。
在寄生虫感染中,尤其是感染了曼氏血吸虫的C57BL/6小鼠会产生肝脏的虫卵肉芽肿性炎症,已经发现这种炎症主要是以Th1型免疫应答产生的IFN-γ水平过高引起,但近来有学者发现这种虫卵肉芽肿性炎症也和高水平的IL-17有关。为了探究这种免疫病理的病因,研究者特地使用了IL-12p40基因和IL-12p35基因分别敲除的小鼠,因为IL-12与IL-23共享IL-12p40和IL-12Rβ1亚单位,而且两者在生物学功能方面有着许多相似之处,众所周知,IL-23是Th17的重要存活因子,用SEA/CFA免疫IL-12p40基因敲除的小鼠,因其不能产生IL-12或IL-23所以也不能刺激淋巴细胞分泌IFN-γ详或IL-17,因此减轻了肝脏肉芽肿性炎症的严重程度。相反,用SEA/CFA免疫IL-12p35基因敲除的小鼠则对肝脏肉芽肿性炎症无明显影响。
5 结语
目前,研究者基本认同Th17细胞是不同于Th1和Th2的一种CD4+T细胞的新亚型。同Th1调节细胞内病原微生物感染和Th2调节寄生虫感染相似,Th17细胞可能也具有调节某种病原微生物感染的功能,这需要进行更深入和细致的实验研究和探讨。在Th17调节自身免疫和机体防御反应中,仍有许多问题有待解决,如病原微生物及其产物如何不同调节IL-23和IL-12表达并导致免疫病理效应?在慢性炎症疾病中,Th17和Th1免疫反应是否具有拮抗或者互补效应?但勿庸置疑,随着一种新的免疫调节途径的发现,必将促进免疫病理学机制研究和有助于建立并形成新的免疫相关疾病治疗方法,并且对疫苗的设计、传染病、自身免疫病、肿瘤和移植排斥反应的研究具有重要的理论和实际意义。

