亚临床甲状腺功能减退与原发性高血压患者动脉粥样硬化的相关性研究
徐敏 茅臻贞 缪培智 郑宏超
200031 上海市徐汇区中心医院心内科
亚临床甲状腺功能减退(甲减)在老年人中发病率较高,且女性高于男性,在大于60岁的女性中发病率可达20%,但因临床症状不明显,常被人们所忽视。已有研究表明,亚临床甲减可引起动脉粥样硬化和心功能不全等不良心血管事件[1]。原发性高血压能促进动脉粥样硬化的发生和发展,是导致心脑血管疾病发生的危险因素之一。然而,较少研究评估亚临床甲减合并原发性高血压对动脉粥样硬化的发生是否有叠加作用。本研究通过对218例原发性高血压患者进行分析,探讨亚临床甲减与原发性高血压患者动脉粥样硬化的关系。
1 对象和方法
1.1 研究对象
本研究为回顾性研究,选择2016年在上海市徐汇区中心医院住院的原发性高血压患者218例,高血压的诊断采用2009年《中国高血压防治指南》(基层版)。排除糖尿病、脑血管疾病、冠心病、心脏瓣膜病、严重肝肾功能不全、恶性肿瘤、急性感染、血液病、临床甲亢或甲减及正在服用影响甲状腺功能的药物者。本研究符合医学伦理学要求,经本院伦理委员会批准。
1.2 分组
依据2007年中华医学会内分泌学分会《中国甲状腺疾病诊治指南》,亚临床甲减的诊断标准为血清促甲状腺激素(thyroid stimulating hormone,TSH)>4.8 mIU/L,血清游离甲状腺素(free thyroxine,FT4)在正常范围(10.3~24.5 pmol/L)。将所有入选患者分为甲状腺功能正常组(157例)和亚临床甲减组(61例)。
1.3 研究方法
所有入选患者于入院次日采集空腹静脉血5 ml,测定血脂、高敏C反应蛋白(hs-CRP)和空腹血糖(FPG),同位素法测定TSH、游离三碘甲状腺原氨酸(free triiodothyronine,FT3)和FT4。应用ACUSON X300 彩色多普勒超声仪(德国西门子公司)测量颈动脉内膜中层厚度(intima-media wall thickness,IMT),探头频率为10 MHz,以颈动脉膨大下1 cm或以颈动脉壁IMT最厚处及靠近心脏1 cm,远离心脏1 cm 3个点的厚度,左右两侧6个点的平均值为IMT,同时观察血管腔内有无斑块形成,将IMT≥1.2 mm视为粥样斑块形成。
1.4 统计学方法
2 结果
2.1 基线资料
甲状腺功能正常组和亚临床甲减组患者的年龄、性别、收缩压、舒张压、吸烟史、高血压病程、血清hs-CRP、FPG、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、FT3、FT4均无统计学差异(P>0.05)。亚临床甲减组血清TSH、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、IMT和颈动脉斑块发生率明显高于甲状腺功能正常组(P<0.05)。详见表1。

表1 两组患者的临床资料
2.2 TSH与颈动脉IMT的多元线性回归分析
在校正了年龄、性别、血压、高血压病程、血脂、FPG、hs-CRP、甲状腺功能等因素后,颈动脉IMT与TSH、年龄、FPG、DBP及HDL-C独立相关,见表2。
2.3 Logistic回归分析
在校正性别、吸烟史、血压、血脂、FPG、hs-CRP等因素后,以是否发生颈动脉粥样斑块为因变量,以TSH为自变量,采用多变量logistic回归分析,发现TSH和年龄进入回归模型,回归系数分别为0.122、0.037(表3),提示血清TSH水平升高可能是原发性高血压患者颈动脉粥样硬化的一项独立危险因素。
3 讨论
甲状腺疾病是内分泌代谢系统疾病中最常见的一类疾病,而高血压更是心血管系统疾病中的多发病,常见病。近年随着对亚临床甲状腺功能减退的深入研究,人们对亚临床甲减和高血压的关系有了新的发现。近期一项国外研究显示,在血压正常人群中,合并亚临床甲减患者的收缩压、舒张压、平均动脉压比对照组显著升高,发生非杓型血压的风险也比对照组高[2]。刘龙华等[3]研究发现,在亚临床甲减患者中,隐匿性高血压的发生明显增高。甲状腺疾病对血压的影响,可能与甲状腺疾病能引起神经激素波动、压力反射变化、血管内皮功能改变、外周血管阻力增加、肾素-血管紧张素-醛固酮系统紊乱等有关,进而引起血压异常。
众所周知,高血压患者的血管结构和功能的改变广泛存在于各级动脉,可导致全身血管病变,促发心脑血管事件。有研究发现高TSH可促进动脉粥样硬化进展,从而导致心血管事件的发病率升高[4]。那么亚临床甲减合并原发性高血压是否对动脉粥样硬化的发展有协同作用呢?2013年国外的一项研究发现,高血压合并亚临床甲减患者的动脉粥样硬化较单纯高血压患者严重[5]。颈动脉IMT能反映全身动脉粥样硬化情况,对早期发现大血管并发症有重要意义。杜海梅[6]研究发现,亚临床甲减合并原发性高血压患者组比单纯原发性高血压患者组的颈动脉粥样硬化发生率明显升高,高TSH是颈动脉粥样硬化的独立危险因素。在本研究中发现与单纯原发性高血压患者组比,原发性高血压合并亚临床甲减组的IMT明显增厚,颈动脉斑块发生率明显升高。在多元线性回归分析中,校正性别、年龄、血压、血脂等动脉粥样硬化危险因素后发现,高血清TSH与颈动脉IMT具有独立正相关性,而在logistic回归分析中发现高血清TSH是颈动脉粥样斑块发生的独立危险因素。这些研究结果均与上述研究结论相一致。提示亚临床甲减可促进原发性高血压患者的动脉粥样硬化进展。本研究存在不足之处,HDL-C与颈动脉IMT具有独立负相关性,与既往研究结果相符,但其他血脂指标如LDL-C、TC、TG等,与IMT相关分析中未得出阳性结果,可能和样本量不够大有关。
亚临床甲减促进原发性高血压患者血管动脉粥样硬化的进展,可能有多方面的原因。首先,脂代谢方面,脂质代谢紊乱是动脉粥样硬化的独立危险因素,亚临床甲减患者的血脂水平变化存在较大争议,但绝大多数研究还是倾向于亚临床甲减患者存在血脂紊乱,而脂质紊乱可导致动脉粥样硬化的发生发展。Zha等[7]研究发现,亚临床甲减患者的脂质过氧化作用及血清LDL-C水平比甲状腺功能正常者高,亚临床甲减引起的高水平脂质过氧化作用及LDL-C可导致动脉粥样硬化的风险增高。在本文基线资料中,亚临床甲减合并原发性高血压患者的血清TC、LDL-C水平比单纯原发性高血压组明显升高,与上述研究结论一致。表明亚临床甲减可加重原发性高血压患者的脂代谢紊乱,促进血管动脉粥样硬化的进展。其次,炎症方面,目前已明确慢性炎症与动脉粥样硬化的发生发展有关,特别是CRP作为炎症因子,参与了动脉粥样硬化的过程。虽然目前对于亚临床甲减与炎症因子之间的关联研究较少,但已有研究发现亚临床甲减可引起血清CRP水平升高,血清CRP水平与TSH水平呈正相关[8]。在本研究中亚临床甲减合并原发性高血压患者组血清CRP水平与单纯高血压组比较有所升高,虽无统计学意义,可能与样本量小有关,但或可表明亚临床甲减可提高原发性高血压患者的炎症反应水平,促进动脉粥样硬化的进展,此结论有待以后大样本量的研究进一步论证。最后,最近的一项研究显示,亚临床甲减可合并血管内皮功能障碍,导致血管扩张功能减弱,使血压水平升高同时加重高血压患者的动脉粥样硬化[9]。
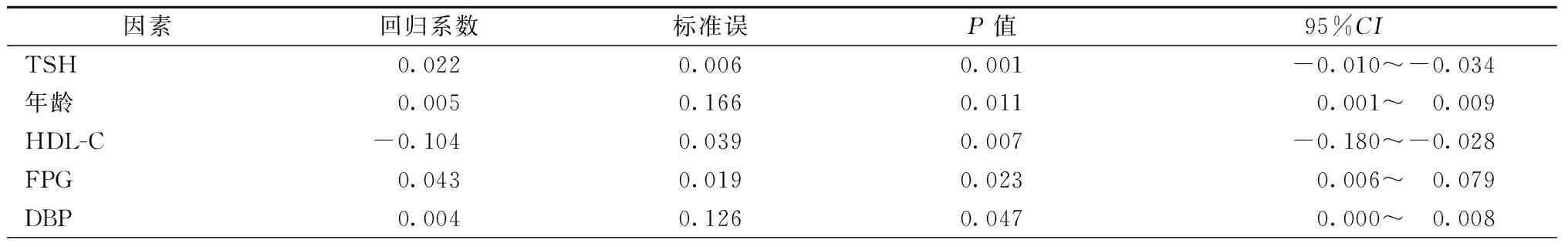
表2 TSH与颈动脉IMT的多元线性回归分析

表3 TSH与颈动脉斑块发生与否的logistic回归分析
2007年版《中国甲状腺疾病诊治指南》中,对于亚临床甲减患者倾向于TSH>10 mU/L时应开始甲状腺素替代治疗[10]。有学者建议治疗目标TSH降到3 mU/L以下。而且国外已有研究证实,甲状腺素替代治疗可使亚临床甲减患者血管内皮功能改善,进而使血管舒张功能改善[9]。国内亦有研究显示,短期左甲状腺素替代治疗可改善亚临床甲减患者类花生四烯酸部分代谢通路异常导致的炎症反应、血栓形成、氧化应激等反应[11],这些都对预防动脉粥样硬化的发生发展起积极作用。
综上所述,亚临床甲状腺功能减退可通过多种机制导致或加重血压升高,最终加剧原发性高血压患者的动脉粥样硬化的发生发展。高血压患者有必要常规、定期检测甲状腺功能。临床医师应该加强对亚临床甲减的认识,重视亚临床甲减的危害性。
利益冲突:无