直肠癌术后吻合口狭窄的临床分析
周小兵 李冰心 周欣 陈爱军
近年来由于腹腔镜下全直肠系膜切除术(total mesorectal excision,TME) 观念的引进并在临床上实施,使得更低位的直肠癌病人肛门得以保留,但超低位直肠癌术后吻合口狭窄发生率在国外仍然高达17.6%~24%[1],国内为22.5%[2-4]。吻合口狭窄降低了病人生活质量,因此分析腹腔镜下直肠癌TME术后吻合口狭窄的原因和防治方法具有重要意义。
资料与方法
一、一般资料
回顾性分析三峡大学第一临床医学院2010年1月至2014年12月在该院行腹腔镜下直肠癌TME术的直肠癌病人486例为研究对象,所有病例均按TME原则施行腹腔镜下直肠癌切除术, 均在术前经肠镜及病理学检查确诊为原发性直肠腺癌,无重复癌,均为第一次腹部手术。
二、发生吻合口狭窄及治疗情况
共发生吻合口狭窄27例,27例均经肛门指诊、电子结肠镜及钡剂灌肠证实吻合口直径<12 mm。根据吻合口狭窄特点,选择经肛门扩张吻合口、手术切除吻合口狭窄环、结肠造口等不同治疗方法。
三、随访方式及时间
采用门诊、电话、邮件、住院等方式进行随访。治疗后6个月内每2周随访1次并行经肛门指诊扩张吻合口,6个月后每3个月随访1次,24个月后每6个月随访1次。随访时间8~50个月,中位随访时间为20个月。
四、统计学分析
应用SPSS(16.0版)统计学分析软件包进行处理。计数数据采用χ2检验,对各影响因素进行Logistic回归分析,P<0.05为差异有统计学意义。
结 果
一、独立危险因素分析结果
对病人的临床资料进行单因素分析, 结果显示:男性、吻合口漏、术前新辅助放疗、肿瘤下缘距肛缘距离<5 cm与吻合口狭窄的发生密切相关(P<0.05)。(表1)
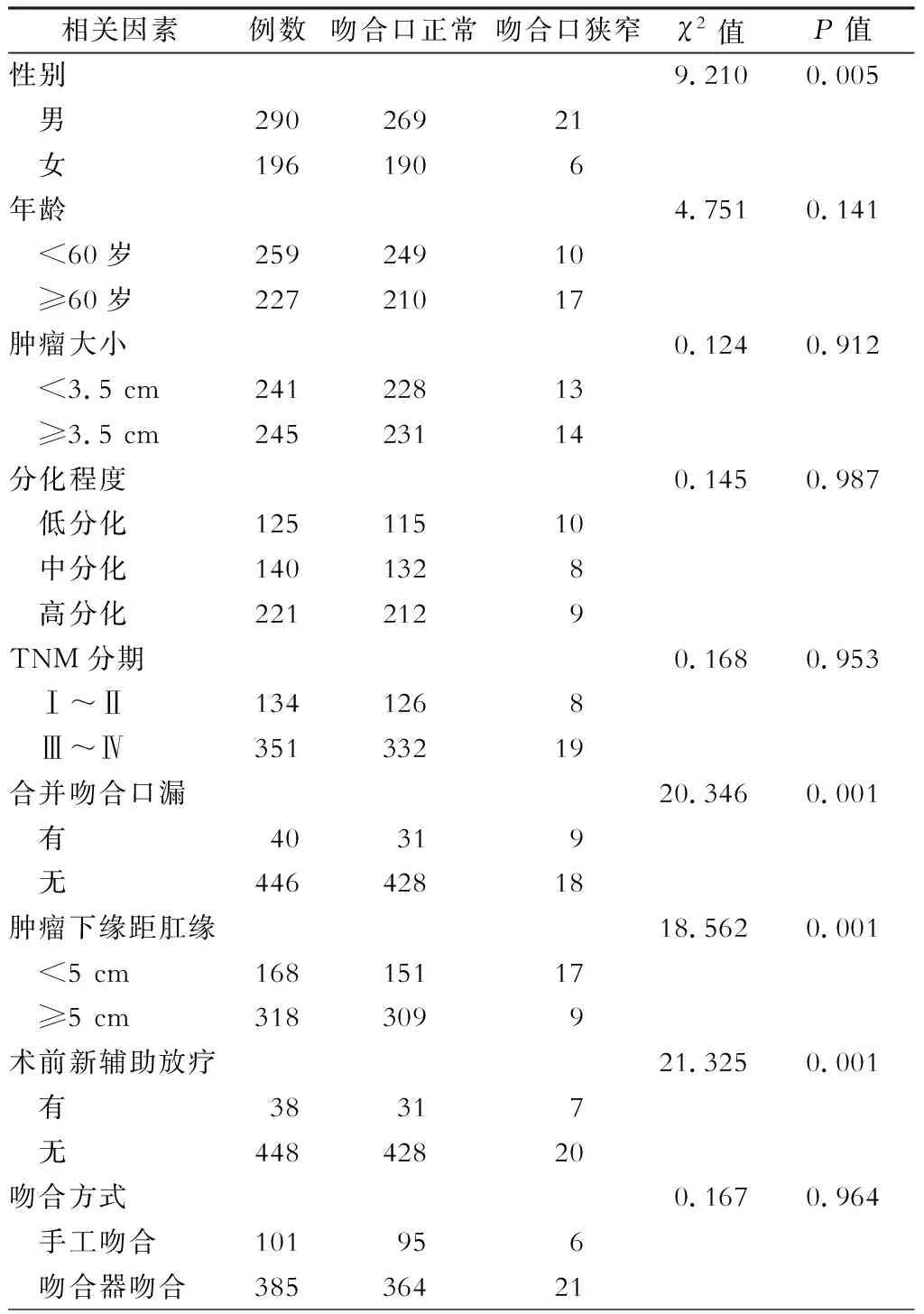
表1 486例直肠癌病人临床资料(例)
二、多因素非条件Logistic回归分析结果
将是否发生术后吻合口狭窄为应变量,将可能影响吻合口狭窄发生的10个因素作为自变量,做多因素非条件Logistic回归分析后显示:男性、吻合口漏、术前新辅助放疗、肿瘤下缘距肛缘距离<5 cm是发生吻合口狭窄的独立危险因素(P<0.05)。(表2)
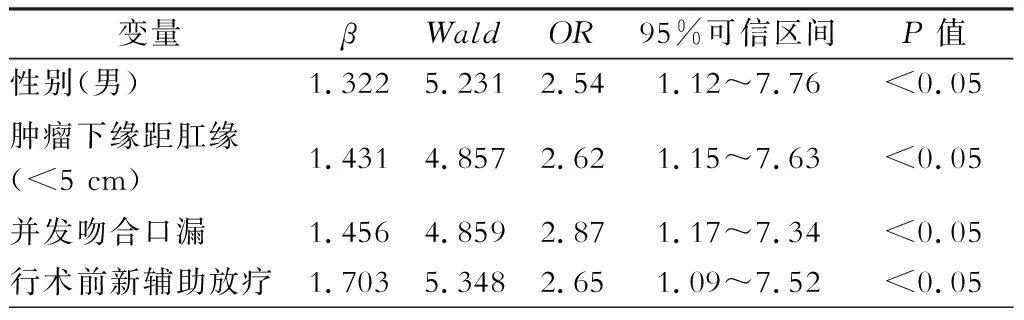
表2 多因素非条件Logistic回归分析
三、直肠癌术后吻合口狭窄治疗及随访情况
27例吻合口狭窄病人,其中1例为肿瘤局部复发并肝转移,行永久降结肠双腔造口。26例吻合口瘢痕狭窄病人中,行剖腹切除狭窄吻合口后一期吻合4例;经肛门完整切除膜状狭窄环7例;6例经肛门放射状切开狭窄环,并于术后4 d经肛门每日人工扩张吻合口2~3次,共扩张3个月;9例未行手术,每日经肛门行人工扩张吻合口1次,共扩张3个月。吻合口狭窄病人再次术中未发生肠管损伤、输尿管损伤、骶前大出血等并发症。吻合口狭窄病人中位随访时间为20个月。27例病人均获得随访,2例随访期间死于肿瘤复发及转移,余25例吻合口检查通畅,直径均≥12 mm。
讨 论
随着腹腔镜微创外科学技术的提高和精准医学理念的发展,直肠癌外科近年取得了很大的进步,但是吻合口狭窄仍是直肠癌TME术后常见的并发症, 严重影响病人的生活质量。因此,明确直肠癌TME术后发生吻合口狭窄的危险因素,及如何预防吻合口狭窄至关重要。
一、直肠癌术后吻合口狭窄的原因分析
本研究有1例为肿瘤局部复发导致的吻合口狭窄,其余26例吻合口狭窄均与肿瘤局部复发无关。发生吻合口狭窄的根本原因在于吻合口一期愈合失败后的继发肉芽组织广泛增生和纤维化瘢痕形成。吻合口狭窄的原因很多,结合本研究观察的指标分析如下:①吻合口漏: 有学者[5-8]认为吻合口漏二期愈合时瘢痕形成是吻合口狭窄主要原因,部分病例为微小漏临床很难察觉,吻合口漏造成吻合口周围组织感染坏死,形成慢性炎症,愈合后产生瘢痕挛缩,纤维化致吻合口狭窄。本研究有40例临床诊断吻合口漏,有9例发生吻合口狭窄(22.5%,9/40)。②术前新辅助放疗:有学者[9-10]认为术前新辅助放疗导致放射性肠炎,可增加直肠癌术后吻合口漏的发生率。本研究有38例行术前新辅助放疗,有7例发生吻合口狭窄,独立危险因素分析及多因素非条件Logistic回归分析后均显示术前新辅助放疗为发生吻合口狭窄的独立危险因素。③性别:有学者[11-13]研究表明男性病人吻合口狭窄的发生率高于女性,这可能与男性骨盆狭窄、骨盆腔相对较深、术野显露不佳,操作解剖及吻合困难所致。本研究同样证实了男性直肠癌术后吻合口狭窄发生率较高。④保护性造口:有文献[14-15]报道低位直肠癌行保护性肠造口后,因吻合口处于废用状态,且易出现吻合口出黏膜与其下层组织愈合口径不一致的现象,也可导致吻合口狭窄。⑤肿瘤下缘距肛缘距离:通常认为肿瘤距离肛缘7 cm以内为低位直肠癌,5 cm以内为超低位直肠癌,4 cm以内为极限低位直肠癌。肿瘤位置越低,直肠游离的范围也越低,若吻合口上方结肠保留过短或游离不充分, 吻合口有张力,加重血运障碍, 故组织缺氧致使纤维组织过度增生,导致吻合口狭窄;而且低位吻合,肛管括约肌张力过大,肛门括约肌痉挛,因为括约肌的收缩功能,易形成直肠癌吻合后狭窄[16]。本研究以肿瘤下缘距离肛缘5 cm为分界点进行研究,证实肿瘤下缘距肛缘距离<5 cm是发生吻合口狭窄的独立危险因素。另外,本研究还分析了肿瘤大小、肿瘤分化程度、TNM分期、吻合方式等因素对吻合口狭窄的影响,由于随着技术改善,这几项因素对吻合口的血运、张力、所使用切割闭合器钉夹数目等的影响程度降低,加之样本量偏少,故本研究未得出独立危险因素结论。
二、直肠癌术后吻合口狭窄的预防
腹腔镜下直肠癌TME术前应评估病人一般情况,并积极处理贫血、低蛋白等不利因素,做好肠道准备,术中充分游离结肠至脾区以降低吻合口张力,超低位直肠癌可保留乙状结肠动脉以确保吻合口血运,在使用直线切割闭合器时尽量使切割器在一平面,吻合时采用双吻合器技术将两次切割交界角处切除[17]。完成吻合后经肛门预置两根硅胶肛管跨越吻合口以达到局部减压及支撑作用。随着外科学技术发展,腹腔镜下切割闭合器、3D腹腔镜、超声刀等的应用有利于术者的精准操作。
三、直肠癌术后吻合口狭窄的治疗
直肠癌术后吻合口狭窄治疗难度较大,在治疗前需行结肠镜及活检、钡剂灌肠造影检查、腹部CT等明确吻合口狭窄程度、位置、长度、性质、是否合并梗阻等明确诊断。文献报道吻合口狭窄治疗方法很多:低位直肠癌保肛术后吻合口膜状狭窄,多用手指、一次性肛门镜、金属扩张器扩张,疗程3个月至1年[18];但国内外均有报道可回收支架治疗直肠癌术后吻合口狭窄,病人置入支架后均有不同程度的肛门区不适、胀痛,少数病例出现少量血水样便等[9-10],临床不宜推广。我们的经验是对较轻微的吻合口狭窄,可每日规律经肛门用手指或扩肛器等机械扩肛,效果比较理想;对于低位的膜性狭窄,经肛门直视或内镜引导下切除膜性狭窄组织;对于低位的长度短的管状狭窄,经肛门直视或内镜引导下纵行切开狭窄环,有文献[19]报道放射状切开狭窄环是有效的;对于位置较高及狭窄长度较长的吻合口狭窄病例,直接行剖腹切除狭窄吻合口并重新进行吻合,有文献[20]报道对该类病人经腹腔镜下结合内镜行狭窄吻合口切除,但我们考虑腹腔镜直肠癌TME创面大,盆底粘连严重,易损伤盆腔组织器官,故再次手术行腹腔镜需慎重,应由高年资经验丰富的胃肠外科医师开展;对于因肿瘤局部复发导致的吻合口狭窄并肠梗阻,根据病人情况采取姑息性手术,如1例为肿瘤局部复发并肝转移,行永久降结肠双腔造口。多篇报道对如何有效缓解直肠癌术后吻合口狭窄,保证排便通畅,提高病人生存质量,进行了探讨,临床应根据不同狭窄原因及部位选择相应的治疗方法。
综上所述,男性、吻合口漏、术前新辅助放疗、肿瘤下缘距肛缘距离<5 cm为直肠癌术后吻合口狭窄的危险因素;直肠癌术后吻合口狭窄重在预防,应根据吻合口不同狭窄原因及程度采取不同方法解除梗阻,治疗效果较满意。

