能力验证提供者质量管理体系内审结果分析与改进
郭晓俊,范基农,徐 翀,朱 俊,杨 雪,娄 娇,黄妍君
(上海市临床检验中心,上海 200126)
内部审核是实验室对自身质量管理体系进行自查的审核方式,是实验室按照管理体系文件规定,对各个环节开展的有计划、系统、独立的检查活动。审核的目的是验证实验室活动是否符合CNAS-CL03《能力验证提供者认可准则》[1]和管理体系的要求。
上海市临床检验中心于2012年9月通过了中国合格评定国家认可委员会认可,本研究对2012—2017年6年的内部审核不符合项进行分析,以评价和探讨通过认可以来质量管理体系运行的符合性及有效性,以促进质量管理体系的持续改进。
1 材料和方法
1.1 资料来源
收集2012—2017年上海市临床检验中心能力验证计划提供者质量管理体系内部审核报告中的不符合项。
1.2 审核的依据、范围、方式、过程和内容
1.2.1 审核依据 以CNAS-CL03《能力验证提供者认可准则》[1]、上海市临床检验中心《质量手册》《程序文件》《作业指导书》《生物安全手册》及有关技术文件、外部受控文件和外部签订的合同等作为审核依据。
1.2.2 审核范围 覆盖质量管理体系所有要素和活动;涉及上海市临床检验中心质量管理体系相关的所有部门、场所和人员。
1.2.3 审核方式 分组审核,每组至少2人,采取交叉现场检查、人员交谈、核对记录、调查验证等方式进行。分组时,做到内审员独立于被审核的工作,确保内审工作的客观性与独立性[2]。
1.2.4 审核过程 按照《程序文件》的规定,每年至少组织1次内部审核。内审前质量主管授权成立内审组,质量管理部门制定《内审实施计划》,准备审核工作文件并确保现行有效,编制《现场审核检查表》,按计划进行现场审核,审核后编写内审报告,出具不符合项报告,并对不符合项进行跟踪验证。
1.2.5 审核内容 CNAS-CL03《能力验证提供者认可准则》所有要素包括总则,人员,设备、设施和环境,能力验证计划的设计,方法或程序的选择,能力验证计划的运作,数据分析和能力验证计划结果的评价,报告,与参加者的沟通,保密,组织,管理体系,文件控制,要求、标书和合同的评审,分包服务,服务和供应品的采购,服务客户,投诉和申诉,不符合工作的控制,改进,纠正措施,预防措施,记录的控制,内部审核,管理评审,共25项。
2 结果
2.1 不符合项年度分布情况
2012—2017 年共进行6次内审,涉及中心所有业务部门,发现不符合项118项。其中2012年25项、2013年18项、2014年18项、2015年15项、2016年14项、2017年28项。
2.2 不符合项的分布情况
内审中发现的不符合项分为一般性不符合和严重不符合。2012—2017年6次内审发现的118项不符合项均为一般性不符合,其中与技术要素相关的82项,约占70%。不符合项主要分布在25个要素中的7个要素中,占所有要素的82%,前3位分别为设备、设施和环境(17.80%),人员(16.10%),能力验证计划的设计(13.56%),占不符合总数的47.46%。见表1。
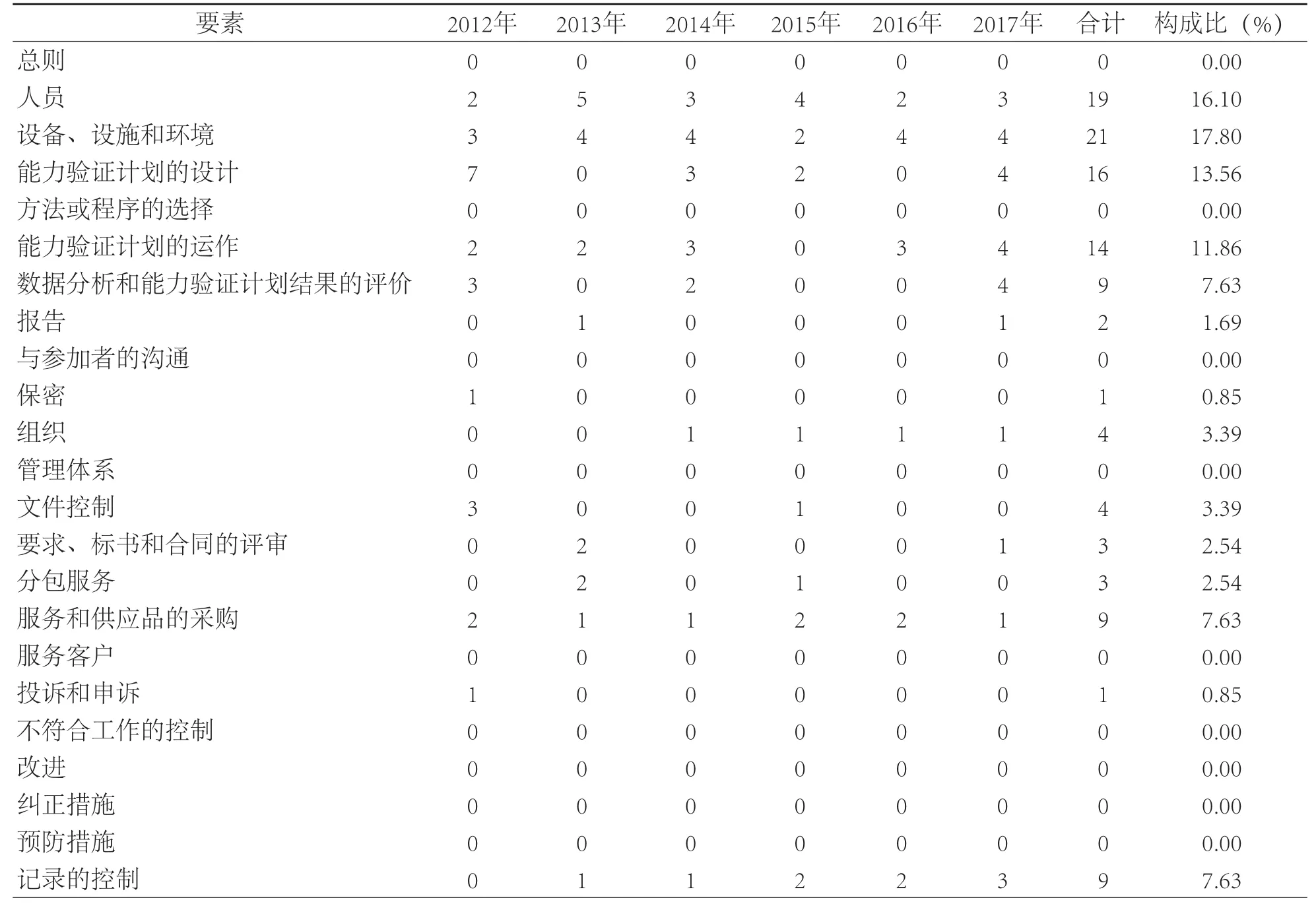
表1 2012—2017年内审不符合项分布一览表 (项)
续表1
2.3 不符合项性质分布情况
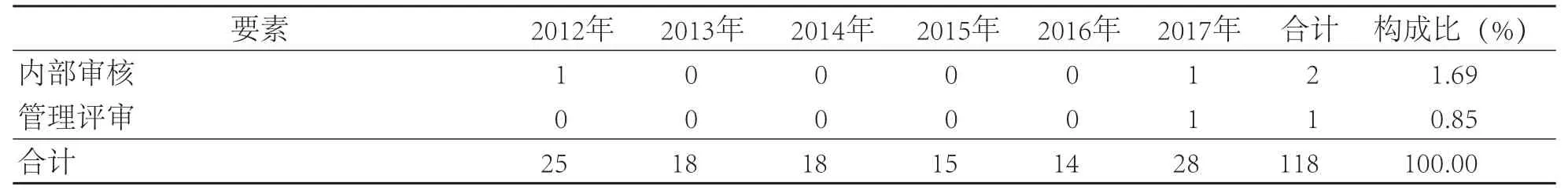
按照不符合项的性质,一般分为体系性不符合、实施性不符合。体系性不符合是指体系文件规定不妥当、资源配备不充足、规划不合理等问题;实施性不符合是指没有执行规定的要求,实际工作与规定不符的现象(实施效果不佳的不符合统一归纳为实施性不符合)。经统计,2012—2017年内部审核体系性不符合17项(14.4%),实施性不符合101项(85.6%)。见表2。

表2 2012—2017年内审不符合项性质分布情况 (项)
3 讨论
3.1 不符合项的年度分布
2012—2016 年不符合项呈逐年减少的趋势。每次审核的内审员、审核的依据、审核的范围及部门的职能等基本一致,结果具有可比性。随着质量管理体系的运行和持续改进,员工的质量意识逐步增强,质量工作取得明显效果。2017年不符合项增加主要有3个原因,一是由于重新调整了内审工作方案,改变以往以科室为单位的内审模式,尝试采用新的、按体系条款审核的模式,进行地毯式的审核,使得内审的不符合项增加;二是扩项项目的增加,2017年年度目标要求在原来通过认可的118项的基础上扩项173项,合计291项;三是体系文件增加了微生物领域能力验证计划组织的相关内容,内审检查表中也相应地增加了新的内容。为了保证能力验证提供者复评审和扩项评审的顺利通过,内审要求更加严格,因此不符合项也上升至28项。
3.2 不符合项的要素分布
不符合项主要分布在25种要素中的7个要素中,前3位要素分别为设备、设施和环境,人员,能力验证计划的设计,占总数的47.46 %。其他4个要素共占不符合总数的34.75 %,分别是能力验证计划的运作(11.86%)、数据分析和能力验证计划结果的评价(7.63%)、服务和供应品的采购(7.63%)以及记录的控制(7.63%)。
不符合项列第1位的是设备、设施和环境的问题,以2016和2017年发现的问题最多,反映出设备、设施管理以及环境控制问题一直是薄弱环节。不符合内容主要是仪器设备的使用、管理不规范,存在使用的环境控制、验收、档案、标识等问题。由于人员变动、交接和培训工作未及时跟上,使设备和环境条件控制的规范管理在体系建立后没有得到良好的延续是不符合产生的原因。
不符合项列第2位的是人员问题,如新进和转岗人员培训不及时和监督不到位;在岗人员培训效果评价不全面,未及时进行年度能力评估;专业技术人员业绩档案有关信息不全等问题。主要原因是:(1)质量体系宣贯力度不够,未能充分认识质量管理的重要性和必要性;(2)培训和管理的专职部门工作没有做到位,体系文件的执行力不够;(3)质量监督力度不够,不能充分发挥把关作用。
不符合项列第3位的是能力验证计划的设计问题。表现为不同定性项目和定量项目的统计设计不恰当;设计方案中缺少准则条款,如能力验证物品丢失或损坏时应采取的措施、防止参加者串通或伪造结果的合理预警措施等;文件中缺少准则的内容,如相关技术专家及其职责规定等问题。主要原因是对方案设计的人员培训不到位,导致对准则的理解不到位,有些是不知道如何处理,甚至在方案设计中没有明确。
其他不符合项内容有记录控制工作,渗透入实验室工作的各个领域,也是最容易出现问题的地方。表现为记录内容填写不全,质量记录信息不全;个别文件无受控标识,作废文件未按程序处理;报告信息填写不规范等。
3.3 内审不符合项的性质
2012—2017 年内审不符合项的性质分类中,体系性不符合17项,实施性不符合101项,绝大部分为实施性不符合,占85.6%;而体系性不符合仅占14.4%。分析两类不符合的分布时间,实施性不符合存在于各个年份,并始终占最大的比例,说明在体系运行过程中,主要问题表现在体系文件的执行不彻底方面,没有严格按文件的要求开展工作,导致符合性和有效性方面未达到标准的要求。体系性不符合项基本分布在2012和2017年。2012年是因为在实验室质量体系建立初期,对标准和体系文件的学习不够,理解存在偏差;体系文件还存在不少问题,内容规定的不全面、不便于操作,甚至有些与实际工作不符;而2017年,由于管理层的扩项要求和增加了微生物领域能力验证提供者的特殊要求,因此作业指导书未能及时覆盖扩项项目导致体系性不符合增加,随着体系的运行和持续改进,质量体系、程序文件和作业指导书进一步完善。
以上出现不符合项的根本原因大致可归纳为:对标准和体系文件的学习不够,理解存在偏差;导致编写体系文件出现内容规定的不全面、不便于操作、有些与实际工作不符;体系培训不到位,监督不到位;体系文件的执行不彻底,没有严格按文件的要求开展工作,导致符合性和有效性方面未达到要求。
3.4 建议
3.4.1 加强培训 体系运行的好坏,一定程度上取决于全体员工对体系的认识程度,因此需要不断加强质量管理体系相关知识的培训。针对不同人群开展相关培训,一是对内审员的培训,能否发现问题是关键,因此需要加大对内审员的培养力度,除要求客观、公正外,还应提高审核水平和能力,熟悉被审核部门的业务工作,掌握现场审核技巧[3]。二是领导层面,包括对最高管理者、技术主管、质量主管和其他质量管理人员着重讲解准则条款“组织”、“管理体系”、“人员”等要素;三是相关科室的技术主管,即科室主任或项目负责人,可着重讲解能力验证计划运作中的技术要素问题,对策划、数据分析和统计以及能力评定等关键控制点的监督;最后一个层面是相关的重点人员,包括科室内部的质量监督员、仪器设备管理员、样品管理人员、试剂耗材管理人员和文件管理人员等应着重讲解质量管理体系的重要性以及如何具体操作流程和关键控制点等。通过以上培训可以覆盖质量管理体系所涉及的所有人员。对于每层人员应根据其工作特点进行有针对性的培训。
3.4.2 加强质量监督 通过内部审核发现,绝大部分的不符合项都是实施性的问题,除了加强培训之外,员工对待质量管理工作的态度在主观上仍然存在被动性、依赖性。质量监督渗透在质量管理的各个环节,除了质量管理人员经常检查质量体系外,每个科室可指派1~2名质量监督员,掌握质量监督工作范围及重点,采取多种方式对实验室进行监督,提高监督频次,确保质量监督工作不流于形式,督促全体员工按照体系文件规定的要求执行,以确保质量管理体系的不断改进,保障质量体系的有效运行。
3.4.3 调动人员积极性 如何有效提高人员的积极性是一个值得深入研究的问题。体系在运行一段时间以后,员工容易出现体系惰性,可以通过建立质量监督激励机制,在实验室内部进行交叉检查,定期进行质量管理交流和小组培训,增加员工参与质量管理的机会,有利于提高整体的质量意识,有效提高人员积极性。
综上所述,随着体系的持续运行,我们更加体会到内审工作的重要性,通过内审工作的有效开展,能够及时发现问题并采取整改措施,对实验室质量管理体系实现持续改进和自我完善具有重要意义。

