乙酰氨基阿维菌素原位凝胶注射剂对小鼠的急性毒性研究
张振东 杨亚军 刘希望 孔晓军 马宁 申栋帅 李剑勇
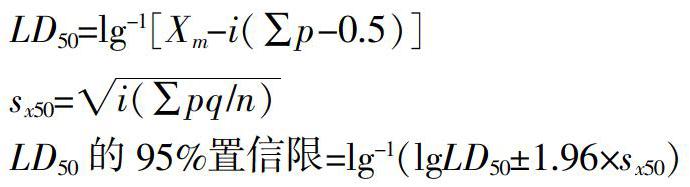
摘要:为了对乙酰氨基阿维菌素原位凝胶注射剂的安全性进行评价,采用简化寇氏法进行了小鼠的急性毒性研究。首先通过预试验的最小致死剂量(LD100)和最大耐受剂量(LD0)确定给药剂量及试验分组。皮下注射给药,观察7 d,记录死亡数,计算LD50及95%的置信区间。结果表明,乙酰氨基阿维菌素原位凝胶注射剂对小鼠的急性毒性LD50为5.903 g/kg,95%置信区间为5.105 3~6.415 0 g/kg。按照化学药物剂量分级,乙酰氨基阿维菌素原位凝胶注射剂可认定为实际无毒物质,说明该药临床皮下注射使用安全。
关键词:乙酰氨基阿维菌素原位凝胶注射剂;LD50;小鼠;急性毒性
中图分类号:S859.83 文献标识码:A 文章编号:0439-8114(2018)11-0068-02
DOI:10.14088/j.cnki.issn0439-8114.2018.11.016
Abstract: An acute toxicity test of Eprinomectin in situ gel injection on mice was taken to evaluate its safety by simplified Karber's method. The dosage and grouping were determined based on the minimum lethal dose(LD100) and the maximum tolerated dose(LD0) in preliminary experiment. The mice were administered with Eprinomectin in situ gel injection and observed seven days. The number of deaths was recorded for calculating the LD50(lethal dose 50%) and the 95% confidence limit. The results showed that the acute toxicity LD50 of Eprinomectin in situ gel injection on mice was 5.903 g/kg,95% confidence limit ranges was from 5.105 3~6.415 0 g/kg. It indicated that the Eprinomectin in situ gel injection was non-toxic substances according to chemically drug classification.
Key words: Eprinomectin in situ gel injection;LD50;mice;acute toxicity
乙酰氨基阿维菌素(Eprinomectin,EPR)是由Merk公司1997年开发出的大环内酯类体内外杀虫剂,是一种高效、广谱、低残留的兽用新一代抗寄生虫药物[1]。EPR在防治畜类(特别是产乳期)的虱、螨、蝇等各种内外寄生虫时效果很好并且休药期很短,在治疗奶牛寄生虫病时休药期仅为1 d[2,3]。它也通过了美国FDA批准可在动物孕期和哺乳期安全使用,由于它在牛奶中的分布系数极低,目前在国外已被广泛用于乳制品的生产行业。EPR是目前世界上使用较多的动物抗寄生虫用药物[4,5]。EPR杀灭寄生虫的作用机理与其他阿维菌素类药物非常相似。EPR属于γ-氨基丁酸(GABA)激动剂,当它达到一定浓度时可以和动物体内的神经细胞、神经传导器等有效结合,这样就会阻断氯离子通道,进而阻断动物的神经末梢或者神经肌细胞相互间的传递,从而使动物体内的寄生虫麻痹,继而杀死寄生虫[6]。为此,以小鼠为试验动物进行乙酰氨基阿维菌素原位凝胶注射剂的急性毒性试验,旨在为指导临床科学、安全地使用该注射剂提供依据。
1 材料与方法
1.1 材料
试验动物:SPF级昆明系小鼠110只,购自中国农业科学院兰州兽医研究所,体重18~22 g,雌雄各半,雌性未产未孕。雌雄分笼饲喂,自由采食饲料、饮水。试验前临床健康观察7 d,以适应试验环境。
供试药品:乙酰氨基阿维菌素原位凝胶注射剂,中国农业科学院兰州畜牧与兽药研究所农业部兽用药物创制重点实验室制备,批号:171016。试验前,精密称定处方中主藥及辅料,配制成0.05 g/mL的原位凝胶注射剂,待用。按照处方中各辅料的用料配比,配制辅料对照组(不含主药乙酰氨基阿维菌素)。
1.2 试验方法
1.2.1 预试验 采用递加法分别进行乙酰氨基阿维菌素原位凝胶注射剂组预试验以及辅料对照组预试验。
乙酰氨基阿维菌素原位凝胶注射剂预试验:将20只昆明系小鼠平均分为5组,每组4只,雌雄各半,分别给小鼠称重,计算给药剂量。最高剂量组为10.0 g/kg,最低剂量组为1.0 g/kg。皮下注射,观察7 d,记录小鼠的死亡数,得到最小致死剂量(LD100)(记为b)和最大耐受剂量(LD0)(记为a)。确定组数N以及各组间剂量比r。
N由预试验的最小致死剂量(LD100)b与最大耐受剂量(LD0)a的比值来确定。
r=lg-1[(lgb-lga)/(N-1)]
辅料对照组预试验方法同上。
1.2.2 正式试验 由预试验结果可知,辅料预试验的LD100大于5.0 g/kg,将小鼠样本量增至10只,雌雄各半,仍未出现死亡现象,按照化学药物毒性分级属于实际无毒,因此得到结论,该注射剂辅料实际无毒。根据乙酰氨基阿维菌素原位凝胶注射剂预试验得到的最小致死剂量(LD100)和最大耐受剂量(LD0),采用简化寇氏法[7]计算正式试验组数N以及各组间剂量比r。
根据乙酰氨基阿维菌素原位凝胶注射剂预试验结果将正式试验分为6组,其中包括空白对照组1组以及不同剂量给药组5组。将60只昆明系小鼠随机分为6组,每组雌雄各半。试验组的给药剂量分别为10.000、6.750、4.500、3.000、2.000 g/kg,空白对照组给予等量的饮用水。皮下注射给药,观察7 d,自由饮水,采食,观察小鼠的外观体征、饮食欲、行为活动、大小便等相关症状。给药后4 h,持续观察;4~8 h内每30 min观察一次;8~12 h,每1 h观察一次;12~48 h,每3 h观察一次;3 d后每天观察3次,直至第7天结束。记录每组小鼠死亡只数,对死亡动物进行剖检,与空白组对照,观察各组织器官的病理变化。用简化寇氏法计算LD50及95%的置信区间。
2 结果与分析
2.1 预试验结果
辅料预试验组的LD100大于5.0 g/kg,增加试验动物数量至10只,仍未出现死亡现象,按照化学药物的毒性分级可以视为实际无毒。
乙酰氨基阿维菌素原位凝胶注射剂试验组预试验的LD100为10.0 g/kg,LD0为2.0 g/kg。从而确定正式试验的组数N为5。各组之间的剂量比值r=1.5。由此将正式试验分为6组,其中5组为不同剂量给药组,1组为空白对照组。
2.2 正式试验结果
观察给药后动物表现出的症状为:小鼠被毛逆乱、精神沉郁,全身颤栗,眼睛微闭,食欲不振,对外界刺激反应迟钝,个别小鼠出现四肢无力等现象,死亡前出现全身震颤、侧翻现象,持续10~30 min死亡。高剂量组的症状明显,低剂量组症状较轻微。小鼠死亡时间集中在1~3 h,1 d后再无死亡现象,症状逐渐缓解。
对死亡动物剖检,与空白对照组相比,死亡动物的口唇、四肢、尾巴青紫。高剂量组中,肝脏肿大,颜色为深褐色,有针尖状散在出血点分布于肝脏边缘,且高剂量组症状明显。
正式试验小鼠死亡情况见表1。根据简化寇氏法计算LD50以及95%置信限,公式如下:
式中,Xm为最大剂量的对数;i为组距,即相邻两组剂量对数值之差;p为各剂量组死亡率,q为各剂量组存活率;∑p为各剂量组死亡率之和;n为各组动物数;sx50为lgLD50的标准误差。
计算得到LD50为5.903 g/kg,95%置信区间为5.105 3~6.415 0 g/kg。根据化学物急性毒性(LD50)剂量分级可知,乙酰氨基阿维菌素原位凝胶注射剂为实际无毒物质。
3 小结
试验严格遵守《兽药研究技术指导原则汇编》[8]中对药物急性毒性试验的相关规定。试验选用SPF级昆明系小鼠为试验动物,保证试验动物本身清洁无污染,有效消除试验误差。在给药过程中,严格按照皮下注射给药[9]中的操作,以防由于操作方法不当而导致小鼠死亡,影响试验结果的准确性。由试验结果可知,小鼠给予乙酰氨基阿维菌素原位凝胶注射剂后,出现精神倦怠、食欲减退、生长迟缓等现象,根据小鼠的死亡数计算乙酰氨基阿维菌素原位凝胶注射剂的半数致死剂量(LD50)为5.903 g/kg,95%置信区间为5.105 3~6.415 0 g/kg。由化学物毒性分级可知,乙酰氨基阿维菌素原位凝胶注射剂为实际无毒物质。乙酰氨基阿维菌素作为一种高效、广谱、低残留的兽用新一代抗寄生虫药物[10],本研究对其新制剂乙酰氨基阿维菌素原位凝胶注射剂的安全性进行了评价,以期为该制剂的后续研究及临床推广应用奠定基础。
参考文献:
[1] 杨二爽,李小莲,沈 雁,等.高效液相色谱法测定乙酰氨基阿维菌素的含量[J].黑龙江畜牧兽医,2017(12):162-164.
[2] 中国兽药典委员会.中华人民共和国兽药典[M].北京:中国农业出版社,2015.
[3] 高三玉,周芷锦,罗成江,等.高效液相色谱法测定牛奶中乙酰氨基阿維菌素的残留量[J].畜牧与饲料科学,2017,38(4):14-16.
[4] 廖党金,汪 明,何万平,等.乙酰氨基阿维菌素浇泼剂对奶牛线虫病的疗效试验[J].中国动物传染病学报,2017,25(4):60-63.
[5] 冒玉娟,陈晓兰,赵 丽.乙酰氨基阿维菌素在动物医学中的研究进展[J].畜牧与饲料科学,2013,34(7):86-89.
[6] 于 童.乙酰氨基阿维菌素在牦牛体内的药物动力学、残留消除规律及药效学研究[D].北京:中国农业大学,2015.
[7] 张吉丽,司鸿飞,李 冰,等.大鼠口服五氯柳胺混悬剂的急性毒性研究[J].湖北农业科学,2016,55(20):5313-5315.
[8] 农业部兽药评审中心.兽药研究技术指导原则汇编[M].北京:化学工业出版社,2012.
[9] 郑 婷.乙酰氨基阿维菌素/PLGA缓释微球的研究[D].石家庄:河北科技大学,2012.
[10] 次素英,马丽娟,何双燕.RP-HPLC测定乙酰氨基阿维菌素的含量[J].药物分析杂志,2010(6):1129-1131.

