AngioJet机械性血栓抽吸装置在急性下肢动脉缺血中的应用
周 密 王超楠 陈 雷 李明轩 单海丰 李章木 邓洪儒
首都医科大学附属复兴医院血管外科,北京 100038
急性下肢缺血是临床常见疾病,具有发病突然、致残率高的特点,如不及时诊断和迅速有效处理,可造成肢体坏死引起截肢甚至死亡的不良后果。常见引起急性下肢缺血的原因主要包括下肢动脉栓塞和急性下肢动脉血栓形成。下肢动脉栓塞往往常见于房颤及主动脉附壁血栓[1-2],而急性下肢动脉血栓形成患者常既往有明确的间歇性跛行或者静息痛病史。以前多采用Fogarty导管取栓或者置入溶栓导管药物溶栓,效果尚可,但是前者在下肢动脉血栓形成患者中往往插管困难,而后者针对威胁肢体的急性缺血又不能起到即刻的效果。机械性血栓抽吸(percutaneous mechanical thrombectomy, PMT)[3]具有微创、减容充分、围手术期死亡率低等优点,笔者采用AngioJet血栓抽吸装置进行充分的血栓减容,联合球囊扩张和支架植入取得了非常理想的效果,现将结果汇报如下。
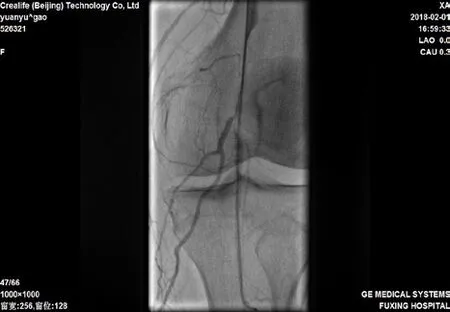
图1 腘动脉栓塞
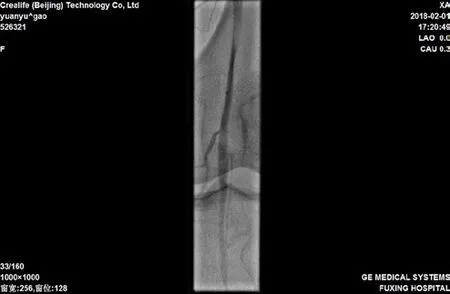
图2 腘动脉单纯吸栓术后
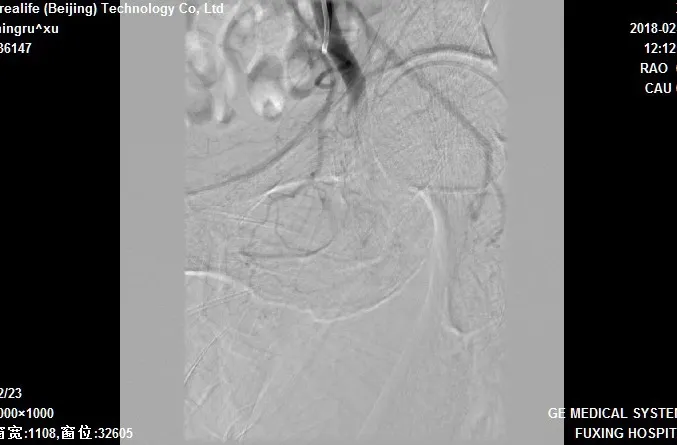
图3 股动脉栓塞
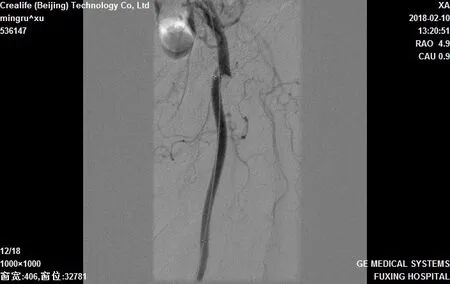
图4 股动脉吸栓+球囊扩张支架植入
1 资料与方法
1.1 一般资料
回顾性分析2017年2月至2018年1月因急性下肢缺血于本院住院治疗的患者共36例,共包括患肢37条,其中男性25例,女性11例,年龄41~93岁,发病时间约2~18 h,中位发病时间6.5 h,其中有27例合并有持续性心房纤颤,急性肢体缺血分级(美国血管外科协会SVS/国际心血管外科学会ISCVS)[4-5]Ⅰ级2例,Ⅱa级25例,Ⅱb级9例;其中缺血平面在股总及以上水平者6例,股浅动脉(合并股深动脉2例)19例,腘动脉水平8例,膝下动脉水平3例。采用AngioJet单纯吸栓12例,合并球囊扩张者18例,见图1,图2,支架植入6例,见图3,图4。
1.2 手术方法
采用1%利多卡因行健侧腹股沟局部浸润麻醉,其中1例因双侧股动脉搏动未触及(考虑髂动脉闭塞)采用左侧肘窝局部麻醉,麻醉满意后行股动脉穿刺置管(采用改良Seldinger技术),将5 F猪尾导管留置于腹主动脉远端造影,用于了解患者双侧髂动脉、股动脉的血流情况以及有无动脉瘤和主动脉夹层,交换JR4导管,泥鳅导丝超选入患侧股总动脉内,导管跟进后行患侧下肢动脉分段造影,评估患侧股浅动脉、股深动腘动脉及膝下动脉的血流情况,明确病变后交换加硬导丝,更换6 F 55 cm动脉长鞘,路图模式下,利用0.018 in(1 in=0.0254 m)导丝(ASAHI Treasure 12)及支持导管(EV3 TrailBlazer)缓慢通过病变部位至远端血管,导管跟进后造影确认位于血管真腔后,采用AngioJet血栓清除装置(0.035系统35例,0.014系统1例)进行血栓清除:将血栓抽吸导管与机器连接,导管尾端与肝素盐水相连(0.9% Nacl溶液+普通肝素6250 U),导管头端浸于含肝素0.9%Nacl溶液中运行15 s,排空导管内气体;机器调整为抽吸模式,将导管缓慢送入血栓近心端,导管由近心端至远心端(2 mm/s)行血栓抽吸,抽吸时间原则上应小于260 s,对于完全闭塞病变可延长到480 s,术中吸栓平均时间160 s。吸栓完成后常规造影进行血管评估,造影确认残余狭窄大于30%或者有限制血流的夹层存在时继续行球囊扩张及支架植入术。病变部位完成血管再通后要求完成膝下动脉造影评估有无远端异位栓塞,膝下动脉如出现异位栓塞采用普通6 F导管抽吸,同时配合球囊扩张成形。术后严格按照体重给与患者低分子肝素抗凝7 d,配合应用前列地尔,罂粟碱扩血管,改善循环,每天复查血常规、尿常规、生化、凝血功能、血栓弹力图,房颤患者术后逐渐过渡为利伐沙班20 mg,1次/d,或者华法林3 mg,1次/d,根据国际标准化比值(INR)2.0~3.0调整剂量,无房颤患者逐渐过渡为口服阿司匹林100 mg,1次/d,氯吡格雷75 mg 1次/d,3个月后改为口服阿司匹林10 mg,1次/d,长期服用。
1.3 疗效评价及术后随访
介入吸栓成功根据Cooley疗效评分[6]为⑴痊愈:肢体远端脉搏恢复正常,无肌肉皮肤坏死,无感觉运动障碍;⑵良好:肢体远端脉搏恢复,较对侧弱,症状消失;⑶一般:肢体远端血运部分恢复,能够代偿;⑷较差:肢体远端动脉未通,通过侧支代偿,仍有缺血症状;⑸截肢和死亡。
2 结果
36例患者中有32例造影可见血流中断,出现“截断征”,4例造影可见不规则充盈缺损,形态可见长条状及团块状。AngioJet血栓抽吸技术成功率为94.4%(34/36),部分患者直接采用吸栓模式,未使用喷药模式,术中平均肝素盐水用量200 ml,手术时间0.5~2.5 h,中位手术时间1.5 h,术中出血20~150 ml,中位失血量60 ml,吸栓后即刻TIMI分级0级3例(8.3%),1级6例(16.7%),2级27例(75%),3级0例(0.0%),吸栓术后行球囊扩张成形术者18例,支架植入者6例,吸栓术后出现远端动脉栓塞者3例,其中2例行球囊扩张成形将血栓贴壁旷置,所有患者术后即刻症状缓解明显,术后28例出现明显血红蛋白尿,为一过性,经充分水化后血尿消失,血尿持续中位时间约17.5 h,血红蛋白平均下降(1.1±0.2)g/L,6例出现一过性肌酐尿素氮升高。
患者平均住院(7.5±1.8)d,临床成功率为100%,根据Cooley疗效评分痊愈9例(25%),良好22例(61%),一般5例(14%),无截肢及死亡患者。32例患者于出院后1个月、3个月规律门诊随诊,4例失访,随诊患者均行下肢动脉彩超进行血流通畅度评估,根据Cooley疗效评分,其中痊愈6例(18.8%),良好21例(63.6%),一般5例(14%),无下肢溃疡、静息痛、截肢及死亡患者。术后患肢ABI较术前提高(0.5±0.06),术后患肢同健侧肢体ABI差小于0.1。
3 讨论
急性下肢动脉缺血发病急、进展快,如诊断处理不当可迅速造成下肢肌肉神经坏死,继发感染可造成截肢,甚至感染中毒性休克导致死亡的不良后果,随着社会老龄化的发展,心脑血管疾病呈现发病率高、发病人群年龄逐渐降低的特点,该病的发病症状有明显特点,绝大多数患者均有不同程度的“6 P”症状(疼痛、苍白、无脉、感觉异常、运动障碍和皮温改变),感觉的异常和运动障碍常常提示已经出现植物神经和运动的缺血、濒临坏死,患者常常表现为触觉的减退和垂足,一旦诊断应尽早行手术治疗。尽快恢复缺血患肢的血运是治疗该病的关键。
急性下肢缺血的常见病因主要是下肢动脉栓塞和下肢动脉狭窄基础上的继发血栓形成,两者在鉴别诊断上相对容易,但是在部分患者往往出现病症重叠和鉴别困难的情况,下肢动脉栓塞患者大多既往没有下肢酸胀不适,间歇性跛行、静息痛等症状,往往合并有心房纤颤、风湿性心脏病,主动脉附壁血栓,栓子多为陈旧性血栓脱落[7-8],而栓子脱落造成的下肢动脉急性缺血又会造成继发的近端动脉血栓形成。而下肢动脉狭窄基础上的继发血栓形成往往患者有下肢间歇性跛行甚至静息痛等病史,病变部位以髂动脉、股浅动脉为主,往往继发近端和远端的血栓形成,部分患者双侧髂动脉闭塞基础上会继发肾下腹主动脉远端的血栓形成(Leriche综合症),既往针对下肢动脉急性缺血的治疗,以开放手术行股动脉切开取栓为主,但是部分动脉狭窄患者往往存在取栓导管插入困难,无法直视下插管,容易进入侧支造成侧支动脉出血及动脉内膜损伤,甚至有部分患者因动脉严重狭窄,在取栓过程中可能出现动脉破裂的后果,因此往往需要在Forgarty导管取栓后继续植入溶栓导管行尿激酶等药物溶栓(catheterdirected thrombolysis, CDT),CDT作为腔内治疗的一种有效方法[9],可以有效的减轻血栓负荷,可以同时溶解主干动脉及膝下动脉的血栓,有效的解决了膝下动脉插管困难和取栓困难的问题,在临床上得到了广泛应用,取得了良好的效果,但是CDT在主干动脉血流通畅,膝下动脉流出道好,术前和取栓术后SVS/ISCVS分级在I级、IIa级的患者中取得较好的效果,但是针对插管困难的患者以及严重急性缺血,威胁患肢及生命的患者中常无法实现有效的治疗,这些患者要求尽早开通病变血管,尽快减轻血栓负荷,在临床治疗中无法给与术者溶栓的时间窗,因此在临床应用中存在一定的限制和约束,特别是当患者存在溶栓禁忌(凝血功能异常、血液病、新发脑梗、胃溃疡、胃出血等)时,溶栓风险高,溶栓过程中造成出血等并发症的可能性极大,同时长期卧床也增加了患者住院时间及经济负担。
AngioJet血栓抽吸系统最初首先被应用于进行心肌梗死患者中冠状动脉血栓的抽吸[10],后来逐渐在外周急性缺血中得到了应用,它的特点是微创、高效地清除血栓(减少血栓负荷)、迅速恢复患肢血流、同时应用于动脉疾病及静脉疾病[11],在急性下肢动脉缺血、下肢动脉支架内再狭窄、人工血管血栓形成、透析用动静脉瘘血栓形成、肠系膜动脉/肾动脉血栓形成及肺动脉栓塞的吸栓治疗中取得了非常理想的治疗效果。
AngioJet血栓抽吸系统的工作原理是通过高速水流将血管内的血栓击碎,同时经过导管尖端的双腔设计将血流重新吸除,从而在导管尖端局部形成负压区域,利用压力的变化(伯努利原理)将水流及击碎的血栓残块通过导管内腔吸出体外。AngioJet有两种模式,在动静脉吸栓过程中可以首先采用喷药模式,将溶栓药物(尿激酶等)注入靶血管内,在局部血管内形成高浓度的溶栓区域,充分将溶栓药物与血栓接触[12],达到更好的溶栓效果以及软化血栓的目的,同时减少了溶栓药物的用量,从而大大的减少了溶栓时间和溶栓过程中的出血风险,国内对于AngioJet在急性下肢动脉缺血中的应用报道相对较少,笔者在使用该系统的过程中也及时总结了一些体会。
AngioJet血栓抽吸系统在使用过程前应严格按照操作规范进行预处理,将导管内空气排空,防止空气进入血管造成气栓,同时可以在预处理的过程中发现导管有无漏液,压力有无报警等导管相关质量问题,在髂动脉、股总动脉、股浅动脉、腘动脉的吸栓时常规选用0.035 6F AngioJet Solent Omni导管,膝下动脉采用0.014 4F AngioJet Solent Omni导管,国外已经上市0.035 8F AngioJet Solent Omni导管有相关报道其在静脉吸栓中有更好的效果。同时要求在术前尽可能完善下肢动脉CTA检查,根据原始断层CT图像诊断下肢动脉血栓的性质进行初步的判断,同时结合患者病史以及术中导管导丝通过时的困难程度对及行下肢缺血的病因进行鉴别。在下肢动脉栓塞的患者中,笔者的经验是不需要首先采用喷药模式,而是直接采用抽吸模式,因为栓塞后近端形成的血栓往往比较松软,单纯抽吸模式完全可以达到充分减容的效果,而对于下肢动脉狭窄后血栓形成的患者,往往是新鲜血栓合并有陈旧血栓,首先采用喷药模式不仅可以更快的溶解血栓,而且可以将陈旧血栓部分溶解,尽可能的减轻血栓负荷,暴露原发病变。在喷药-抽吸模式的应用患者中,尿激酶的用量较传统CDT明显减少[4],平均尿激酶用量为(21.5±5.8)万U,大大提高了溶栓效率。但是即使在喷药-吸栓模式的应用患者中也存在血栓无法完全吸除的问题,原因有如下两点,其一是针对陈旧血栓和质韧斑块,该系统所依靠的负压抽吸无法有效吸除,其二是绝大多数患者的病变血管很长,血栓负荷量较大,而抽吸时间一般限定为260 s(完全闭塞病变可以延长至480 s),过长时间的抽吸可能造成红细胞破坏过多引起贫血和肾小管的损伤,术后患者出现长时间血尿和肾功能不全甚至肾衰竭的情况。因此,在该系统的使用过程中应充分了解病变的性质及病变长度、血栓负荷量,精准的控制吸栓的时间以及单纯抽吸/喷药-抽吸模式的选择,尽可能多的减少血栓负荷同时降低红细胞的破坏。
在AngioJet应用完成后要即刻进行病变血管的评估,在下肢动脉狭窄的病变中常规应用球囊扩张成形,再次评估后如出现残余狭窄大于30%及限制血流的夹层形成可以植入支架进行补救,对于下肢动脉栓塞,该系统对于栓子头端的吸除效果一般,往往需要球囊碎栓,必要时可以植入支架将栓子充分贴壁旷置[13]。AngioJet是利用高速水流碎栓,回吸形成负压从而清除血栓的一套系统,因此在吸栓的过程中不可避免的会造成动脉血栓的前移,异位栓塞会造成远端动脉的继发栓塞和“垃圾脚”的出现,因此在使用过程中强调将导管由近端向远端进行逐步的抽吸,操作轻柔缓慢,也可以采用远端球囊阻断和远端栓子保护装置来预防,但是会明显的增加手术难度和患者的经济负担。如患者首发症状为腘动脉及膝下动脉的急性缺血,可以直接选用0.014 4F AngioJet Solent Omni导管对膝下动脉进行抽吸。在AngioJet抽吸的过程中,由于高速水流的冲击,血管壁受到刺激,患者会产生明显的酸胀感,甚至疼痛,但是绝大多数患者可以耐受。同传统的开放手术一样,AngioJet血栓抽吸系统可以迅速地清除血栓负荷,达到血管再通的目的,但是也面临血管复通后的缺血再灌注损伤问题,如高血钾、血红蛋白尿[14]、肌红蛋白尿、坏死物质吸收、下肢肿胀甚至骨筋膜室综合症,因此术后需要严密的监控患者的电解质水平,肾功能的变化以及下肢的张力以及远端肢体血运的情况。
综上,AngioJet是一种将药物溶栓和机械吸栓相结合的清除下肢动脉血栓的非常有效的系统,大大缩短了住院时间,降低了溶栓风险和溶栓药物用量,总体上降低了住院患者的经济费用,具有微创、高效、简单、并发症少的优点,但是在部分患者中存在血栓抽吸不完全的情况,有一定的局限性,因此需要结合球囊扩张和支架植入进行补救性治疗,同时也存在血栓远端异位栓塞的问题,需要充分了解该系统的特点,选择合适的适应症,同时在操作中轻柔细致,不断积累相关的经验。

