北京市典型重污染过程中PM2.5载带水溶性无机离子污染特征分析
石梦双,韩 斌,杨 文,张 蕊,陈 莉,白志鹏
1.天津师范大学城市与环境科学学院,天津 300387 2.中国环境科学研究院,环境基准与风险评估国家重点实验室,北京 100012
大气颗粒物(也称气溶胶)是指分散在大气中的固态或液态颗粒状物质[1],因富集有毒有害物质及微生物而危害人体健康[2-3];并通过光散射和光吸收等消光效应降低大气能见度[4]。水溶性无机离子(water soluble inorganic ions)是大气PM2.5的重要组成成分[5-6],直接影响大气降水的酸度[7-8]。同时,因其具有吸湿性,能够在低于水的饱和蒸气压下形成雾滴,而影响云凝结核(CCN)的浓度引起间接的辐射强迫作用[9],进而影响全球气候变化[10]。二次无机气溶胶包括SO42-、NO3-、NH4+(SNA)是主要的水溶性离子[11]。
2013年1月,中国北方平原地区多次出现空气重污染过程[12],京津冀地区特别是北京地区在1月遭受了严重的空气污染[13]。对于该时期,JIANG等[12]发现,颗粒物严重超标时存在风速低且湿度大的气象条件;SUN等[14]指出除停滞的气象条件,煤炭燃烧、二次颗粒物的产生、区域传输也是此次重污染事件形成和演变的主要原因;HUANG等[15]研究也表明,二次气溶胶对国内重污染事件频发产生影响。
传统的滤膜采样均为日均浓度分析[16],且多侧重于研究颗粒物水溶性组分的季节变化[17],无法满足针对单日或多日内水溶性无机离子组分变化研究[18]。现采用在线连续采样和分析的方法[19],研究北京市2013年1月大气PM2.5中水溶性离子特性,以揭示该重污染过程的污染特征及其成因,以期为今后该地区空气质量改善提供科学依据。
1 实验部分
1.1 采样时间和地点
2013年1月1—30日对PM2.5开展采样。采样地点位于中国环境科学研究院大气所风洞实验室楼顶(40°02′29″N, 116°24′51″E),距地面高度约6 m。
1.2 样品采集和分析
采用大气细颗粒物水溶性组分在线监测分析仪(URG-9000B,AIM-IC,美国)[19],连续监测PM2.5中的水溶性无机离子SO42-、NO3-、Cl-、K+、Ca2+、Na+、Mg2+、NH4+。采样头为旋风式切割头,去除空气动力学当量直径大于2.5 μm颗粒物。仪器由气溶胶收集装置和水溶性离子分析装置两部分组成。收集装置包括湿式平行板溶蚀器和蒸汽发生器。样品经过溶蚀器后气体(SO2,NH3、HNO3)会被去除。此后颗粒物进入气溶胶过饱和蒸汽发生室,快速吸湿长大形成液滴。长大的颗粒物冷凝后通过惯性分离器分离,经分流存储在样品收集器——注射泵中,注射泵每小时将样品分别注入,进行阴阳离子分析。时间分辨率为1 h,采样流速为3 L/min。
在离子色谱系统,阴离子色谱采用ICS2100(美国),阴离子分离柱采用IonpacAS11(2×250 mm),采取梯度淋洗,流速为0.38 mL/min;阳离子色谱采用ICS1100(美国),阳离子分离柱采用CS12 A(2×250 mm),采取等度淋洗,流速为0.25 mL/min。混合标准溶液由单标配置而成。
离子色谱系统检测的8种离子Cl-、NO3-、SO42-、Na+、NH4+、K+、Mg2+、Ca2+方法检测限分别为0.01、0.05、0.04、0.05、0.05、0.09、0.06、0.10 μg/m3。该仪器在使用前需进行温度、湿度、压力的校准,并做好预检测离子的标准曲线。本实验各离子的标准曲线的相关系数均在0.996以上。
1.3 PM2.5浓度数据获取
PM2.5的小时浓度值从北京市朝阳区气象局获得,采样点距离气象局10 km。采样仪器为GRIMM-365全天候颗粒物分析仪,该仪器采用光散射法测定PM2.5每小时质量浓度。同期气象参数(温度、相对湿度、大气压、风速、风向)小时均值数据均从该气象站点获得。
2 结果与讨论
2.1 重污染期间PM2.5污染特征
2013年1月,京津冀地区发生多次大规模空气重污染事件[20-21]。该月PM2.5小时浓度均值为126.36 μg/m3,最大达到632 μg/m3(1月12日16:00),PM2.5日均最大浓度达到386 μg/m3(1月12日)。根据图1的PM2.5浓度变化时间序列,研究划分了5段重污染时期:P1为1月6—8日,P2为1月10—14日, P3为1月18—19日,P4为1月22—23日,P5为1月26—30日;其中,P2、P5重污染持续时间最长,污染最严重。

图1 PM2.5小时及日均浓度变化序列Fig.1 Hourly and daily average concentration of PM2.5
2.2 水溶性无机离子的浓度与组成
该采样点采样期间,PM2.5样品中各水溶性无机离子的小时浓度变化序列如图2所示。其中数据的间断是由于仪器故障或停电关机造成的缺测,以及因数据质控出现的空缺。以小时计算,采样期间共采集水溶性无机离子的有效样品644组。整个观测期内总水溶性无机离子(TWSI)浓度的小时均值为61.01±63.92 μg/m3,变化范围为6.40~432.83 μg/m3,详见表1。
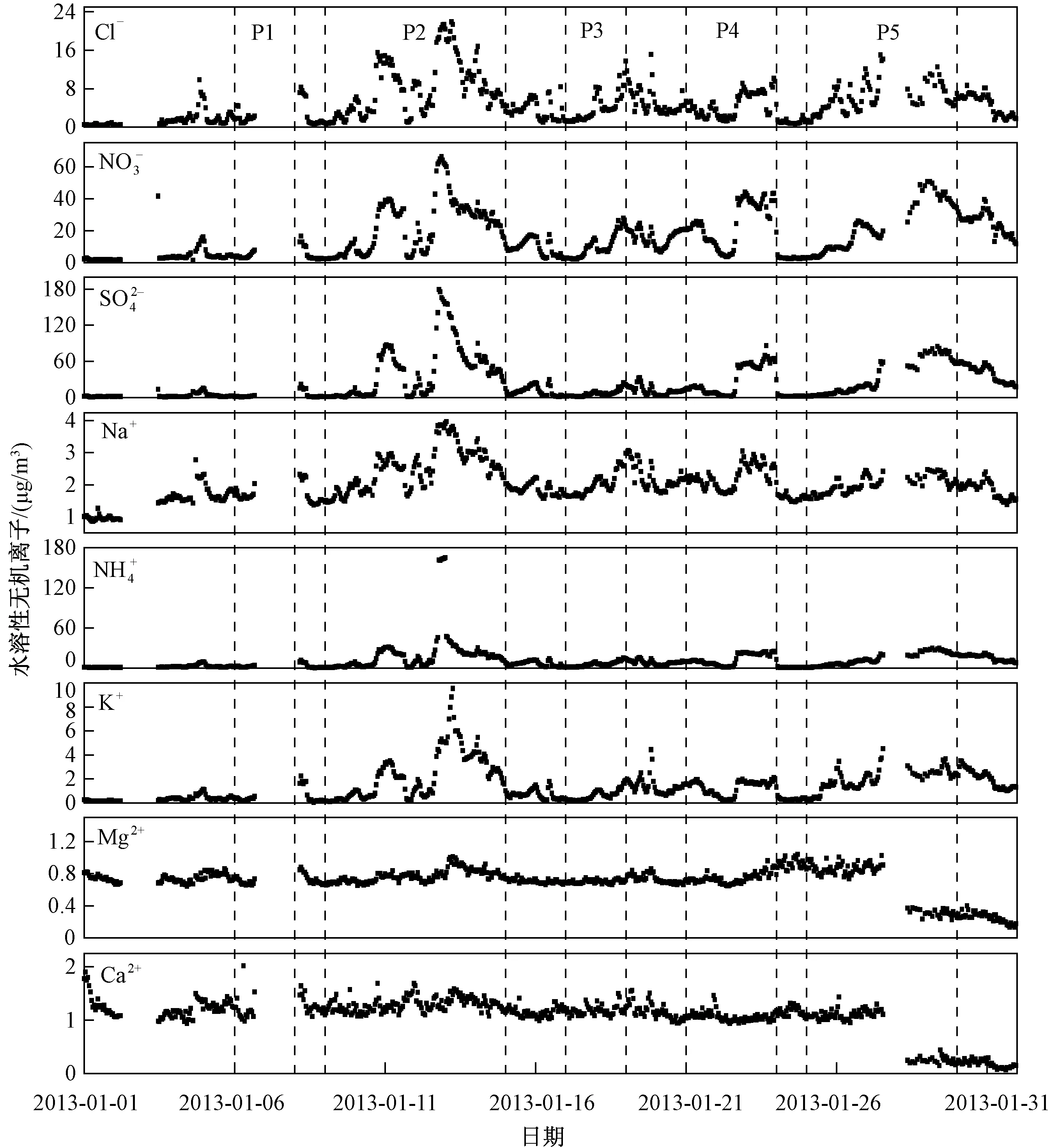
图2 PM2.5中水溶性无机离子的小时浓度变化序列Fig.2 Variation of water-soluble ions hourly concentrations in PM2.5
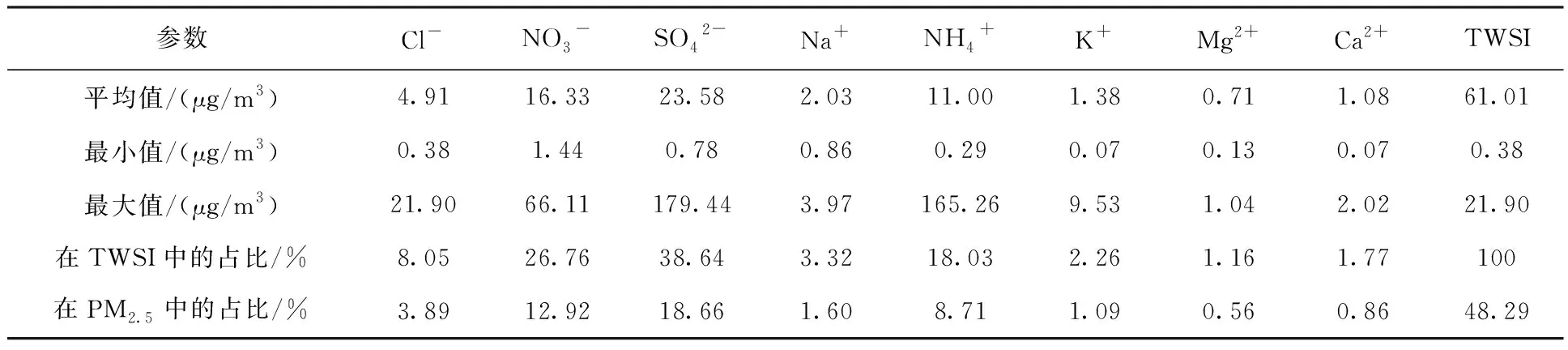
参数Cl-NO3-SO42-Na+NH4+K+Mg2+Ca2+TWSI平均值/(μg/m3)4.9116.3323.582.0311.001.380.711.0861.01最小值/(μg/m3)0.381.440.780.860.290.070.130.070.38最大值/(μg/m3)21.9066.11179.443.97165.269.531.042.0221.90在TWSI中的占比/%8.0526.7638.643.3218.032.261.161.77100在PM2.5中的占比/%3.8912.9218.661.608.711.090.560.8648.29
PM2.5中水溶性无机离子的小时浓度变化序列较好地对应了其中4次PM2.5重污染事件(由于仪器故障造成P1重污染事件对应的离子数据缺失),P2、P3、P4、P5重污染期间,Cl-、NO3-、SO42-、NH4+、K+浓度均有不同程度上升;SO42-浓度波动最为明显,可能由于北京采暖季煤炭的大规模燃烧。
SNA是采样期间大气PM2.5中主要的水溶性无机离子,其小时浓度均值分别为23.6±30.8、16.4±13.9、11.0±17.3 μg/m3,SNA占PM2.5中TWSI的83.4%,在PM2.5中占比为39.98%。对比近年来北京地区冬季细颗粒物中SNA的浓度水平(表2),2013年冬季的SNA浓度水平比其他年份高。与同时期膜采样相比,本研究中SO42-浓度较低,但NH4+浓度居中。这可能是由于采样点设置不同。
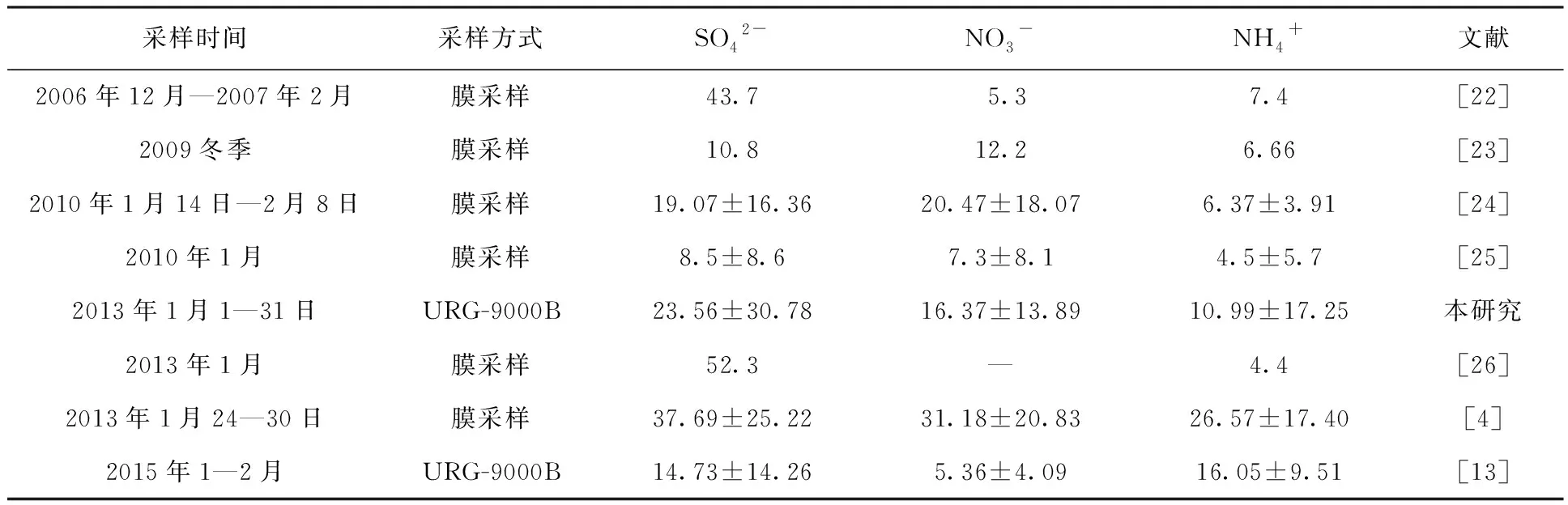
表2 北京冬季不同研究PM2.5中水溶性无机离子浓度对比Table 2 Comparison of water soluble ions concentration of PM2.5 in winter in Beijing μg/m3
注:“—”表示未明确给出数值。
如前所述,Mg2+、Ca2+在PM2.5中的占比分别为0.56%、0.86%,含量较低;Mg2+、Ca2+离子浓度在1月28日前相对稳定,28日后浓度下降。主要原因可能是由于该时期内政府部门对重污染事件频发做出了紧急应对,关停了部分建筑工程建设项目,减少了建筑扬尘,从而减少了Mg2+、Ca2+的排放。
研究期内,重污染天(日均PM2.5质量浓度大于75 μg/m3)和非重污染天PM2.5和SNA浓度的日变化如图3所示。重污染天时,PM2.5在中午12:00达到最低值,在20:00累积达到最大;二次离子SNA在14:00—18:00逐渐累积,在20:00—01:00)达到最高。非重污染天时,PM2.5在16:00—21:00呈明显上升趋势,此后逐渐降低,在次日的04:00浓度达到最低;二次离子在上午08:00—11:00、15:00—21:00时段呈上升趋势。
[NO3-]/[SO42-]可以反映移动源与固定源对大气颗粒物的贡献的相对重要性[27]。当[NO3-]/[SO42-]大于1时,表明冬季交通排放成了主要影响因素[16]。非重污染天[NO3-]/[SO42-]大于重污染天,重污染天的[NO3-]/[SO42-]均小于1。重污染天固定源污染较移动源更为显著。
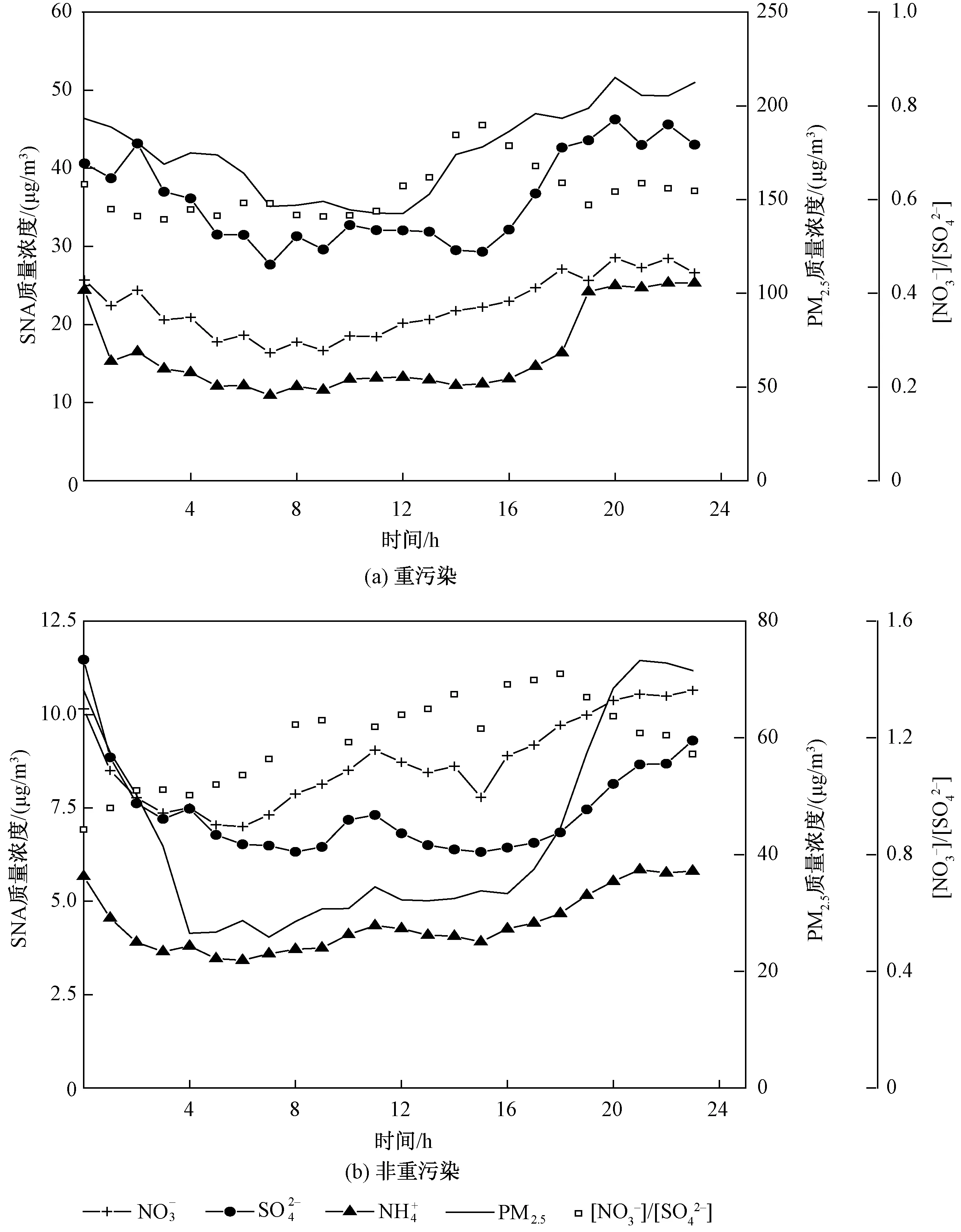
图3 PM2.5和SNA浓度的日变化Fig.3 Diurnal variations of PM2.5 and SNA
2.3 不同空气质量气溶胶特性
2.3.1 气溶胶酸碱度
大气颗粒物酸碱性对降水pH产生重要影响,既可能引起降水酸化,也可能对降水的酸度进行中和[28]。通常可利用大气气溶胶中水溶性离子总阳离子电荷与总阴离子电荷的比值来表示大气气溶胶中离子平衡状况,来评估气溶胶的酸碱度:
(1)
(2)
式(1)~式(2)中:Cl-、NO3-、SO42-、Na+、NH4+、K+、Mg2+、Ca2+分别为颗粒物中各离子的质量浓度,将其换算成电荷当量,即摩尔浓度与离子所带电荷乘积;C代表阳离子电荷当量,A代表阴离子电荷当量,C、A的单位均为μeq/m3。
当C/A>1时,阴离子相对亏损,气溶胶表现为偏碱性;当C/A<1时,阳离子相对亏损,气溶胶表现为偏酸性。空气污染(中度污染至严重污染)时期气溶胶呈酸性,可能由于受到化石燃料燃烧的影响。对于严重污染时期,C/A较重度污染时期有部分回升,但总体呈酸性,表明严重污染时期水溶性无机离子呈复杂特性,见表3。

表3 按空气质量分级后C与A比值Table 3 Ratio of C/A at different PM2.5 range
此外,对不同空气质量级别下的阴阳离子当量浓度进行回归计算,并得到回归方程,见图4。在空气优良情况下,气溶胶中阳离子占主导,气溶胶呈碱性。可能是由于北京地区地处北方,土壤背景值中Ca2+、Mg2+离子含量相对稳定,土壤偏碱性,而地面扬尘是洁净天气时主要的气溶胶来源。随着空气污染加剧,回归方程斜率减小,阴离子逐渐占主导,颗粒物呈酸性。
由图4可以看出,阴阳离子当量浓度拟合性较好(r为0.96~0.99),表明离子受到主导污染源的影响,且未有重要离子在测量中被遗漏。
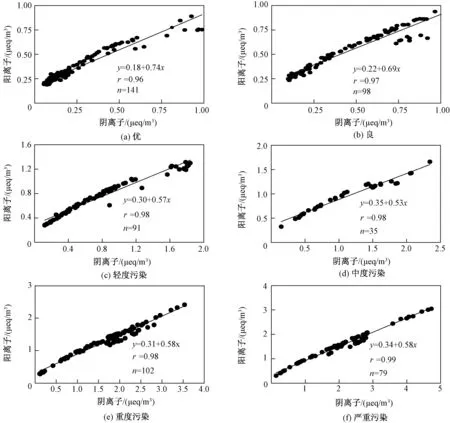
图4 北京城区不同PM2.5污染浓度下的阴阳离子平衡Fig.4 The charge balance at different PM2.5 range in Beijing
2.3.2 SNA三角图分布特征
大气颗粒物中硫酸盐离子的主要来源是排入大气中的SO2进行气液相氧化成硫酸盐,且这些硫酸盐均是水溶性的;硝酸盐主要是由NOx在大气中发生均相反应形成HNO3之后再与NH3气反应而生成的硝酸铵粒子,或与已有的细颗粒物发生反应。NH4NO3不稳定,在高温低湿条件下易分解成气态的硝酸和氨;NH4+是PM2.5中最主要的阳离子,是由NH3在酸性颗粒物表面上反应或凝结而形成的,通常以(NH4)2SO4、NH4HSO4、NH4NO3等形式存在。
研究显示,不同空气质量等级SNA在TWSI浓度中的占比增大,分别为61.51%(优)、72.09%(良)、76.38%(轻度污染)、80.43%(中度污染)、83.50%(重度污染)、84.67%(严重污染)。表明随空气污染加剧,SNA在TWSI中的比重增大。
由于SNA是水溶性无机离子的主要组成成分,本文借鉴以往三角图解的研究[17, 28],选择以上3种离子的物质的量浓度值绘制NH4+-NO3--SO42-的三角图(图5)。大多样品分布在NH4+-NO3--SO42-三角图的左下角,NH4+所占百分比的变化范围为30.33%~77.88%,SO42-所占百分比变化范围为4.72%~33.60%(表4)。
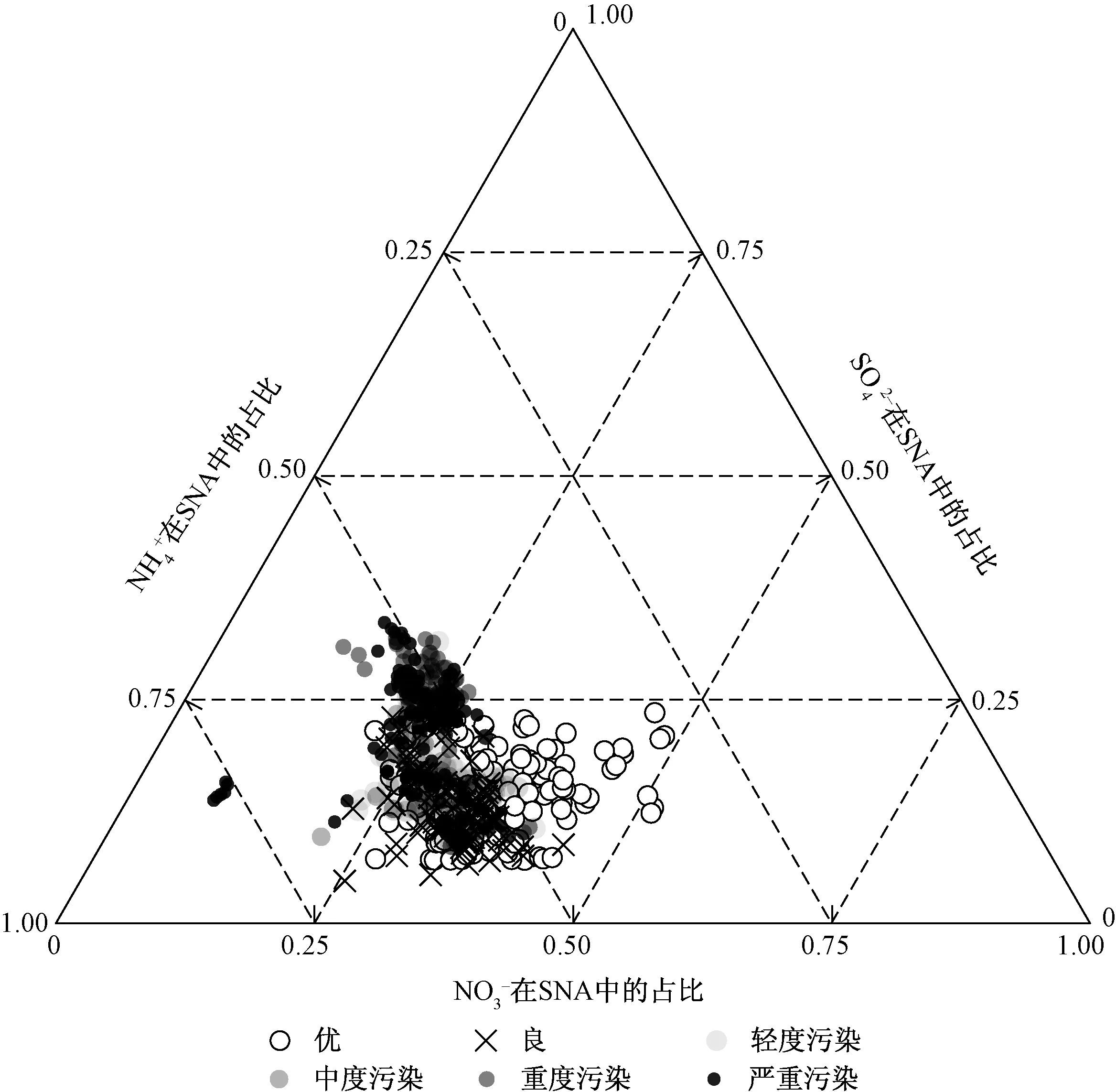
图5 NH4+-NO3--SO42-的三元相图Fig.5 Triangular diagram of NH4+-NO3--SO42-
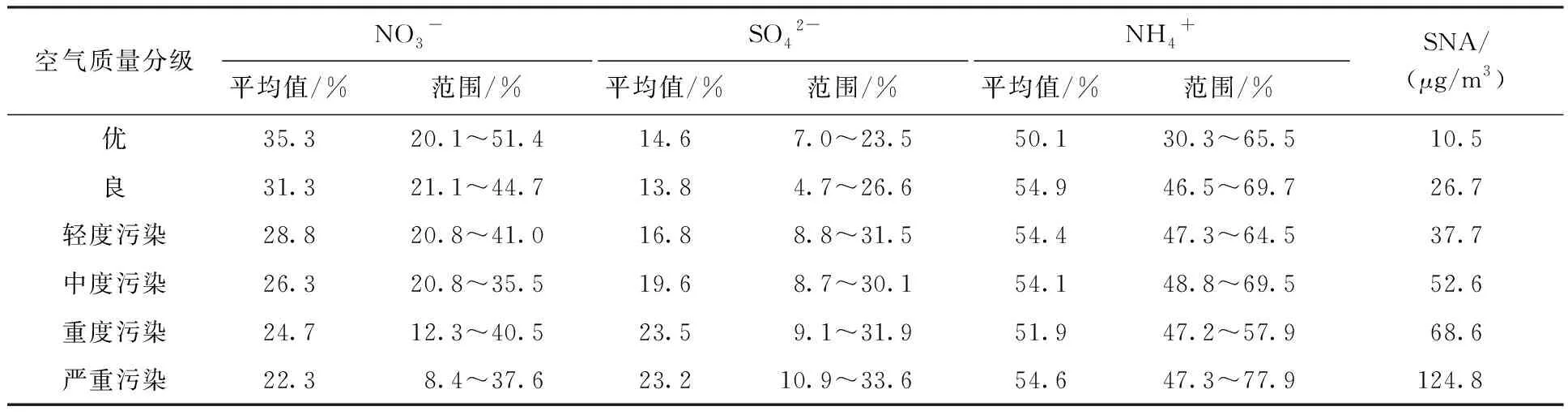
空气质量分级NO3-SO42-NH4+平均值/%范围/%平均值/%范围/%平均值/%范围/%SNA/(μg/m3)优35.320.1^51.414.67.0^23.550.130.3^65.510.5良31.321.1^44.713.84.7^26.654.946.5^69.726.7轻度污染28.820.8^41.016.88.8^31.554.447.3^64.537.7中度污染26.320.8^35.519.68.7^30.154.148.8^69.552.6重度污染24.712.3^40.523.59.1^31.951.947.2^57.968.6严重污染22.38.4^37.623.210.9^33.654.647.3^77.9124.8
可见,随着空气质量恶化,SO42-在SNA中占比增加,与HAN等[19]的研究结果一致。在空气质量为优的情况下,NO3-为主要阴离子(占SNA 35.32%),且主要以NH4NO3的形式存在,较少比例以(NH4)2SO4存在,其余NH4+可能会以碱性NH4+形式存在。在严重污染时期,颗粒物呈酸性,颗粒物中SO42-的物质的量占比(占SNA 23.16%)略高于NO3-(占SNA 22.29%),在SO42--NO3--NH4+-H2O无机气溶胶体系中,SO42-与NO3-争夺与NH3结合的机会;由于NH3倾向于与SO42-结合,因此当SO42-浓度高时,NO3-在气态与颗粒态之间的分配有利于以气态存在,因此主要以(NH4)2SO4形式存在,其次以NH4NO3的形式存在,其余NH4+以NH4Cl的形式存在。
3 结论
通过在线监测重污染时段PM2.5及水溶性无机离子组分浓度,了解重污染时段PM2.5及水溶性无机离子的污染特征,研究了不同空气质量分级下气溶胶的酸碱度和水溶性无机离子可能的存在形式,得出以下结论:
1) 2013年1月可分为五段重污染时期,其中P2(1月10—14日),污染持续时间最长,污染最为严重。1月12日16:00 PM2.5小时浓度均值最大,达到632 μg/m3。
2) 观测期内8种水溶性离子总质量浓度为61.01 μg/m3,其中SNA为主要成分,占所测TWSI的 83.43%,占PM2.5质量浓度的39.98%。重污染天[NO3-]/[SO42-]日变化均小于1,表明重污染天固定源污染较移动源更为显著。
3) 随着空气污染加剧,SNA在TWSI中的比重增大。在空气质量为优的情况下,采样点气溶胶呈碱性;水溶性离子主要以NH4NO3的形式存在,较少比例以(NH4)2SO4存在。随着PM2.5污染加重,该采样点的气溶胶逐渐呈酸性,严重污染时,主要以(NH4)2SO4形式存在,其次以NH4NO3的形式存在,多余的NH4+以NH4Cl的形式存在。
参考文献(References):
[1] 胡敏. 北京大气细粒子和超细粒子理化特征、来源及形成机制[M]. 北京:科学出版社, 2009.
[2] CHEN R, CHU C, TAN J, et al. Ambient Air Pollution and Hospital Admission in Shanghai, China[J]. Journal of Hazardous Materials, 2010, 181(1/3): 234-240.
[3] World Bank Washington D C. Cost of Pollution in China: Economic Estimates of Physical Damages[M]. Washington D C: World bank, 2007.
[4] 刘庆阳,刘艳菊,杨峥,等. 北京城郊冬季一次大气重污染过程颗粒物的污染特征[J]. 环境科学学报, 2014(1): 12-18.
LIU Qingyang, LIU Yanju, YANG Zheng, et al. Daily Variations of Chemical Properties in Airborne Particulate Matter During a High Pollution Winter Episode in Beijing[J]. Acta Scientiae Circumstantiae,2014(1): 12-18.
[5] WANG Y, ZHUANG G, TANG A, et al. The Ion Chemistry and the Source of PM2.5Aerosol in Beijing[J]. Atmospheric Environment, 2005, 39(21): 3 771-3 784.
[6] 孟琛琛,王丽涛,张芬芬,等. 邯郸市PM2.5中水溶性无机离子污染特征及来源解析[J]. 环境科学学报. 2015, 35(11): 3 443-3 451.
MENG Chenchen, WANG Litao, ZHANG Fenfen, et al.Pollution Characteristics and Source Apportionment of Water Soluble Inorganic Ions in PM2.5in Handan City[J]. Acta Scientiae Circumstantiae, 2015, 35(11): 3 443-3 451.
[7] HE K, ZHAO Q, MA Y, et al. Spatial and Seasonal Variability of PM2.5Acidity at two Chinese Megacities: Insights Into the Formation of Secondary Inorganic Aerosols[J]. Atmospheric Chemistry and Physics, 2012, 12(3): 1 377-1 395.
[8] XUE J, LAU A K H, YU J Z. A Study of Acidity on PM2.5in Hong Kong Using Online Ionic Chemical Composition Measurements[J]. Atmospheric Environment, 2011, 45(39): 7 081-7 088.
[9] 贺克斌,杨复沫,段凤魁,等. 大气颗粒物与区域复合污染[M]. 北京:科学出版社, 2011.
[10] RAMANATHAN V. Aerosols, Climate, and the Hydrological Cycle[J]. Science, 2001, 294(5549): 2 119-2 124.
[11] HU G, ZHANG Y, SUN J, et al. Variability, Formation and Acidity of Water-Soluble Ions in PM2.5in Beijing Based on the Semi-Continuous Observations[J]. Atmospheric Research, 2014, 145/146: 1-11.
[12] JIANG J, ZHOU W, ZHEN C, et al. Particulate Matter Distributions in China During a Winter Period with Frequent Pollution Episodes (January 2013)[J]. Aerosol and Air Quality Research, 2015.
[13] 程念亮,李云婷,张大伟,等. 2013年1月北京市一次空气重污染成因分析[J]. 环境科学, 2015(4): 1 154-1 163.
CHENG Nianliang, LI Yunting, ZHANG Dawei, et al. Formation Mechanism of a Serious Pollution Event in January 2013 in Beijing[J]. Acta Scientiae Circumstantiae,2015(4): 1 154-1 163.
[14] SUN Y, JIANG Q, WANG Z, et al. Investigation of the Sources and Evolution Processes of Severe Haze Pollution in Beijing in January 2013[J]. Journal of Geophysical Research: Atmospheres, 2014, 119(7): 4 380-4 398.
[15] HUANG R, ZHANG Y, BOZZETTI C, et al. High Secondary Aerosol Contribution to Particulate Pollution During Haze Events in China[J]. Nature, 2014.
[16] 古金霞,吴丽萍,霍光耀,等. 天津市PM2.5中水溶性无机离子污染特征及来源分析[J]. 中国环境监测, 2013, 29(3): 30-34.
GU Jinxia, WU Liping, HUO Guangyao, et al. Pollution Character and Source of Water-Soluble Inorganic Ions in PM2.5over Tianjin[J]. Environmental Monitoring in China, 2013, 29(3): 30-34.
[17] 张棕巍,胡恭任,于瑞莲,等. 厦门市大气 PM2.5中水溶性离子污染特征及来源解析[J]. 中国环境科学, 2016, 36(7): 1 947-1 954.
ZHANG Zongwei, HU Gongren, YU Ruilian, et al. Characteristics and Sources Apportionment of Water-Soluble Ions in PM2.5of Xiamen City, China[J]. China Environmental Science, 2016, 36(7): 1 947-1 954.
[18] 寿幼平,高晓梅,王静,等. 济南秋季大气PM2.5中水溶性离子的在线观测[J]. 环境科学研究, 2010(1): 41-47.
SHOU Youping, GAO Xiaomei, WANG Jing, et al.Online Measurement of Water-Soluble Ions in Fine Particles from The Atmosphere in Autumn in Jinan[J]. Research of Environmental Science, 2010(1): 41-47.
[19] HAN B, ZHANG R, YANG W, et al. Heavy Haze Episodes in Beijing During January 2013: Inorganic Ion Chemistry and Source Analysis Using Highly Time-Resolved Measurements from an Urban Site[J]. Science of The Total Environment, 2016, 544: 319-329.
[20] HUANG K, ZHUANG G, WANG Q, et al. Extreme Haze Pollution in Beijing During January 2013: Chemical Characteristics, Formation Mechanism and Role of Fog Processing[J]. Atmospheric Chemistry and Physics Discussions, 2014, 14(6): 7 517-7 556.
[21] JI D, LI L, WANG Y, et al. The Heaviest Particulate Air-Pollution Episodes Occurred in Northern China in January, 2013: Insights Gained from Observation[J]. Atmospheric Environment, 2014, 92: 546-556.
[22] LI X, WANG Y, GUO X, et al. Seasonal Variation and Source Apportionment of Organic and Inorganic Compounds in PM2.5and PM10Particulates in Beijing, China[J]. Journal of Environmental Sciences, 2013, 25(4): 741-750.
[23] LIU Y, ZHANG T, LIU Q, et al. Seasonal Variation of Physical and Chemical Properties in TSP, PM10and PM2.5at a Roadside Site in Beijing and Their Influence on Atmospheric Visibility[J]. Aerosol and Air Quality Research, 2014, 14:954-969.
[24] ZHAO P S, DONG F, HE D, et al. Characteristics of Concentrations and Chemical Compositions for PM2.5in the Region of Beijing, Tianjin, and Hebei, China[J]. Atmospheric Chemistry and Physics, 2013, 13(9): 4 631-4 644.
[25] ZHANG R, JING J, TAO J, et al. Chemical Characterization and Source Apportionment of PM2.5in Beijing: Seasonal Perspective[J]. Atmospheric Chemistry and Physics, 2013, 13(14): 7 053-7 074.
[26] 杨懂艳,刘保献,张大伟,等. 2012—2013年间北京市PM2.5中水溶性离子时空分布规律及相关性分析[J]. 环境科学, 2015(3): 768-773.
YANG Dongyan, LIU Baoxian, ZHANG Dawei, et al. Correlation, Seasonal and Temporal Variation of Water-Soluble Ions of PM2.5in Beijing During 2012-2013[J]. 2015(3): 768-773.
[27] WATSON J G, CHOW J C, LURMANN F W, et al. Ammonium Nitrate, Nitric Acid, and Ammonia Equilibrium in Wintertime Phoenix, Arizona[J]. Journal of the Air & Waste Management Association, 1994, 44(4): 405-412.
[28] SHON Z, KIM K, SONG S, et al. Relationship Between Water-Soluble Ions in PM2.5and their Precursor Gases in Seoul Megacity[J]. Atmospheric Environment, 2012, 59: 540-550.

