氯化两面针碱肠吸收研究
赵 森姜 黎慕杨娜 邹 明*
(1大连大学附属中山医院药剂科,辽宁 大连 116001;2辽宁中医药大学附属第二医院伦理教研室,辽宁 沈阳 110032)
两面针药味辛、苦、微温,小毒,具有祛风通络、胜湿止痛、消肿解毒等作用。主要成分为生物碱,氯化两面针碱为两面针的主要成分,测定不同含量的两面针提取物在大鼠小肠的吸收情况,采用紫外分光光度法测定肠循环液中酚红的含量,标定体积,采用高效液相色谱法测定氯化两面针碱的含量。目前对两面针的药动学研究较少,本实验在体法预测氯化两面针碱的吸收情况。
1 材料与方法
1.1 仪器与试药 LC6A高效液相色谱仪 (日本岛津);Agilent色谱工作站 (美国);HH-S11-Z型电恒温水浴锅(北京长安科学仪器厂);电子天平 (Sartorius,德国);SHB-3循环水多用真空泵 (郑州杜甫仪器厂);T101-100型蠕动泵 (保定兰格恒流泵有限公司);氯化两面针碱对照品 (上海纯优科技有限公司,批号:6872-57-7);酚红 (上海试剂三厂);乌拉坦溶液 (自制);Kerbs-Ringer营养液 (以下简称K-R营养液,自制)[1]。
1.2 实验动物 雌雄Wistar大鼠40只,雌雄各半 (大连医科大学实验动物中心);合格证号SCXK(辽)2008-0002]。
1.3 样品溶液的测定方法
1.3.1 在体吸收的实验原理 被动扩散是消化吸收的最重要途径,用Fink方程式可以描述这一过程,方程变换后inX=inX0-式中的X0为初始药物量;X为吸收后药物量;t为吸收时间;以时间t对inX作图应为一条直线,斜率Kα为药物在小肠吸收的速率。
1.3.2 循环液中酚红的测定方法
1.3.2.1 空白循环液 (以下简称K-R营养液) 称取氯化钠7.8 g,氯化钾0.35 g,氯化钙0.37 g,氯化镁0.02 g,碳酸氢钠1.37 g,磷酸二氢钠0.32 g,葡萄糖1.4 g,加纯化水溶解定容至1000 mL容量瓶中,即得。
1.3.2.2 酚红测定波长的选择 酚红KR营养液、对照品储备液、对照品酚红KR营养液,于700~200 nm范围扫描,结果在558 nm处KR营养液、氯化两面针碱对酚红无干扰。
1.3.2.3 酚红测定方法 按照大鼠小肠吸收实验方法,在肠循环液中加入定量的酚红。
精密配制浓度为10 μg/mL、25 μg/mL、 50 μg/mL酚红K-R营养液,置洁净试管中,加入0.2 mol/L的NaOH溶液5 mL,摇匀,按紫外-可见分光光度法在558 nm波长处测定吸光度。
1.3.2.4 酚红标准曲线制备 精密量取酚红储备液适量,稀 释 成 浓 度 为 5.0 μg/mL、 10.0 μg/mL、 25.0 μg/mL、50.0 μg/mL、 100.0 μg/mL酚红溶液, 按酚红测定方法操作,测定吸光度。得标准曲线方程:A=0.0172C+0.0212, r=0.9999。 (n=6) 酚红在5 μg~100 μg/mL范围内,线性关系良好。
1.3.2.5 精密度考察 取低、中、高三种浓度的酚红储备液,按酚红测定方法操作,测定吸光度,RSD=0.3%,结果表明,精密度良好。
1.3.2.6 稳定性考察 分别于0、2、4、6、8 h取样,按酚红测定方法操作,测定吸光度,RSD=0.3%,结果表明,稳定性良好。
1.3.2.7 重复性考察 取同一样品5份,按酚红测定方法操作,测定吸光度,RSD=0.4%,结果表明,重复性良好。
1.3.2.8 加样回收率考察 取酚红适量 (含酚红1 mg、2.5 mg、5 mg),分别置具塞锥形瓶中,分别加入浓度为10 μg/mL、 25 μg/mL、 50 μg/mL的酚红溶液50 mL。平均RSD为1.1%,结果表明,方法回收率良好。
1.3.3 循环液中氯化两面针碱HPLC测定方法
1.3.3.1 色谱条件 Diamonsil XDB-C18(150×4.6 mm,5.0 μm); 磷酸盐缓冲液-乙腈 (55∶45), pH=3.5; 流速:1.0 mL·min-1;检测波长:328 nm;柱温:室温;进样量: 10 μL。
1.3.3.2 干扰项考察 以上述色谱条件,取K-R营养液、氯化两面针碱K-R营养液、酚红溶液各10 μL进样。
氯化两面针碱的保留时间为12.466 min,K-R营养液、酚红溶液的保留时间均在5 min以内,通过实验表明K-R营养液及酚红中组分对氯化两面针碱无干扰。
1.3.3.3 标准曲线 精密吸取浓度为9.792 μg/mL的氯化两面针碱对照品溶液,分别进样5.0 μL、8.0 μL、10.0 μL、 15.0 μL、 20.0 μL, 回归方程为y=8.5089x+90.361, r=0.9994, 表明进样量在0.049~0.1958 μg线性关系良好。
1.3.3.4 精密度试验 连续进样5次,每次10 μL,测定其峰面积,RSD=1.4%,结果表明,试验方法精密度良好。
1.3.3.5 稳定性试验 分别在0、2、4、6、8、10 h,进样,测定氯化两面针碱的色谱峰面积,RSD=0.4%,结果表明,试验方法稳定性良好。
1.3.3.6 重复性试验 取样品5份,按照拟定的色谱条件,分别精密量取上述供试品溶液10 μL, 注入液相色谱仪,测定峰面积,RSD小于3,结果表明,实验方法重复性符合有关规定。
1.3.3.7 加样回收率试验 按供试品溶液制备方法制备供试品溶液,取已知氯化两面针碱含量 (20.22 mg/g)的样品适量,精密称定,共5份,置具塞锥形瓶中,分别精密加入浓度为0.2448 mg/mL的氯化两面针碱对照品溶液4 mL,精密吸10 μL,注入液相色谱仪,计算回收率,氯化两面针碱低、中、高浓度平均回收率为(100.81%±1.1)%、 (99.87%±1.2)%、 (101.3%±1.1)%。本方法回收率良好。
1.4 动物实验设计 取Wistar大鼠15只,随机分成高、中、低3个剂量组,将实验前禁食 (自由饮水)12 h的大鼠称重后,以0.6 mL/100g的20%的乌拉坦溶液腹腔注射麻醉大鼠,麻醉后的大鼠固定在手术台板上,保持体温37℃,沿腹中线切开约3 cm,以直径为0.5 cm的玻璃管做胃肠道插管,与循环泵的胶管连接组成回路,先用37℃的盐水5 mL/min冲洗肠道,约10 min,直至肠道冲洗干净,然后用K-R营养液平衡5 min,将样品溶液200 mL连入循环装置中,以2.0 mL/min循环3 h,自实验开始后0 min、 15 min、 30 min、 60 min、 90 min、120 min、150 min、180 min分别取回流液1 mL,并补充等量的酚红储备液,以酚红标定体积,测定浓度分别为3.31 μg/mL、 6.62 μg/mL、 33.11 μg/mL氯化两面针碱的吸收率。
2 结果
将大鼠随机分成3组,按照实验方法,定时取样并测定,计算各时间点的剩余药量X,以剩余药量对数和时间作图,利用公式inX=inX0Kα·t计算出Ka,吸收半衰期T1/2,结果见表1~3。

表1 氯化两面针碱在大鼠小肠剩余药量-时间
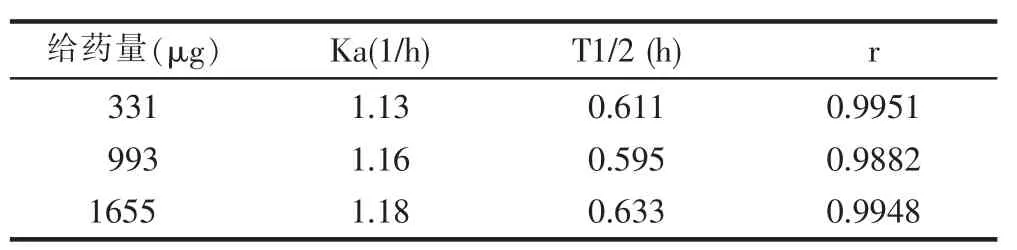
表2 氯化两面针碱在体小肠吸收的药代动力学参数

表3 低、中、高浓度氯化两面针碱吸收百分率 (x±sD,n=5)
在大鼠小肠吸收百分率经t检验分析 (P>0.05),无显著差别,高、中、低、三种浓度的吸收百分率基本相似,吸收百分率与药物浓度无关,结果表明氯化两面针碱在3.31~33.11 μg/mL浓度范围内吸收为被动扩散。
3 讨论
在碱性溶液中,酚红的最大吸收为558 nm,而不是550 nm,离子型酚红被认为在小肠中无吸收,但有文献报道酚红在大鼠小肠段也有吸收[10],在实验中用酚红标示回流液体积变化,定容后计算回流液中的氯化两面针碱吸收量更准确,克服了标定体积造成的误差。
大鼠在体循环接近体内环境,实验设备简便。
实验结果可以看出,氯化两面针碱在大鼠体内的吸收情况与药物浓度相关性不大,低、中、高浓度的药物吸收百分率无显著差别,半衰期约为0.6h,氯化两面针碱的吸收较好,方法简便可行,为中药制剂的研制提供参考。
氯化两面针碱为两面针主要成分,两面针在镇痛方面的文献被广泛报道,本文采用大鼠在体肠吸收模型研究氯化两面针碱在大鼠小肠的吸收为被动扩散,实验设备简单,接近体内环境,对高、中、低浓度的氯化两面针碱吸收良好,为中药制剂研发提供参考。
[1]国家药典委员会.中华人民共和国药典2010版(一部)[S].北京:中国医药科技出版社,2010:116-117.
[2]张蓉,卢来春,蒋学华.格列美脲大鼠小肠吸收的研究[J].第三军医大学学报,2004,26(10):886-888.
[3]江敏,张恩娟.原儿茶醛大鼠小肠吸收机理的研究 [J].中国药房,2003,14(9):528-530.
[4]胡一桥,郑梁元,钱陈钦,等.离子型药物酚红的小肠吸收研究[J].中国药科大学学报,1996,27(6):355-359.
[5]吴刚,孙长海,吴洪斌,等.大鼠小肠循环液中酚红的双波长分光光度法的测定[J].中国现代药学,2001,18(2):123-124.
[6]陆世惠,龙盛京.从两面针中提取总生物碱的工艺研究[J].西北药学杂志,2012,27(6):514-516.
[7]刘延成,程风杰,蒙衍强,等.两面针化学成分、药理活性及抗肿瘤机制研究进展[J].天然产物研究与开发,2012,24(4):550-555.
[8]雷欣潮,杨焕琪,赖茂祥,等.广西不同产区两面针HPLC指纹图谱研究[J].中草药,2012,43(5):1003-1008.
[9]韩建军,宁娜.两面针的药理作用研究进展[J].药学研究,2013,32(8):473-474.
[10]江敏,张恩娟.原儿茶醛大鼠小肠吸收机理的研究 [J].中国药房,2003,14(9):528-530.

