X -线引导3D重建半月节射频热凝治疗复发性三叉神经痛
梁欣洁 钟伟洋 周泽军 杨晓秋
(重庆医科大学附属第一医院疼痛科,重庆 400010)
三叉神经痛(trigeminal neuralgia,TN)是一种发病率高、难治愈、易复发的神经病理性疼痛,严重影响病人及家属的生活质量。Koopman 等统计报告TN 发病率约为 12.6 /10 万,多见于50岁以上人群,女性多于男性(约1.75:1)[1]。目前TN的发病机制尚不明确,国内外常见的TN手术方法:微血管减压术、三叉神经周围支撕脱术、甘油神经毁损术、伽马刀放射治疗及三叉神经半月节射频热凝术等。相关研究报道TN术后1年疼痛缓解率为68.0%~85.0%[2,3]。Tatli通对TN各种手术方式长期效果的文献研究,得出结论:TN术后5年复发率约46%[4]。由于技术水平、定位方式和治疗程序不同,导致疼痛缓解率、复发率相差甚远。目前国内外研究多集中于TN初发病人的疗效评估,对于术后复发的TN治疗研究较少。目前常见X线及CT引导经皮三叉神经半月节射频热凝术(percutaneous radiofrequency thermocoagulation therapy,PRT),其各有优缺点,本研究利用X线引导3D重建技术,术中建模、动态定位、高效、价廉;治疗术后复发性TN简便、微创、重复性好、疗效显著,值得大力推广。
方 法
1.一般资料
收集我科2012年2017年X -线引导3D重建PRT 治疗的55例复发性TN病人一般情况(见表1)。
纳入标准:符合国际头痛协会(IHs)公布的ITN诊断标准[5];既往行手术治疗复发的病人。排除标准:①面部感染者;②颅内、颅底肿瘤压迫,耳源性或牙源性等继发性三叉神经痛者;③凝血功能障碍;④有精神疾病等不合作者。
初次手术方式:微血管减压术 10例 (18.19%),三 叉 神 经 周 围 支 撕 脱 术 7 例 (12.73%),酚甘油神经毁损术 3 例(5.45%),伽马刀放射治疗8例(14.54%),无水乙醇毁损术3例(5.45%),三叉神经PRT 24 例 (43.64%)。
2.仪器设备
X光机:SIEMENS公司生产。射频仪:加拿大Bails公司生产230-TD型射频仪。
3.治疗方法
手术在X -线引导3D重建辅助下进行。病人取仰卧位,采用3种方式确保穿刺到位:①体表定位:参照Harte前人路穿刺方法。使用长10 cm前端裸露5 mm的绝缘电极针穿刺.进针约6~7 cm时,病人出现同侧面部剧痛感,此时针尖接近或进入卵圆孔。②3D重建成像:行X -线头颅正、侧、侧斜位摄片及3D重建定位(见图1)。③神经电
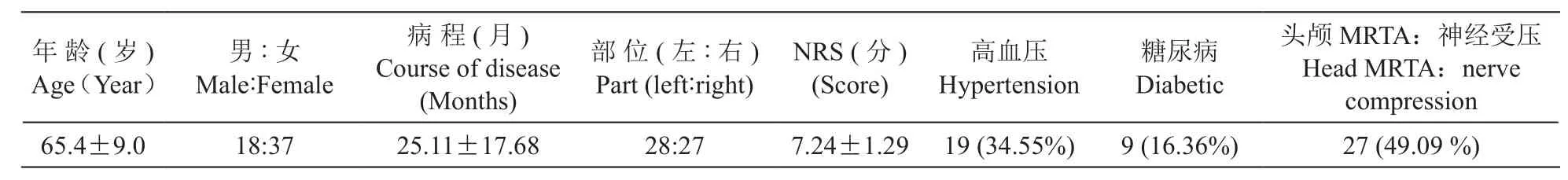
表1 病人一般资料Table 1 The general data of patients
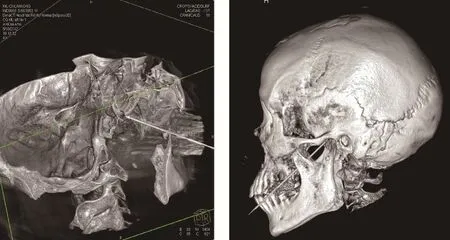
图1 3D重建定位图Fig.1 3D reconstruction radiograph
采用SAS统计软件分析,计量资料均数±标准差(±SD)表示,计数资料采用秩和检验,P≤0.05为差异有统计学意义。病人术后疼痛缓解率采用Kaplan - Meier 法分析。生理测试:插入射频电极针,测试阻抗,予高频(50 Hz)、低频(2 Hz)方波电刺激病变三叉神经分支,诱发支配区域疼痛及肌肉收缩反应。予以2%利多卡因局部麻醉,减少刺激。予脉冲射频热凝治疗,射频热凝温度及治疗时间为60℃、65℃各60 s,70℃、75℃各 120 s,80℃ 240 s。术中予以止吐降压等对症处理,持续监测病人生命体征。术后返回病房,局部冰敷,仰卧位持续心电监护24小时。
4.随访及疗效评估
由主管护士或医师电话随访,于术后1月、3月、6月、12月及2017 年8 月末次随访,平均随访时间为(24.40±18.41)个月。记录病人TN疼痛缓解率、复发率及并发症情况,记治疗前NRS评分为A,治疗后NRS评分为B,则疼痛缓解率R = (A-B)/A×100%。评判标准:临床治愈R≥75%;显效为R 50%~75%;有效R 25%~50%;无效R≤25%。记录术后并发症。
5.统计分析
结 果
1.临床疗效
本组55例病人均成功行X -线引导3D重建PRT手术。术后55例病人疼痛缓解率100%,术后1年疼痛缓解率为81.46%,病人随访期间疼痛缓解率见图2。随访术后1年复发率为14.55%,终末复发率约18.18%,术后随访复发情况见表2 。10例复发病人再次PRT治疗后随访4月至4年未再复发。
2.并发症
病人术后患侧三叉神经分布区麻木感、触觉减退52例(94.55%)。面部肿胀10例(18.18%)给予局部冰敷,1~2 天后肿胀消退,咀嚼力下降7例(12.73%)、口腔溃疡4例(7.27%)、复视0例。
讨 论
目前国内外对于TN 发病机制尚不明确,常见假说理论包括:①病损相关的理论,认为血管病因导致三叉神经周围及中枢部的血管形态及功能的紊乱[6]、多发性硬化与三叉神经根入髓区的神经脱髓鞘有关、糖尿病周围病变导致感觉神经痛觉过敏引发病理性神经痛[7]。②自身损伤理论包括周围支与中枢部神经损伤如:慢性上颌窦炎、牙周炎、骨膜炎、蜂窝织炎、血管及其他压迫。③多病因理论如:“过敏假说”、“生物活性物质”、“生物共振假说”[8]。④分子理论主要研究降钙素相关肽、P物质、β-内啡肽、5-羟色胺等[9]。而TN术后复发的原因尚不清楚,可能因素有:术后神经纤维再生、新责任血管压迫、存在交通支、蛛网膜黏连等[10]、手术穿刺准确性、射频温度时间是否足够等。此外复发性TN需二次手术时,往往初次手术创伤较大,局部组织严重粘连,无明显责任血管,年龄较大,基础疾病多,已不再适合神经外科治疗,而且二次手术手术死亡风险更高,术后的并发症不容忽视,脑神经损害的几率也较初次手术明显。
射频热凝利用痛、触觉纤维对热敏感性不同,而通过控温选择性的毁损细α和无髓C痛觉神经纤维,保留传导触觉的β纤维,避免外科手术的高风险。较外科手术:设备简单、操作简单、重复性强、微创、并发症少,重复性好、对局部解剖结构影响小等优点。Tang等报道TN病人行 PRT后复发再次行 PRT 治疗取得了与首次 PRT相近有效率[11]。PRT及时止痛,保留触觉,适用于高龄体弱、合并症多、复发性TN病人。
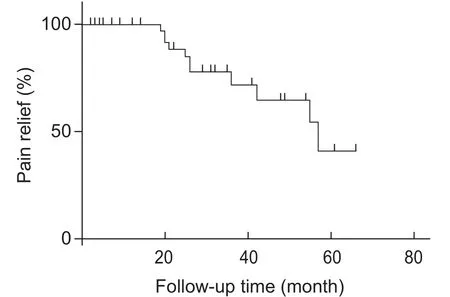
图2 随访期间疼痛缓解情况Fig.2 The degree of pain relief

表2 病人PRT术后复发情况Table 2 The Recurrent data of patients by PRT
为提高PRT治疗TN的有效率,减少并发症,我科采用X -线引导3D重建PRT治疗复发性TN。X -线引导3D重建与CT、MRI比较:成本低,辐射小,易推广,较普及。较传统的X线引导更精确,清晰[12,13]。3D重建技术实时动态定位、360°全方位立体定位,术中可以任意选取斜坡、冠状位、矢状位等切面,清楚地判断针尖与卵圆孔的位置关系、针尖的朝向、进针深度等。术中用神经电生理测试可以见到明显的肌肉跳动、感觉异常,提示3D重建技术有利于提高穿刺定位准确性。国内相关研究CT引导下PRT术后1年疼痛缓解率75.65%,术后95.1%病人出现不同程度的并发症,其中角膜反射减弱6例(8.57%),颞下颌关节炎2例 (5.5%)[14,15]。相比较我科3D重建PRT后随访1年疼痛缓解率81.46%,病人疼痛缓解情况较好,且未出现角膜反射减弱等严重并发症。X -线引导3D重建PRT因其微创、高效、廉价、疗效显著、并发症少、可重复治疗、不损伤局部解剖结构等优点,推荐为复发性三叉神经痛有效的治疗手段。
本研究提示,X -线引导3D重建PRT,靶点定位精确、穿刺成功率高、手术重复性好且并发症轻微,对复发性三叉神经痛的预后有积极影响。可以作为复发性三叉神经痛病人理想的治疗方法。但研究病例数尚少,后续需增加病例数及长期随访观察。
参 考 文 献
[1]Koopman JS,Die leman JP,Huygens FJ,et al.Incidence of facial pain in the general population.J Pain,2009,147:122 ~ 127.
[2]Dworkin RH,O' Connor AB,Kent J,et al.Interventional management of neuropathic pain: NeuPSIG recommendations.J Pain,2013,154:2249 ~ 2261.
[3]Sables GJ,Wang HL.Etiology and pathogenesis of trigeminal neuralgia: a comprehensive review.J Joralmail Loaches,2013,3:2 ~ 127.
[4]Tatli M,Satiei O,Kanpolat Y,et al.Various surgical modalities for trigeminal neuralgia: literature study of respective long-term outcomes.J Acta Neurochir(Wien),2008,150: 243 ~ 255.
[5]Headache Classi fi cation Subcommittee of the International Headache Society.The international classification of headache disorders: 2nd edition.J Cephalalgia,2004,24:9 ~ 160.
[6]Cruccu G,Finnerup NB,Jensen TS,et al.Trigeminal neuralgia: N classification and diagnostic grading for practice and research.Neurology,2016,87:220.
[7]Todorovic SM.Is Diabetic Nerve pain Caused by Disregulation Channels in Sensory Neurons.J Diabetes,2015,64:3987.
[8]Jia DZ,Li G.Bioresonance hypothesis a new mechanism the pathogenesis of trigeminal neuralgia.J Med Hypothesses,2010,74:505.
[9]Dworkin RH,O' Connor AB,Kent J,et al.Interventional management of neuropathic pain: NeuPSIG recommendations.J Pain,2013,154:2249 ~ 2261.
[10]Xu Z,Schlesinger D,Moldovan K,et al.Impact of target location on the response of trigeminal neuralgia to stereotactic radiosurgery.J Neumsurg,2014,120:716 ~724.
[11]Tang YZ,Jin D,Li XY,et al.Repeated CT-guided percutaneous radiofrequency thermocoagulation for recurrent trigeminal neuralgia.J Eur Neurol,2014,72: 54 ~59.
[12]Tang YZ,Wu BS,Ni JX,et al.The Long-term effective rate of different branches of idiopathic trigeminal neuralgia after single radionfrequence themper regulation.J Med,2015,94:e1994 .
[13]Li X,Yue J,Yang L,et al.Application of antidromic conduction monitoring in ganglion radiofrequency thermocoagulation for locating trigeminal branches in trigeminal neuralgia.Pain Pract,2015.10:1111.
[14]罗芳,申颖,孟岚,等.CT引导下半月神经节脉冲射频治疗重度原发三叉神经痛.中国疼痛医学杂志,2014,20 (5): 314 ~ 317.
[15]Singh S,Verma R,Kumar M,et al.Experience with conventional radiofrequency thermorhizotomy in patients with failed medical management for trigeminal neuralgia. Korean J Pain,2014,27: 260 ~ 265.

