航空发动机用TWIP钢电化学充氢曲线的模拟研究
昝娜,骆小鹏
(1.中国航发商用航空发动机有限责任公司设计研发中心,上海 200241;2.中国核工业第五建设有限公司,上海 201512)
0 引言
航空发动机制造所涉及的材料众多,其中新型复合材料的应用和新结构设计,为大幅减轻发动机质量提供了可能。压气机采用金属基复合材料不仅减轻了质量,同时也可提高叶片切线速度;燃烧室和涡轮部件采用陶瓷基复合材料、碳/碳复合材料,在提高部件耐高温性能的同时减轻了质量。整体叶盘、整体叶环、对转涡轮等新结构的采用,也大大减轻了部件质量。双金属、陶瓷、低导热性热障涂层和复合材料等技术的逐步应用,将大幅提高涡桨发动机的性能、寿命及可靠性[1-3]。
在现代社会倡导节能环保的背景下,航空发动机用钢需要向轻量化的方向发展,这对航空发动机用钢提出了更高的要求,即要求航空发动机用钢具有良好的力学性能、优良的抗冲击能力和成形性。TWIP钢的强塑积高于50000 MPa%,单位体积的撞击吸收能为传统深冲用钢的2~3倍。因此,在先进高强钢中,TWIP钢是较好的选择。但是,TWIP钢易于发生氢脆,对其生产应用造成很大的困难[4-7]。
氢对金属材料的性能的影响在过去几十年已有广泛的研究,形成了多种理论机制。目前大部分的研究集中在某个特殊钢种氢脆行为的研究如亚稳奥氏体不锈钢,但是关于微观结构、合金成分和晶体缺陷的变化对氢脆行为的影响的研究报道还不多,尤其是对这种新颖的高锰奥氏体TWIP钢延迟断裂的氢脆方面的研究甚少,但TWIP钢具有良好的力学性能、优良的抗冲击能力和成形性,在航空发动机中的应用前景广阔[8-10]。氢能促进位错发射和运动(即促进局部塑性变形),当扩散、富集的氢浓度大于临界值时就会发生氢致局部塑性变形。当它发展到临界条件,某些地区(如裂尖无位错区、位错塞积群前端)的应力集中σmax将等于被氢降低的原子结合力σth(H),从而导致氢致裂纹在该处形核。原子氢进入微裂纹就复合成H2,产生氢压,它能使微裂纹稳定化,同时也能协助应力集中使微裂纹扩展。这个氢致开裂新机理考虑了氢促进局部塑形变形,氢降低原子键和力以及氢压的作用[11-15]。
为了研究氢对航空发动机用TWIP钢性能的影响,本文对部分TWIP钢进行电化学充氢,并研究了电化学充氢过程中溶液成分对充氢的影响,充氢后氢在材料中分布和扩散和充氢时间对氢含量的影响。
1 实验材料与方法
实验用Fe-22Mn-0.6C和Fe-17Mn-1Al-0.6C两种TWIP钢。两种TWIP钢采用真空感应冶炼+真空电弧重熔工业冶炼而成,其中Fe-22Mn-0.6C实验钢热轧后厚度为1.75 mm,分别对原始材料在800℃进行1 h固溶处理,在900 ℃和1000 ℃进行30 min固溶处理,得到晶粒尺寸为7 μm,20 μm和45 μm的实验钢。Fe-17Mn-1Al-0.6C实验钢为冷轧板材,冷轧后的厚度1.4 mm,实验钢冷轧后厚度1.4 mm,分别对原始材料在900 ℃和1000 ℃进行30 min固溶处理,得到晶粒尺寸为17 μm和45 μm的实验钢两种实验钢的成分分别如表1所示。

图1 恒电位阴极保护法充氢设备Fig.1 Constant potential cathodic protection method for hydrogen filling
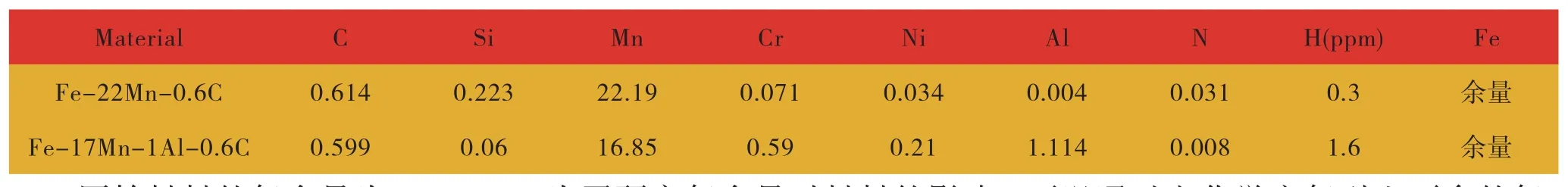
表1 Fe-22Mn-0.6C TWIP钢和Fe-17Mn-1Al-0.6CTWIP钢的化学成分(质量分数,%)Table 1 Chemical constituents of fe-22mn-0.6c TWIP Steel and FE-17MN-1AL-0.6CTWIP steel (mass fraction,%)
原始材料的氢含量为1~2ppm,为了研究氢含量对材料的影响,可以通过电化学充氢引入更多的氢。由于Fe-22Mn-0.6C和Fe-17Mn-1Al-0.6C TWIP钢抗腐蚀性能较差,所以选用恒电压仪阴极保护法进行充氢。实验设备如图1所示。
2 结果与讨论
2.1 电化学充氢参数确定
和普碳钢相比较,氢在奥氏体钢中扩散较慢。在实验室条件下,非薄膜试样通过电化学充氢很难实现氢均匀分布。根据菲克第二定律,式1和式2所示。计算在理想状态奥氏体中氢原子的扩散。

其中,D表示在温度TK时的扩散系数,D0表示在0K时的扩散系数,Ea表示扩散激活能,X表示在时间t时扩散距离,t表示时间。根据扩散定律计算发现,1 mm后板材充氢十几小时甚至几个月时间,才能使材料中的氢均匀分布。表2列举了不同作者的实验结果。

表2 氢原子在奥氏体和铁素体中的扩散系数和均匀分布所需时间Table 2 The time required for the diffusion coefficient and uniform distribution of hydrogen atoms in austenite and ferrite
随着充氢温度的升高,充氢所需时间呈指数下降,本文暂不考虑温度对充氢结果的影响,恒电压充氢在室温下进行,同时减少电解质分解和电解液的挥发。氢在材料中的进入和电解充氢过程中的参数密切相关,如催化剂、电流密度和温度。由于高锰奥氏体钢抗腐蚀性能较差,因此电化学充氢选择阴极恒电压充氢,恒电压充氢比较容易控制电解液对材料的腐蚀情况。酸性较强的溶液不宜用于高锰钢的电化学充氢,用0.5 mol/L H2SO4溶液时,进入试样的氢浓度较高,但是H2SO4中阴极充氢时试样容易变黑,金相检查发现已发生点蚀,如图2所示。这是一种阴极腐蚀现象。进入试样的氢浓度和所用的充氢溶液有关,也和是否加入毒化剂有关。(NH2)2CS能够抑制氢的脱附,提高试样表面氢的浓度,因而氧化电流也就大大提高。在本实验中,选用1.4 g/L硫脲溶液1和20 mg/L硫脲溶液2,根据两种溶液极化曲线如图3所示,充氢电压选为-800 mV vs. SCE,Fe-22Mn0.6C的腐蚀电压在溶液1的腐蚀电压为-485 mV vs. SCE,在溶液2的腐蚀电压为-550 mV vs. SCE,溶液1在-800 mV vs. SCE充氢过程中电流密度-2.39 mA/cm2,溶液2在-800 mV vs. SCE充氢过程中电流密度-6.92 mA/cm2,溶液1电流密度较小,在充氢过程中不易腐蚀实验材料,所以本实验选用溶液1作为电解液。
通常氢不能以分子态进入金属,而是通过在金属表面上的物理吸附、化学吸附、溶解、扩散等一系列过程才进入金属内部一定位置。既使在常温常压下,在金属表面也会有一定数量的原子氢,它通过吸附就可以进入金属内部。

图2 不同溶液充氢166 h后试样表面(a) 溶液1 (b) 溶液2Fig. 2 Sample surface after hydrogen filling 166 h with different solutions(a) Solution 1 (b) Solution 2
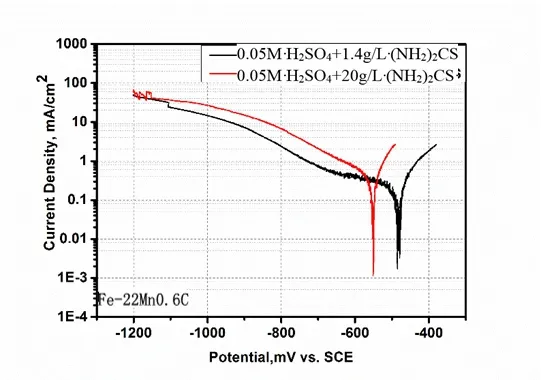
图3 Fe-22Mn-0.6C在不同电解液中的极化曲线Fig. 3 Polarization curves of Fe-22Mn-0.6C in different electrolytes
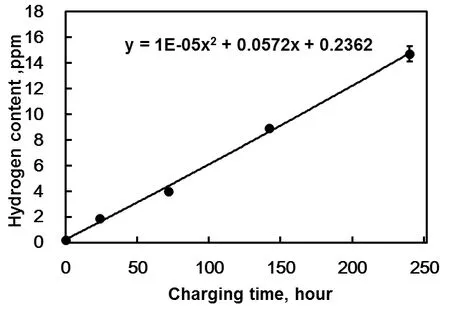
图4 不同充氢时间后试样在空气中放置8min后试样中的氢含量Fig.4 Hydrogen content in sample after 8min is placed in air after different hydrogen filling time
2.2 电化学充氢曲线的模拟
为了精确控制试样中氢含量,对材料A分别进行24 h,72 h,142 h,240 h电化学充氢。充氢后的试样迅速在酒精溶液中用超声波清洗,通过热熔融法测定其氢含量,由于清洗和干燥最快需要8 min,所以测得氢含量为空气中放置8 min的实验结果,测量结果如表3所示。

表3 充氢不同时间试样在空气中放置8 min后试样的氢含量(ppm)Table 3 Hydrogen content of sample after 8 min in air at different time of hydrogen filling(ppm)
根据表3,可以得出氢含量和充氢时间的关系,如图4所示。通过这个关系式可以计算试样中的氢含量。最终确定试样充氢时间分别为76 h和144 h,试样中的氢含量可分别达到5 ppm和10 ppm。
电化学充氢后试样表面的氢在室温条件下很容易逸出,所以测量了电化学充氢时间分别为24 h,72 h,142 h,240 h的试样,在室温条件下放置不同时间后试样中氢含量。结果如表4至表7所示。从表中发现,充氢后的试样在室温中放置24 h之内氢含量降低较多,之后的时间氢含量降低较少。可以认为氢在试样中均匀分布,达到稳定状态。
从图5可以看出,在充氢后的24 h后,试样放置在空气中氢含量迅速降低,但是在随后的时间里,氢含量降低较少。随着放置时间的增加,试样氢含量趋于稳定。

表4 原始试样充氢24 h后放置在空气中不同时间试样中的氢含量(ppm)Table 4 Hydrogen content of samples placed in air at different time after hydrogen filling 24 h(ppm)

表5 原始试样充氢72h后放置在空气中不同时间试样中的氢含量(ppm)Table 5 Hydrogen content in sample placed in air at different time after hydrogen filling 72h(ppm)

表6 原始试样充氢142 h后放置在空气中不同时间试样中的氢含量(ppm)Table 6 Hydrogen content of samples placed in air at different time after hydrogen filling 142 h(ppm)

表7 原始试样充氢240 h后放置在空气中不同时间试样中的氢含量(ppm)Table 7 Hydrogen content of samples placed in air at different time after hydrogen filling 240 h (ppm)

图5 材料A充氢不同时间的氢含量Fig. 5 Hydrogen content at different times of hydrogen filling in material A
为了进一步明确材料中可扩散氢原子和不可扩散氢原子的含量,采用热脱附法测量材料B和材料C电化学充氢166 h后试样中的氢含量,测量结果如图6所示。充氢后的试样有两个峰值,在220 ℃左右出现的峰值表示可扩散氢原子,这些氢原子主要集中在能量较低的氢陷阱中,如位错和晶界。在600℃左右出现的峰值表示不可扩散氢原子,这些氢原子陷阱主要包括碳化物、氮化物和孪晶界等。
随后对热处理后的材料B、材料C和材料D进行电化学充氢。根据材料A电化学充氢时间和氢含量的曲线,计算出材料B、材料C和材料D的充氢时间分别为72 h和166 h。材料A、材料B、材料C和材料D分别充氢72 h和166 h的氢含量如图7所示。
图8为材料A、B、C、D分别充氢72 h和166 h后在室温条件下,可以看出:材料中的氢含量在开始的24 h,氢含量降低量较大,随后氢含量较低较少。
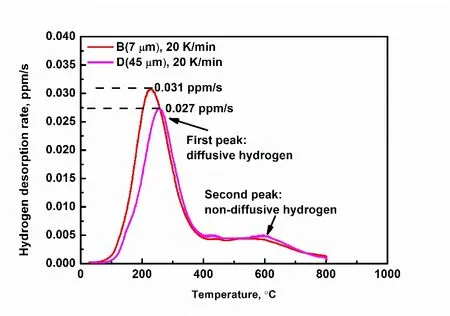
图6 材料B和材料C充氢166 h在空气中放置24 h的热脱附图Fig.6 Material B and material C charge hydrogen 166 h in the air to place a 24 h thermal desorption diagram
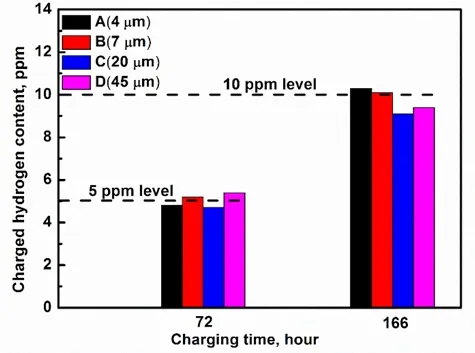
图7 热熔融法解析法测量实验材料的氢含量Fig.7 Determination of hydrogen content in experimental materials by thermal melting and melting method

图8 不同材料充氢后在空气中放置不同时间后试样中的氢含量(a)充氢72 h,(b)充氢166hFig.8 After different materials are placed in the air for different time after hydrogen filling, hydrogen content in the sample(a) is 72 h, and (b) hydrogen filling 166h
3 结论
(1)分析了氢在金属表面的吸附、扩散和溶解,在电化学充氢中分析了溶液成分和电流密度对充氢的影响,最终选用电解液0.05 mol/L H2SO4+1.4 g/L (NH2)2CS。
(2)原子氢在钢中的扩散服从菲克定律。根据菲克第一定律和第二定律,模拟充氢后氢在试样中的分布。通过对不同材料电化学充氢后跟踪测试,发现充氢后的试样在室温中放置24 h之内氢含量降低较多,之后的时间氢含量降低较少。
(3)充氢后72 h后材料中的氢含量约为5 ppm,充氢166 h后材料中的氢含量约为10 ppm。通过热脱附法测定了可逆转氢含量和不可逆转氢含量,220 ℃左右出现的峰值表示可扩散氢原子,这些氢原子主要集中在能量较低的氢陷阱中,如位错,晶界。在600 ℃左右出现的峰值表示不可扩散氢原子,这些氢原子陷阱主要包括碳化物,氮化物,孪晶界等。
[1] 肖蔓.航空发动机研制中科技情报需求分析[J].新型工业化, 2017, 7 (5): 47-50.XIAO Man. Analysis of Needs of Science and Technology Information in the Development of Aero Engine[J]. The Journal of New Industrialization, 2017, 7 (5): 47-50.
[2] 董彦非, 黄明, 李瑞琦.通用航空发动机发展综述[J].西安航空学院学报, 2017, 35(5): 8-13.DONG Yan-fei, HUANG Ming, LI Rui-qi. Overview of the Development of General Aviation Engines[J]. Journal of XIAN Aeronautical University, 2017, 35(5): 8-13.
[3] ZHANG Y, LAI X, ZHU P, et al. Lightweight Design of Automobile Component Using High Strength Steel Based on Dent Resistance [J].Materials and Design, 2006, 27(1): 64-68.
[4] ZHANG J M, JI L K, BAO D J, et al. Gigacycle Fatigue Behavior of 1800 MPa Grade High Strength Spring Steel for Automobile Lightweight[J]. Journal of Iron and Steel Research, International. 2014, 21(6): 614-618.
[5] Kastensson A. Developing Lightweight Concepts in the Automotive Industry: Taking on the Environmental Challenge with the Project[J].Journal of Cleaner Production, 2014, 66(1): 337-346.
[6] Park K T, Jin K G, Han S H, et al. Stacking Fault Energy and Plastic Deformation of Fully Austenitic High Manganese Steels: Effect of Al Addition[J]. Materials Science and Engineering A, 2010, 527(16): 3651-3661.
[7] 褚武扬. 氢损伤和滞后断裂[M]. 北京:冶金工业出版社, 1998: 14-15.CHU Wu-yang. Hydrogen Damage and Lag Fracture[M]. Beijing: Metallurgical Industry Press, 1998: 14-15.
[8] Oriani R A. The Diffusion and Traping of Hydrogen in Steel[J]. Acta Metallurgica, 1970, 18(1): 147-156.
[9] Perng T P, Altstetter C J. Effects of Deformation on Hydrogen Permeation in Austenitic Stainless Steels[J]. Acta Metallurgica, 1986, 34(20):1771-1780.
[10] Pressure G M. Classification of Hydrogen Traps in Steel[J]. Metallurgical and Materials Transactions A, 1979, 10(6): 1571-1576.
[11] Birnbaum H K, Sofronis P. Hydrogen-enhanced Localized Plasticity-A Mechanism for Hydrogen-related Fracture[J]. Materials Science and Engineering A, 1994, 176(1): 191-202.
[12] LU G, ZHANG Q, Kioussis N. Hydrogen-enhanced Local Plasticity in Aluminum: an Ab Initio Study[J]. Physical Review Letters, 2001,87(9): 5501-5506.
[13] Oriani R A, Josephic P H. Equilibrium Aspects of Hydrogen-induced Cracking of Steels[J]. Acta Metallurgica, 1974, 22(9): 1065-1074.
[14] Olden V, Thaulow C, Johnsen R. Modelling of Hydrogen Diffusion and Hydrogen Induced Cracking in Super martensitic and duplex stainless steels[J]. Material and Design, 2008, 29(12): 1934-1948.
[15] ZAN N, DING H, GUO X F, et al. Effects of grain size on hydrogen Embrittlement in A Fe-22Mn-0.6C TWIP Steel[J]. International Journal of Hydrogen Energy, 2015, 40(33), 10687-10696.

