春季东海挥发性有机硫化物(VSCs)分布的研究
孙茗歆,张洪海, ,马乾耀 ,朱 蓉,杨桂朋,2,* (.中国海洋大学化学化工学院,山东 青岛 26600;2.青岛海洋科学与技术国家实验室,海洋生态与环境科学功能实验室,山东 青岛 26607;.中国海洋大学海洋化学研究所,山东 青岛 26600)
硫循环是全球最重要的地球化学循环之一.海洋是硫的第二大储库[1],在全球硫循环中地位尤为重要.海洋中的微生物通过同化作用将硫酸盐(SO42-)同化为有机硫化物,再经由一系列复杂的生物化学反应生成具有挥发性和还原性的硫化物,如羰基硫(COS)、二甲基硫(DMS)、硫化氢(H2S)和二硫化碳(CS2)等.排放入大气的挥发性有机硫化物(VSCs)可以通过光化学反应实现无机硫的转化,从而完成海洋与大气间的硫循环,并对环境和气候产生影响.其中在大气中含量较为丰富的VSCs是DMS、COS和CS2[2].
DMS是海洋排放的最主要的挥发性生源硫化物,约占自然硫源释放的90%左右[3].DMS在大气中的寿命一般为1~2d,在一系列氧化作用之后生成非海盐硫酸盐(NSS-SO42-)气溶胶,增加了云凝结核(CCN)在大气中的数量,从而影响全球的气候[4].COS是大气中最稳定也是含量最高的含硫气体,在大气中寿命可达 2~7a.由于稳定的化学性质,使得COS可以在大气中充分混合并通过传质作用上升到平流层,与臭氧发生光化学反应,其产物是平流层含硫气溶胶的主要来源[5].这些SO42-气溶胶既会影响全球的辐射平衡,又能给非均相化学反应提供反应平面,进而加快臭氧层损耗[6].大气中的COS主要来源于前体物质CS2在平流层的氧化[7-8].CS2在大气中的含量不高,主要来源于人为以及海洋排放[9].CS2在大气中的氧化产物会在对流层中为 SO42-气溶胶做出贡献.鉴于 VSCs及其氧化物都会对气候造成直接间接的影响,VSCs排放及环境效应也逐步地成为国内外学者关心的重点问题.
东海作为全球海域中具有代表性的陆架边缘海之一,海域面积为 77×104km2,大陆架面积约占海域总面积的 66.7%.平均水深约为 370m,最深处处于东海东部深海槽,水深约为2719m.因此东海具有浅海性质的同时,兼具部分深海的特征.每年长江径流携带大量冲淡水(9.24×1011m3/a),沉积物(4.14×108t/a),悬浮泥沙(4.86×108t/a),营养盐和污染物输入,对东海生态环境造成了显著影响,特别是会形成利于近岸地区浮游植物的富营养条件[10],进而对东海海水中 VSCs的生产分布产生影响.目前,国内学者对中国海域海水中DMS浓度分布与海-气通量等进行了较为系统的研究[11-16],然而对其它 VSCs的研究较少[11,17].此外,有关中国近海大气中 VSCs浓度水平的文献报道更少.因此,本论文采集了春季东海海水及大气 VSCs样品,分析了海水及大气中 COS、DMS和CS2的浓度分布,并讨论了3种物质与生态环境因子的相关性,估算了它们的海-气通量,这对于深入了解我国近海有机硫的生物地球化学循环过程及环境效应具有重要的意义.
1 材料与方法
1.1 样品采集
于2017年3月~ 4月期间搭载中国海洋大学“东方红 2号”科考船对东海海域进行了现场调查取样.本航次调查共包括7条断面的42个站点(图1),其中在15个站点采集大气样品.海水样品均采用 12L Niskin Rosette 采水器进行采集,各站位海水温度、盐度和深度由 CTD(Seabird 911plus)在采集海水样品时测定.风速以及经纬度由DAK-500风速风向仪和MX200GPS定位系统(美国 Sperry公司)测定,并经过校正得出真实风速.

图1 2017年3 ~ 4月中国东海调查站位Fig.1 Sampling stations in the East China Sea in Spring
海水样品选用100mL透明钳口瓶(德国CNW公司)进行采集.先用海水润洗两遍样品瓶内壁,将润洗海水倒出,正式采样时要将水管插到瓶底并控制流速,避免产生涡旋和气泡对溶解气体造成影响[18].采样完成后瓶口要有凸液面,以免压盖后瓶顶有气泡存在.样品采集完毕,现场进行测定.如果样品过多无法短时间内全部测完,样品采集完毕立即放入冰箱(<4℃)中冷藏保存,尽快分析.大气样品使用抽成真空的2.5L苏玛罐(美国Restek公司)采集.为了避免在采集过程当中受到船体自身燃油排放的污染,到站之前,船体减速后,到顶层甲板(距海平面约10m)上采集大气.
1.2 样品分析
1.2.1 海水样品的测定 海水样品采用气提冷阱捕集-气相色谱法进行测量[19].用注射器取30mL海水样品注入大体积吹扫室中,通入60mL/min的高纯氮气吹扫15min,吹扫室下部设置玻璃砂芯,使得吹扫气体能与样品充分接触.吹扫出的VSCs先后经过填装了CaCl2的干燥管和填装了 100%脱脂棉的 1/4Teflon管以除去水分和氧化物,最后通过六通阀(美国Valco公司)富集于浸在液氮中的 1/16Teflon 捕集管内.吹扫15min后将捕集管放入热水中进行加热解析,热水温度不得低于90℃.解析出的VSCs气体在高纯氮气的携带下进入到配置火焰光度检测器(FPD)的GC-7890A气相色谱(美国Agilent公司)中进行测定.色谱柱选用的 CP7529(CP-Sil 5CB for Sulfur 30m×0.32mm×4.0 µm)毛细管柱(美国Agilent公司).柱温采取程序升温方式:起始温度55℃,以10℃/min的速度升至100℃,再以15℃的速度升至 150℃.进样口温度 150℃,分流比 10:1.该方法VSCs的检出限为2.5~3.5ng,精密度范围是3.2%~5.1%.
1.2.2 大气样品的测定 大气样品采用气相色谱-质谱检测器(GC-MSD)联用仪进行分析.将不锈钢苏玛罐连接在预浓缩仪 8900DS(美国Nutech公司)上,经三级冷阱预浓缩仪富集,随后由高纯氦气带入 GC–MSD(美国 Agilent公司,7890A-5975C)进行测定.色谱柱同样使用CP7529毛细管柱.柱温采取程序升温方式:柱温起始温度为55℃(保留3min),以10℃/min的速率升至100℃,再以15℃/min的速率升至150℃(保留 3min).载气(He)流量为 2.0mL/min;分流比为10:1;色谱柱进样温度为150℃.MSD的离子源为:电子电离源(EI).电压 70eV,离子源接口温度:230℃.通过全扫描模式(SCAN)和选择离子扫描模式(SIM)对待测组分进行定性和定量分析.该方法对 VSCs 的检出限为 0.1×10-12~0.5×10-12ng,精密度小于2%.
1.2.3 叶绿素a (Chl-a)的测定 首先用量筒量取300mL海水样品,采用 Whatman GF/F滤膜(直径47mm)进行过滤(压力低于 15kPa),再将过滤完的滤膜折叠包裹于锡纸中,冷冻保存(-20℃),尽快分析.实验室分析时,将滤膜放入离心管,加入 10mL 90% (V/V)丙酮水溶液在低温避光的条件下萃取24h,在4000r/min转速下离心10min,取上清液使用F-4500分子荧光仪(日本 HITACHI公司)进行测定[20].首先用纯品 Chl-a配制一系列标准溶液,根据浓度与信号值绘制标准曲线,再用外标法测定海水中Chl-a浓度,方法检测限为0.01µg/L.
2 结果与讨论
2.1 海水中COS、DMS和CS2的水平分布
春季东海表层海水温度和盐度分别在9.75~23.81℃和25.81~35.10之间,从图2可以看出,东海表层水温总体分布趋势为北低南高,而东海南部海域受高温高盐的黑潮水影响,水温表现为近岸低,外海高.东海盐度分布由于受到长江冲淡水与黑潮水的影响,表层低盐区域主要分布在长江口附近及其南部的近岸海域,并且在近岸形成盐度锋面,表明春季长江等陆地径流输入沿岸南下.此外,东海南部盐度锋面延伸至台湾海峡中部,表明调查期间黑潮水有强烈入侵陆架的趋势.
调查海域表层水中 Chl-a的浓度范围为0.03~8.80µg/L 之间,平均值为(1.16 ± 1.93)µg/L.此结果明显高于杨剑等[21]报道的2011年春季东海 Chl-a的浓度 0.60(0.09~2.17)µg/L 的结果.Chl-a的浓度高值区分别在出现在舟山群岛东南侧的E3站位与北麂列岛附近的S2站位.本航次E3与S2站位溶解无机氮(DIN)浓度分别为5.29和 8.11µmol/L,由图 2可以看出该高值区是闽浙沿岸流与台湾暖流交汇的区域,长江冲淡水与东海沿岸的淡水输入沿闽浙沿岸南下[22],与该区域的沿岸上升流混合向该区域输送了大量的营养盐[23-24].此外,该区域西侧是台湾暖流的主干[25],台湾暖流带来了大量温度较高的海水,丰富的营养盐与温暖的海水令浮游植物大量生长,从而使该站位Chl-a浓度产生了高值.另外,由于长江输送的淡水蕴含了大量泥沙,导致长江口及杭州湾附近海域海水透明度较低[26],影响了浮游植物的光合过程,限制了细菌和浮游植物的生长,尽管近岸区域存在较高的营养盐水平,但是浮游植物生物量明显低于舟山群岛东南侧的E3站位与北麂列岛东部的S2站位附近海域.
春季表层海水中COS、DMS和CS2的浓度分别在 0.3~2.1、0.6~34.3 和 0.2~1.7nmol/L 之间,平均值为(1.0 ± 0.4)、(6.8 ± 6.8)和(0.6 ± 0.4) nmol/L,其中DMS在VSCs中浓度最高.该结果明显高于田旭东等[12]于 2003年测量的青岛近岸海夏季数据(COS和CS2浓度分别为69.6和60.5pmol/L)以及欧洲主要河口数据[27]的研究结果.这可能是由于近些年来中国经济的快速发展,人为干扰对海洋环境的影响日益严重.长江等河流的陆源输入极大地影响了中国东部陆架海域的生态环境,营养盐和可溶性有机物(DOM)等浓度的上升使VSCs浓度有着明显的上升趋势.以DMS为例,94年夏季东海 DMS平均浓度仅为 1.8nmol/L[28],Yang等[29]和Zhuang等[30]在2006和2009年春季东海分别测得DMS浓度数据为3.4和4.9nmol/L,可以看出近20a来中国近海DMS浓度变化明显.
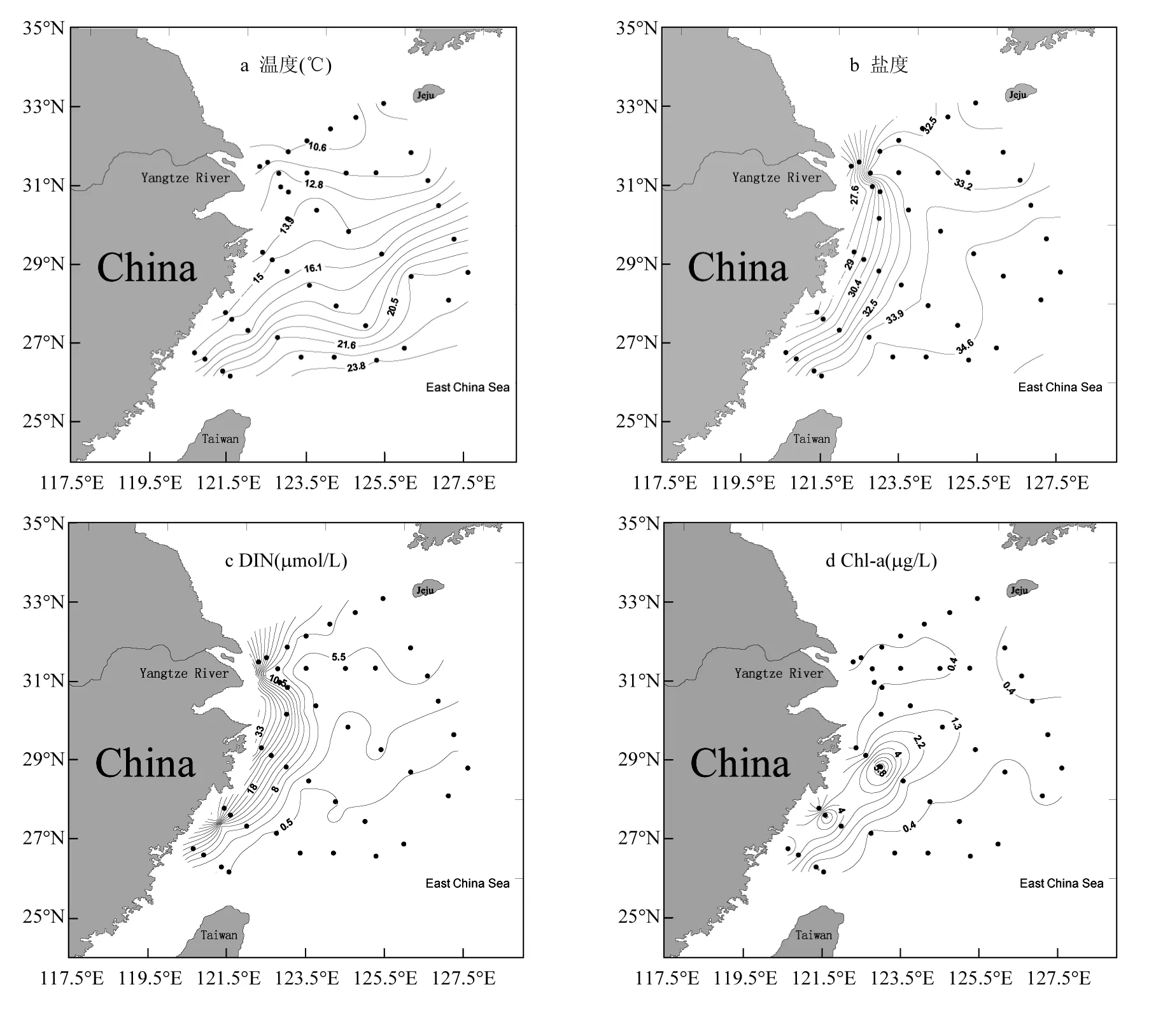
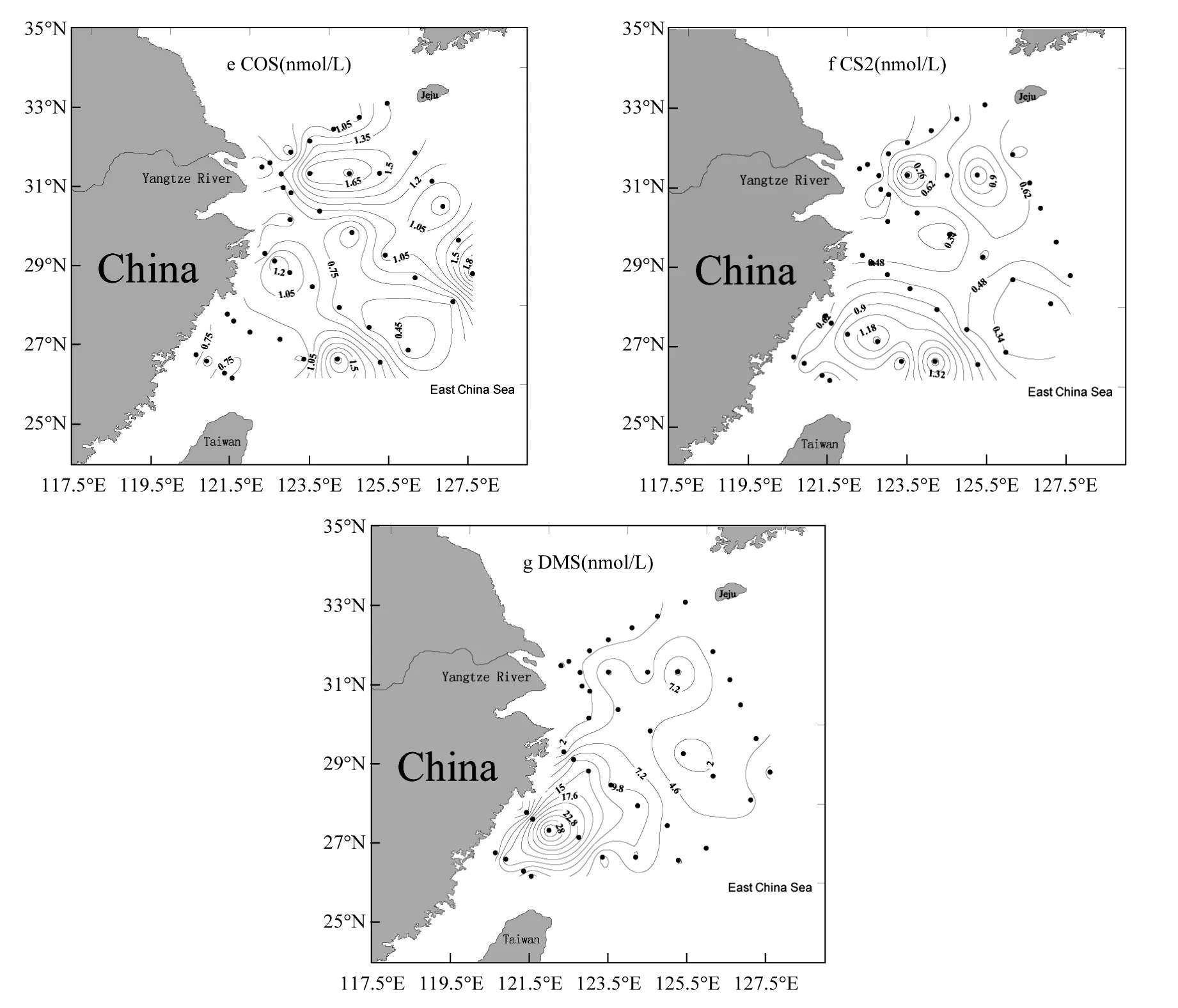
图2 春季东海表层海水中温度、盐度、DIN、Chl-a、COS、CS2和DMS的水平分布Fig.2 Horizontal distributions of temperature, salinity, DIN, Chl-a, COS, CS2 and DMS in the surface seawater of the East China Sea during spring
尽管这 3种物质的产生机制都与生物的硫酸盐同化作用有关,但具体的生产机制有很大区别[10],导致它们的浓度分布也出现了较大差异.春季东海DMS浓度最高值出现在南麂列岛西侧的S3站位附近海域,从图2可以看出,DMS浓度分布基本与Chl-a相类似,呈现近岸高,外海低的趋势.适宜藻类细菌生长的环境使其大量繁殖,促使了DMS浓度的提升.海洋中COS和CS2的浓度与CDOM关系密切[31],Flock等[32]认为COS主要的前体物质是含有-SH(巯基)的含硫化合物,如甲硫醇(MeSH),谷胱甘肽等,这些含硫化合物受光敏剂有色溶解有机物(CDOM)等的催化作用,发生光化学反应生成COS.Xie等[33]研究发现CS2与 COS有着相似的光化学产生路径,CS2的生产同样受CDOM的影响.春季东海表层海水中COS和 CS2的浓度高值区均出现在长江口外侧海域和台湾岛东北部的S6站位.COS和CS2在长江口外侧海域的浓度高值区可能是由于河口区域的富营养化导致浮游动植物、大型植物等的大量繁殖与死亡,其内部的生物化学过程以及陆地径流的输入增大了 CDOM 的浓度[34],加快了含有-SH(巯基)的含硫化合物的光反应过程,进而导致了COS和CS2浓度的增大.这表明浮游生物内部的生物化学过程是该区域CDOM浓度保持在较高水平的主要原因,进而也影响了 COS和CS2的浓度.与之类似,药怡良[35]发现春季东海CDOM浓度的高值区出现在S6站位附近与COS和CS2浓度高值区位置相吻合.另外,东海南部海水透明度较高[26],提供了有利于光反应发生的环境,使得该区域COS和CS2浓度呈现高值.
2.2 海水中COS、DMS、CS2和Chl-a之间的相互关系
为了更好地研究3种VSCs的源汇关系以及影响其浓度分布的因素,利用 SPSS 22软件对本航次所得的COS、DMS、CS2和Chl-a浓度数据进行相关性分析(表1).结果表明DMS与CS2浓度具有显著的相关性,这可能是由于海水中DMS主要来源于藻细胞破裂释放出二甲基巯基丙酸内盐(DMSP),海水中的细菌等微生物降解DMSP产生了 DMS,而这些死亡的藻类有机体降解则会产生CS2,包括这些有机体中的氨基酸如光肽氨酸在厌氧条件下也会分解产生CS2[36-37].两者在来源上具有一定的共性,导致了两者存在相关性.此外Ferek等[38]和Mihalopoulos等[39]分别在秘鲁海域、地中海和印度洋发现了COS与DMS也存在相关性,但是国内外学者对此现象并未做出明确解释.另外,调查发现Chl-a与DMS表现出显著的相关性,这与 Yang等[40],张洪海等[41]和孙婧等[42]在东海的调查结果相一致.东海浮游植物优势藻种为硅藻,虽然硅藻在浮游植物群体中通常被认为是DMS的低产种,但是Keller等[43]认为硅藻在海区成为优势藻种后,其巨大的数量优势导致所产生的DMS量也是巨大的.这就导致了春季东海表层海水中的DMS与Chl-a具有良好的相关性.

表1 东海表层水中COS、DMS、CS2和Chl-a间的相互关系Table 1 Relationships between COS, DMS, CS2 and Chl-a in the surface water of the East China Sea
2.3 大气中COS、DMS和CS2的浓度
春季东海大气中COS、DMS和CS2的浓度范围分别为(85.1~778.9)×10-12、(3.4~45.4)×10-12和(27.2~276.6)×10-12,平均浓度为(294.7±158.8) ×10-12、(22.7±18.0)×10-12和(108.8±88.1)×10-12.总体上,大气中VSCs的浓度呈现近岸高、远海低的分布趋势.COS和 CS2的浓度高值都出现在韭山列岛附近的E1站位,这是由于近岸大气受到人为排放的贡献所致.已有研究表明大气中 CS2的重要来源就是人为排放,Chin等[44]调查显示全球大气中CS2的来源中人为输入达到其50%左右.
另外,将本航次白天(6:00~18:00)与夜晚(18:00~次日6:00)采集大气样品的站位进行分类比较,发现夜晚大气中COS、DMS和CS2的浓度范围分别为(206.2~227.1)×10-12、(2.1~34.0)×10-12和(28.9~118.5)×10-12,平均浓度为(215.3±10.7)×10-12、(13.2±18.0)×10-12和(66.4±46.5)×10-12.而白天站位的浓度范围分别为(85.1~778.9)×10-12;(3.4~45.4)×10-12和(27.2~ 276.6)×10-12,平均浓度为(314.6±173.0)×10-12、(24.7±19.2)×10-12和(123.0±96.0)×10-12.此结果表明白天采集的样品VSCs浓度明显比夜晚的高得多,COS、DMS和CS2分别高出约46%,87%和85%.白天尤其是中午的日照强度大,促使了COS和CS2的光氧化产率的增高,这与田旭东等[11]的研究结果相一致.另外,研究表明大气中的DMS在光照条件下,会有少量转化为 COS[45].浮游植物的生物化学作用受光照影响明显,使得白天海水中DMS浓度上升,通量增加,导致大气中DMS浓度明显上升[46],进而表现出明显的周日变化.
2.4 VSCs的海-气通量
VSCs的海-气交换是全球硫循环中的一个重要过程,对于 VSCs通量的估算有助于更准确地评价大气与海洋中 VSCs的源汇关系.本文采用 Liss等[47]提出的双层滞膜模型结合本航次测定的海水与大气中VSCs的浓度来估算VSCs的海-气通量.计算公式为:

式中:F为海-气通量,µmol/(m2⋅d);kw为海-气传输速率,m/d;cw和cg分别代表VSCs在表层海水和大气中的平衡浓度,pmol/L;H代表亨利系数.本文采用田旭东等[11]所采用的公式计算亨利系数H,公式源于Sander的个人数据库.计算公式见表2,其计算出来的单位为:mol(L⋅atm),再利用Sander[48]的转化公式计算成无量纲的常数进行通量计算.

表2 亨利常数计算公式Table 2 The calculation formulas of Henry constant
同时还要计算VSCs的气体交换常数kw,其中kw是风速u (m/s)和气体常数Sc的函数.本文采用国际上最通用的N2000[49]来计算.

式中:U为海面上风速,m/s;Sc代表 Schmidt数.Schmidt数的计算是根据 Saltzman等[50]建立的方程计算得出:

式中:t代表海水温度,℃.
由于DMS在海水中的浓度比在大气中的浓度要高两个数量级以上,所以在计算DMS的海-气通量时,公式(1)可以简化成如下形式:

本文采用的温度为各站位CTD实测表层海水温度值,风速为各站位海面上方10m处的实时风速.通量计算时大气中 VSCs浓度为本航次实测的各站位的平均浓度.
春季东海表层海水中COS、DMS和CS2的海-气通量范围分别是 0.3~18.6、1.2~178.0和0.2~16.8µmol/(m2⋅d).平均值为(4.0±3.4)、(25.8±33.8)和(2.6±2.9)µmol/(m2⋅d).DMS 通量的最大值出现在S2站位,海水浓度为18.9nmol/L,与D5站位的浓度(0.8mol/L)相差23倍,而风速相近(分别为14.4和10.2m/s).表明2站位DMS通量主要受浓度影响.COS与 CS2通量最小值都出现在 E4站,最大值则均出现在S6站.两站位浓度相近(E4站分别为1.0和0.7nmol/L,S6站浓度分别为1.9和1.7nmol/L),而风速相差6倍以上(2站位风速分别为2.0和13.5m/s),表明两站位COS和CS2通量主要受风速控制.由以上分析可以看出,各站位VSCs的海-气通量相差较大,是风速与浓度共同作用的结果.
与田旭东[11]于2003年在青岛近海的调查结果相比较,本航次春季东海的COS与CS2的海-气通量较高,主要由于本航次调查中 VSCs浓度较大,且该航次调查期间风速普遍偏高(平均风速达 8.6m/s).同样是由于本航次高风速与 DMS高浓度的存在,DMS的通量明显高于2011年杨剑[21]春季东海的调查结果.此外,3种VSCs海-气通量的计算结果均为正值,表明春季东海是 3种VSCs的源.与Xu等[51]的大西洋VSCs通量数据相比较,显示出陆架海域相对远海在 VSCs通量上具有很大优势,说明陆架海域在全球 VSCs通量上具有更重要的贡献.
3 结论
3.1 春季东海表层海水中3种VSCs的浓度大小顺序为 DMS>COS>CS2, COS、DMS和 CS2平均浓度分别为1.0、6.8和0.6nmol/L.而大气中3种 VSCs浓度大小顺序为 COS>CS2>DMS,COS、DMS和CS2平均浓度分别为294.7、22.7和108.8×10-12表明DMS和COS分别是海水和大气中浓度最高的VSCs.
3.2 相关性分析结果表明 DMS与 CS2存在显著相关性,说明两者在来源上存在一定共性.此外DMS与Chl-a具有显著相关性,表明浮游植物生物量是影响东海海水中DMS的主要因素.
3.3 大气中3种VSCs的昼夜浓度对比表明,日间浓度明显高于其夜间浓度.由于调查期间较高的 VSCs浓度和较大风速,春季东海 3种 VSCs的海-气通量较大.表明春季东海是大气中 VSCs重要的源.
参考文献:
[1]Ivanov M V, Freney J R. Global biogeochemical sulphur cycle [J].Scope Report, 1981,19:61-78.
[2]王艳君,郑晓玲,何 鹰,等.大气中总挥发性有机硫化物检测方法的研究 [J]. 环境科学, 2011,32(12):3617-3622.
[3]胡 敏,唐孝炎,李金龙,等.海水中二甲基硫测定方法的研究[J]. 环境化学, 1995,14(2):157-163.
[4]Charlson R J, Lovelock J E, Andreae M O, et al. Oceanic phytoplankton, atmospheric sulphur, cloud albedo and climate [J].Nature, 1987,326(6114):655-661.
[5]Crutzen P J. The possible importance of CSO for the sulfate layer of the stratosphere [J]. Geophysical Research Letters, 1976,3(2):73–76.
[6]Engel A, Schmidt U. Vertical profile measurements of carbonylsulfide in the stratosphere [J]. Geophysical Research Letters, 1994,21(20):2219–2222.
[7]Brown K A, Bell J N B. Vegetation-The missing sink in the global cycle of carbonyl sulphide (COS) [J]. Atmospheric Environment, 1986,20(3):537-540.
[8]Toon O B, Kasting J F, Turco R P, et al. The sulfur cycle in the marine atmosphere [J]. Journal of Geophysical Research Atmospheres, 1987,92(D1):943-963.
[9]Xie H. A study of the ocean source of carbon disulphide [D].Dalhousie University, 1999.
[10]Zhang J. Nutrient elements in large Chinese estuaries [J].Continental Shelf Research, 1996,16(8):1023-1045.
[11]田旭东.中国近海大气和海水中挥发性硫化物的测定 [D]. 北京:北京大学, 2004.
[12]田旭东,胡 敏,马奇菊.青岛环境大气和海洋表层水中挥发性硫化物的测定 [J]. 环境科学学报, 2005,25(1):30-33.
[13]耿春梅,吴 海,牟玉静,等.秋季 COS和 DMS在草坪与大气间的交换 [J]. 环境化学, 2004,23(1):12-16.
[14]马奇菊,胡 敏,田旭东,等.青岛近岸海域二甲基硫排放和大气中二甲基硫浓度变化 [J]. 环境科学, 2004,25(1):20-24.
[15]胡 敏,陆 昀.离子色谱法测定大气中的甲磺酸 [J]. 环境化学, 2000,19(6):572-576.
[16]张洪海.中国东海,黄海 DMS和 DMSP的生物地球化学研究[D]. 青岛:中国海洋大学, 2009.
[17]邱天雪,陈进生,陈衍婷,等.厦门近海域大气中挥发性有机硫化物特征研究 [J]. 环境科学与技术, 2015,38(1):111-116.
[18]Lu X L, Yang G P, Song G S, et al. Distributions and fluxes of methyl chloride and methyl bromide in the East China Sea and the Southern Yellow Sea in autumn [J]. Marine Chemistry,2010,118(1):75-84.
[19]Yang G P, Xiao-Lan L U, Song G S, et al. Purge-and-Trap Gas Chromatography Method for Analysis of Methyl Chloride and Methyl Bromide in Seawater [J]. Chinese Journal of Analytical Chemistry, 2010,38(5):719-722.
[20]张洪海,杨桂朋.胶州湾及青岛近海微表层与次表层中二甲基硫(DMS)与二甲巯基丙酸(DMSP)的浓度分布 [J]. 海洋与湖沼,2010,41(5):683-691.
[21]杨 剑.中国东部陆架海生源硫的分布,通量及其对气溶胶中非海盐硫酸盐的贡献 [D]. 青岛:中国海洋大学, 2014.
[22]孙学诗,范德江,刘鹏飞,等.春季长江口及邻近海域水体 Eh和pH的分布 [J]. 海洋科学进展, 2017,35(1):96-106.
[23]颜廷壮.中国沿岸上升流成因类型的初步划分 [J]. 海洋通报,1991,10(6):1-6.
[24]陈 鑫,宋金明,袁华茂,等.东海 2012年夏季海-气界面碳交换及其区域碳汇强度变化趋势初探 [J]. 海洋学报, 2014,36(12):18-31.
[25]伍伯瑜.黑潮和中国近海环流 [J]. 应用海洋学学报, 1991,10(1):25-32.
[26]薛宇欢,熊学军,刘衍庆.中国近海海水透明度分布特征与季节变化 [J]. 海洋科学进展, 2015,33(1):38-44.
[27]Sciare J, Mihalopoulos N, Nguyen B C. Spatial and temporal variability of dissolved sulfur compounds in European estuaries[J]. Biogeochemistry, 2002,59(1/2):121-141.
[28]Uzuka N, Watanabe S, Tsunogai S. Dimethylsulfide in coastal zone of the East China Sea [J]. Journal of Oceanography, 1996,52(3):313-321.
[29]Yang G P, Jing W W, Li L, et al. Distribution of dimethylsulfide and dimethylsulfoniopropionate in the surface microlayer and subsurface water of the Yellow Sea, China during spring [J].Journal of Marine Systems, 2006,62(1):22-34.
[30]Yang G P, Zhuang G C, Zhang H H, et al. Distribution of dimethylsulfide and dimethylsulfoniopropionate in the Yellow Sea and the East China Sea during spring: Spatio-temporal variability and controlling factors [J]. Marine Chemistry, 2012,138–139:21-31.
[31]Uher G, Meinrat. Andreae. Photochemical production of carbonyl sulfide in North Sea water: A process study [J]. Limnology &Oceanography, 1997,42(3):432-442.
[32]Flöck O R, Andreae M O, Dräger M. Environmentally relevant precursors of carbonyl sulfide in aquatic systems [J]. Marine Chemistry, 1997,59(1/2):71-85.
[33]Xie H, Moore R M, Miller W L. Photochemical production of carbon disulphide in seawater [J]. Journal of Geophysical Research Oceans, 1998,103(C3):5635–5644.
[34]Zhang Y, van Dijk M A, Liu M, et al. The contribution of phytoplankton degradation to chromophoric dissolved organic matter (CDOM) in eutrophic shallow lakes: field and experimental evidence [J]. Water Research, 2009,43(18):4685.
[35]药怡良.黄东海水体及沉积物中有色溶解有机物的研究 [D].青岛:中国科学院研究生院(海洋研究所), 2016.
[36]刘 莉,杨桂朋,陈 岩.秋季中国东海海水中溶解氨基酸的分布与组成 [J]. 海洋环境科学, 2013,32(4):510-517.
[37]张晋华,王 雷,聂亚峰,等.水稻土中半胱氨酸分解产生含硫气体的研究 [J]. 环境化学, 2001,20(4):356-361.
[38]Ferek R J, Andreae M O. The supersaturation of carbonyl sulfide in surface waters of the Pacific Ocean off Peru [J]. Geophysical Research Letters, 2013,10(5):393-396.
[39]Mihalopoulos N, Nguyen B C, Putaud J P, et al. The oceanic source of carbonyl sulfide (COS) [J]. Atmospheric Environment Part A General Topics, 1992,26(8):1383–1394.
[40]Yang G P, Li L, Qi J L, et al. Dimethylsulfide in the surface water of the East China Sea [J]. Continental Shelf Research, 2000,20(1)69-82.
[41]张洪海.中国东海,黄海 DMS和 DMSP的生物地球化学研究[D]. 青岛:中国海洋大学, 2009.
[42]孙 婧,张洪海,张升辉,等.夏季东海生源硫的分布,通量及其对非海盐硫酸盐的贡献 [J]. 中国环境科学, 2016,36(11):3456-3464.
[43]Keller M D, Bellows W K, Guillard R R L. Dimethyl Sulfide Production in Marine Phytoplankton [J]. Biogenic Sulfur in the Environment, 1989,393(1):167-182.
[44]Chin M, Davis D D. Global sources and sinks of OCS and CS2and their distributions [J]. Global Biogeochemical Cycles,1993,7(2):321-337.
[45]Barnes I, Becker K H, Patroescu I. The tropospheric oxidation of dimethyl sulfide: A new source of carbonyl sulfide [J].Geophysical Research Letters, 1994,21(22):2389–2392.
[46]Yang G P, Jing W W, Li L, et al. Distribution of dimethylsulfide and dimethylsulfoniopropionate in the surface microlayer and subsurface water of the Yellow Sea, China during spring [J].Journal of Marine Systems, 2006,62(1):22-34.
[47]Liss P S, Slater P G. Flux of Gases across the Air-Sea Interface[J]. Nature, 1974,274(5438):181-184.
[48]Sander R. Compilation of Henry's law constants (version 4.0) for water as solvent [J]. Atmospheric Chemistry & Physics, 2015,14(21):29615-30521.
[49]Nightingale P D, Malin G, Law C S, et al. In situ evaluation of air-sea gas exchange parameterizations using novel conservative and volatile tracers [J]. Global Biogeochemical Cycles, 2000,14(1):373-387.
[50]Saltzman E S, King D B, Holmen K, et al. Experimental determination of the diffusion coefficient of dimethylsulfide in water [J]. Journal of Geophysical Research Oceans, 1993,98(C9):16481–16486.
[51]Xu X, Bingemer H G, Georgii H W, et al. Measurements of carbonyl sulfide (COS) in surface seawater and marine air, and estimates of the air-sea flux from observations during two Atlantic cruises [J]. Journal of Geophysical Research Atmospheres, 2001,106(D4):3491–3502.

