食品中单核细胞增生李斯特氏菌的测量不确定度评定
岳 苑,贾冰凝,马桂娟
(宁夏回族自治区食品检测中心,宁夏 银川 750001)
单核细胞增生李斯特氏菌(Listeriamonocytogenes)简称单增李斯特氏菌,是一种人畜共患病的病原菌。它能引起人畜感染,主要表现为败血症、脑膜炎和单核细胞增多。它广泛存在于自然界中,食品中存在的单增李斯特氏菌对人类的安全具有危险,该菌在4 ℃的环境中仍可生长繁殖,是冷藏食品威胁人类健康的主要病原菌之一[1]。因此,在食品卫生微生物检验中,必须加以重视。
2017年6月23日,GB 4789.30—2016《食品安全国家标准 食品微生物学检验 单核细胞增生李斯特氏菌检验》[2]颁布实施。与旧标准相比,新标准增加了第二法平板计数法和第三法MPN计数法[2],同时,新版的CL09中5.4.6规定了微生物检测领域在某些情况下需要列出各主要的不确定度分量,并做出合理的评估[3]。由于单增李斯特氏菌的定量方法是国标修订后新增的检验方法,所以目前对该方法的测量不确定度评估的研究尚有不足,但是由于该方法与GB 4789.10—2016《食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验》[4]中的第二法相似,所以在不确定度评定时可以借鉴金黄色葡萄球菌检验的不确定度评定。
本文中,笔者根据 JJF 1059.1—2012《测量不确定度评定与表示》[5]和 GB 4789.30—2016《食品安全国家标准 食品微生物学检验 单核细胞增生李斯特氏菌检验》[2]第二法平板计数法,探讨对食品中单增李斯特氏菌检验不确定度及评定方法,以期对测量数值作出合理评估。
1 材料与方法
1.1 材料
酱牛肉购自银川市银华百货超市;单核细胞增生李斯特氏菌(ATCC19115)购自中国工业微生物菌种保藏管理中心;0.85%生理盐水,李氏增菌肉汤LB,李斯特氏菌显色培养基购自青岛海博生物技术有限公司。
1.2 方法
1.2.1样品的制备
无菌操作称取酱牛肉样品25 g,放入盛有225 mL LB肉汤的无菌均质袋内均质,制成1∶ 10的样品匀液[3]。将活化后的单增李斯特氏菌(ATCC19115)制成0.5麦氏浓度的菌悬液,加0.5 mL于上述1∶ 10的样品匀液,混匀。制备10倍系列稀释样品匀液,选择2~3个适宜连续稀释度的样品匀液,每个稀释度的样品匀液分别吸取1 mL,以0.3、0.3和0.4 mL的接种量分别加入3块李斯特氏菌显色平板,用无菌L棒涂布[2]。(36±1) ℃倒置培养24~48 h。
1.2.2样品的测定
选择有典型单增李斯特氏菌菌落的平板,且同一稀释度3个平板所有菌落数合计在15~150 CFU之间的平板,计数典型菌落数[1]。实际测量数值为1∶ 100 000的样品匀液在3个单增李斯特氏菌显色培养基上的菌落数分别为9、9和11 CFU,合计29 CFU。乘以稀释倍数后,样品最终测量数值为2.9×106CFU/g。两组人员同时操作,每组进行10次重复测量。
2 结果与讨论
2.1 不确定度来源分析
分析不确定的来源为单次样品测量过程中产生的不确定度及重复测量过程中产生的不确定度,见图1。
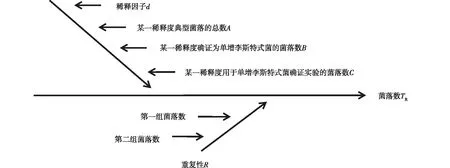
图1 单核细胞增李斯特氏菌菌落数不确定度来源因果Fig.1 The causality diagram of Listeria monocytogenes colony uncertainty sources
2.2 数学模型建立
依据GB 4789.30—2016《食品安全国家标准 食品微生物学检验 单核细胞增生李斯特氏菌检验》第二法,设定某一个稀释度典型菌落总数为A,该稀释度确证为单增李斯特式菌的菌落数为B,该稀释度用于确证试验的菌落数为C,稀释因子为d,则单次测量单增李斯特氏菌菌落总数T可通过下式得出:
(1)
考虑重复性影响后,加入重复性后单增李斯特氏菌菌落总数TR为
TR=T+R
(2)
2.3 不确定度评定
2.3.1样品制备过程中引入的不确定度
样品制备过程包括称量和稀释过程,不确定度主要是由电子天平称量(B 类)、玻璃器皿(B类)引入的。
1)电子天平称量引入的不确定度u天平
在样品制备过程中,如1∶ 10初始稀释液时,将25 g样品加入225 mL增菌液中制得。此时,使用电子天平称取样品。电子天平检定证书显示量程为0~500 g的允差绝对值为0.5 g,认为均匀分布;重复性标准差为1.0 g,两项线性叠加,计算见式(3)。
(3)
即实际称量25 g样品时,
2)量筒量取引入的不确定度u量筒
在样品稀释过程中,如1∶ 10初始稀释液时,使用250 mL量筒量取增菌液,根据JJG 196—2006中规定,250 mL量筒允许误差绝对值为1.0 mL,按三角分布处理,则
(4)
即实际量取225 mL LB培养基时,
2.3.2样品稀释过程中引入的不确定度
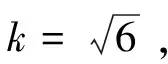
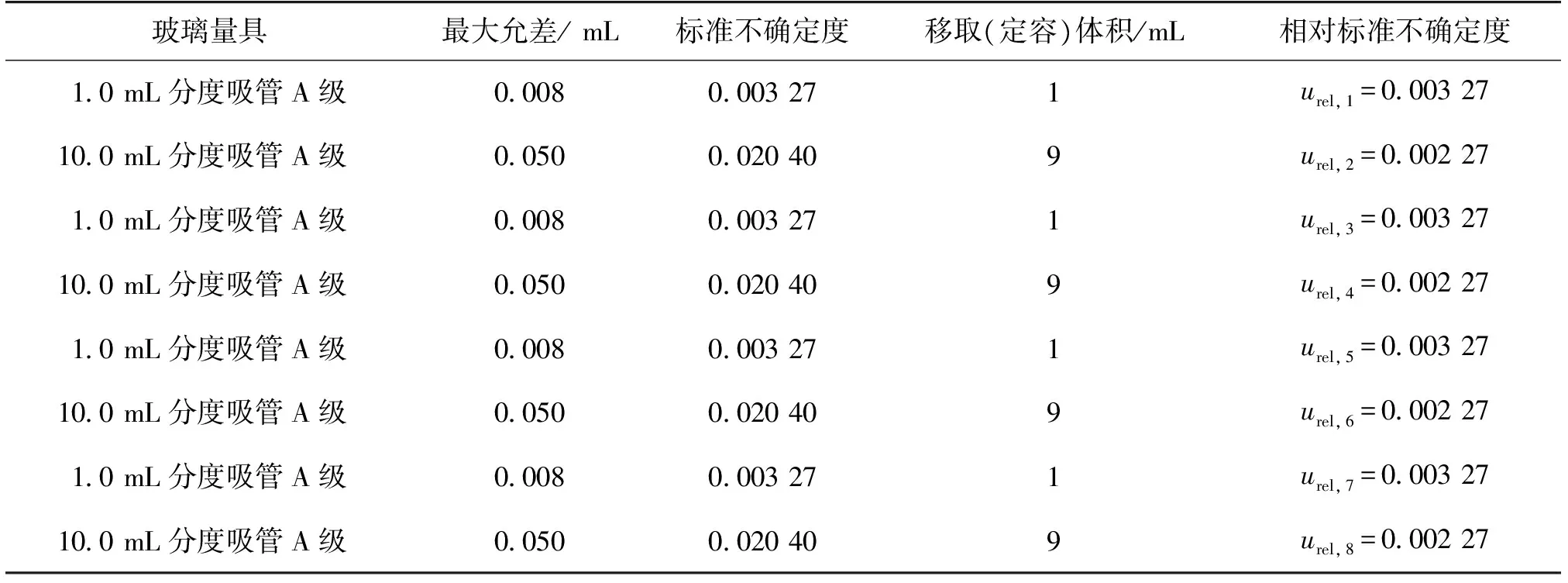
表1 逐级稀释过程中量具校准引起的不确定度
1)逐级稀释引入的不确定度
由于第一步稀释的方法( 25 g样品+225 mL LB肉汤) 与以后各步稀释的方法(1 mL样液前一步稀释的样液+9 mL LB肉汤) 不同,而第二步稀释的方法与以后各步的相同,本试验的结果在105数量级上,所以从第二步以后稀释了4次,逐级稀释的相对标准不确定度urel(d)的计算见式(5)。
(5)
2)加入样液引入的不确定度
一般情况下,对菌落培养来说,平皿上的菌落数肉眼观察菌落的结果是清晰可辨的。因此,平皿上菌落数的不确定度可以忽略不计。但是,由于加样体积1 mL分别以0.3 mL(V1)、0.3 mL(V1)和0.4 mL(V2)的接种量分别加入3块单增李斯特菌显色培养基上,所以这会因为分度吸量管的最大允许误差而引入新的不确定度,根据JJG 196—2006,1 mL分度吸管最大允差绝对值为0.008 mL,按三角分布考虑,所以加入样液的相对标准不确定度urel(V)为
(6)
(7)
(8)
(9)
3)评定菌落总数测量的相对标准不确定度
菌落总数的相对标准不确定度urel(T)由逐级稀释引入的相对标准不确定度urel(d)和加入样液引入的相对标准不确定度urel(V)组成。
(10)
=0.019 3
单次测量单增李斯特氏菌菌落总数T=290 000 0 CFU,所以单次测量的不确定度
u(T)=0.019 3×290 000 0=559 70(CFU)
(11)
2.3.3样品重复测量的不确定度u(R)
由于正常检验测量次数少,为提高自由度,做A类标准不确定度的预评定,由两组人员同时操作,采用分两组各10次重复测量的方法,评定其合并样本标准差及标准不确定度。重复测量数据见表2。
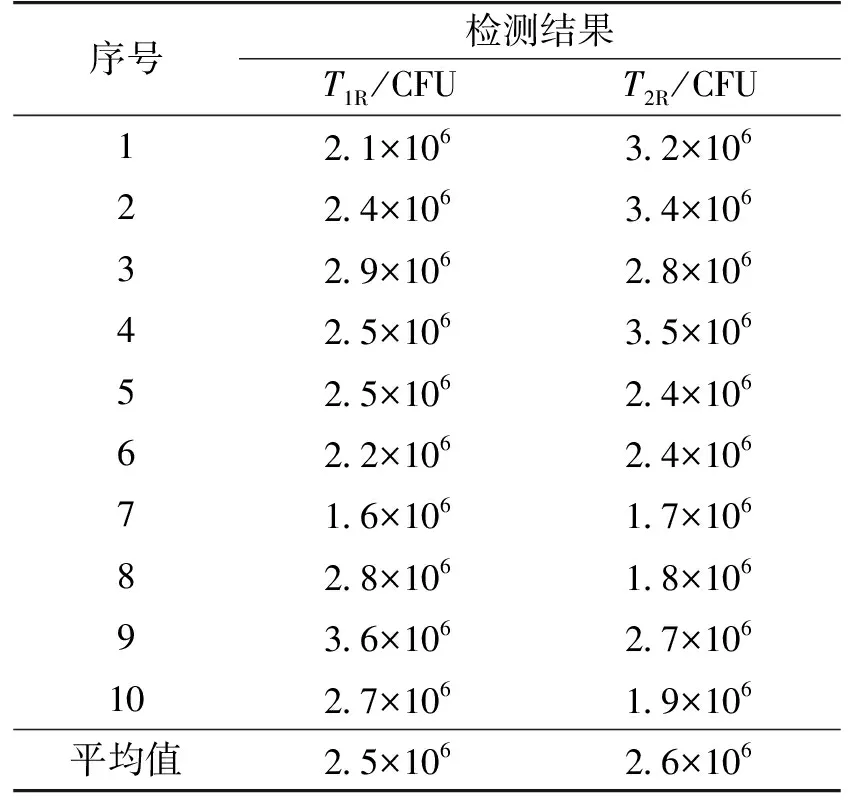
表2 重复测量数据表
试验过程中,同一样品共制作10份稀释液,每份稀释液测得一个测量值A参与计算T值,测量次数为1。
由表1数据,用贝塞尔公式[4]计算标准差sP及标准不确定度
(12)
(13)
(14)
正常检测时,测量次数为1,重复测量的不确定度
(15)
自由度ν=(10-1)×2=18
(16)
2.3.4合成标准不确定度
合成不确定度uc(TR)由单次测量的不确定度u(T)和重复性检测的不确定度u(R)合成计算。
(17)
=600 943(CFU)
2.3.5评定扩展不确定度U
根据文献[5],当k=2,则扩展不确定
U=ku(TR)=2×600 943=120 188 6 (CFU)
(18)
2.3.6不确定度结果报告
本次单核细胞增生李斯特氏菌平板计数法的检测结果为(2.9±1.2)×106CFU/g,第二项为扩展不确定度U的值,k=2。
2.4 讨论
2.4.1致病菌中测量不确定度评定的必要性
食品中致病菌的含量直接反映出食品质量的优劣。新修订的单核增生李斯特氏菌检验方法[2]增加了平板计数法和MPN计数法,第二法适用于单增李斯特氏菌含量较高的食品,第三法适用于单增李斯特氏菌含量较低但是杂菌含量较高的食品[2]。新标准将单增李斯特菌的检测逐步从定性转为定量,因而在实际检测过程中增加了实验操作环节、扩大了检测范围,这就对实验室提供的检测数据提出了更高要求。在实际检测工作中,肉制品中单增李斯特氏菌的检出率较其他致病菌更高,因此在检测的过程中要特别注意。此外,文献[7]中规定:检测实验室应有能力对每一项有数值要求的测量结果进行测量不确定度评估,测量结果不确定度的评定可以使实验室提供的数据更具有效性、科学性、公正性和可靠性。
2017年6月新增了单增李斯特菌定量检测方法,之前的检验方法为定性方法,所以目前的研究较少,但是由于该定量方法与金黄色葡萄球菌检验的定量方法相类似,因而能够参考沈小芳等[8]和邓小鸿等[9]的研究结果。
2.4.2不确定度数学模型的建立
食品化学样品分析结果常以微量为主,且化学物质有均一性,有较成熟计算不确定度的方法,而微生物污染的样品分析结果常以宏量为主,测定的是活的物质,不同的菌落之间有互生或拮抗等相互作用,是微生物测量不确定度评定的难点[10]。正是由于每次检测菌落总数的结果较分散,很多人认为微生物的不确定度可以忽略不计,在研究时采用Y=X的数学模型[11-13],没有考虑称量、稀释等过程对不确定度产生的影响,因而不能得出正确的评定结果。
另外,因为不同样品之间菌落总数结果的发散性较大,所以很多研究者认为直接使用贝塞尔公式计算合并样本标准差所得到的不确定度不太合理[11,16-17],而是将检测结果取对数后,计算对数样本标准偏差,再计算不确定度。但本文是重复多次测量同一样品,检测结果之间发散性不大,所以可以直接使用贝塞尔公式计算。本研究确立的数学模型以及不确定度的来源分析能够为同类研究提供参考依据。
2.4.3多次检测同一样品来评定不确定度的问题
虽然有专家认为为对同一样品进行重复多次检测在微生物学检测是不适宜的[18],并且在日常工作中,对同一样品进行多次重复检测的可能性不大,但是不同样品由于生产工艺、储存条件等的不同,致病菌含量有较大差异,而且微生物数量是动态变化,再者新的标准刚颁布实施不久,对于单增李斯特氏菌平板计数法的检测数据较少,寻找自然污染的样品比较困难,所以本试验选择使用标准菌株人为污染样品进行测定。从新开方法及保证结果的角度考虑,还是需要安排两名或两名以上检测人员对样品进行重复检测,因而此结论的普遍性有待提高。
2.4.4其他几个不确定度分量
由于在微生物检验中,B类不确定度对合成不确定度贡献较小,重复测量带来的不确定度占主要部分,所以,采用A类评定测量不确定度。
除了本文列出的不确定分量以外,样品的存储采集、样品的均质、培养基配制的时间、培养基灭菌温度、培养箱温度以及培养时间这些分量不便于计算,而且对总不确定度的贡献较小,所以不予考虑。这一方面可以通过制定作业指导书,统一规范操作规程,最大程度减少由此带来的不确定度。
3 结论
本文中,笔者通过建立数学模型T=AB/Cd,分析不确定度来自样品制备、样品稀释及重复测量的过程。样品的存储采集、样品的均质、培养基配制的时间、培养基灭菌温度和培养箱温度、培养时间对总不确定度的贡献较小。
本研究中,单核细胞增生李斯特氏菌平板计数法的检测结果为(2.9±1.2)×106CFU/g,第二项为扩展不确定度U的值,k=2。
参考文献:
[1]BUCHANAN R L,GORRIS L G M,HAYMAN M M,et al.A review ofListeriamonocytogenes:an update on outbreaks,virulence,dose-response,ecology,and risk assessments[J].Food Control,2017,75(3):1-13.
[2]中华人民共和国国家卫生和计划生育委员会,国家食品药品监督管理总局发布.食品安全国家标准 食品微生物学检验 单核细胞增生李斯特氏菌检验:GB 4789.30—2016[S].北京:中国标准出版社,2015.
[3]中国合格评定国家认可委员会.检测和校准实验室能力认可准则在微生物领域的应用说明:CNAS CL09—2013[S].北京:中国标准出版社,2013.
[4]中华人民共和国国家卫生和计划生育委员会,国家食品药品监督管理总局发布.食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验:GB 4789.10—2016[S].北京:中国标准出版社,2015.
[5]国家质量监督检验检疫总局.中华人民共和国国家计量技术规范 测量不确定度评定与表示:JJF 1059.1—2012[S].北京:中国标准出版社,2012.
[6]中华人民共和国国家质量技术监督检验检疫总局.常用玻璃量器检定规程:JJG 196—2006[S].北京:中国标准出版社,2006.
[7]中国合格评定国家认可委员会.测量不确定度评估和报告通用要求:CNAS CL07—2007[S].北京:中国标准出版社,2007.
[8]沈小芳,张雁,陆咏梅.金黄色葡萄球菌计数结果不确定度的评定[J].中国卫生检验杂志,2012,11(22):2785-2786.
[9]邓小鸿,强敏,朱新生,等.食品中致病微生物检测结果的不确定度评定[J].食品研究与开发,2016,37(11):160-165.
[10]袁平,吴春敏,林仲,等.食品中菌落总数测定不确定度评定数学模型的建立[J].预防医学论坛,2016,7(7):540-545.
[11]王晓红,姜娴.食品中菌落总数检测结果的不确定度评定[J].中国卫生检验杂志,2011,21(11):2799-2800.
[12]张霞.微生物检验中不确定度的评定[J].中国卫生检验杂志,2003,13(2):141-142.
[13]肖亚涵.食品微生物学菌落总数测定测量结果的不确定度评定[J].计量与测试技术,2007,34(7):75-77.
[14]王海华,兰茜.能力验证菌落总数测定结果不确定度的评定[J].食品安全质量检测学报,2015,6(6):2352-2355.
[15]杨兰花,卢力.化妆品微生物检验菌落总数不确定度评定[J].香料香精化妆品,2010(1):31-32.
[16]周婕,姚羚羚,瘳惠青.农村饮用水菌落总数测量不确定度的评定[J].医学动物防制,2014,30(7):814-816.
[17]李玉玲,宋莉莉.食品微生物学菌总数检验中不确定度的评定[J].中国卫生检验杂志,2005,15(7):880-897.

