锂离子扣式电池的组装,充放电测量和数据分析
王其钰,褚 赓,张杰男,王 怡,周 格,聂凯会,郑杰允,禹习谦,李 泓
锂离子扣式电池的组装,充放电测量和数据分析
王其钰,褚 赓,张杰男,王 怡,周 格,聂凯会,郑杰允,禹习谦,李 泓
(中国科学院物理研究所,北京 100190)
锂离子电池材料在研发以及初期生产检测阶段,需要通过扣式电池对电化学性能进行测量。测试方法和分析方法的准确规范是精确分析评价电池材料、开发新材料及开发新电池体系的基础。本文总结了以往文献资料,结合实际工作经验,介绍实验室锂离子扣式电池组装流程、充放电性能测量和数据分析方法。
锂离子扣式电池;充放电性能
一种新的电池材料或体系的开发通常历经实验室研发、小试、中试以及规模放大和商业化应用5个阶段,其中实验室研发阶段是对材料或体系性能测试、验证以及价值判断的关键。实验室数据除了具有重要的科研价值外,还有助于在早期开发阶段判断某些材料及电池体系是否具有实际应用价值及商业开发价值。实验室扣式电池除了用于对现有材料的性能进行检测之外,还用于对新材料、新工艺产品进行初步的电化学性能测试与评价。显然,对新电池材料的性能进行较为准确的测量,对该材料的开发与制备、全电池设计与应用有着重要意义[1-2]。而不同的电池测试方法对材料性能参数的测试结果会有明显的影响,因此,实验室扣式电池电化学性能测评方法的规范化,扣式电池测试数据如何对全电池设计提供更为准确的信息,如何根据扣式电池数据实现对电池材料的准确测试与电池整体的早期评价十分重要且必要[3]。
现行的锂离子电池测试标准多针对电池单体或电池包等产品的安全性及电性能的测试,如IEC 62133、UL2054、UL 1642和JIS—C—8714等标准主要侧重于电池产品的安全性能方面,欧盟发布的IEC 61960,日本推出的JIS—C—8711则主要侧重于锂离子电池的电性能测试,国内针对单体电池制定的GB/T 18287《移动电话用锂离子蓄电池及蓄电池组总规范》则包含了部分安全检测和性能测试项目。国内外也相继出台了多个特定领域的标准电池测试手册,且多是针对产业化的电池产品制定的,如《电动汽车动力性能试验方法》、《电动汽车能量消耗率和续驶里程试验方法》、《电动汽车用锂离子蓄电池》、《USABC电池试验程序手册》等。在参考以上行业标准的基础上,结合科研工作中的实际情况,本文主要介绍了锂离子电池扣式电池在实验室阶段的组装、充放电性能测试分析以及针对工业生产线电池极片的极片处理等内容。
文中介绍的充放电性能测试针对实验室锂离子扣式样品电池,包括半电池(half cell,正极极片/金属锂片、负极极片/金属锂片)、全电池(正极极片/负极极片)以及对称电池(正极极片/正极极片、负极极片/负极极片)。其中对称电池多用于阻抗测试分析,后续会再做讨论。扣式电池由成套的扣式电池壳及内部组件构成,不锈钢电池壳电化学稳定性好、密封性良好、尺寸较小、组装较为简单、价格便宜、适用温度为-40~80 ℃,适合大量测试使用。最近国内外企业开始研制高通量扣式电池自动组装设备,用于电池关键材料的批量加速验证和研发。一般的扣式电池壳型号有CR2032、CR2025、CR2016等,实验室中常采用CR2032型电池壳(即直径为20 mm,厚度为3.2 mm)。扣式电池壳用后则报废,需增加金属回收环节以免浪费和污染环境[4]。Swagelok电池,又称为模拟电池,也经常用于实验室测试,其电池壳采用不锈钢外壳和聚四氟乙烯内胆,可重复使用[5]。Swagelok型电池拆解便捷,适合用于电池拆解分析。但模拟电池相对成本较高,且组装出一致性较好的电池需要规范的训练和一定经验。
扣式电池的充放电模式包括恒流充电、恒压充电、恒流放电、恒阻放电、混合式充放电以及阶跃式等不同模式充放电[6-7]。实验室中常采用恒流充电(CC)、恒流-恒压充电(CC-CV)、恒压充电(CV)、恒流放电(DC)对电池充放电行为进行测试分析,而阶跃式充放电模式则多用于直流内阻、极化和扩散阻抗性能的测试。考虑到活性材料的含量以及极片尺寸对测试电流的影响,恒流充电中常以电流密度形式出现,如mA/g(单位活性物质质量的电流)、mA/cm2(单位极片面积的电流)。充放电电流的大小常采用充放电倍率来表示,即:充放电倍率(C)=充放电电流(mA)/额定容量(mA·h),如额定容量为1000 mA·h的电池以500 mA的电流充放电,则充放电倍率为0.5 C。目前电动汽车用锂离子电池已发布使用的行业标准QCT/743—2006中指出锂离子通用的充放电电流为C/3,因此含C/3的充放电行为测试也常出现在实验室锂离子电池充放电测试中[8]。
倍率性能测试有3种形式,包括采用相同倍率恒流恒压充电,并以不同倍率恒流放电测试,表征和评估锂离子电池在不同放电倍率时的性能;或者采用相同的倍率进行恒流放电,并以不同倍率恒流充电测试,表征电池在不同倍率下的充电性能;以及充放电采用相同倍率进行充放电测试。常采用的充放电倍率有0.02 C,0.05 C,0.1 C,C/3,0.5 C,1 C,2 C,3 C,5 C和10 C等。
对电池的循环性能进行测试时,主要需确定电池的充放电模式,周期性循环至电池容量下降到某一规定值时(通常为额定容量的80%),电池所经历的充放电次数,或者对比循环相同周次后电池剩余容量,以此表征测试电池循环性能。此外,电池的测试环境对其充放电性能有一定的影响。
下文将详细介绍扣式电池组装、充放电测试和数据分析各过程及影响扣式电池测量和数据分析准确性的影响因素。
1 锂离子扣式电池的组装
1.1 极片的制备
1.1.1 材料的选择、称量
实验室用正负极材料可以采购,也可以实验室自行制备,一般为粉末材料,颗粒尺寸不宜过大,便于均匀涂布,同时避免由于颗粒较大导致测试结果受到材料动力学性质的限制较大以及造成的极片不均匀性问题。实验室研究一般最大颗粒直径(max)不超过50mm,工业应用一般max不超过30mm。较大颗粒、团聚体或者纳米级别,需做颗粒筛选和研磨处理。常用导电剂为碳基导电剂,包括乙炔黑(AB)、导电炭黑、Super P、350G等导电材料。常用黏结剂体系包括聚偏氟乙烯-油性体系[即poly(vinylidene fluoride),PVDF体系]以及聚四氟乙烯-水性体系[即poly(fluortetraethylene),一般为乳液,简称PTFE体系],SBR(丁苯橡胶)乳液等。油系溶剂常采用NMP(-甲基吡咯烷酮)。
实验室制备极片时,混料比例和步骤依据测试材料及混料工艺的不同而有差别。如常见的石墨负极极片中,CMC(羧甲基纤维素钠)的含量一般低于10%,SBR的含量一般低于10%,导电添加剂的含量一般低于10%(高倍率电池除外)。而在硅基负极材料中,考虑到硅基负极材料的导电性较差,因此需增加极片中的黏结剂含量和改变导电添加剂的种类,一些研究将CMC的比例调整为20%,SBR的比例调整为20%,导电添加剂中加入CNT(碳纳米管);对于高功率电池极片研发测试时,可以适当增加导电剂的含量,比例可调整为20%左右。高比例黏结剂和导电添加剂是为了充分展示正负极活性材料的电化学特性,而实际锂离子电池中电极极片的黏结剂质量比一般在2%左右,导电添加剂比例一般在1%~2%。
材料的称量应选择精度不低于称量质量1%的电子天平,防止引入较大的称量误差。活性材料及导电剂的称量可以直接粉体称量,黏结剂的称量则是先称量粉体后与对应量的溶剂继续配比制备黏结剂溶液(如PVDF溶于NMP中溶解比例为10%,质量分数),再根据实际加入体积计算其中的黏结剂固体含量。
1.1.2 集流体的选择
锂离子电池极片的正、负极集流体分别为铝箔和铜箔,如果选用单面光滑的箔材,建议在粗糙的一面上涂布,以增加集流体与材料之间的结合力。箔材的厚度没有特殊要求,但对箔材的面密度均匀性有很高要求。如果是硅基负极材料,可以选用涂碳铜箔以提高黏附性,降低接触电阻,增加测试结果的重现性,提高循环性能。
1.1.3 极片涂覆制备工艺
实验室用极片制备过程可分为混料和涂覆两个步骤。其中混料工艺主要包括手工研磨法和机械混浆法,涂覆工艺则包括手工涂覆和机械涂覆。
实验室进行混料时,依据供料的多少来确定采用手工研磨法或机械混浆法,如活性材料的质量在0.1~5.0 g时建议采用手工研磨法,活性材料的质量超过5.0 g时,建议采用实验室用混料机进行混料。实验室中每次混浆量有限,常采用手工涂覆,当浆料足够时可采用小型涂覆机。整个极片制作过程需要在干燥环境下进行,所用材料、设备都需要保持干燥。图1为手工混料、手工涂覆方法制备极片过程,包括材料准备、活性材料和导电剂的称取和研磨、加入黏结剂、浆料研磨、取出浆料手工涂布极片、极片烘烤等步骤。
机械混浆过程中,则包含材料准备、仪器准备、配置黏结剂浆料、加入导电添加剂、配置浆料、加入电极材料配置浆料,涂布以及极片烘烤等步骤(图2)。

图1 手工混料涂覆流程

图2 机械混料、手工涂覆流程
其中要注意的是需先将黏结剂(如PVDF)加入溶剂NMP中,在50 ℃以下搅拌至PVDF完全溶解,然后根据浆料配制比例进行配比。在混料过程中需将黏在壁上的材料处理并混入浆料中,防止因为比例不对造成计算材料比例时出现偏差。混浆过程时间过短或过长、浆料不匀或过细都会影响到极片整体质量和均匀性,并直接影响材料电化学性能发挥及对其的评价。
此外,特别需要注意的是,一般极片的面容量设为2~4 mA·h/cm2,最低不建议低于1 mA·h/cm2,这样的活性物质负载量与工业应用的更为接近,便于准确对标评价材料的倍率和低温特性。个别情况下,可以超过这一负载量,例如针对厚电极的研究。低于这一面容量制作的极片,一方面,称量误差较大;此外,由于极片薄,动力学性能较好,体积变化较小,电解液相对远远过量,这样有利于测到材料的最高容量,但半电池测到的倍率、循环性有可能会显著高于实际全电池工作条件下的性能,此时的动力学及循环性数据结果并不能和大容量实际电池有较好的对应关系。当然,即便和实际体系的要求有差异,但如果所有材料按照同一极片的制作条件来对比,对于比较材料的性能差异也有一定意义。但不同极片制作条件下的动力学、循环性能数据对比,往往可靠性低,而实验室手工制作的薄极片的一致性往往很难保证。
1.1.4 极片干燥条件、辊压工艺、极片压切与称量、真空烘烤
极片的干燥一般需要考虑3点,烘烤温度、烘烤时间、烘烤环境,对于NMP油系的烘烤温度需要100 ℃以上,在能够烘干的前提下,尽量降低烘烤温度,增加烘烤时间。对于一些容易氧化或者在高温空气中不稳定的材料,需要在惰性气氛烘箱中烘烤。还可以通过直接测量极片水分含量来确定干燥条件。
极片的辊压过程中需要将极片压实,压实密度尽量接近工业中极片的压实密度。为了测量材料的动力学极限,可以按研究目的调控压实密度。
将制备好的极片,用称量纸上下夹好,放到冲压机上冲出小极片(图3),小极片直径可根据冲压机的冲口模具尺寸进行调整,实验室常采用直径为14 mm(对应CR2032扣式电池)冲口模具。对冲好的小极片进行优劣选择,尽量挑选形貌规则、表面及边缘平整的极片,若极片边缘有毛刺或起料,可采用小毛刷进行轻微处理。冲压制备的小极片数量根据测试要求和涂片面积进行调整,一般用于充放电测试的极片数量不低于5片(建议挑选8片以上完整测试极片)。

图3 手工冲压极片流程
将挑选合格后的小极片移到精度较高的天平(精度不低于0.01 mg)进行称量,称好的极片放到待装电池的袋子里,并记录对应数据(图4)。除了极片的质量称量之外,在采用厚度仪对极片的厚度进行测量时,多个极片的测量数值误差在3%以内则认为该极片厚度均一性良好,并记录厚度平均值。

图4 冲压后的极片称量及标记
将称好的极片放入真空干燥箱,抽真空至0.1 MPa,设定干燥温度和时间,可以采用120 ℃烘烤6 h,这一步骤的目的是进一步去除极片中的水分。启动运行升温后建议标注实验信息(图5),防止其它人误操作。
1.2 双面极片处理方法
在实验室测试分析中,还包括对一些工业生产线上制备极片以及从电芯拆解取出极片的电化学性能进行分析评估。上述极片多为双面涂覆极片,因此在组装扣式电池测试之前需将双面极片处理成单面极片(暴露出集流体)。常用的处理方法包括刮刀法、擦拭法以及背面贴胶法。
刮刀法主要采用手术刀对目标极片一侧进行刮划,可直接在手套箱内操作,但该方法较易损伤集流体,且耗时较长,不建议采用。
擦拭法需要采用水作溶剂对负极片一侧进行擦拭,正极片则可采用NMP(-甲基吡咯烷酮)作溶剂擦拭。擦拭至背面无明显活性材料(目视观测即可)后,用冲压机进行冲片处理,制备成标准尺寸的单面极片。该方法操作简单,但易出现溶剂渗透或气氛渗透,对极片另一侧表面产生影响。另外,该方法难以制备极片边缘处样品,多用于制备极片中心区域样品。
背面贴胶法是中国科学院物理研究所(以下简称物理所)失效分析团队近期发展的一种双面极片处理方法,即采用边缘折叠和背面贴导电胶,将目标极片的背面包裹于集流体和导电胶内部,形成单面极片。该方法操作简便,可以方便地在双面极片上任意部位取样制作单面极片,整个过程可以在手套箱内完成[9]。
单面处理后的目标极片样品需要进行清洗,目的是去除极片表面的锂盐和残余电解液。常采用的方法是将单面极片浸泡于DMC等溶剂中6~8 h,或用钝头镊子夹起目标极片样品,并利用移液器或滴管吸取DMC,对目标极片含活性物质一侧进行正面冲洗数次,或者两种方法结合使用。清洗后,将极片置于真空舱内,真空干燥去除溶剂。清洗及真空干燥均在手套箱内进行。干燥后的极片可置于平整的模具中以保持极片平整,方便后期扣式电池组装。
1.3 扣式电池组装方法
将准备好的极片转移到惰性气氛手套箱内,准备扣式电池组装部件:负极壳、金属锂片、隔膜、垫片、弹簧片、正极壳、电解液,此外还需要压片模具、移液器和绝缘镊子。
组装过程如下图所示:将负极壳平放于绝缘台面,将金属锂片置于负极壳中心,并用压片模具对金属锂片进行平整化处理,然后将隔膜平放于锂片上层,用移液器取适量电解液滴加入隔膜表面。用绝缘镊子将测试极片、垫片、弹簧片和正极壳依次置于隔膜上层,其中测试极片的活性材料一侧需贴近隔膜(图6)[10]。进一步,用绝缘镊子将扣式电池负极侧朝上置于扣式电池封口机模具上,可用纸巾垫于电池上方以吸收溢出的电解液,调整压力(一般为800 Pa)压制5 s完成组装制备扣式电池,用绝缘镊子取出,观察制备外观是否完整(图7)并用纸巾擦拭干净。

图6 扣式电池组装流程

图7 扣式电池封装流程
模拟电池的组装过程与扣式电池相似,以物理所自行设计的模拟电池组装为例[11],需准备组装材料包括:模拟电池模具(一个聚四氟乙烯内胆,一个聚四氟乙烯套管,正负极壳和金属导体柱),金属锂片,隔膜,电解液及待测极片。其中待测极片尺寸不能超过聚四氟乙烯内胆尺寸。依照图8,将金属锂片、隔膜、聚四氟乙烯内胆依次放入负极壳模具内,然后用移液器滴加一定量电解液,并将待测极片和金属导体柱依次放入内胆中,保证活性材料一侧贴近隔膜。进一步地,将套有聚四氟乙烯套管的正极壳模具安装在负极壳模具上,完成模拟电池的组装。

图8 模拟电池组装流程图
1.4 实验室扣式电池制备中的注意事项
1.4.1 金属锂片、隔膜、电解液的选择和处理
实验室用金属锂片能够提供远远过量的锂源 (1 mA·h/cm2相当于5mm厚锂箔,实际购买的锂片往往在400~500mm,相当于80~100 mA·h/cm2, 工业级别的正负极极片单面容量一般在2~ 4 mA·h/cm2),杂质少且尺寸需大于待测极片,一般可从相关企业或供应商处直接采购惰性气氛保护下的金属锂片,并于惰性气氛保护手套箱内拆解、使用。要求使用锂片纯度不低于99.9%,用于制备扣式半电池时经常采用直径15~15.8 mm(对应极片尺寸为14 mm的CR2032扣式电池),厚度0.5~0.8 mm,表面平直、银白色光亮、无油斑、穿孔和撕裂。
隔膜的类型需根据实验要求进行选择,一般为具有纳米孔隙的绝缘膜,吸附电解液后可允许离子双向传输,常采用单层或多层的聚乙烯或聚丙烯隔膜,一般选择采购商业隔膜,并采用冲片机隔膜制备成尺寸规则的圆形,尺寸需大于金属锂片和待测极片以便隔离正负极片,通常与扣式电池壳的内径相同(如CR2032的使用隔膜直径为15.5~16.5 mm)。实验室中常采用Celgard2400或Celgard2500型号的工业用聚丙烯膜。
在组装实验室用扣式锂离子电池时,通常选择LiPF6体系电解液[如磷酸铁锂电池的电解液一般为浓度1 mol/L的LiPF6溶液,以EC/DEC为1∶1(体积比)混合液作为溶剂[12]],并且可根据实验要求进行选择,如选择普通配比电解液、含有某种或多种添加剂的电解液等。扣式电池组装时电解液的使用量通常为过量,如在扣式电池2032中电解液的使用量一般为100~150mL,在模拟电池中电解液的使用量一般为200mL。如需进行长循环测试,可对电解液的量进行适当增加。
1.4.2 制备极片及电池的优劣选择
制备后的极片表面平整,无明显大颗粒物,且在烘烤、常温冷却、转移过程中无明显掉料现象,可初步判断极片制备合格。进一步可通过对极片的质量、厚度、冲片后边缘的掉料程度进行对比,如果极片的质量、厚度相差很大,极片圆片的边缘掉料有好有坏,说明极片制备的并不合格。应选择其中质量、厚度和边缘掉料均一的极片组装电池进行测试。
制备好的扣式电池和模拟电池外壳模具平整无损坏,表面无腐蚀痕迹、无明显漏液现象。采用万用表或电池测试仪对制备电池进行开路电压测试,正极材料半电池开路电压在3 V以上,负极材料半电池开路电压在2.5~3.5 V内,表明组装电池无明显短路情况,若开路电压异常则可视为组装电池不合格。在筛选合格的扣式电池正极壳上用记号笔标注必要电池信息。
1.4.3 其它注意事项
在以金属锂作为负极的扣式半电池中,全电池中的负极材料此时实际上在扣式电池中也是正极。在扣式电池中需保证隔膜的直径>锂片的直径>极片的直径。在用镊子移动整个扣式电池的时候,需要采用绝缘镊子,防止正负极接触短路。为保证后期电化学测试项目及考虑到误差和操作失误,实验室组装同一种材料的扣式电池或模拟电池数量一般不低于5个。
扣式电池和模拟电池制备过程放置锂片步骤,需将锂片边缘光滑面朝隔膜一侧放置,必要时可以用平整的与锂不反应的硬物压平金属锂片的表面,以防止锂片边缘毛刺穿破隔膜导致电池短路。扣式电池和模拟电池各组件在使用前需进行清洗,其中不锈钢部件可分别用去油污清洁剂、丙酮、乙醇、水依次进行超声清洗,在使用去油污清洁剂清洗时可适当提高清洗温度达到去除部件表面油污的目的。聚四氟乙烯部件则使用除丙酮以外的其它几种试剂进行清洗。清洗后的部件需在烘箱中进行烘干处理。模拟电池组装放置极片时,需注意极片易发生移动翻转。使用镊子调整时容易发生极片破损和电解液侧漏,建议使用钝头绝缘镊子处理。
2 充放电测试方法
2.1 实验仪器介绍
锂电池的充放电测试一般采用恒流-恒压充电、恒流放电模式,记录该过程中的测试时间、电压和电流等数据,通过分析该过程中数据的变化来表征电池或材料的容量、库仑效率、充放电平台以及电池内部参数变化等电化学性能参数。
现阶段国内外相关单位使用的电池测试系统包括Arbin公司的电池测试系统、新威公司的电池测试系统、蓝电公司的系列电池测试系统以及MACCOR公司的电池测试系统等[13],见表1。此外拜特电池测试系统和Bitrode电池测试系统则多用于大容量电池、电池组等装置的测试分析。一些电化学工作站也具有扣式锂电池电化学性能测试功能,但由于通道设计、功能设计等原因,多用于电池的循环伏安法测试分析、阻抗测试及短时间的充放电测试,电化学工作站仪器厂家包括Autolab、Solartron、VMP3、Princeton、Zahner(IM6)、上海辰华等。
在实验室锂电池的测试过程中,还经常要用到防爆箱和恒温箱(图9)。实验室用电池防爆箱多用于大容量电池的测试,在研究扣式电池一些特殊性能测试的时候也会用到,如高倍率、高温性能测试等。实验室用恒温箱温控多为25 ℃,且实际温度与设定温度间的温差精度不超过1 ℃。在电池的高低温性能测试中,最低温度可达到-70 ℃,最高温度可达150 ℃。考虑到宽温度范围的恒温箱价格较贵,且应用较为集中,因此建议多台恒温箱设定不同温度集中测试使用,即同一种验证材料组装多支扣式电池分别测试常温及高低温性能,实验室测试常用温度为25 ℃、55 ℃和80 ℃(图10)。在选择恒温箱时,尽量采用专门用于电池测试的恒温箱,此类恒温箱含有专业的绝缘绝热口用于连接电池测试导线。电池在连接测试夹具时,需使用绝缘镊子,且测试电池需整齐置于防爆箱或恒温箱内,设定测试温度,待温度达到设定温度后开启电池测试程序,测试过程中建议贴标签注释测试信息(图11)。

表1 几种电池测试系统主要性能对比

图9 实验室用电池防爆箱和恒温箱

图10 不同设定温度的实验室用恒温箱

图11 恒温箱中扣式电池安装图
2.2 充放电测试常规实验流程
将测试电池安装在测试仪器上,置于(25±1)℃测试环境中。设置以下程序:静置10 min;以1.0 C电流恒流充电至4.2 V,然后恒压充电至电流下降至 0.05 C,充电停止;静置5 min;然后以1.0 C电流恒流放电至3.0 V;重复上述充放电步骤5~10次。
上述测试参数为常规全电池测试参数,一般正极材料/金属锂扣式电池的电压范围为3.0~4.3 V,负极材料/金属锂扣式电池的电压范围为0.005~1.0 V,特殊高电压正极材料(如高电压钴酸锂、尖晶石镍锰酸锂、富锂锰基层状氧化物等材料)或其它正极材料(如磷酸铁锂材料)可依据电极材料特性和电解液、固态电解质耐受氧化电压进行电压范围调整,其它参数不变。负极材料/金属锂扣式电池以及无锂正极材料(如MnO2等)/金属锂扣式电池在测试时首先放电至最低电压窗口,然后进行充电。需要注意的是,目前在许多文章中的负极材料测试范围为0.005~3.0 V,而在全电池测试过程中,一般能够采用的电压范围对应于负极半电池测试实际上不超过1.0 V,例如对于石墨或者硅基负极材料,可用的电压范围为0.005~0.8 V,对于钛酸锂这种负极材料,可用的电压范围为1.2~1.9 V。因此对于某些文章中在宽电压范围内获得的高容量和高首次库仑效率,其在全电池中并不能发挥出来,实际意义并不大。针对软碳或硬碳负极材料,或者目前正在开发的复合金属锂负极材料,放电截止电压可以更低,如0 mV甚至-50 mV,具体情况需要具体分析。建议多数负极材料的半电池测试控制电压范围在0.005~1.0 V,超过这个电压范围,在结果的陈述及应用前景的描述上需要特别声明,以免夸大结果。
测试电池材料实际容量的时候,尽量使用小倍率进行充放电,以减小极化产生的容量误差,得到电池的真实容量,一般选择0.1 C的倍率进行测试。
操作人员在测试仪器上装卸扣式电池时需佩戴绝缘手套及口罩和防护眼镜;由于测试通道较多,需对测试电池、测试通道进行特殊标记,并在相关仪器前贴醒目标签注释以防他人误操作。
2.3 倍率充放电测试常规实验流程
倍率充放电测试一般分为3种形式,相同倍率充电不同倍率放电、不同倍率充电相同倍率放电和不同的倍率充放电测试。下面以充放电电压窗口为3.0~4.2 V的扣式电池测试为例进行介绍。
电池连接测试仪器并置于稳态环境中,静置 5 min;以0.5 C电流放电至3.0 V,静置10 min后以0.5 C恒流充电至4.2 V,在4.2 V恒压至电流下降为0.05 C截止,然后以不同形式进行倍率充放电测试。
相同倍率充电不同倍率放电的实验流程为:静置5 min后以不同的倍率放电至3.0 V,并记录放电容量,静置10 min后以0.5 C恒流充电至4.2 V,在4.2 V恒压至电流下降为0.05 C截止。
不同倍率充电相同倍率放电的实验流程为:静置5 min后,以0.5 C倍率恒流放电至3.0 V,静置10分钟,然后以不同倍率恒流充电至4.2 V,在4.2 V恒压至电流下降为0.05 C截止。
不同的倍率充放电的实验流程为:静置5 min后,以不同的倍率恒流放电至3.0 V,静置10 min,然后以相同的倍率(电流)进行恒流充电至4.2 V,在4.2 V恒压至电流下降为0.05 C截止。
根据测试形式,改变不同的倍率重复上述某个实验流程,充放电倍率由低到高(一般为0.2 C、0.5 C、1 C、2 C以及5 C等更高倍率)。建议相同倍率充放电循环5~10次。
2.4 充放电循环测试常规实验流程
在对电池的循环性进行测试时,可在上述充放电测试(2.2节内容)的基础上,增加循环次数,对比相同循环次数后的容量保持率。或重复充放电循环,当放电容量连续两次低于初始放电容量的80%时,确定此时的循环周数。
2.5 高低温测试常规实验流程
锂离子电池高低温性能测试中,高温性能测试一般设置为45 ℃、55 ℃、80 ℃或更高温度,低温性能测试一般设置为0 ℃、-10 ℃、-20 ℃、-30 ℃或-40 ℃,测试流程同2.2、2.3、2.4节内容。
测试数据需要与室温的数据进行对比,因此在高低温测试之前需进行常温的充放电测试(即2.2测试内容)。而在进行放电效率测试的时候,建议采用室温(25±1)℃下进行恒流-恒压(CC-CV)模式充电至100%SOC,在不同温度下静置30 min后进行恒流放电(DC)。
3 数据分析
3.1 充放电测试数据分析
3.1.1 基本数据分析
(1)电压分析
组装的锂离子电池的开路电压是指外电路没有电流通过时的正负极电位差,可通过万用表(精确度不低于0.1 mV,建议采用高内阻抗的专用电压表防止自放电)直接测量,或连接至电池测试系统后直接读取数值[14]。该值仅为组装电池后的初始开路电压,全SOC下的开路电压需通过恒电流间歇滴定(GITT)方法测得[15],将在后续文章中介绍。工作电压则是指外电路有电流通过时正负极即时电位差,可直接体现在电池测试系统数据中。工作电压=0±SR,式中,0为热力学平衡电压,R为扣式电池内部或接触存在的某一种电阻,如某一结构组元的欧姆电阻、电荷转移阻抗、扩散阻抗,为测试电流。工作电压与电流大小有关。
(2)容量分析
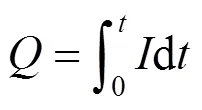
对于测试的电池材料来说,容量分析一般需要确定3个数据:首次充电容量、首次放电容量(正极材料)和可逆容量。其中,首次充电容量即为锂离子电池首次充电结束时的充电容量,首次放电容量即为锂离子电池首次放电结束时的放电容量,可逆容量则为电池循环稳定后的容量值(常温下测试值又称额定容量),一般选取第3~5周的放电容量,有时可能需要选取10周以后的放电容量。在实际应用中,对测试材料或极片的克容量、面容量及体积容量的分析更具有参考价值。如克容量即单位活性物质质量的放电容量,=/;面容量即单位测试极片面积的放电容量,=/;体积容量即单位极片体积的放电容量,=/。式中,为放电比容量mA·h/g(毫安时每克)、mA·h/cm2(毫安时每平方厘米)或mA·h/cm3(毫安时每立方厘米),为放电容量mA·h(毫安时),为活性材料的质量g(克),为测试极片面积cm2(平方厘米),为测试极片的体积cm3(立方厘米)。克容量参数用于对比测试材料的性能更加直观,而面容量和体积容量对于测试材料的实际应用,正负极容量匹配时则更具有参考价值。建议发表文章时同时提供3种比容量的信息。
扣式电池数据也可以评价正极活性材料的能量密度(W),指的是单位质量的正极活性材料所能够存储和释放的能量,=/,即放电平均电压与克容量的乘积,常用单位为W·h/kg(常称为比能量),也包括体积能量密度W·h/L。一般电芯中正极活性物质占的质量比为30%~50%,具体比例取决于正极材料的压实密度和真实密度。因此,根据正极活性物质的能量密度,也可以粗略估算相应的全电池的能量密度,这对于没有条件研制全电池,但又希望评价正极材料和预测电芯能量密度具有参考意义。
3.1.2 充放电曲线分析
充放电曲线体现的是电池材料的充放电行为,对扣式电池充放电曲线进行分析对理解材料的性能及电化学行为有着重要意义,尤其对半电池充放电曲线的分析,能够针对性地分析某一种材料的特性行为。充放电曲线有几种不同的展现形式,如较为常见的“交叉式”曲线(图12)以及“循环式”曲线(图13)。

图12 几种不同材料组装半电池的“交叉式”充放电曲线

图13 几种不同材料组装半电池的“循环式”充放电曲线
从扣式电池充放电曲线中可读取大量数据信息,下面对部分数据的读取和分析做简单介绍。
正负极材料内锂离子的脱嵌对应了充放电曲线上的平台或斜坡区域(以及循环伏安曲线和微分差容曲线中的氧化还原峰),根据每个平台区域的变化可分析研究材料的电化学反应行为。通常充电和放电的电位平台或斜坡的数量相同,若充电和放电的总容量相同,但对应的每个平台/斜坡的容量有差异,则说明材料嵌脱锂的热力学反应路径或嵌脱锂动力学特性有显著差异。图14为典型的石墨负极材料的充放电曲线。充放电曲线显示,石墨/金属锂片半电池充放电时,石墨电极充放电过程中分别存在0.08/0.1 V,0.11/0.14 V以及0.2/0.22 V处3个对应明显的充放电平台,分别对应了3个锂石墨层间化合物的两相转变过程[16]。平台的起始点,对应相变的开始,平台的终止点,对应相变的结束点,平台行为意味着主体材料的电化学势与离子在材料中的占有率无关。充放电曲线中的斜坡一般对应于固溶体反应或者电容行为[17],斜坡行为意味着主体材料的电化学势与离子在材料中的占有率直接关联。因此,通过充放电曲线可以初步判断材料在反应过程中有几次相变反应,是两相转变反应还是固溶体、吸脱附电容行为,这可以辅助指导X射线衍射等结构研究[18-19]。在同一个SOC下,小电流充放电时,充电电位平台与放电电位平台电压的中间值近似为热力学平衡电位,用循环伏安曲线或微分差容曲线对应的氧化峰与还原峰的中间电位值更容易准确估算。全SOC下准确的热力学平衡电位的测量建议采用低电流密度下的GITT方法。

图14 石墨/金属锂片扣式半电池的充放电曲线
在全电池放电行为中,电池的放电电压为正极材料的嵌锂电压减去负极材料的脱锂电压,因此负极的平均脱锂平台越高,则全电池的放电电压越低。当负极材料的脱锂平台超过2.0 V时,全电池电压已经很低了,此时测到的容量对全电池匹配和实际应用的意义不大,因为每种电器应用都有允许的下限电压范围,如一般用于消费电子电器的锂离子电池的放电电压截止到2.7 V。
能量效率即同一循环周次的放电能量与充电能量的比值,可以表示为=(DD)/(CC)×100%。在充放电曲线中,可近似于充放电曲线的积分面积差,该值的变化在“循环式”充放电曲线中更容易读取。典型的锂离子电池的能量效率在92%~95%,锂硫电池和锂空气电池的能量效率则分别在80%和70%左右[20]。
对前5周充放电循环数据进行分析,可获得首周放电容量、首周充电容量、首周库仑效率、可逆容量、极化电压和电阻大小、能量效率等信息。
首周充放电数据最为重要。首周放电容量可在曲线中直接读取,用于分析首周循环后极片实际释放容量。电池的首周充放电平台奠定了后续循环的基础,多数材料的结构是否稳定也是由第1周产生的,平台长短也影响着锂离子的嵌入脱出效率。第2周及后面的充放电容量也基本都是在首周放电容量的基础上涨落。库仑效率(即充放电效率)是指同一循环过程中电池放电容量与充电容量之比,即=D/C×100%,首周库仑效率(即首效)则是电池在第1周的放电容量与充电容量的比值(正极材料=D1/C1×100%)。多款电池测试系统均可直接输出该值,用于分析首周循环过程中活化及其它反应消耗的极片容量的情况,并且可直接表征材料结构的稳定性和动力学性能的优劣。
首次放电容量及首周库仑效率可直接影响全电池的设计与材料的评价。前5周的库仑效率一般会呈现先增后降或小幅波动的趋势,这是由于在前几周的循环过程中存在SEI膜生长、材料活化等反应引起活性锂源的不可逆损失[21]。以新鲜负极材料的半电池为例,其首次放电容量则高于首次充电容量,即负极首次嵌锂量要多于负极首次脱锂量。如果测试结果相反,则可能是由于非新鲜极片或电池短路等因素导致。
最高容量,即测试电池充放电过程中表现出来的容量最高数值,一般出现在前五周的充放电过程中。有些负极材料的测试结果显示可逆容量随着循环次数增加而持续增长,这与材料的持续氧化、缓慢活化、SEI膜持续增长、其它材料逐渐参与氧化反应有关。这类负极材料对于锂离子全电池的设计和应用来说是缺点而不是优点。一般而言,电池测量的可逆容量会在前5周趋于相对稳定,库仑效率不能很快达到99.95%意味着界面或材料结构一直不稳定,这样的材料用于全电池测试,相对于半电池,循环性会差很多。
3.1.3 极化情况分析
在锂电池的充放电过程中,极化是不可避免的,尤其在高倍率充放电过程中。研究由极化引起的容量变化以及根据充放电曲线分析极化情况十分必要,相对于通过GITT、恒电压间歇滴定(PITT)或电化学交流阻抗谱(EIS)分析电极过程动力学,通过充放电曲线获取的动力学信息更加直观。通常较低充放电倍率(如0.05 C、0.02 C、0.01 C或更低倍率,取决于材料)下测得的容量可基本忽视极化引起的容量变化。某倍率下测试得到的容量值与上述低倍率下测试的容量值差则可视为极化引起的容量变化。在恒流-恒压(CC-CV)充电恒流放电曲线中,可通过充电曲线中恒流充电容量与恒压充电容量所占总容量的比值来表征极化情况。恒流充电容量与总充电容量比值越低或恒压充电容量与总充电容量比值越高,则极化越大。此外,充放电曲线中充放电平台电压差值增加也可反映出电极极化的增加,该差值在“循环式”充放电曲线中更易读取。可通过在该曲线的充放电曲线的纵轴差距进行初步认识,如图15中,富锂正极材料(Li1.2Ni0.13Co0.13Mn0.54O2)的充放电曲线,对比第1周循环曲线,第2周循环曲线的纵轴差距较小,表明极化下降。此外,该值也可由微分差容曲线中嵌脱锂峰位的电位差进行表征,电位差变大,极化则增加[22]。
3.1.4 微分曲线分析
在对电池充放电曲线进行分析的过程中,为了方便充放电曲线的研究,将该曲线进行微分处理,将平台区域转换为峰曲线。通常使用的方法是微分差容曲线(incremental capacity,d/d.)和微分电压曲线(differential voltage,d/d.)对充放电曲线进行分析[23]。
其中微分差容曲线,简称IC曲线(图16[24]),应用较为广泛,但由于存在电压平台(即d=0),数据处理需谨慎。曲线中的氧化峰和还原峰对应了充放电曲线中的充电平台和放电平台,并且与循环伏安曲线中的氧化峰和还原峰有着对应关系。根据该曲线中峰位,参考文献可对氧化还原反应进行确认和判断。将同循环周次充放电曲线都进行微分处理并进行峰位比对展现,对应氧化还原峰电位的中间值则为热力学平衡电位。此外,峰位的移动和衰减也具有一定的对比价值。如峰位的移动则表明该电位附近的充放电平台电位出现移动,与材料的结构变化引起锂的嵌入脱出难易有关;某峰位的强度变化可表征该电位的充放电平台长短变化。
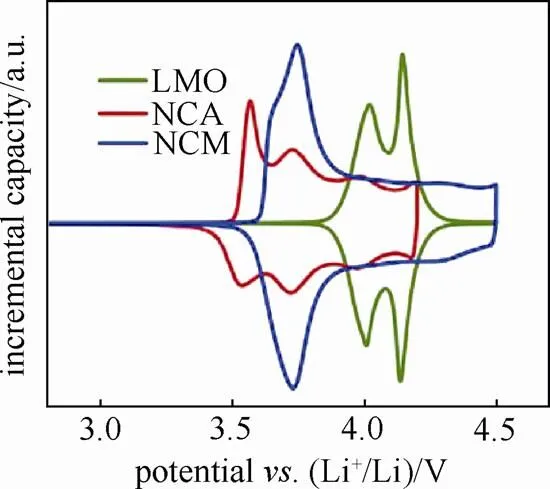
图16 几种正极材料半电池的微分差容曲线[24](版权属于Journal of Power Sources杂志)
微分电压曲线,简称d曲线,可根据文献或实验对比曲线峰位归属,并根据峰位的横坐标来初步判断不同材料或平台的容量发挥情况,该曲线的数据处理较为方便,且多用于混合材料极片的分析中。图17所示为硅碳混合材料/金属锂片半电池放电过程的d曲线,通过对比分析可以得出,在第三周循环放电容量中,硅材料发挥容量为293 mA·h,石墨发挥容量为697.6 mA·h,并且硅和石墨发挥容量随循环均有所降低[25]。
需要说明的是,微分电容和微分电压曲线的数据是否光滑、与充放电仪的电压测量精度、电流控制精度、测试时的温度稳定性、采样点的密度都有影响。
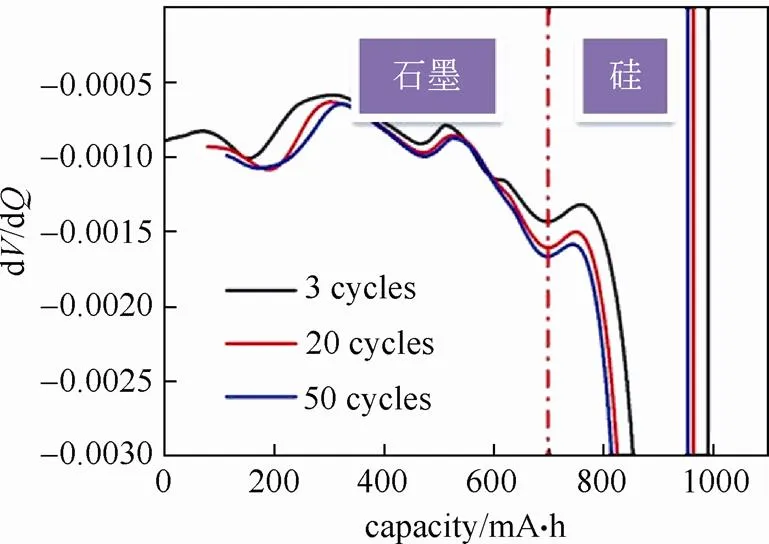
图17 硅碳混合材料/金属锂片半电池放电过程的微分电压曲线[25]
3.2 倍率充放电测试数据分析
在上述文章中提及的3种倍率充放电测试,相同倍率充电不同倍率放电的测试应用较多,用于测试材料的放电功率特性;不同倍率充电相同倍率放电的测试多用于“快充”材料和技术;不同的倍率充放电测试多用于功率型电池材料的性能测试。
以相同倍率充电不同倍率放电的测试为例对倍率充放电测试数据分析进行介绍。如以0.2 C电流放电至3.0 V并计算(或在测试仪器配套软件中读取)放电容量0.2C;以0.5 C电流放电至3.0 V并计算放电容量0.5C;以1.0 C电流放电至3.0 V并计算放电容量1C;以2.0 C电流放电至3.0 V并计算放电容量2C。
容量比率计算如下:设定0.2 C放电容量比率为100%;0.5 C下的容量比率为0.5c=0.5C/0.2C×100%;1 C下的容量比率为1c=1C/0.2C×100%;2 C下的容量比率为2c=2C/0.2C×100%。
根据容量比率值对电池的倍率性能做出一定判断,例如设定容量比率为80%为合格,而低于80%的放电倍率则不符合测试电池或材料的放电要求。可定义最接近且高于80%容量比率的倍率为该电池或材料的最大放电倍率,注意这一定义和全电池测试时的脉冲功率不一样。在许多公开发表的文章中,经常可以看到作者测试了很高的倍率,而高倍率充放电时,容量保持率已经远远低于80%的0.2 C下的可逆容量,此时再宣称倍率性能非常好,没有太大意义。如图18所示,该材料在超过3 C的倍率下充放电引起容量衰减加快[26]。特别需要指出,目前的高功率锂离子电池可以实现15~20 C的放电,2000~4000 W/kg的脉冲放电能力。在对比说明材料倍率性能优异时,需要说清楚室温下容量保持率在80%的最高倍率是多少,这样便于比较。此外,扣式电池测试的倍率特性和全电池测试的倍率相比,有时各有优势,取决于具体的设计,根据扣式电池的倍率测量结果下结论需要特别慎重,最好是从本征动力学参数上解释清楚为何可以实现高功率,并计算出理论上的倍率特性。不同材料之间,不同团队测试结果的倍率特性的比较需要在同一或接近的材料、电极、电芯的测试条件下比较。
除了容量比率的分析之外,对电池不同倍率充放电时的库仑效率的分析也有着重要意义。当在某个倍率(一般为高倍率)充放电时,库仑效率的变化可用于分析电池可能产生锂枝晶以及电池体系动力学性能优劣。
研究电池材料不同倍率下的放电性能可使用电池的功率密度进行表征,即单位质量的活性材料放电时能量输出的快慢。功率密度=/,式中,为电池放电平均电压,为放电电流,为活性材料的质量。单位为W/kg或W/L。
在电池充放电过程中,某个放电平台的中值电压与开路电压(热力学平衡电压)的差值被称为放电过电位。不同倍率下的过电位分析对理解材料的动力学性能十分重要。可将不同倍率下的过电位与充放电电流进行对应作图并分析。当过电位与电流呈线性关系,则动力学速率控制步骤为欧姆电阻;当过电位与电流的平方根呈线性关系,则为扩散控制过程;当过电位与电流的对数值呈直线关系,则为电荷转移过程。图19为LiFe1-xMnPO4材料不同电流密度下Mn放电平台的过电位与电流的对应图,根据该曲线可分析Mn的放电区域中,倍率控制为扩散控制,并非电荷转移。同时,可从图19(a)中得出,将近似的线性曲线进行反向延伸与原点接近(即电流密度平方根为0时,过电位也为0),表明该区域产生的过电位主要来源于电荷转移,并非其它热力学因素导致[22]。图20中,显示在电流密度为0时,仍有过电压,则表明存在导致电位差的热力学因素[27]。需要注意的是,某平台的中值电压通过微分曲线中的峰位进行读取更为准确。

图19 LiFe1−xMnxPO4/C电池中Mn区域过电位与不同电流密度对应曲线
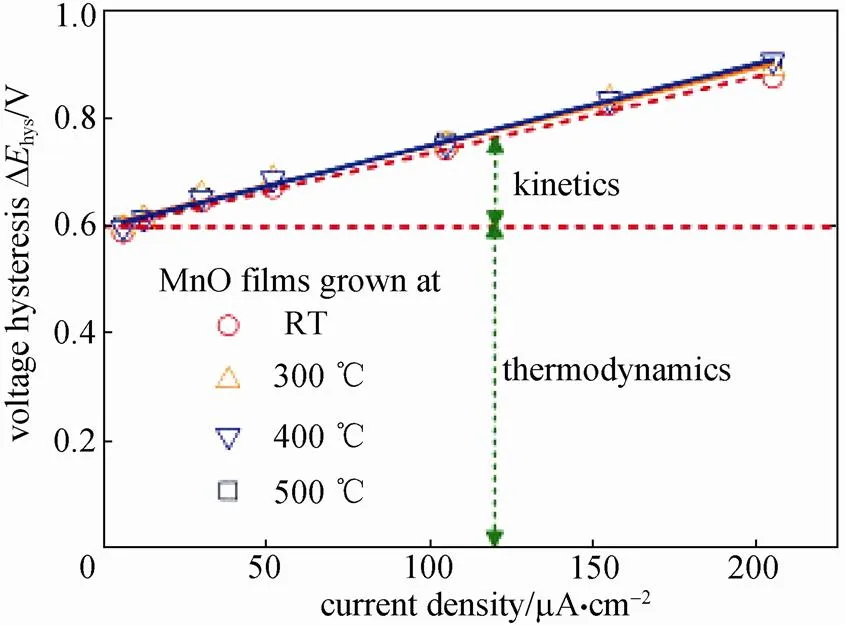
图20 不同温度制备的MnO薄膜电极在不同电流密度下的过电位
3.3 充放电循环测试数据分析
对充放电循环测试曲线的展现可以是充放电行为随时间的变化图、性能参数(如充放电容量、库仑效率等)随循环周次的变化图以及某些周次充放电行为的叠加图。其中,充放电行为随时间的变化图是基础输出信息,另外两个图则是测试软件处理或根据基础输出信息读取的数据,并且性能参数随循环周次变化图以及某些周次的充放电行为叠加图为常见的循环信息展示,如图21所示。根据性能参数循环图,可对电池充放电容量、库仑效率变化进行直观判断,对电池循环性能以及可能存在容量“跳水”、电池析锂等情况进行分析判断。组装后的扣式电池在循环过程中会存在一定的衰减情况,对电池容量衰减率随循环周次变化的分析对材料性能分析、全电池设计、电池失效预判有着十分重要的意义。不同材料在相同循环周次或相同材料不同周次的剩余容量也是重要的对比参数。对不同循环周次、存在的容量“跳水”行为或其它异常循环行为的特征性周次的充放电曲线进行叠加对比,则可对材料循环过程中的充放电行为变化进行表征,如平台的数量及长度变化等,可对材料结构在循环过程中可能产生的变化进行初步判断。
需要提到的是,在循环性能中库仑效率的展示需要对纵坐标范围进行调整。大多数文献中,库仑效率在循环5周以后呈水平直线,接近100%。而在实际反应中,库仑效率的变化较为微弱,而有效的展示有助于对材料性能及反应过程的精准理解。因此,建议将库仑效率展示范围定义在95%~105%之间,曲线波动较大的可适当放宽范围,如图22所示。文献中往往展示的是0~110%,看起来库仑效率接近100%,很稳定。但这种障眼法对于开发材料和电池来说会掩盖电芯中发生的副反应及自放电行为,不利于全面解决问题,到了全电池测试问题会更明显地暴露出来。除此之外,“交叉式”充放电曲线更容易展示库仑效率,因此循环充放电曲线的重叠也可以用于直观判断电池库仑效率的变化。


除了100%DOD放电循环模式之外,对电池进行满充及不同DOD放电循环来对电池材料的非满充满放状态下的循环性能进行测试也具有一定意义。通常为满充后50%或70%DOD放电循环。
在长循环测试过程中,充放电曲线的变化规律可用于分析电池极化及材料性能的变化情况。另外,可在循环一定周期后(如循环50周)设置低倍率(低于0.1 C)充放电一次,用于分析极化等因素对循环性能的影响。
特别需要说明的是,在高倍率下测量的循环性不代表材料在低倍率下拥有同样的循环性,高倍率充放电有时候意味着较浅的充放电深度,反而拥有更好的循环性。此外,不同的电位范围测量获得循环性差别很大。循环性需要结合高低倍率、高低温条件来测量,讨论循环性,也需要明确测量的条件,不能以偏概全。此外,扣式电池测量循环性,特别是半电池,往往还受负极金属锂循环性的显著影响,这一点对于大容量的极片尤其突出。
3.4 高低温充放电测试数据分析
在电池的高低温充放电测试中,分析的数据包括电池容量变化、放电平均电压变化、充放电曲线、循环数据以及极化分析等。其中对电池容量和平均放电电压的变化分析对表征材料的高低温性能最为直接、有效。放电效率测试则更多用于分析电池低温性能。
在高温下,影响材料中锂离子扩散的动力学和热力学性能会有所改善,但高温会加速极片表面副反应,导致SEI膜增厚引起阻抗增加,降低锂离子在活性材料表面的扩散速率。在低温下,材料中锂离子扩散的动力学和热力学性能则会降低,加之电解液黏度增大,导致锂离子扩散阻力更大。对比分析高低温下锂离子电池充放电曲线,对电池及材料可能存在的性能不足可以进行更充分的表征和分析;高温测试还可以起到加速老化分析的作用。图23为LiCoO2/MCMB电池在不同低温条件下的充电和放电曲线[28]。充电曲线显示随充电温度的下降,整体电池容量有所下降,且恒压充电比例增高,即电池出现极化增大。放电曲线显示随放电温度的下降,放电容量和放电平均电压也随之下降。负极表面易在低温循环时形成锂镀层或锂枝晶,这一点可根据低温下充放电过程中库仑效率的变化以及充放电曲线的异常进行分析和预判。
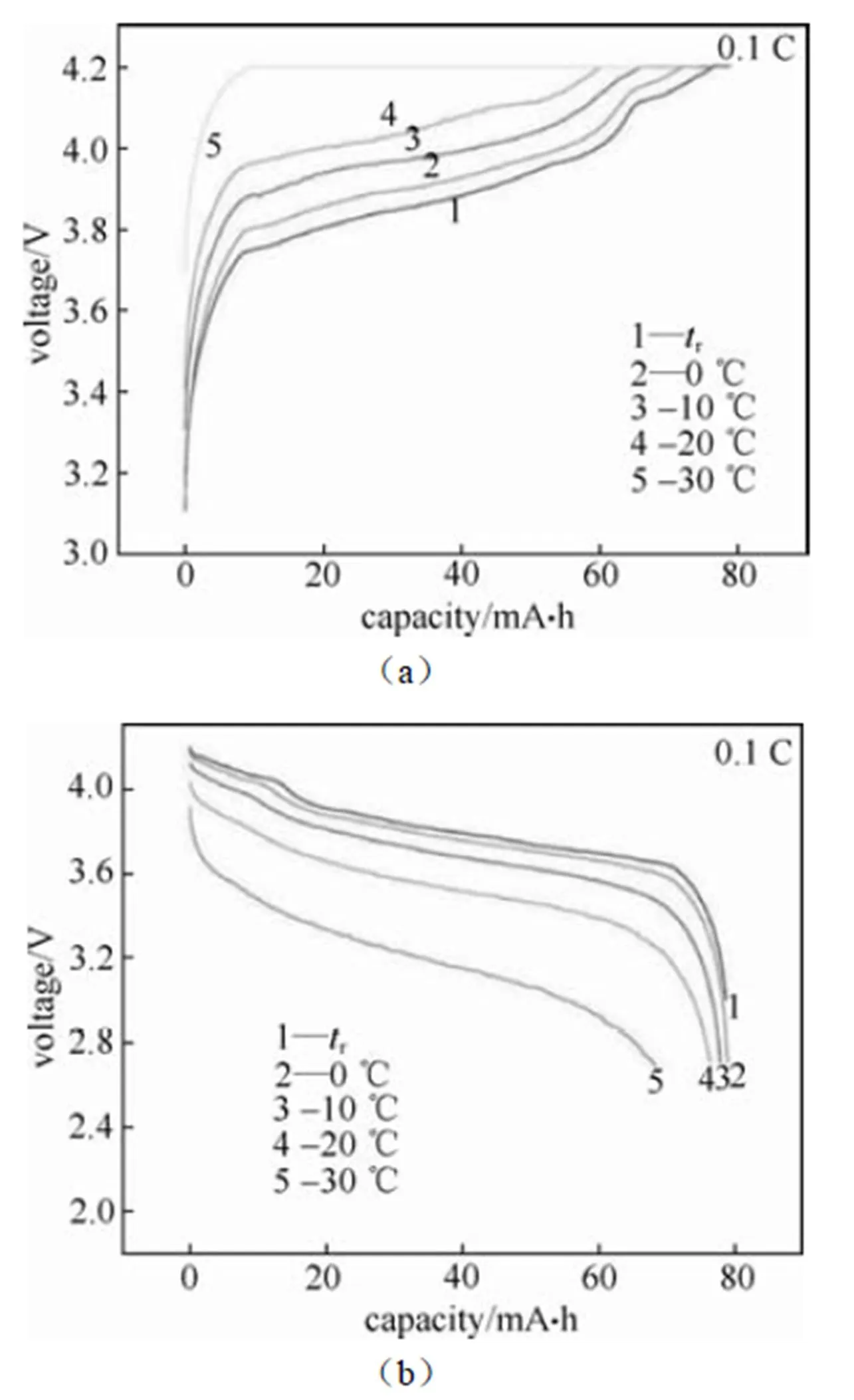
图23 LiCoO2/MCMB电池在不同低温条件下的充电(a)和放电曲线(b)[28](版权属于化学世界杂志)
3.5 分析数据与误差
综合上文所述,我们将部分主要分析数据进行总结,如表2所示。
电池材料或极片的测试过程中,误差是难以避免的,表3总结了锂离子电池在极片制备、电池组装和电池测试过程中可能存在的误差。测试人员在操作过程中,应尽量避免此类误差,以达到准确测量锂离子扣式电池性能的目的。

表2 充放电曲线获得信息及数据分析总结
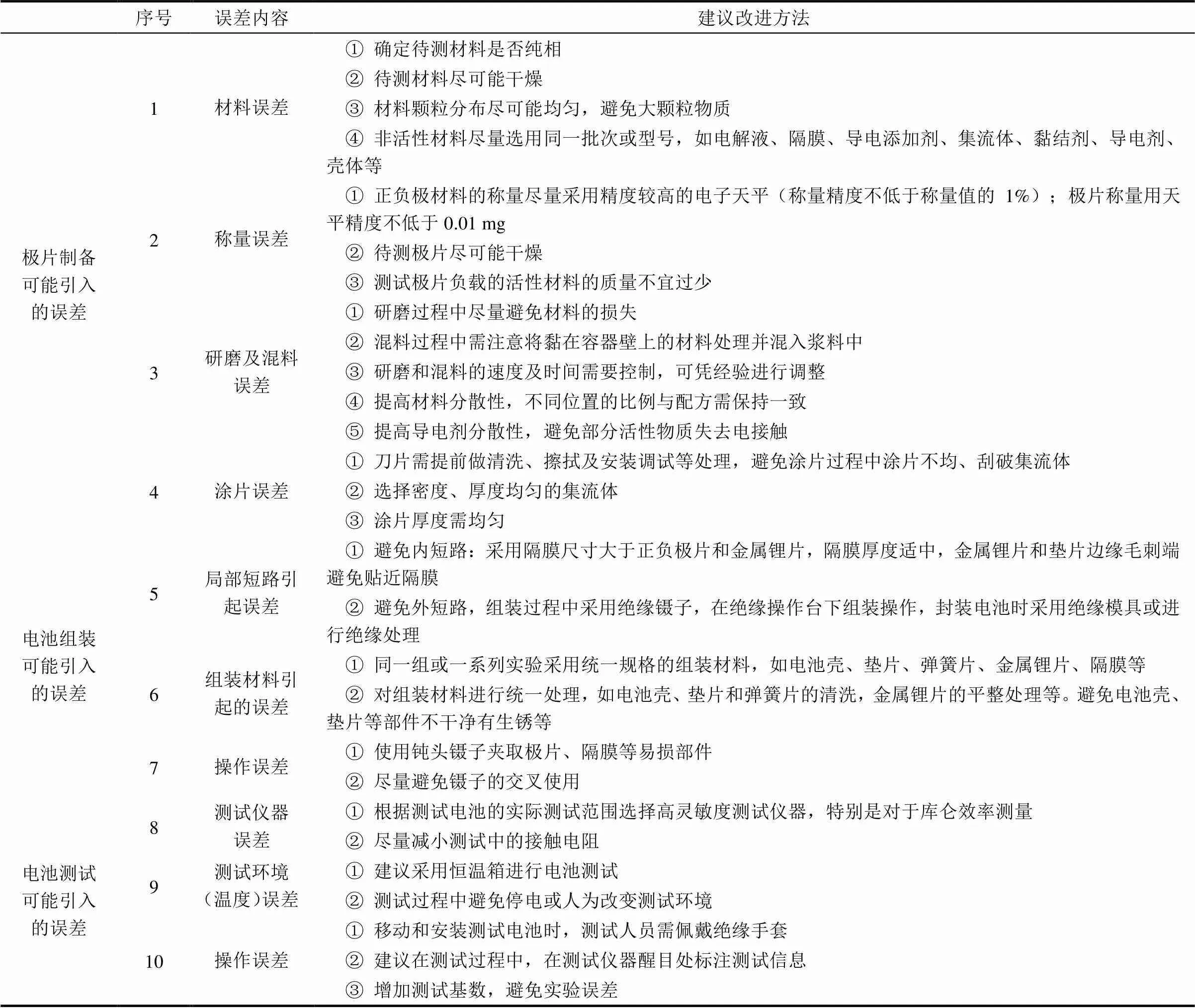
表3 锂离子扣式电池中正负极材料充放电测试中存在的误差及改进方法
4 总 结
在锂离子电池的发展过程中,我们需要通过多种不同的测试方法来获取大量的有效信息,以帮助我们更好地了解新材料和新电池体系各方面的性能。实验室中锂离子扣式电池的电化学测试是最为基础、同时也是最重要的分析测试技术,包括充放电测试、循环伏安法测试以及阻抗测试等多种电化学测试方法以及原位的测试方法。其中充放电测试则是最为直接和普遍的测试分析方法,包括材料的容量、库仑效率、过电位、倍率特性、循环特性、高低温特性、电压曲线特征等。在锂离子电池以及其它锂电池中,大量的研究结果和对材料性能、应用前景的判断以及辅助全电池设计是基于扣式电池测试的结果,所以标准化和规范操作要求,尽可能减少测量误差,规范测量条件十分重要。本文的一些具体的测试建议是基于我们扣式电池测量数据和全电池测量数据的对比而获得的经验介绍,未经过广泛的讨论和全面的论证。在此总结的目的,是希望并欢迎行业内专家批评指正,尽早形成标准或规范,以共同提高我国锂离子电池及下一代电池及新材料研发的基础研究数据的可靠性,提高电池材料开发的效率。此外,有了标准与规范,也有利于未来自动高通量扣式电池测试装备的设计和改进。
[1] STOLLER M D, RUOFF R S. Best practice methods for determining an electrode material's performance for ultracapacitors[J]. Energy & Environmental Science, 2010(3): 1294-1301.
[2] POP V, BERGVELD H J, DANILOV D, et al. Battery management systems: Accurate state-of-charge indication for battery-powered applications[M]. Berlin: Springer Science & Business Media, 2008.
[3] 王其钰, 王朔, 张杰男, 等. 锂离子电池失效分析概述[J]. 储能科学与技术, 2017, 6(5): 1008-1025.
WANG Qiyu, WANG Shuo, ZHANG Jienan, et al. Overview of the failure analysis of lithium ion batteries[J]. Energy Storage Science and Technology, 2017, 6(5): 1008-1025.
[4] 王金良, 王琪. 再谈废电池的污染及防治[J]. 电池工业, 2003, 8(1): 37-40.
WANG Jinliang, WANG Qi. About the wasted batteries: Pollution, prevention and cure[J]. Chinese Battery Industry, 2003, 8(1): 37-40.
[5] POIZOT P, LARUELLE S, GRUGEON S, et al. Nano-sized transition-metal oxides as negative-electrode materials for lithium-ion batteries[J]. Nature, 2000, 407: 496-498.
[6] 黎步银, 谢京州, 苏乐雨, 等. 锂离子电池电化学参数测试仪[J]. 仪表技术, 2006(3): 20-22.
LI Buyin, XIE Jingzhou, SU Leyu, et al. Tester for electrochemistry parameter of lithium-ion battery[J]. Instrumentation Technology, 2006(3): 20-22.
[7] COPE R C, PODRAZHANSKY Y. The art of battery charging. Battery Conference on Applications and Advances[C]//1999 The Fourteenth Annual: IEEE; 1999: 233-235.
[8] 吴锋, 汪继强, 王子冬. QCT 743—2006电动汽车用锂离子蓄电池[M]. 北京: 中国计划出版社, 2006.
WU Feng, WANG Jiqiang, WANG Zidong. QCT 743—2006 Lithium-ion batteries for electric vehicles[M]. Beijing: China Planning Press, 2006.
[9] ZHOU Q, GE W, WANG S, et al. A facile electrode preparation method for accurate electrochemical measurements of double-side-coated electrode from commercial Li-ion batteries[J]. J. Power Sources, doi: org/10.1016/j.jpowsour.2018.02.070.
[10] 张勇, 武行兵, 王力臻, 等.扣式锂离子电池的制备工艺研究[J]. 电池工业, 2008, 13: 86-90.
ZHANG Yong, WU Xingbin, WANG Lizehn, et al. Study on preparation technology of coin-type Li-ion battery[J]. Chinese Battery Industry, 2008, 13: 86-90.
[11] ZHANG B, WANG X, LIU Z, et al. Enhanced electrochemical performances of carbon coated mesoporous LiFe0.2Mn0.8PO4[J]. Journal of the Electrochemical Society, 2010, 157: A258-A285.
[12] ZHOU X, WANG F, ZHU Y, et al. Graphene modified LiFePO4cathode materials for high power lithium ion batteries[J]. Journal of Materials Chemistry, 2011, 21: 3353-3358.
[13] 蔡勇. 锂离子电池电化学性能测试系统及其应用研究[D]. 长沙: 湖南大学, 2015.
CAI Yong. The lithium-ion battery electrochemical performance test system and its application research[D]. Changsha: Hunan University, 2015.
[14] LEE S, KIM J, LEE J, et al. State-of-charge and capacity estimation of lithium-ion battery using a new open-circuit voltage versus state-of-charge[J]. Journal of Power Sources, 2008, 185: 1367-1373.
[15] ZHONG K, XIA X, ZHANG B, et al. MnO powder as anode active materials for lithium ion batteries[J]. Journal of Power Sources, 2010, 195: 3300-3308.
[16] KOMABA S, KUMAGAI N, KATAOKA Y. Influence of manganese (II), cobalt (II), and nickel (II) additives in electrolyte on performance of graphite anode for lithium-ion batteries[J]. Electrochimica Acta, 2002, 47: 1229-1239.
[17] LYU Y, BEN L, SUN Y, et al. Atomic insight into electrochemical inactivity of lithium chromate (LiCrO2): Irreversible migration of chromium into lithium layers in surface regions[J]. Journal of Power Sources, 2015, 273: 1218-1225.
[18] 高健, 吕迎春, 李泓. 锂电池基础科学问题 (III)—相图与相变[J]. 储能科学与技术, 2013, 2(3): 250-266.
GAO Jian, LV Yingchun, LI Hong. Fundamental scientific aspects of lithium batteries (III)—Phase transition and phase diagram[J]. Energy Storage Science and Technology, 2013, 2(3): 250-266.
[19] 高健, 吕迎春, 李泓. 锂电池基础科学问题(IV)—相图与相变(2)[J]. Energy 2013;2.
GAO Jian, LV Yingchun, LI Hong. Fundamental scientific aspects of lithium batteries(IV)—Phase transition and phase diagram(2) [J]. Energy Storage Science and Technology, 2013, 2(4): 383-401.
[20] 李泓. 锂离子电池基础科学问题 (XV)—总结和展望[J]. 储能科学与技术, 2015, 4(3): 306-317.
LI Hong. Fundamental scientific aspects of lithium ion batteries (XV)—Summary and outlook[J]. Energy Storage Science and Technology, 2015, 4(3): 206-317.
[21] PASTOR-FERNÁNDEZ C, UDDIN K, CHOUCHELAMANE G H, et al. A comparison between electrochemical impedance spectroscopy and incremental capacity-differential voltage as Li-ion diagnostic techniques to identify and quantify the effects of degradation modes within battery management systems[J]. Journal of Power Sources, 2017, 360: 301-318.
[22] ZHANG B, WANG X, LI H, et al. Electrochemical performances of LiFe1−xMnPO4with high Mn content[J]. Journal of Power Sources, 2011, 196: 6992-6996.
[23] BLOOM I, JANSEN A N, ABRAHAM D P, et al. Differential voltage analyses of high-power, lithium-ion cells: 1. Technique and application[J]. Journal of Power Sources, 2005, 139: 295-303.
[24] LANG M, DARMA M S D, KLEINER K, et al. Post mortem analysis of fatigue mechanisms in LiNi0.8Co0.15Al0.05O2-LiNi0.5Co0.2Mn0.3O2-LiMn2O4/ graphite lithium ion batteries[J]. Journal of Power Sources, 2016, 326: 397-409.
[25] 褚赓. 锂离子电池硅基负极材料的研究[D]. 北京: 中国科学院大学, 2017.
[26] CUI Z, GUO X, LI H. High performance MnO thin-film anodes grown by radio-frequency sputtering for lithium ion batteries[J]. Journal of Power Sources, 2013, 244: 731-735.
[27] CUI Z, GUO X, LI H. Improved electrochemical properties of MnO thin film anodes by elevated deposition temperatures: Study of conversion reactions[J]. Electrochimica Acta, 2013, 89: 229-238.
[28] 谢晓华, 解晶莹, 夏保佳. 锂离子电池低温充放电性能的研究[J]. 化学世界, 2008, 49: 581-583.
XIE Hua, XIE Jingying, XIA Baojia. Study on the charge and discharge performance of lithium ion batteries at low temperature[J]. Chemical World, 2008, 49: 581-583.
The assembly, charge-discharge performance measurement and data analysis of lithium-ion button cell
WANG Qiyu, CHU Geng, ZHANG Jienan,WANG Yi, ZHOU Ge, NIE Kaihui, ZHENG Jieyun, YU Xiqian, LI Hong
(Institute of Physics, Chinese Academy of Sciences, Beijing 100190, China)
In the initial stage of basic research and evaluation of products, electrochemical performances of lithium ion batteries are measured commonly through button cell. Accurate measurements and standard analysis are essential for screening materials, exploring new materials and batteries. Based on previous literature and practical experience, this paper summarizes the assembly, charge-discharge measurements and data analysis of lithium-ion button cell in laboratory.
lithium-ion batteries; button cell; assembly; charge-discharge performances; data analysis; standard
10.12028/j.issn.2095-4239.2018.0022
TM 911
A
2095-4239(2018)02-0327-18
2018-02-10;
2018-02-22。
国家重点研发计划新能源汽车试点专项项目(2016YFB0100300,2016YFB0100100),中国科学院战略性先导科技专项项目(XDA09010000)。
王其钰(1987—),男,博士,研究方向为锂电池失效分析与逆向分析,E-mail:qywang10@iphy.ac.cn;
李泓,研究员,研究方向为高能量密度锂离子电池,固态电池及失效分析,E-mail:hli@iphy.ac.cn。

