磷酸铁锂与碳复合材料的电化学制备及性能研究
, ,
(上海电力学院 环境与化学工程学院, 上海 200090)
目前,有很多方法都可以有效改善磷酸铁锂(LiFePO4)正极材料的电子导电率和离子扩散率,但是这些举措所采用的的工艺方法更多的是固相法.虽然固相法在操作难度上较低,便于工业化、规模化生产,但是固相法所需要的反应时间较长,且高温状态下制备出的材料粒度常常比较大,同时颗粒容易混合不均,这些不利条件在一定程度上会导致电化学活性不足.在磷酸铁锂正极材料的发展过程中,由于磷酸铁锂具有稳定有序的橄榄石型结构,且作为锂离子二次电池的电极材料所表现出的优异电化学性能,引起了广大研究者的兴趣[1].目前,实验室或工业应用上合成磷酸铁锂正极材料的方法主要有高温固相法[1-3]、溶剂热法[4-6]、溶胶-凝胶法[7-8]、水热法[9-10]、共沉淀法[9]、微波法[10]、碳热还原法,以及近几年新兴起的生物模板合成法.大量实验证明,通过减小晶粒粒径可以增大比表面积,增加反应物质的接触可以增加电化学反应位,有利于颗粒内部活性材料中锂离子的嵌入/脱出,从而提高活性材料的利用率和充放电性能.因此,制备出更小的纳米级别的活性材料颗粒可以使磷酸铁锂的电化学性能得到明显提高.本文采用电化学法提高磷酸铁锂正极材料与集流体的结合力、导电性,该工艺不仅可以摆脱传统固相制备法的缺点,同时还可以柔性控制磷酸铁锂的晶体结构和尺寸,并实现磷酸铁锂电极材料和铝箔集流体一体化的制备,以提高磷酸铁锂正极材料的晶粒结构稳定性和电化学性能.
1 实验原理及步骤
1.1 实验原理
本文使用电化学沉积的方法,阴极为铝箔,阳极为碳钢板,锂源为磷酸二氢锂,配合以草酸亚铁或乙酸亚铁作为铁源,在pH值为2.5左右的电解液环境中完成电化学沉积.在电镀液中掺杂导电炭黑生成LiFePO4/C复合材料,这种方法在工艺上非常独特.通过电化学的方法将集流体表面的晶粒尺寸可控化,电镀液中的掺碳又能在一定程度上提高磷酸铁锂的导电性.通过对比磷酸铁锂市售样品、铝箔集流体表面样品、电镀液底部沉淀样品这3种样品的物理表面形貌、电化学性能曲线、组装电池后的循环充放电性能曲线,从而得出电化学沉积法制备LiFePO4/C复合材料的可行性.
1.2 实验步骤
1.2.1 电化学沉积制备磷酸铁锂的步骤
(1) 取一块市售碳钢片,在10%盐酸溶液中浸泡酸洗至灰色氧化膜完全脱落,直至表面呈现银白色,接着用去离子水冲洗过后再用无水酒精擦洗碳钢板表面,按照阳极(碳钢板)∶阴极(铝箔)=1.5∶1的面积比,截取铝箔一张.
(2) 铝箔表面经过去离子水水洗和无水酒精擦洗后再用去离子水清洗一遍去除表面的油污,之后放入烘箱中,80 ℃干燥2 h,取500 mL去离子水加热至沸腾,封口冷却至室温.
(3) 按照电沉积反应液中Li∶Fe物质的量之比3∶1的比例,向溶液中加入0.3 mol的LiH2PO4再加入0.1 mol的C4H6FeO4搅拌至完全溶解.
(4) 在准备好的溶液中以铝箔作为阴极,碳钢板作为阳极,设置可调直流电源电压为7 V,电流为0.2 A,开始电沉积,电沉积进行1 h后,取出铝箔集流体阴极,用去离子水对铝箔表面进行冲洗.
(5) 真空干燥箱80 ℃烘干2 h,在惰性气体N2的保护气氛下,在管式炉中700 ℃煅烧10 h后冷却到室温,得到电沉积磷酸铁锂样品.管式炉煅烧期间的升温速率为5 ℃/min,这样可以避免因快速结晶造成的晶体结构坍塌.
1.2.2 电镀液中沉淀的处理步骤
(1) 将电镀液真空抽滤,用去离子水冲洗滤纸表面物质,将滤纸放入真空干燥箱中80 ℃的条件下烘干12 h,取出后将滤纸表面的晶体物质剥落.
(2) 将晶体置于惰性气体N2氛围的管式炉中,在700 ℃的温度条件下焙烧10 h,升温速率依旧设置为5 ℃/min.
(3) 焙烧完成后的电镀液沉淀样品晶体在玛瑙研钵中研磨0.5 h,得本次试验中的电镀液沉淀样品.将聚偏二氟乙烯(Polyvinylidene Fluoride,PVDF)溶解于N-甲基吡咯烷酮当中,并在磁力搅拌器上持续搅拌12 h.将经过研磨的电镀液沉淀样品粉末与Super P Li导电乙炔黑粉末以质量比为8∶1的比例混合,然后在玛瑙研钵中充分研磨0.5 h后加入制得的PVDF溶液中,用磁力搅拌器搅拌12 h使其混合均匀.
(4) 将搅拌均匀的混合物匀浆,用标准涂覆器均匀涂覆于铝箔集流体表面.将涂覆完的铝箔集流体置于真空干燥箱内,在80 ℃的条件下烘干12 h,使用台式压片机将含有活性物质的铝箔集流体压制成直径为14 mm的正极电极片.
2 结果与讨论
2.1 材料的表征
2.1.1 X射线衍射图谱分析
图1为实验中所用的磷酸铁锂市售样品、电化学沉积法样品(以下简称“电沉积样品”)、电镀液沉淀样品三者的X射线衍射(XRD)对比图谱.由图1可知,市售磷酸铁锂样品的XRD图谱衍射峰形尖锐,强度高,没有出现杂相衍射峰;而电沉积样品的XRD图谱相比之下同样尖锐,出峰明显.因此,认为电沉积样品具有与市售样品相近的层状结构的磷酸铁锂.电镀液沉淀样品的XRD图谱经Jade软件吻合比对后,认为具有部分磷酸铁锂结构,但是有部分铁氧化物混杂在其中,因此可能会对之后的电化学性能测试结果造成影响.

图1 3种样品的XRD图谱
2.1.2 扫描电子显微镜
图2为市售样品和电沉积样品的扫描电子显微镜(SEM)形貌图.从图2(a)中可以清晰地看出颗粒为球形或椭球形,且分布均匀,无明显团聚现象.颗粒的平均粒径小,较小的晶粒尺寸增大了材料的比表面积,缩短了锂离子的扩散路径,有利于提高材料的电化学性能.从图2(b)中也能清晰地看出颗粒为球形或扁球形,分布较图2(a)中略为逊色,但是没有明显团聚现象,可以认为电沉积制得的样品比表面积同样优秀.

图2 样品的SEM示意
2.2 电化学性能测试
2.2.1 充放电曲线
图3为磷酸铁锂市售样品、电沉积样品、电镀液沉淀样品的充放电曲线.
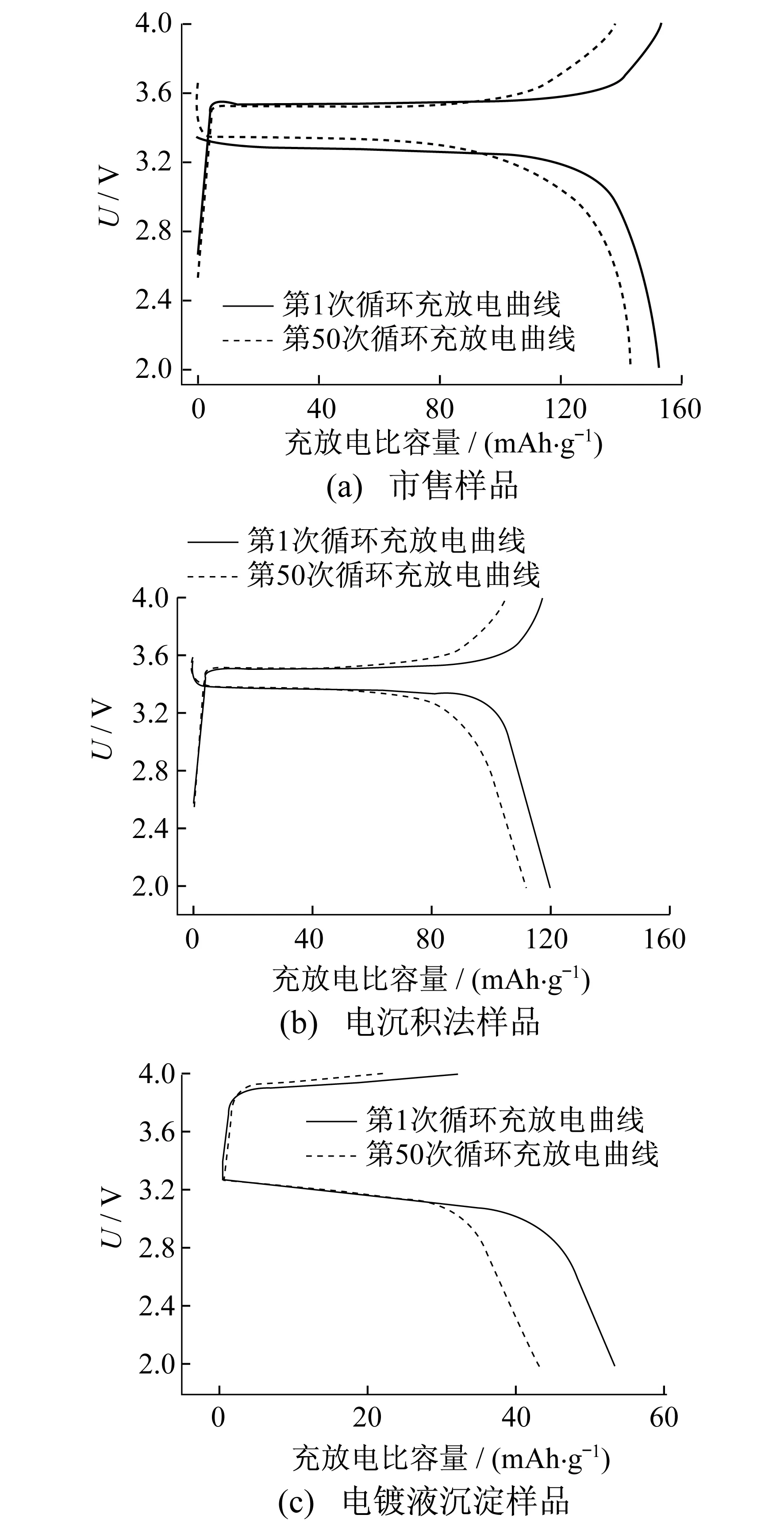
图3 3种样品的充放电曲线
由图3(a)中可以看到,磷酸铁锂市售样品首次充电比容量达到了158 mA/g,首次放电比容量为157 mA/g,符合磷酸铁锂正极材料理论容量170 mA/g,商业容量140 mA/g左右的数值.市售样品在3.6 V左右出现了较稳定的电压平台.这是由于活性物质磷酸铁锂内部结构脱嵌锂离子行为的过程稳定进行而显现的.可见市售样品的活性物质结构优良.由图3(b)可以看到,电沉积样品首次充电比容量为125 mA/g,首次放电比容量为116 mA/g.达到磷酸铁锂市售样品充电比容量的79.1%,放电比容量的73.9%.电沉积样品充放电曲线的电压平台比市售样品更稳定,但由于充放电比容量上的劣势,可见电沉积法样品的活性物质结构仍存在缺陷.由图3(c)可以看到,电镀液沉淀样品首次充电比容量为54.1 mA/g,首次放电比容量为43.7 mA/g,分别是市售样品的40.6%,32.3%.从充放电比容量这一项可知,电镀液样品的有效物质成分及结构较市售、电沉积两个样品有较大的差距.
2.2.2 循环性能曲线
图4为磷酸铁锂市售样品、电沉积样品、电镀液沉淀样品的循环性能曲线.

图4 3种样品的循环性能曲线
由图4(a)可以看出,市售样品在0.5C倍率的条件下,首次充放电比容量分别为158 mAh/g和157 mAh/g,经过50次循环充放电之后仍然保持为146 mAh/g和143 mAh/g,充放电容量保持率分别为92.5%和91.3%.由图4(b)可以看到,电沉积样品在0.5C倍率的条件下,首次充放电比容量分别为118 mAh/g和117 mAh/g.经过50次循环充放电之后充放电比容量分别为111 mAh/g和115 mAh/g,容量保持率分别为94.3%和98.0%.由图4(c)可以看到,电镀液沉淀样品在0.5C倍率的条件下,首次充放电比容量分别可以达到58 mAh/g和51 mAh/g,经过40次循环充放电之后充放电比容量分别为45 mAh/g和43 mAh/g,容量保持率分别为77.3%和84.5%.
2.2.3 多倍率循环性能曲线
图5为磷酸铁锂市售样品、电沉积样品、电镀液沉淀样品的多倍率下循环性能曲线.
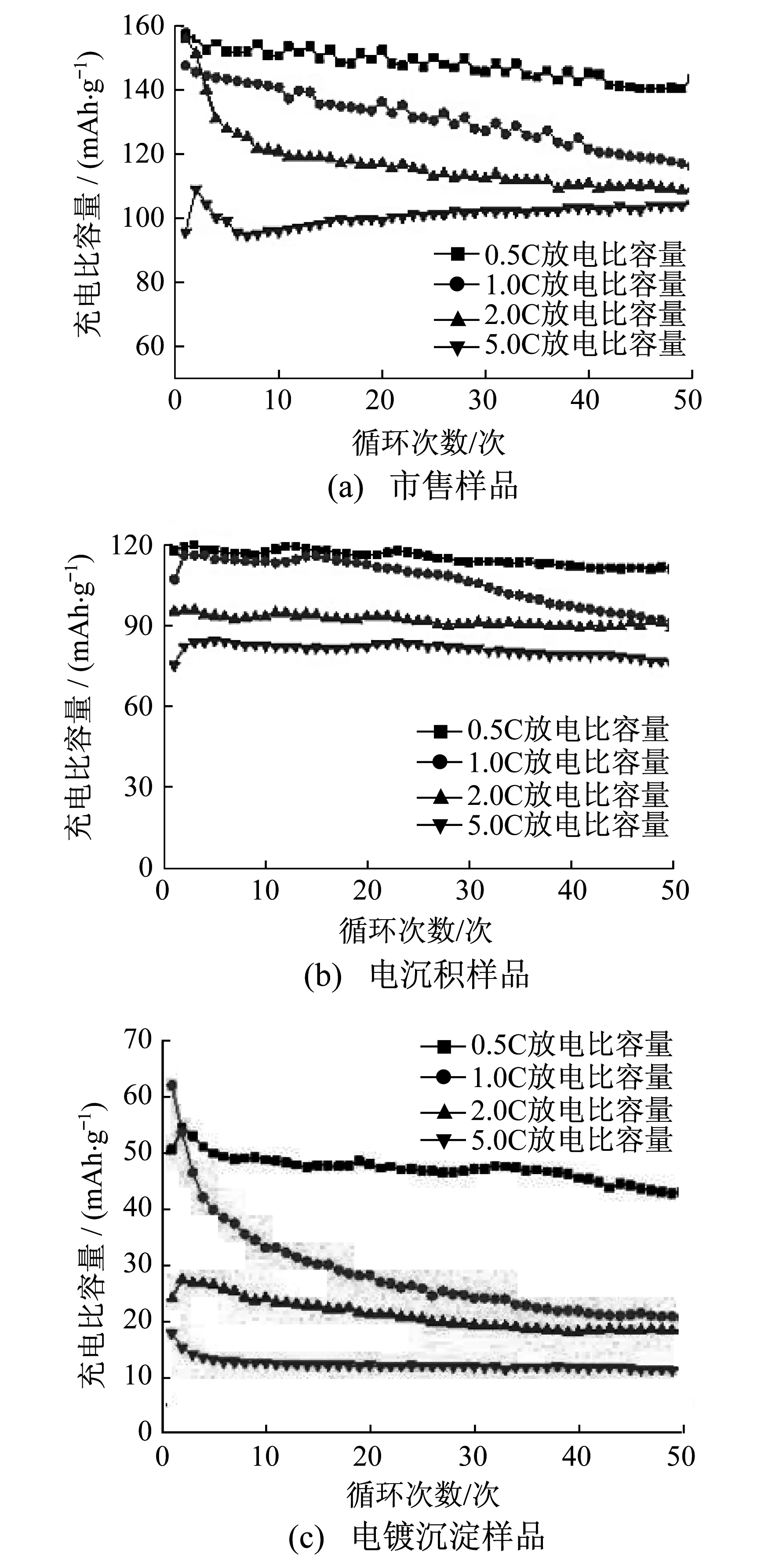
图5 3种样品的多倍率下循环性能曲线
由图5(a)可看到,市售样品在0.5C,1C两个较低倍率下的放电性能较优异,容量保持率分别为91.2%,79.8%;2C和5C循环测试初期放电比容量骤降,这是因为电池内部在充放电过程会发生体积收缩和膨胀,而充放电的电流越大,这种收缩膨胀的效应越剧烈,应力越大也会造成正极有效物质的颗粒体积快速变化,从而更容易发生破裂,导致循环衰减加快.正极材料的充放电电流越大,颗粒中心的锂离子越难扩散到颗粒表面中去,因此颗粒的表面更容易发生过充现象,导致析氧而晶格结构坍塌,从而使电池容量下降,循环衰竭.由图5(b)可以看到,电沉积样品在0.5C,2C,5C 3个测试倍率条件下的放电容量都有相较市售样品更好的循环性能,分别为98.1%,97.2%,95.2%.由图5(c)可以看到,电镀沉淀样品在各种倍率条件下放电的比容量都非常低,且在1C倍率条件下放电比容量衰减非常快,性能较差.由此可见,电沉积样品具有优异的容量保持率.
2.2.4 循环伏安法曲线
为了进一步研究在电极反应中锂离子嵌入/脱出过程、氧化还原过程和相转变过程,绘制了3种样品的循环伏安法(C-V)曲线,如图6所示.
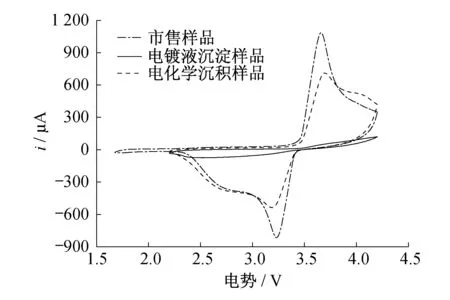
图6 3种样品的CV测试曲线
图6是3个样品在电压范围2.2~4.2 V,以 0.15 mV/s速率完成的.图6中,市售样品的C-V曲线在3.3~3.6 V电压范围内有一对还原氧化峰,3.3 V左右还原过程中,锂离子发生嵌入反应,相对脱出反应发生在3.6 V左右的氧化过程.相对电沉积样品,市售样品的C-V曲线具有较高的出峰强度,但两条曲线都具有良好的对称性.这跟锂离子在电池有效物质中的脱嵌反应有关,说明电池具有良好的循环对称性能,且电沉积样品表现出的反应可逆性相对市售样品更好.电镀液沉淀样品的C-V曲线表现出的氧化还原峰较另两个样品有较大的差距,没有出现明显的谷峰,可知,其中的有效物质在发生锂离子的嵌入/脱出反应的过程中并不像另两个样品一样稳定.
3 结 论
(1) 电化学沉积法制备的样品,拥有更好的循环充放电性能,电压平台更稳定;充放电比容量保持率更好,多倍率充放电性能也更胜一筹.
(2) 电镀液中的沉淀样品整体表现较差,主要是因为晶体主体结构的缺陷,最大程度地降低了电化学性能.
[1] PADHI A K,NAJUNDASWAMY K S,GOODENOUGH J B.Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J].Journal of the Electrochemical Society,1997,144(4):1188-1194.
[2] ANDERSSON A S,THOMAS O.The source of first-cycle capacity loss in LiFePO4[J].Journal of Power Sources,2001,97(3):498-502.
[3] MA Z P,SHAO G J,WANG G L,etal.Electrochemical performance of Mo-doped LiFePO4/C composites prepared by two-step solid-state reaction[J].Ionics,2013,19(3):437-443.
[4] LIU W L,TU J P,QIAO Y Q,etal.Optimized performances of core-shell structured LiFePO4/C nanocomposite[J].Journal of Power Sources,2011,196(18):7728-7735.
[5] DOKKO K,KOIZUMI S,NAKANO H,etal.Particle morphology,crystal orientation,and electrochemical reactivity of LiFePO4synthesized by the hydrothermal method at 443K[J].Journal of Materials Chemistry,2007,17(45):4803-4810.
[6] LIU H,KONG L B,ZHANG P,etal.A facile hydrothermal method to prepare LiFePO4/C submicron rod with core-shell structure[J].Ionics,2014,20(1):15-21.
[7] YANG S L,ZHOU X F,ZHANG J G,etal.Morphology controlled solvothermal synthesis of LiFePO4as a cathode material for lithium-ion batteries[J].Journal of Materials Chemistry,2010,20(37):8086-8091.
[8] CHOI D,KUMTA P N.Surfactant based sol-gel approach to nanostructured LiFePO4for high rate Li-ion batteries[J].Journal of Power Sources,2007(2):1064-1069.
[9] DING Y,JIANG Y,XU F,etal.Preparation of nano-structured LiFePO4/graphene composites by co-precipitation method[J].Electrochemistry Communications,2010,12(1):10-13.
[10] WANG S P,YANG H X,FENG L J,etal.A simple and inexpensive synthesis route for LiFePO4/C nanoparticles by co-precipitation[J].Journal of Power Sources,2013(7):43-46.

