恩替卡韦联合硫普罗宁治疗慢性乙型肝炎患者肝功能及其肝纤维化指标的变化
翁艳
乙型肝炎系乙型肝炎病毒(hepatitis B virus,HBV)感染引起的肝脏炎性病变,是病毒性肝炎中最常见的类型。其病程多为慢性,发病早期症状不明显,长期感染的乙型肝炎患者临床症状主要表现为肝区不适、乏力、黄疸、肝脾肿大、肝功能受损和肝纤维化,其中肝功能受损和肝纤维化最常出现,可作为临床观察的主要指标。肝脏受损可导致凝血因子和白蛋白等合成障碍,进而引起肝脏之外的全身多器官、系统损害,严重影响患者的生活质量[1]。有研究表明[2],乙型肝炎患者可发展至肝硬化和肝细胞癌,对患者的生命安全构成威胁。HBV作为一种DNA病毒,具有较强的传染性。由于HBV感染不直接损害肝脏,而HBV能够被机体免疫系统识别,诱发机体免疫功能紊乱,造成肝损害。临床通过血生化和特异性病原学检测即可确诊,在必要时可采取肝脏穿刺活检进行确定病情或鉴别诊断。研究表明[3],乙型肝炎患者经诊断后早期进行药物治疗能显著改善患者的预后。由于发病人群庞大,乙型肝炎的临床治疗一直是我国临床研究的热点之一。慢性乙型肝炎患者的临床治疗多应用抗病毒药物,如α-干扰素和核苷(酸)类似物等。但临床数据显示单一药物治疗患者的临床疗效不够理想,需采用联合用药才能显著改善患者肝脏功能和抑制肝脏纤维化。有文献报道[4],甘氨酸衍生物硫普罗宁联合核苷类药物恩替卡韦治疗慢性乙型肝炎患者临床效果显著,对患者肝功能和肝纤维化指标的改善作用明显。本研究应用恩替卡韦联合硫普罗宁治疗慢性乙型肝炎患者,观察了肝功能和肝纤维化指标的变化,现将研究结果报告如下:
1 资料与方法
1.1 一般资料 2015年6月~2016年6月我院消化内科收治的慢性乙型肝炎患者116例,男性63例,女性53例;年龄范围为41~61岁,平均年龄(42.45±9.52)岁。平均病程为(5.97±2.26)年。诊断符合中华医学会肝病学分会和感染病学分会发布的慢性乙型肝炎防治指南(2015年版)的标准[5],入选患者血清HBeAg均为阳性,无合并心脑血管、肺和肾脏疾病,不伴有其他肝脏疾病,入院治疗前6月内未进行过抗病毒治疗。排除标准[6]:①对本研究治疗药物过敏的患者;②合并其他病毒性肝炎、肝癌、酒精性肝病或合并其他脏器严重疾病的患者;③合并严重的免疫系统、循环系统疾病或恶性肿瘤患者;④伴有肺结核、艾滋病等传染性疾病的患者;⑤处于妊娠或哺乳期的妇女。采用随机数字表法将116例患者平均分为观察组58例和对照组58例,两组在性别、年龄、乙型肝炎病程和病情等一般资料方面比较,差异无统计学意义(P>0.05),故具有可比性。患者对本研究内容知情并签署知情同意书,且本研究经医院医学伦理委员会批准。
1.2 治疗方法 两组患者治疗前,均禁烟酒,不服用具有肝脏毒性的药物,接受高蛋白和维生素的食物。给予两组患者恩替卡韦胶囊(正大天晴制药有限公司,国药准字H20120038)0.5 mg口服,1次/d;在此基础上,给予观察组患者硫普罗宁肠溶片(湖北午时药业股份有限公司,国药准字H20123078)0.2 g口服,3次/d。观察12 w。
1.3 检测与检查 使用普朗牌全自动生化分析仪检测肝功能指标(安徽信灵检验医学科技有限公司);采用ELISA法检测血清HBV标记物(上海康成生物工程有限公司);常规检测血清肝纤维化指标和HBV DNA。
1.4 统计学方法 应用IBM公司SPSS 23.0统计分析软件分析数据,以n(%)表示计数资料,行x2检验,以(±s)表示计量资料,并行 t检验,P<0.05 被认为差异具有统计学意义。
2 结果
2.1 两组治疗前后肝功能指标变化的比较 两组患者在接受治疗前,肝功能各项指标均无显著性差异(P>0.05);经过12 w治疗,观察组患者血清 ALT、AST、TBIL 水平均明显低于对照组(P<0.01,表1)。
表1 两组治疗前后肝功能指标(±s)的比较
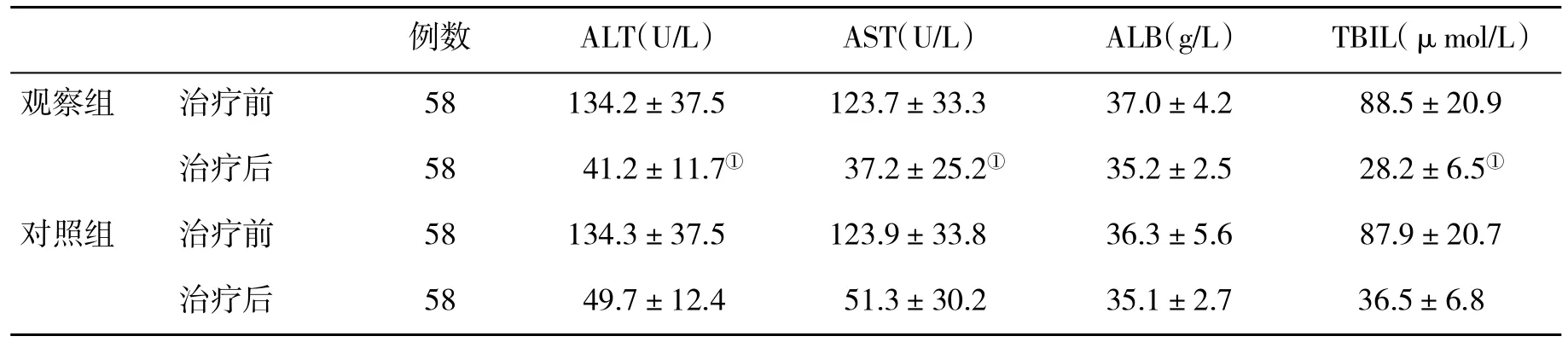
表1 两组治疗前后肝功能指标(±s)的比较
与对照组比,①P<0.05
例数 ALT(U/L) AST(U/L) ALB(g/L) TBIL(μmol/L)观察组 治疗前 58 134.2±37.5 123.7±33.3 37.0±4.2 88.5±20.9治疗后 58 41.2±11.7① 37.2±25.2① 35.2±2.5 28.2±6.5①对照组 治疗前 58 134.3±37.5 123.9±33.8 36.3±5.6 87.9±20.7治疗后 58 49.7±12.4 51.3±30.2 35.1±2.7 36.5±6.8
2.2 两组治疗前后血清肝纤维化指标的比较 两组患者在接受治疗前血清HA、LN、C-IV和PCⅢ水平比较均无显著性差异(P>0.05);经过12 w治疗后,观察组患者血清HA、LN、C-IV和PCⅢ水平均显著低于对照组(P<0.01,表2)。
2.3 两组治疗前后血清学和病毒学指标比较 治疗后,两组患者血清HBV DNA转阴率差异无统计学意义(P>0.05,表3)。
2.4 两组不良反应发生率的比较 两组慢性乙型肝炎患者在治疗过程中均未出现严重的不良反应,个别患者出现恶心呕吐、腹痛腹泻、食欲不振和头晕等,但这些反应系疾病发作的表现抑或是药物的不良反应,还不明确,两组不良反应发生率的差异无统计学意义(P>0.05,表4)。
表2 两组血清肝纤维化指标(μg/L,±s)的比较

表2 两组血清肝纤维化指标(μg/L,±s)的比较
与对照组比,①P<0.05
例数 HA LN C-IV PCⅢ观察组 治疗前 58 199.3±19.4 195.7±35.5 218.3±66.7 152.6±46.3治疗后 58 93.9±34.2① 103.6±38.2① 105.2±40.3① 75.3±16.7①对照组 治疗前 58 199.3±19.4 195.7±35.6 218.4±66.8 150.8±42.9治疗后 58 116.5±35.1 127.9±40.5 133.8±35.1 91.2±18.5

表3 两组治疗后血清学和病毒学指标(%)的比较
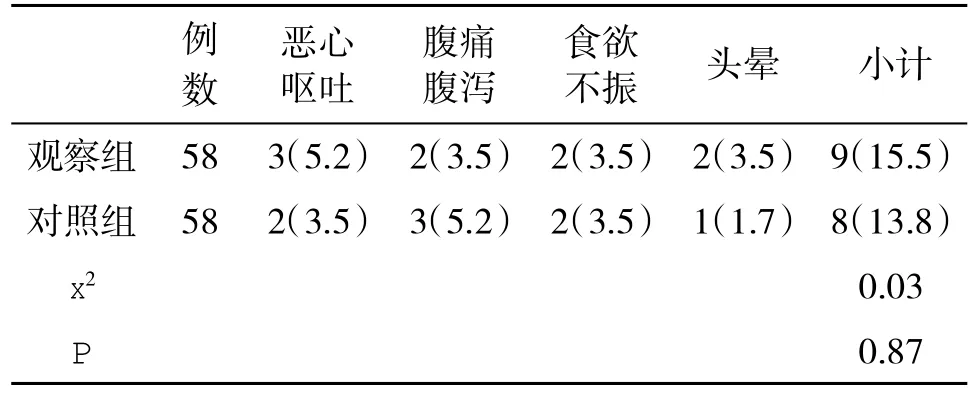
表4 两组不良反应发生率(%)的比较
3 讨论
肝脏为人体消化系统中最大的消化腺,也是人体代谢和排毒的主要器官之一,其功能与人体生命活动的正常维持密切相关[10]。肝脏亦是人体内脏最大的器官,可以储存肝糖元,从而为人体代谢和运动提供能量。肝脏还具有分泌胆汁的功能,能合成体内具有重要作用的蛋白和尿素,在人体正常生命活动的维持中发挥着至关重要的作用。慢性乙型肝炎对肝脏造成渐进性的损害,且患者的病程较长,在早期对患者肝脏的功能影响不明显,而患者发觉时往往已经系活动性疾病。慢性乙型肝炎对肝脏的损伤主要是由于HBV感染导致,HBV感染的预防一直是临床研究的重点,而我国预防乙型肝炎的方式为接种乙肝疫苗。但我国人口基数大,乙型肝炎发病群体庞大。研究表明[11-13],HBV是一种具有嗜肝细胞性的DNA病毒,能侵犯体内单核细胞和肾小管上皮细胞等,但HBV并不直接对这些细胞造成损害,而是通过与人体免疫系统发生免疫反应所致。目前,抗HBV感染的主要药物有干扰素和核苷类似物。干扰素是一种能够调节人体免疫功能的糖蛋白,能够抑制乙型肝炎病毒在肝细胞内复制;核苷类似物能直接抑制HBV DNA复制,抗HBV感染治疗的效果主要通过肝功能和肝纤维化指标检查来观察,血清病原学检测也能直接反应HBV的清除情况。有文献报道[14-15],甘氨酸衍生物硫普罗宁联合核苷类药物恩替卡韦治疗慢性乙型肝炎患者临床效果好,对患者肝功能和肝纤维化程度改善显著。
硫普罗宁系一种含有巯基的甘氨酸衍生物,化学成分为N-(2-巯基丙酰基)-甘氨酸[16]。硫普罗宁可通过其巯基与代谢过程中产生的氧自由基可逆性结合,进而在免疫系统中清除这些物质,而达到抗细胞氧化的作用,亦能够抑制成纤维细胞中编码I、Ⅲ前胶原的信使RNA的转录,使得肝脏胶原蛋白的合成受到抑制,进而抑制了肝脏纤维化的进一步发展。有研究表明[17-21],硫普罗宁能降低线粒体有氧代谢时呼吸链酶的活化阈浓度,从而提高了ATP的生成,为肝脏细胞提供能量,有助于肝细胞和肝组织功能的恢复。目前,硫普罗宁已作为一种具有解毒作用的护肝药而广泛应用于临床[18]。有文献报道[22-25],甘氨酸衍生物硫普罗宁联合核苷类药物恩替卡韦能够实现抑制肝脏组织中HBV复制的同时,抑制肝脏的纤维化,促进肝脏细胞和肝脏组织的恢复并保护肝脏功能,从而达到了改善HBV感染患者的肝功能以及肝脏纤维化的效果。
本研究通过设计观察组和对照组,对比了慢性乙型肝炎患者接受硫普罗宁联合恩替卡韦治疗与恩替卡韦单一治疗的疗效,旨在为临床慢性乙型肝炎的临床用药提供参考。研究结果显示,经过联合治疗的观察组患者治疗后,患者肝功能指标较治疗前显著下降,且各指标均显著低于对照组。两组患者肝纤维化指标较治疗前亦显著下降,且治疗后观察组各指标均显著低于对照组,观察组HBV DNA转阴率与对照组比,差异无统计学意义。两组患者均出现不良反应,且未出现因不良反应而停止治疗的情况,说明硫普罗宁联合恩替卡韦治疗慢性乙型肝炎患者的疗效显著,能有效改善肝功能和肝纤维化指标,且使用安全。综上所述,硫普罗宁联合恩替卡韦治疗能显著改善慢性乙型肝炎患者肝功能以及肝纤维化指标,且无明显不良反应。
[1]Keating GM.Entecavir:a review of its use in the treatment of chronic hepatitis B in patients with decompensated liver disease.Drugs,2011,71(18):2511-2529.
[2]Nishikawa H,Nishijima N,Enomoto H,et al.A predictive model for carcinogenesis in patients with chronic hepatitis B undergoing entecavirtherapy and itsvalidation.Medicine,2016,95(36):e4832.
[3]Liaw YF,Sheen IS,Lee CM,et al.Tenofovir disoproxil fumarate(TDF),emtricitabine/TDF,and entecavir in patients with decompensated chronic hepatitis B liverdisease.Hepatology,2011,53(1):62-72.
[4]潘静,陆伦根.核苷(酸)类似物初始治疗慢性乙型肝炎患者疗效和安全性的网络Meta分析.实用肝脏病杂志,2017,20(1):29-33.
[5]Zhao BS,Dong JL,Xie F,et al.Clinical observation of tiopronin combined with telbivudine in treatment of chronic hepatitis B.Drugs Clin,2016,22(3):472-475.
[6]Xue M,Wu C,Cen W,et al.Prostecdtive efficacy observation of entecavir in treatment of HBeAg-positive chronic hepatitis B.Clin Med,2016,12(8):236-238.
[7]Papatheodoridis GV,Chan HL,Hansen BE,et al.Risk of hepatocellularcarcinoma in chronic hepatitis B:Assessmentand modification with current antiviral therapy.J Hepatol,2015,62(4):956-967.
[8]Chen C H,Hung C H,Hu T H,et al.Association between level of hepatitis B surface antigen and relapse after entecavir therapy for chronic hepatitis B.Virus Infect,2015,15(6):18-19.
[9]陈雅萍,张勤俭,田楠楠,等.恩替卡韦联合聚乙二醇干扰素治疗慢性乙型肝炎患者疗效观察.实用肝脏病杂志,2016,19(2):208-209.
[10]吕玉芳.硫普罗宁联合促肝细胞生长素治疗慢性乙型肝炎的临床研究. 现代药物与临床,2016,31(1):66-69.
[11]Wei MJ,Pan XN,Wei KP,et al.Efficacy of HBV-pulsed DCS in combination with entecavir in patients with chronic hepatitis B infection.Int Immunop,2015,27(2):238-243.
[12]Kim HS,Yim HJ,Jang MK,et al.Management of entecavir-resistantchronic hepatitis B with adefovir-based combination therapies.World J gastroenterol,2015,21(38):108-114.
[13]Cho EJ,Lee JH,Cho Y,et al.Comparison of the efficacy of entecavir and tenofovir in nucleosid (t) analogue-experienced chronic hepatitis B patients.Plos One,2015,10(6):e0130392.
[14]Dienstag JL,Wei LJ,Xu D,Kreter B.Cross-study analysis of the relative efficacies of oral antiviral therapies for chronic hepatitis B infection in nucleoside-naivepatients.Clin Drug Investig,2007,27(1):35-49.
[15]Li YF.Clinical observation of tiopronin combined with hepatocyte growth promoting factor in treatment of chronic hepatitis B.Drugs Clin,2016,97(2):359-366.
[16]Seto WK,Hui AJ,Wong WS,et al.Treatment cessation of entecavir in Asian patients with hepatitis B antigen negative chronic hepatitis B:a multicentre prospective study.Gut,2015,64(4):667.
[17]Li J,Qiu X,Guo W,et al.Prospective analysis of tiopronin in prevention ofsorafenib and antiviraltherapy inducing liver toxicity in advanced hepatitisB virus-related hepatocellular carcinoma.Med Oncol,2015,32(10):238-239.
[18]Gish RG,Given BD,Lai CL,et al.Chronic hepatitis B:Virology,natural history,current management and a glimpse at future opportunities.Antivir Res,2015(12),121:47-58.
[19]Jonas MM,Chang MH,Sokal E,et al.Randomized,controlled trial of entecavir versus placebo in children with hepatitis B envelope antigen-positive chronic hepatitis B. Hepatology,2016,63(2):377-378.
[20]Ahn J,Nguyen M H,Lim J K,et al.Letter:lessons from the'real-world'entecavir therapy in chronic hepatitis B patientsauthors'reply.Aliment Pharmacol Therapeut,2016,43(7):847-848.
[21]赵宝生,董金玲,谢放,等.硫普罗宁联合替比夫定治疗慢性乙型肝炎的疗效观察. 现代药物与临床,2016,31(1):62-65.
[22]Nishikawa H,Nishijima N,Enomoto H,et al.A predictive model for carcinogenesis in patients with chronic hepatitis B undergoing entecavirtherapy and itsvalidation.Medicine,2016,95(36):e4832.
[23]温青.恩替卡韦与肝康颗粒联合治疗慢性乙型肝炎的价值分析. 基层医学论坛,2016,20(36):5213-5214.
[24]吕玉芳.硫普罗宁联合促肝细胞生长素治疗慢性乙型肝炎的临床研究. 现代药物与临床,2016,31(1):66-69.
[25]梁桂才,黄献球.拉米夫定与恩替卡韦治疗慢性乙型肝炎慢加急性肝功能衰竭的对比研究.成都医学院学报,2016,11(1):58-61.

