颈前路椎间盘切除植骨融合术联合可吸收板内固定治疗脊髓型颈椎病的近期疗效研究
高军红,裴东红
(榆林市第一医院骨二科,陕西 榆林 718000)
脊髓型颈椎病(CSM)是临床常见的颈椎病类型之一,以中老年人群较为多见,常表现为椎间无力、肢体麻木并可伴尿急、尿频等症状,严重影响患者的生活质量[1]。前路椎间盘切除减压植骨融合(ACDF)钛合金钉板内固定是临床治疗CSM的经典术式,但钛合金钉板系统内固定存在内固定物断裂、移位、术后早期吞咽困难、应力遮挡以及MRI图像伪影干扰等缺陷[2]。2005年,S-1TM可吸收板内固定系统被批准上市,已有研究证实其在植入机体后,能够逐渐降解、吸收,从而避免内固定物对于脊柱周围软组织及生物力学等的远期影响[3]。但关于ACDF可吸收板内固定在国内尚鲜见报道,其与钛合金钉板内固定在CSM中的应用优劣尚值得探讨。本文对ACDF治疗的CSM患者进行回顾性队列研究,旨在评价ACDF可吸收板内固定治疗的近期疗效,现报道如下:
1 资料与方法
1.1 一般资料
纳入2013-01-2015-01在我院骨科接受ACDF治疗的CSM患者62例,按照内固定材料分组:31例应用可吸收板内固定为A组,31例采用传统钛合金钉板系统固定为B组。A组男22例,女9例,年龄26~58(48.17±4.97)岁;病程 6~12(8.92±1.34)个月;病变节段:4 例 C3-4,7 例 C4-5,10 例 C5-6,6 例 C6-7,1 例C3-4+C4-5,2 例 C4-5+C5-6,1 例 C5-6+C6-7。B 组男 20 例,女 11 例,年龄 28~55(49.33±5.09)岁;岁;病程 6~12(9.09±1.27)个月;病变节段:3 例 C3-4,6 例 C4-5,12例 C5-6,5 例 C6-7,1 例 C3-4+C4-5,3 例 C4-5+C5-6,1 例C5-6+C6-7。两组基线资料经统计学比较无显著性差异(P>0.05)。
1.1.1 纳入标准 ①符合第三届全国颈椎病专题座谈会[4]上提出的CSM诊断标准;②经足疗程正规保守治疗症状改善不明显或无效;③年龄18~60岁;③影像学检查提示C3-7节段1~2个节段病变;④X线和(或)MRI检查证实为前方脊髓受压;⑤患者及其家属自愿知情并签署了书面知情同意书,研究获医院伦理委员会审批。
1.1.2 排除标准 ①术前CT检查显示存在连续性后纵韧带骨化;②术前影像学检查显示脊髓受压源自脊髓或椎体后方;③合并先天性椎管狭窄、脊柱结核、肿瘤性病变、感染性疾病以及严重骨质疏松症者;④合并骨关节炎性疾病者;⑤合并严重基础疾病或身体素质差无法耐受手术者。
1.2 手术方法
1.2.1 A组 本组行ACDF联合可吸收板内固定治疗。可吸收板为芬兰Inion S-1TM型,分为单、双节段板两种,术中视椎间隙高度与椎体大小选择适宜型号的可吸收板。患者取仰卧位,在全麻状态下,于颈右侧皮肤横纹行3-5 cm横切口,常规经前路入路,经C型臂X线机定位病变节段。切除病变椎间盘实现彻底减压,植入适宜型号的椎间融合器Cage或自体髂骨块进行椎间植骨。准确辨别椎体中线结构,并将椎体前缘骨赘切除,安装试模,确定理想的S-1 TM型号及安装位置,并以定位锥进行钉孔位置标记。将试模取出,充分冲洗并将椎间隙内碎屑清除后,植入相应型号且经70℃水浸泡软化的S-1 TM可吸收板,充分塑形后自然冷却40~50s,然后安装至目标位置。检查椎间植骨情况以及椎体中线位置,确认满意后,应用导向器在椎体及可吸收板上钻孔、攻丝,植入4枚可吸收螺钉,再次经C臂机观察可吸收钉板系统的位置与标记位置一致后,拧紧螺钉。术后常规留置切口引流管,1~2 d后将引流管拔除,术后2-3 d在颈围保护下离床活动,术后7 d将切口缝线拆除,术后颈围固定保护1~3个月。
1.2.2 B组 本组行ACDF联合钛合金钉板系统内固定治疗,手术体位、麻醉方式、术野暴露、减压及植骨方式均同可吸收板内固定组。植骨后选择适宜型号的强生Skyline颈前路钛合金钉板植入病变椎间隙,经C臂机透视钢板位置无误后,常规开口并植入1枚自攻螺钉,然后在其对角线部位再次植入1枚螺钉,C臂机透视植骨融合器以及螺钉位置满意后,常规冲洗切口并留置引流管。术后处理同可吸收板内固定组。
1.3 观察指标
1.3.1 功能指标 (1)运用日本矫形外科学会(JOA)评分系统进行脊髓神经功能评价,总分17分,得分越高则功能越好。(2)运用颈部功能障碍指数(NDI)进行颈部功能评价,总分50分,得分越高则功能障碍越重。(3)运用疼痛视觉模拟量表(VAS)进行疼痛程度评价,总分0~10分,得分越高疼痛越重。(4)参照Odom分级标准进行总体恢复情况评价,优:临床症状完全消失,恢复正常工作及生活;良:偶有颈部不适感,但不影响日常工作;可:颈部症状显著改善,对工作有影响;差:症状无改善或加重。
1.3.2 影像学指标 常规拍摄颈椎侧位X线片,采用Emery法测定椎间高度,采用Cobb角测量方法测量C2-C7颈椎曲度。
1.3.3 术后并发症 统计术后内固定物松脱、折断、失效、吞咽困难、迟发型食道瘘及相邻节段退行性变(ASD)等并发症发生情况。
1.4 随访方法 术后随访24个月以上,统计两组术前、术后3个月、6个月、12个月及末次随访时的JOA评分、VAS评分、NDI评分、颈椎曲度及椎间高度,末次随访时评价Odom分级及随访期间并发症发生情况。
1.5 统计学分析
运用SPSS 18.0统计学软件进行数据分析,计量资料以(±s)表示,组间两两比较经独立样本t检验,组内两两比较经配对t检验;以率(%)表示计数资料,经x2检验或Fisher确切概率法检验,以P<0.05表示差异有统计学意义。
2 结果
2.1 临床评估
2.1.1 两组手术前后JOA、VAS及NDI评分比较术后3、6、12个月及末次随访时,两组的JOA、VAS及NDI评分均显著改善(P<0.05),但组间各时间点比较并无显著性差异(P>0.05),见表1。
表1 两组手术前后JOA、VAS及NDI评分比较(±s,分)
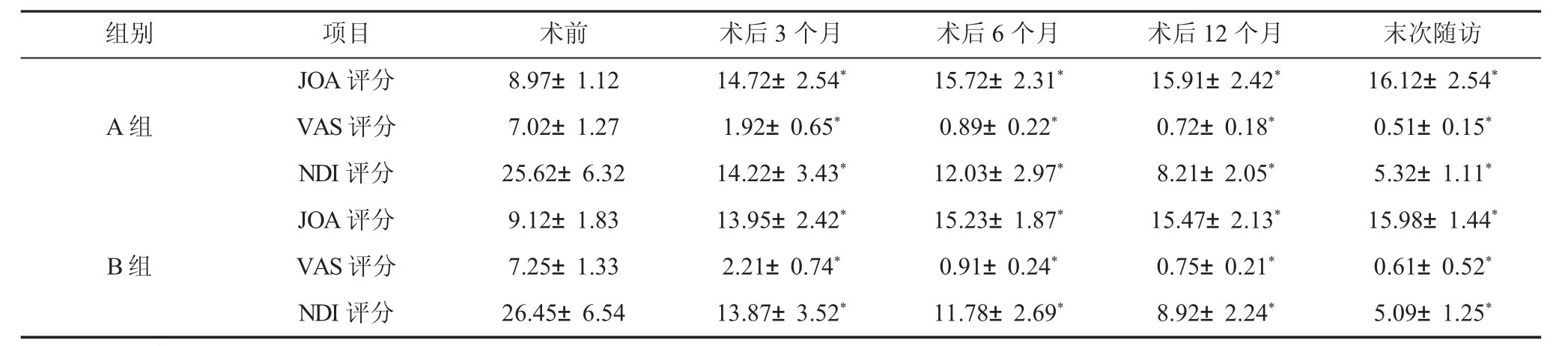
表1 两组手术前后JOA、VAS及NDI评分比较(±s,分)
注:与术前比较,*P<0.05
?
2.1.2 两组术后Odom分级比较 末次随访时,A组与B组的Odom优良率均在90%以上,组间比较差异无统计学意义(χ2=0.217,P=0.641>0.05),见表 2。
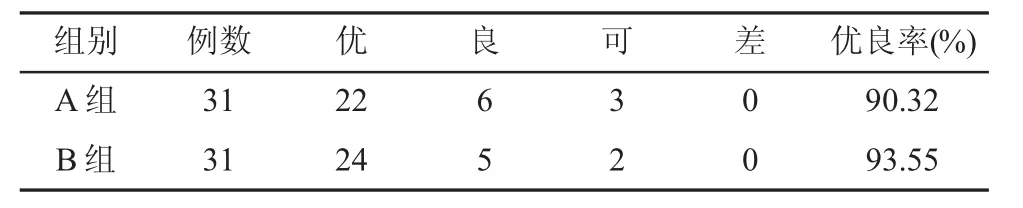
表2 两组术后Odom分级比较(例)
2.2 两组手术前后影像学数据比较
术后1d,A组的MRI上T1W/SE伪影最大面积为(102.34±13.45)mm2,B 组为(271.49±15.69)mm2,A组显著低于B组(P<0.05)。术前两组的颈椎生理曲度以及椎间高度均无明显差异,术后两组均显著性提高(P<0.05),但组间比较差异无统计学意义(P>0.05),见表 3。
表3 两组手术前后影像学数据比较(±s)

表3 两组手术前后影像学数据比较(±s)
注:与术前比较,*P<0.05
?
2.3 术后随访
两组术后均无内固定失效、内固定物松动、脱落或折断等。颈椎屈伸位及正侧位X线片复查显示,A组可吸收钉板固定患者的病变节段均融合良好,融合时间为 7~8个月,平均(7.35±0.42)个月;B 组钛合金钉板患者中1例未融合,融合率为96.77%(30/31),融合时间为 7~8 个月,平均(7.67±0.41)个月,两组融合率及融合时间比较差异无统计学意义(P>0.05);典型病例见图1。末次随访统计显示,两组均无迟发型食道瘘等并发症,A组1例(3.23%)轻度吞咽困难,随访期间未见ASD;B组术后1例(3.23%)轻度吞咽困难,4例(12.90%)ASD。两组总的并发症比较,经 Fisher检验无显著性差异(P=0.039>0.05);但ASD的发生率比较,B组显著高于A组(P<0.05)。
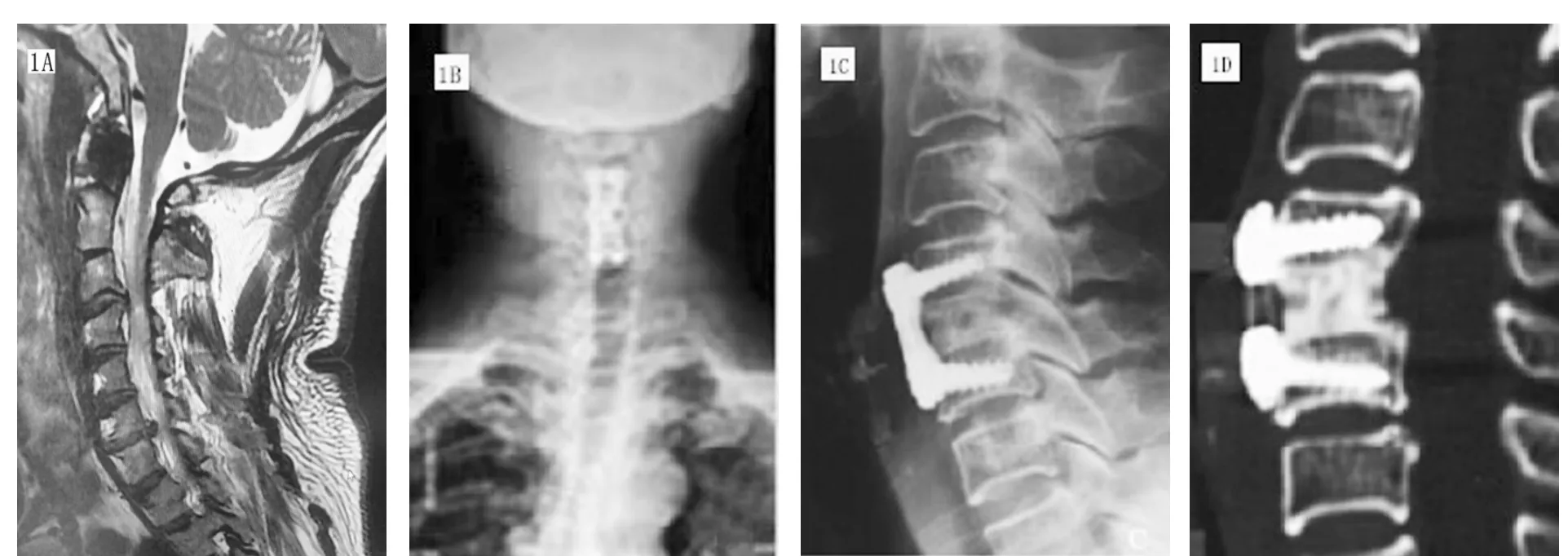
图1 患者,女,58岁,行颈前路椎间盘切除植骨融合术联合可吸收板内固定。1A:术前MRI示椎体明显受压;1B:术后即刻正位X线;1C:术后6个月侧位X线示椎体表面影像学密度增大,提示植骨初步融合;ID:术后12个月CT矢状面三维重建显示植骨块密度增大,植骨基本融合。
3 讨论
CSM手术治疗目的主要是解除神经根以及脊髓受压,重建椎管及颈椎解剖形态及功能,从而促进脊髓功能的恢复。手术效果主要取决于充分减压、骨性融合、术后椎体生理曲度及椎间高度的有效重建[2]。ACDF内固定术能够有效提高术后脊柱稳定性,并维持颈椎生理曲度,从而改善临床预后[1-3]。钛合金钉板系统是目前颈椎病ACDF治疗中最常应用的内固定物,具有生物相容性、材质不易腐蚀、质量较轻等优点,且相比于其他金属材料而言对术后MRI、CT或X线等的影响较小[5]。但钛合金钉板系统存在金属内固定物常见问题,如内固定物松动、脱落或者折断等,且钛合金钉板过长将增加术后ASD发生风险,钉板移位以及应力遮挡等将导致前路软组织结构甚至脊髓神经受压,造成植骨不融合。此外,钛合金钉板系统对于MRI及CT等影像学具有一定的干扰,影像伪影将影响术后评估及后续处理[6]。
S-1TM型可吸收内固定系统是由内消旋乳酸与左旋乳酸共聚形成的一种聚合物材料,具有极强的弹性及可塑性,且其弹性优于钛合金钉板,生物模量较好,故术后可减少应力遮挡,有效减少假关节形成风险[3]。可吸收板系统具有较好的粘弹性以及半刚性,在受到持续压力作用下可出现微小形变,从而分担移植物的负荷,且其具有于人体骨较为接近的弹性模量,在置入体内后能够随着颈椎生理活动而发生微动[7]。因此,可吸收板系统相较于钛合金钉板系统等更加符合人体颈椎生物力学特征,有利于促进植骨融合。Aryan等[8]对52例单节段ACDF中采用可吸收板内固定系统治疗者进行了为期12个月左右的随访,结果显示其植骨融合率高达98.1%,显著优于行内固定术者,且融合率与传统钛合金钉板内固定系统基本一致。本研究随访24个月以上显示,A组可吸收板内固定后均获得植骨融合,B组钛合金板内固定后1例未融合,两种内固定物在融合率及融合时间方面无明显差异,证实可吸收板内固定用于CSM的ACDF治疗可获得与传统钛合金钉板内固定系统相当的融合效果。考虑为可吸收板内固定可随着时间的推移逐步吸收,内固定强度逐渐下降,这有利于颈椎逐步恢复载荷,并可减少应力遮挡,从而促进骨性融合[9]。
ACDF术后生理曲度的恢复以及椎间隙高度的重建及维持是减少CSM患者术后ASD的关键,也是影响临床预后的主要因素,而坚强内固定是重建CSS椎间结构的关键。生物力学测试研究表明,S-1TM型可吸收板对于颈椎及融合器的稳定性作用与传统钛合金钉板系统基本一致,且其能够在体内发生水解反应而随着代谢废物排出体外[10]。郑伟东等[11]研究表明,S-1TM型可吸收板在植入体内后,其强度能够维持16周,术后6~9个月左右强度仍可维持70%-90%左右,此后其强度将逐渐降低、丧失,约2~4年可完全吸收。本研究中,两组术后3、6个月颈椎曲度及椎间隙高度均较术前显著提高,末次随访时虽然存在一定的丢失,但幅度均较小,且A组与B组之间比较并无显著性差异。同时,两组术后JOA评分、VAS评分及NDI指数均相较于术前显著改善,组间比较亦未见统计学差异,证实可吸收板内固定与钛合金钉板系统内固定能够获得相当的近期疗效,均可有效改善和维持颈椎生理曲度以及椎间隙高度。末次随访时患者的临床症状获得了显著改善,A组的Odom优良率为90.32%,与B组的93.55%比较并无明显差异,且术后未见钉板移位、松动及断裂等,近期疗效较好。
既往观点认为,应用可吸收板内固定系统治疗后,在聚乳酸降解过程中可能生成乳酸单体,导致局部组织pH水平异常变化,从而诱导相邻组织异常反应,故术后存在组织肿胀或者吞咽困难发生风险[9]。但Daentzer等[12]研究证实,上述乳酸单体具有较好的组织相容性,几乎不会诱发组织异常反应。Nabhan等[13]前瞻性随机对照研究发现,ACDF中应用生物可吸收板内固定治疗单节段神经根型颈椎病的生物力学稳定性、植骨融合效果、术后VAS评分及NDI指数均与传统钛合金钉板系统基本一致,且术后MRI随访未见颈部组织肿胀、感染或血肿形成等病变。本研究中,A组与B组除各有1例术后即刻轻度吞咽困难外,未见上述反应。此外,由于可吸收内固定板及其螺钉具有射线可穿透性,且其具有钽标记点,术后影像学检查较为方便,能够避免金属内固定物所致影像学伪影,便于术后观察有无内固定系统移位、脱落、断裂等[14]。本研究中,A组术后MRI伪影面积相较于B组显著降低,证实了上述观点。ACDF术后由于相邻椎体的载荷以及活动度增加,更容易发生ASD。同时,钛合金钉板在植入体内后,无法被人体所吸收,部分患者在带板期间存在不适感或心理压力,术后再次手术取出内固定物时将增加患者的痛苦及相关并发症发生风险。可吸收板最终能够完全被吸收,故术后无需再次手术移除内固定物,减少再次创伤。可吸收板内固定系统的螺钉固定角度具有可选择性,故能够为内固定提供最佳的单皮质固定效果及最理想的固定角度。而传统钛合金内固定系统稍有不慎即可导致头尾侧与相邻椎间隙相距过近或者超出椎体边缘,增加术后ASD发生风险[15]。本研究中,B组ASD发生率为12.90%,而A组未见ASD,组间比较差异有统计学意义,认为在CSS患者的ACDF中应用可吸收板内固定较钛合金钉板内固定能够降低ASD发生率,可能与其较高的植骨融合率、生物力学稳定性及无应力遮挡等有关。
综上所述,ACDF联合生物型可吸收板内固定系统治疗CSM能够获得与传统钛合金钉板系统内固定相当的脊柱稳定性,且可避免钛合金钉板系统所具有的内固定失效或失败、内固定物移位或松动、应力遮挡以及影像学干扰等诸多缺陷,且术后无需再次手术取出内固定物,无钉板降解所致相邻组织病变,植骨融合率以及生物力学稳定性均较好,近期疗效满意。
[1]王兴平,杨武军.颈前路零切迹椎间融合固定系统与传统钛板联合Cage融合内固定在双节段脊髓型颈椎病的近期疗效对比[J].颈腰痛杂志,2016,37(6):542-544.
[2]李程,王冰,王一宇,等.两种前路手术治疗邻近双节段脊髓型颈椎病的临床效果[J].中国脊柱脊髓杂志,2015,25(5):433-437.
[3]陈朦村,杨述华,杨操,等.可吸收固定板在脊髓型颈椎病前路减压融合术中的应用[J].中华骨科杂志,2015,35(6):602-609.
[4]李增春,陈德玉,吴德升,等.第三届全国颈椎病专题座谈会纪要[J].中华外科杂志,2008,46(23):1796-1799.
[5]李涛,李志丹,肖启贤,等.颈前路椎体次全切除钛网植骨锁定钢板内固定术治疗双节段脊髓型颈椎病[J].临床骨科杂志,2015,18(1):15-17,22.
[6]沈雄杰,黄象望,张毅,等.颈椎前路减压钛网植骨融合术后内固定早期失败原因及预防[J].医学临床研究,2012,29(2):267-270.
[7]Rodrigo V,Maza A,Calatayud JB,et al.Long-term follow-up of anterior cervical discectomy and fusion with bioabsorbable plates and screws[J].Clin Neurol Neurosurg,2015,136(9):116-121.
[8]Aryan HE,Lu DC,Acosta-FL Jr,et al.Bioabsorbable anterior cervical plating:initial multicenter clinical and radiographic experience[J].Spine,2007,32(10):1084-1088.
[9]杨海松,陈德玉,史建刚,等.生物型可吸收颈椎前路钉板系统应用于单节段颈椎病的初步临床研究[J].中国脊柱脊髓杂志,2015,25(4):304-310.
[10]Whitmore RG,Tykocinski ES,Sanborn MR,et al.Bioresorbable anterior cervical plate device for multi-level degenerative disc disease:case report with 8-year follow-up[J].J Clin Neurosci,2011,18(12):1736-1738.
[11]郑伟东,李亮,章培标,等.左旋聚乳酸颈椎可吸收固定板的力学性能测试[J].中国组织工程研究与临床康复,2010,14(12):2191-2194.
[12]Daentzer D,Floerkemeier T,Bartsch I,el al.Preliminary results in anterior cervical discectomy and fusion with an experimental bioabsorbable cage-clinical and radiological findings in an ovine animal model[J].Springerplus,2013,2(1):1-8.
[13]Nabhan A,Ishak B,Steimer O,et al.Comparison of bioresorbable and titanium plates in cervical spinal fusion:early radiologic and clinical results[J].J Spinal Disord Tech.2009;22(3):155-161.
[14]Tomasino A,Gebhard H,Parikh K,et a1.Bioabsorbable instrumentation for single-level cervical degenerative disc disease:A radiological and clinical outcome study-Clinical article[J].J Neurosurg Spine,2009,11(5):529-537.
[15]张大明,吕游,张洪鑫,等.可吸收钉板在颈椎前路椎体次全切除术中的应用研究[J].生物骨科材料与临床研究,2015,12(5):55-57.

