中、重度特应性皮炎的诊断和治疗进展
孙晓丽 李邻峰
100050北京,首都医科大学附属北京友谊医院皮肤科
特应性皮炎(AD)是一种慢性、瘙痒性、炎症性皮肤病。全世界的患病率成人达2%~5%,儿童达10%~20%[1],其中20%属于中、重度[2]。AD发病机制复杂,涉及免疫系统过度活化、上皮屏障功能障碍和皮肤微生物群失调等诸多方面[3-5]。轻度患者可外用润肤剂、糖皮质激素(简称激素)或钙调磷酸酶抑制剂治疗[6],中、重度患者常需联合免疫抑制剂甚至生物制剂治疗[7]。AD诊断标准众多,如Hanifin和Rajka标准、Williams标准等[8],但对于中、重度AD的诊断目前尚无统一标准。现从近年来国内外常用的AD诊疗指南入手,结合近年中、重度AD患者进行的临床试验,对中、重度AD的诊断标准进行评价并对其治疗进展进行概述。
一、中、重度AD的诊断标准
检索2010年至今国内外指南和临床试验中关于中、重度AD的界定标准,总结见表1。
从表1可以看出:①5种指南中,有4种推荐采用特应性皮炎积分指数(SCORAD)评分评估AD病情严重程度,其中1种指南明确表示SCORAD≥25为中、重度 AD,1种指南SCORAD≥20为中、重度 AD;②8项临床试验中,有6项采用SCORAD评分评估AD病情严重程度,其中3项采用SCORAD≥25为中、重度AD入组标准,2项采用SCORAD≥15为中、重度AD入组标准,1项采用SCORAD≥20为中、重度AD入组标准;③欧洲特应性皮炎工作组/欧洲皮肤性病学会湿疹工作组(ETFAD/EADV)指南中,2009年SCORAD≥15为中、重度AD,2015年改为SCORAD≥25为中、重度AD,表明中、重度AD的界定标准较之前更为严格。Williams诊断标准简单易行,且特异性和敏感性与Hanifin和Rajka标准相似,更适用于临床实践需要,所以中国推荐采用Williams诊断标准诊断AD[15]。SCORAD评分标准快速、简单,包括客观表现(皮损面积、皮损严重程度)和主观症状(瘙痒和影响睡眠程度),在世界范围内应用广泛,曾被一些学者认为是评价AD病情严重程度的金标准。因此,推荐采用SCORAD评分法评估AD病情严重程度,以SCORAD≥25为界定中、重度AD的标准。

表1 诊疗指南和临床试验中对中、重度特应性皮炎(AD)的界定标准
二、中、重度AD的治疗
(一)治疗现状:中、重度AD治疗困难,往往需要在个体化的基础上采取综合疗法。孙彩虹和顾恒[23]综合分析不同国家和地区AD治疗指南认为,患者健康教育及使用润肤剂是基础,同时应避免各种可疑加重病情的因素。一线外用药首选糖皮质激素(激素),皮肤薄弱部位或不适用激素者可选用钙调磷酸酶抑制剂,或二者序贯使用。研究表明,0.1%他克莫司软膏与中强效激素抗炎效果相当,1%吡美莫司乳膏与弱效激素相当。长期外用激素应注意局部感染、萎缩、多毛、毛细血管扩张等不良反应。紫外线光疗作为中、重度AD的二线疗法,能调节T细胞功能及相关炎症介质,适用于>12岁的儿童及成人患者。通常需要坚持照射1~2个月,每周3次,但长期光疗应注意远期皮肤癌的风险。Rodenbeck等[24]研究发现,窄谱中波紫外线(NB-UVB)和中等剂量的UVA-1是对AD最有效的光疗方式。NB-UVB对慢性AD最有效,UVA-1适用于急性发作患者。Goeckerman疗法(煤焦油+BB-UVB)对重度AD有效,但煤焦油致癌的风险限制了它的普及;308 nm准分子激光可能是局部难治性AD的较好选择。儿童患者安全使用NB-UVB有据可查,但其他形式的光疗研究文献尚少,因此必须谨慎使用。湿包具有增加皮肤水合度,增强药物吸收,减少搔抓,保护皮肤屏障的作用。Nicole等[25]研究发现,湿包可有效缓解急性中、重度AD患者的临床症状,并建议将湿包疗法作为对传统治疗无效的中、重度AD患者使用系统免疫抑制剂之前的一种治疗手段。当以上治疗方法均无效时,在除外严重感染、活动性结核、肿瘤等疾病的情况下,可尝试使用免疫抑制剂和新型生物制剂治疗,如环孢素A(CysA)、硫唑嘌呤(AZA)、甲氨蝶呤(MTX)、吗替麦考酚酯(MMF)等。Roekevisch等[26]通过回顾性研究,建议将环孢素A作为中、重度AD系统治疗的一线用药。研究表明,环孢素A较高的初始剂量可快速控制病情,为减少药物不良反应,待症状控制后应逐渐减量至停药,以预防复发,用药期间需监测患者的血压、肾功能等。美国皮肤病学会对各免疫抑制剂应用于AD的推荐等级及用量[7]总结见表2。短期、间断使用有镇静作用的抗组胺药可能对剧烈瘙痒继发睡眠障碍的AD患者有益[7]。无感染证据时,不推荐系统应用抗生素。
(二)治疗进展:
1.生物制剂:Dupixent(dupilumab)是一种全人源化抗IL-4受体α亚基的单克隆抗体,可抑制IL-4和IL-13通路信号过度转导,降低血清IgE水平,抑制嗜酸性粒细胞聚集等。研究显示[1],Dupilumab治疗中、重度AD临床疗效显著(表现为瘙痒明显减轻,皮损几乎完全消退),且没有严重不良事件发生。当前已被美国食品药品监督管理局(FDA)批准治疗成人中、重度AD[27]。Dupixent是目前第一个也是唯一一个获批治疗AD的生物制剂,可单独用药,也可与外用激素联合,每隔1周皮下注射1次。
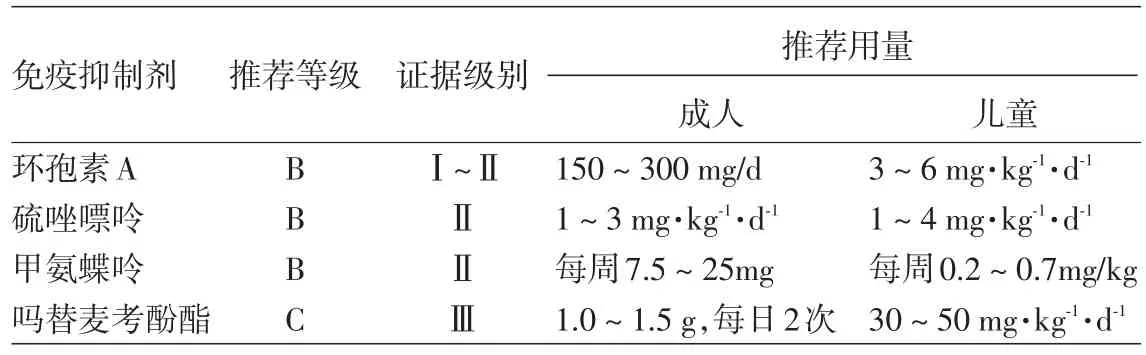
表2 美国皮肤病学会对各免疫抑制剂用于特应性皮炎的推荐等级及用量总结
ustekinumab(乌司奴单抗):是抗IL-12和IL-23共同亚单位p40的全人源性单克隆抗体,其特异性结合p40亚单位,干扰IL-12和IL-23介导的信号转导和细胞因子级联反应,发挥抗炎作用。Khattri等[16]的一项Ⅱ期双盲、安慰剂对照研究表明,乌司奴单抗治疗成年中、重度AD的疗效及安全性均较好,是一种非常有潜力的药物。然而,Saeki等[28]关于乌司奴单抗治疗日本重度AD患者的随机、双盲、安慰剂对照临床研究表明,乌司奴单抗与安慰剂相比,没有表现出显著的疗效。综合来看,乌司奴单抗治疗AD是否有效仍需大量的临床研究加以证实。
nemolizumab(CIM331):是抗IL-31受体A的人源性单克隆抗体。IL-31主要由激活的CD4+Th2细胞产生,可调控炎症和免疫反应,诱导细胞因子和炎症介质分泌,调节细胞增殖与分化等。有研究报道,IL-31在瘙痒性湿疹病变中过度表达,AD患儿的血清IL-31水平与疾病严重程度显著相关[29]。IL-31在AD瘙痒发病机制中发挥重要作用,抑制该途径可能为改善AD患者的瘙痒症状提供抗组胺药的替代方案[30],所以IL-31成为止痒药物研发的新靶点。Ruzicka等[31]研究表明,nemolizumab治疗成人中、重度AD可有效缓解瘙痒,改善湿疹面积及严重程度指数,是一种非常有前景的药物。
omalizumab(奥马珠单抗):是重组人源化抗IgE单克隆抗体,可选择性与IgE受体结合,降低血游离IgE水平,改善炎症反应。有研究表明,约80%以上的AD患者血IgE水平升高。当已致敏的机体再次接触相同抗原时,由IgE介导引发Ⅰ型超敏反应。奥马珠单抗目前已被FDA批准治疗哮喘和慢性特发性荨麻疹。尽管奥马珠单抗可以降低血IgE水平,但临床试验表明,治疗AD的疗效目前尚存在争议[32]。
rituximab(利妥昔单抗):是人鼠嵌合抗CD20单克隆抗体,通过介导抗体和补体依赖的细胞毒作用杀死具有抗原提呈作用的B细胞或诱导B细胞凋亡,从而减少T细胞活化,进而减少炎症介质及细胞因子的释放。对于利妥昔单抗治疗中、重度AD的疗效,尽管有治疗成功的个案报道,但仍缺乏随机、双盲、安慰剂对照的大样本临床试验加以支撑。
alefacept(阿来西普)、efalizumab(依法珠单抗):是针对T细胞的生物制剂,目前认为Th1/Th2平衡失调是特应性皮炎重要的发病机制。阿来西普是淋巴细胞功能蛋白(LFA)-3(CD58)和免疫球蛋白(Ig)G的融合蛋白,可抑制T细胞活化并诱导T细胞凋亡。有研究证明,阿来西普治疗难治性AD有效[12]。抗CD11a的依法珠单抗可阻断T细胞募集,但由于可导致进行性多灶性脑白质病,当前已撤出市场[12]。
etanercept(依那西普)、英夫利西单抗(infliximab)、adalimumab(阿达木单抗):是肿瘤坏死因子(TNF)拮抗剂,目前已被批准治疗银屑病,但治疗AD的临床疗效尚无定论。
pascolizumab(帕考珠单抗,IL-4受体拮抗剂)、mepolizumab(美泊珠单抗,IL-5拮抗剂)、tocilizumab(托珠单抗,IL-6受体拮抗剂)、Ixekinumab和 Brodalumab(IL-17及受体拮抗剂)等生物制剂,理论上均可针对AD免疫发病机制的某个环节发挥作用,但具体疗效及安全性如何,目前尚不清楚,仍在研究中[33]。
2.磷酸二酯酶抑制剂:apremilast是一种口服选择性磷酸二酯酶-4(PDE-4)抑制剂,可减少环磷酸腺苷和环磷酸鸟苷降解,抑制多种促炎症介质(PGE2、TNF-α、IL-2、IFN-γ、白三烯等)的生成而发挥抗炎、调节免疫作用。目前apremilast已完成了治疗成人AD的Ⅱ期临床试验,疗效和安全性俱佳。Saporito等[34]报道apremilast成功治疗1例儿童中、重度AD的病例。但是apremilast治疗中、重度AD的临床疗效仍需大样本临床试验证实。Eucrisa(crisaborole)软膏是一种外用选择性PDE-4抑制剂,已被FDA批准治疗≥2岁轻、中度AD 患儿[35]。
3.人脐血干细胞疗法:人脐血来源的干细胞皮下注射,可能通过降低IL-4、IgE水平,抑制肥大细胞脱颗粒等缓解AD的临床症状。Kim等[18]研究人脐血干细胞治疗中、重度AD患者的Ⅰ/Ⅱa期临床研究表明,受试者的瘙痒及皮损严重程度均有明显改善,且没有严重不良事件发生。干细胞疗法对于中、重度AD可能是一种潜在有效的治疗手段。
4.中医中药:中草药制剂清心培土颗粒由白术、太子参、山药、薏苡仁、白茅根、连翘、甘草、白鲜皮、珍珠粉9味中草药组成,具有培土清心、除烦止痒的功效。Gu等[22]研究表明,清心培土颗粒用于治疗儿童中、重度AD具有较高的疗效及安全性。
三、结语
SCORAD评分在国内外受到了较为广泛的认可,多数学者以SCORAD≥25为界定中、重度AD的标准。生物制剂是目前国际上中、重度AD的主要研究方向,磷酸二酯酶抑制剂、干细胞疗法和中医中药等也已在中、重度AD临床试验中显示出较好的前景。随着未来研究的不断深入和新型药物的研发,中、重度AD的治疗有望得到更加理想的疗效。
[1] Kraft M,Worm M.Dupilumab in the treatment ofmoderate-tosevere atopic dermatitis[J].Expert Rev Clin Immunol,2017,13(4):301-310.DOI:10.1080/1744666X.2017.1292134.
[2] Hamilton JD,Suárez-Fariñas M,Dhingra N,et al.Dupilumab improves themolecularsignature in skin ofpatientswithmoderateto-severe atopic dermatitis[J].JAllergy Clin Immunol,2014,134(6):1293-1300.DOI:10.1016/j.jaci.2014.10.013.
[3] Werfel T,Allam JP,Biedermann T,et al.Cellular and molecular immunologicmechanisms in patientswith atopic dermatitis[J].J Allergy Clin Immunol,2016,138(2):336-349.DOI:10.1016/j.jaci.2016.06.010.
[4] Boguniewicz M,Leung DY.Atopic dermatitis:a disease ofaltered skin barrier and immune dysregulation[J].Immunol Rev,2011,242(1):233-246.DOI:10.1111/j.1600-065X.2011.01027.x.
[5] WilliamsMR,Gallo RL.The role of the skinmicrobiome in atopic dermatitis[J].Curr Allergy Asthma Rep,2015,15(11):65.DOI:10.1007/s11882-015-0567-4.
[6] Eichenfield LF,Tom WL,Berger TG,et al.Guidelines of care for themanagement of atopic dermatitis:section 2.management and treatment of atopic dermatitis with topical therapies[J].J Am Acad Dermatol,2014,71(1):116-132.DOI:10.1016/j.jaad.2014.03.023.
[7]Sidbury R,Davis DM,Cohen DE,etal.Guidelines of care for the management of atopic dermatitis:section 3.management and treatmentwith phototherapy and systemic agents[J].JAm Acad Dermatol,2014,71(2):327-349.DOI:10.1016/j.jaad.2014.03.030.
[8]张建中.特应性皮炎的诊断标准发展及评价[J].中华皮肤科杂志,2017,50(1):67-69.DOI:10.3760/cma.j.issn.0412-4030.2017.01.025.
[9] Wollenberg A,Oranje A,Deleuran M,et al.ETFAD/EADV eczema task force 2015 position paper on diagnosis and treatment of atopic dermatitis in adult and paediatric patients[J].J Eur Acad Dermatol Venereol,2016,30(5):729-747.DOI:10.1111/jdv.13599.
[10] Darsow U,Wollenberg A,Simon D,et al.ETFAD/EADV eczema task force 2009 position paper on diagnosis and treatment of atopic dermatitis[J].J Eur Acad Dermatol Venereol,2010,24(3):317-328.DOI:10.1111/j.1468-3083.2009.03415.x.
[11] Ring J,Alomar A,Bieber T,et al.Guidelines for treatment of atopic eczema(atopic dermatitis)part I[J].JEur Acad Dermatol Venereol,2012,26(8):1045-1060.DOI:10.1111/j.1468-3083.2012.04635.x.
[12] Ring J,Alomar A,Bieber T,et al.Guidelines for treatment of atopic eczema (atopic dermatitis) Part II[J].J Eur Acad Dermatol Venereol,2012,26(9):1176-1193.DOI:10.1111/j.1468-3083.2012.04636.x.
[13] Eichenfield LF,Tom WL,Cham lin SL,et al.Guidelines of care for themanagementof atopic dermatitis:section 1.Diagnosis and assessment of atopic dermatitis[J].JAm Acad Dermatol,2014,70(2):338-351.DOI:10.1016/j.jaad.2013.10.010.
[14] Saeki H,Nakahara T,Tanaka A,et al.Clinical Practice Guidelines for the Management of Atopic Dermatitis 2016[J].J Dermatol,2016,43(10):1117-1145.DOI:10.1111/1346-8138.13392.
[15]中华医学会皮肤性病学分会免疫学组、特应性皮炎协作研究中心.中国特应性皮炎诊疗指南(2014版)[J].中华皮肤科杂志,2014,47(7):511-514.DOI:10.3760/cma.j.issn.0412-4030.2014.07.018.
[16] Khattri S,Brunner PM,Garcet S,et al.Efficacy and safety of ustekinumab treatment in adults with moderate-to-severe atopic dermatitis[J].Exp Dermatol,2017,26(1):28-35.DOI:10.1111/exd.13112.
[17] Wong SM,Ng TG,Baba R.Efficacy and safety of sodium hypochlorite(bleach)baths in patients with moderate to severe atopic dermatitis in Malaysia[J].JDermatol,2013,40(11):874-880.DOI:10.1111/1346-8138.12265.
[18] Kim HS,Lee JH,Roh KH,et al.Clinical Trical of human umbilical cord blood-derived stem cells for the treatment of moderate-to-severe atopic dermatatitis:phase I/IIa studies[J].Stem Cells,2017,35(1):248-255.DOI:10.1002/stem.2401.
[19] Edwards AM,Bibawy D,Matthews S,etal.Long-term use of a 4%sodium cromoglicate cutaneous emulsion in the treatment of moderate to severe atopic dermatitis in children[J].JDermatolog Treat,2015,26(6):541-547.DOI:10.3109/09546634.2015.1034077.
[20] Mehrbania M,Choopani R,Fekri A,et al.The efficacy ofwhey associated with dodder seed extract on moderate-to-severe atopic dermatitis in adults:a randomized,double-blind,placebocontrolled clinical trial[J].JEthnopharmacol,2015,172:325-332.DOI:10.1016/j.jep.2015.07.003.
[21] Nicol NH,Boguniewicz M,Strand M,et al.Wetwrap therapy in children with moderate to severe atopic dermatitis in a multidisciplinary treatment program[J].JAllergy Clin Immunol Pract,2014,2(4):400-406.DOI:10.1016/j.jaip.2014.04.009.
[22] Gu SX,Zhang AL,Coyle ME,et al.Chinese herbal medicine granules(PTQX)for children with moderate to severe atopic eczema:study protocol for a randomised controlled trial[J].Trials,2015,16:294.DOI:10.1186/s13063-015-0806-y.
[23]孙彩虹,顾恒.不同国家和地区特应性皮炎治疗指南解读[J].中华皮肤科杂志,2017,50(03):215-218.DOI:10.3760/cma.j.issn.0412-4030.2017.03.017.
[24] Rodenbeck DL,Silverberg JI,Silverberg NB.Phototherapy for atopic dermatitis[J].Clin Dermatol,2016,34(5):607-613.DOI:10.1016/j.clindermatol.2016.05.011.
[25] Nicole NH,Boguniewicz M.Wet wrap therapy in moderate to severe atopic dermatitis[J].Immunol Allergy Clin North Am,2017,37(1):123-139.DOI:10.1016/j.iac.2016.08.003.
[26] Roekevisch E,Spuls PI,Kuester D,et al.Efficacy and safety of systemic treatments for moderate-to-severe atopic dermatitis:a systematic review[J].J Allergy and Clin Immunol,2014;133(2):429-438.DOI:10.1016/j.jaci.2013.07.049.
[27] FDA approvesnew eczema drug Dupixent.March 28,2017.https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm549078.htm.
[28] Saeki H,Kabashima K,Tokura Y,et al.Efficacy and safety of ustekinumab in Japanese patientswith severe atopic dermatitis:a randomized,double-blind,placebo-controlled,phase IIstudy[J].Br JDermatol,2017,DOI:10.1111/bjd.15493.
[29] Heratizadeh A,Werfel T.Anti-inflammatory therapies in atopic dermatitis[J].Allergy,2016,71(12):1666-1675.DOI:10.1111/all.13065.
[30] Saleem MD,Oussedik E,D′Amber V,et al.Interleukin-31 pathway and its role in atopic dermatitis:a systematic review[J].JDermatolog Treat,2017,2:1-9.DOI:10.1080/09546634.2017.1290205.
[31] Ruzicka T,Hanifin JM,Furue M,et al.Anti-Interleukin-31 Receptor a antibody for atopic dermatitis[J].N Engl J Med,2017,376:826-835.DOI:10.1056/NEJMoa1606490.
[32] Montes-Torres A,Llamas-Velasco M,Pérez-Plaza A,et al.Biological treatments in atopic dermatitis[J].JClin Med,2015,4(4):593-613.DOI:10.3390/jcm4040593.
[33] Guttman-Yassky E,Dhingra N,Leung DY.New era of biologic therapeutics in atopicdermatitis[J].ExpertOpin Biol Ther,2013,13(4):549-561.DOI:10.1517/14712598.2013.758708.
[34] Saporito RC,Cohen DJ.apremilast use for moderate-to-severe atopic dermatitis in pediatric patients[J].Case Rep Dermatol,2016,8(2):179-184.DOI:10.1159/000446836.
[35] FDA approves Eucrisa for eczema.December 14,2016.https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm533371.htm.

