1-(苯氧乙酰基)-3-芳基咪唑啉-2,4-二酮类化合物的合成及除草活性
韩金涛,王秀丽,刘 钰,丛云波,董文凯,柴洪伟,李旭坤
(山东省农药科学研究院,山东省化学农药重点实验室,济南 250100)
咪唑啉酮类除草剂是由美国氰胺公司(现巴斯夫)开发成功的一类高效低毒产品,主要用于大豆田除草。其作用机理与磺酰脲类除草剂类似,通过抑制乙酰乳酸合成酶(ALS),导致侧链氨基酸的生物合成受阻而使杂草死亡[1]。上市之初,该类除草剂因其广谱、高效而迅速占领市场,近年来由于草甘膦抗性杂草逐年增多,以及抗咪唑啉酮类除草剂作物(Clearfield)的上市,此类除草剂迎来了新的发展机遇。咪唑啉酮类除草剂2009—2014年复合增长率为8.4%[2]。
咪唑啉酮类除草剂按其结构主要分为咪唑啉-4-酮和咪唑啉-2,4-二酮,目前6个商品化的咪唑啉酮类品种,均具有咪唑啉-4-酮结构。它们分别是咪唑烟酸(imazapyr)、咪唑乙烟酸(imazethapyr)、咪草酸(imazamethabenz-methyl)、咪唑喹啉酸(imazaquin)、甲氧咪草烟(imazamox)和甲咪唑烟酸(imazapic)。咪唑啉-2,4-二酮虽然至今没有商品化产品,但其衍生物的除草活性已有报道[3-6]。例如,化合物Hydantocidin的除草活性与草甘膦相当,是腺苷酸琥珀酸合成酶(AdSS)的天然抑制剂,能够阻断植物体内嘌呤的合成而造成杂草死亡[7]。已有的构效关系研究表明,咪唑啉酮结构单元是Hydantocidin发挥除草活性的关键部位之一[8]。笔者在前期的研究工作中合成了一系列咪唑啉-2,4-二酮类衍生物,发现了一些具有潜在除草活性的化合物[9-11]。本文在前期工作基础上,根据活性亚结构单元拼接原理,将苯氧乙酰结构单元引入到咪唑啉-2,4-二酮分子结构中,设计、合成了12个未见文献报道的1-(取代苯氧乙酰基)-3-取代芳基咪唑啉-2,4-二酮类化合物(合成路线见图1),并对其除草活性进行了测定,以期发现新的、高除草活性的咪唑啉-2,4-二酮类化合物。

图1 目标化合物的合成路线
1 实验部分
1.1 仪器和试剂
WRS-2微机熔点仪、Bruker DPX 300 MHz核磁共振仪(以CDCl3为溶剂,TMS为内标)、Shimadzu IR-435红外光谱仪(KBr压片法)。氨基酸、苯胺、氢氧化钠等主要化学试剂为国产化学纯;三乙胺经过重新蒸馏后使用;二氯甲烷经过干燥处理。
1.2 1-(取代苯氧乙酰基)-3-取代芳基咪唑啉-2,4-二酮系列化合物的合成
1.2.1 苯基异氰酸酯(中间体2)的合成[12]
以4-氯苯基异氰酸酯的合成为例。称取44.0 g(0.15 mol)固体三光气,溶于500 mL 1,2-二氯乙烷中,冰浴搅拌,慢慢滴加含28.0 g(0.22 mol)对氯苯胺的100 mL 1,2-二氯乙烷溶液,温度保持在5℃以下。滴加过程中,逐渐有白色不溶物析出,滴加完毕后,室温搅拌1 h。然后升温至88℃,回流反应4 h,反应液逐渐变为澄清。TLC监测对氯苯胺反应完毕后,将1,2-二氯乙烷蒸除,得黄色油状物,产物不经分离,直接投入下步反应。
1.2.2 3-取代芳基-5-烷基咪唑啉-2,4-二酮(中间体3)的合成[13]
以3-(4-氯苯基)-5-异丙基咪唑啉-2,4-二酮的合成为例。在150 mL三颈瓶中,加入11.7 g(0.10 mol)缬氨酸、4.4 g(0.11 mol)固体NaOH、100 mL蒸馏水,搅拌溶解,滴加含15.4 g(0.10 mol)4-氯苯基异氰酸酯的丙酮溶液(30 mL),30 min滴加完毕。室温搅拌20 min后升温到40℃继续搅拌2 h,TLC监测。过滤除去不溶物,滤液加入浓盐酸调至pH值接近1时有白色固体析出。固液加热至106~110℃,回流2 h。冷却至室温,析出固体,过滤,滤饼用蒸馏水洗至中性,干燥后称重,得白色粉末状固体20.4 g,产率80.5%,熔点161.4~163.1℃。
其它中间体按此方法合成。
1.2.3 酰氯(中间体4)的合成[14]
以2,4-二氯苯氧乙酰氯的制备为例。在250 mL三颈烧瓶中,加入22 g(0.10 mol)2,4-二氯苯氧乙酸、5滴DMF,装上回流冷凝管、温度计和10%NaOH水溶液的气体吸收装置。磁力搅拌下加入40 mL新蒸的二氯亚砜,加热回流至无气体逸出,反应体系为黄色澄清溶液。把反应液转入100 mL圆底烧瓶中,回收过量的二氯亚砜。产物不经分离,直接投入下步反应。
其它酰氯按照此方法合成。
1.2.4 1-(取代苯氧乙酰基)-3-芳基-5-烷基咪唑啉-2,4-二酮(化合物H)的合成
以1-(2,4-二氯苯氧乙酰基)-3-(4-氯苯基)-5-异丙基咪唑啉-2,4-二酮(H5)的合成为例。在装有磁力搅拌、低温温度计、氯化钙干燥管及恒压滴液漏斗的150 mL的三颈瓶中,加入0.76 g(3 mmol)中间体3-(4-氯苯基)-5-异丙基咪唑啉-2,4-二酮、0.6 g(6 mmol)三乙胺和20 mL二氯甲烷,冰盐浴冷却至0℃左右。搅拌下滴加0.73 g(3 mmol)2,4-二氯苯氧乙酰氯和15 mL二氯甲烷的混合液,30 min滴加完毕。撤除冰盐浴,使反应液温度回升到室温,继续搅拌反应2 h,TLC跟踪至原料反应完全。反应液先用饱和NaHCO3水溶液洗涤至弱碱性,再用饱和食盐水和蒸馏水各洗涤1次,所得有机相用无水Na2SO4干燥过夜。过滤,减压蒸除溶剂,残余物柱层析(V石油醚∶V乙酸乙酯=3∶1),得到白色固体,干燥称重1.13 g,收率83.1%。
其它目标产物按照此方法合成。
目标化合物的主要理化数据见表1,核磁、红外数据见表2。
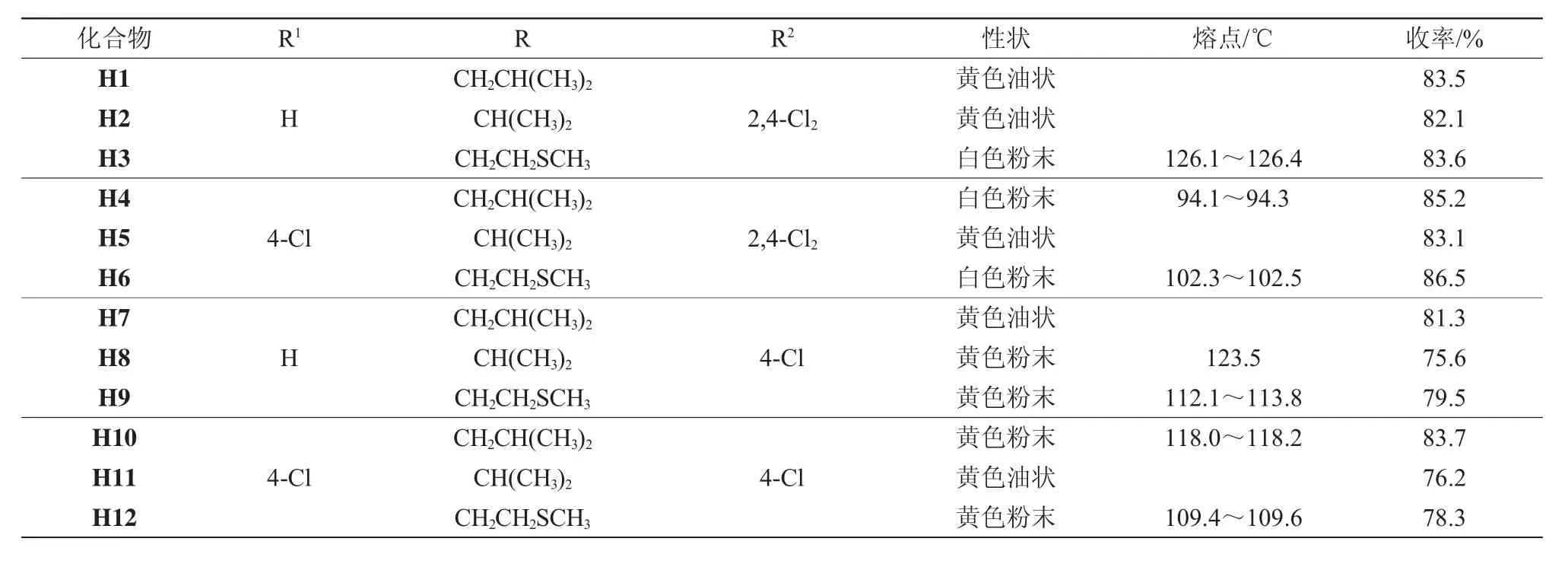
表1 目标化合物的理化数据

表2 目标化合物的核磁、红外数据
2 结果与讨论
2.1 化合物的合成及波谱特征
3-取代芳基-5-烷基咪唑啉-2,4-二酮类化合物的文献报道合成方法采用分步法[13]。异氰酸酯与氨基酸在碱性条件下反应,酸化后首先得到固体取代酰基脲,将取代酰基脲分离,转移至酸性溶液中加热后关环得到目标物。2步反应都需要消耗大量的酸,并且操作较为繁琐。本研究在实际操作时将2步反应合并为1步,将酸化后的取代酰基脲溶液(pH值≈1)直接加热回流得到目标产物,减少了浓盐酸的用量,精简了反应步骤,3-取代芳基-5-烷基咪唑啉-2,4-二酮类化合物(中间体3)的收率均在80%以上。
在目标化合物的1H NMR谱图中,δ 6.7~7.5范围内为杂环咪唑啉-2,4-二酮N-1以及N-3位取代芳环上的氢;δ 5.25处为苯氧乙酸基团中亚甲基的2个氢,由于受到氧原子的诱导效应而向低场移动;δ 4.70左右为咪唑啉酮环上次甲基的氢,受到邻位质子作用,发生耦合形成多重峰。以目标化合物H5的结构为例,δ6.80-7.41范围内分布着2个氯原子取代的苯环上的3个氢,其中δ 7.41处为3-位苯环上的氢,δ 7.16处的2重峰为5-位苯环上的氢,耦合常数为J=8.7 Hz,δ 6.82处的2重峰为6-位苯环上的氢,耦合常数J=8.7 Hz;δ 5.31处为苯氧乙酸基团中次甲基的2个氢,由于受到氧原子的诱导效应而向低场移动;δ 4.68处的2重峰为咪唑啉酮环上次甲基的氢,受到邻位质子作用耦合成双峰,J=3.3 Hz;δ 2.63-2.78处为咪唑啉-2,4-二酮5-位异丙基上次甲基的氢;δ 1.26和0.97处的2个峰为异丙基中2个甲基的氢。
在目标化合物的红外光谱中,2 960 cm-1附近有-CH3、-CH2的伸缩振动吸收峰,1 748 cm-1附近有明显的-CO伸缩振动吸收峰,1 470-1 600 cm-1有苯环碳骨架伸缩振动吸收峰,1 090 cm-1附近有C-O-C不对称伸缩振动吸收峰。
2.2 化合物的生物活性
以稗草和油菜作为测试对象,采用平皿法对目标化合物进行生物活性测试。以2,4-滴为对照药剂,并设空白对照(CK),结果见表3。

表3 目标化合物在100 mg/L下对油菜和稗草的抑制率 %
初步生物活性测试结果表明:在100 mg/L质量浓度下,化合物H3、H5对油菜的根长和株高有良好的抑制作用,抑制率达100%。除目标化合物H7、H8对稗草根的抑制作用稍弱外,其余目标化合物对油菜和稗草的根、茎抑制率均在80%以上。其中化合物H1、H2、H3、H5、H6、H9、H11对稗草的抑制效果好于对照药剂2,4-滴;化合物H3、H5、H10、H11、H12对油菜的抑制效果好于对照药剂。总体而言,目标化合物对双子叶植物油菜的抑制效果好于对单子叶植物稗草,目标化合物具有一定的选择性。对稗草来说,化合物H2、H5、H11均表现出较好的除草活性,说明在其它取代基相同的条件下,咪唑啉-2,4-二酮5-位为CH(CH3)2时的活性好于CH2CH(CH3)2和CH2CH2SCH3;对油菜的除草活性而言,咪唑啉-2,4二酮1-位为2,4-二氯苯氧乙酰基的活性与4-氯苯氧乙酰基的活性相当。
[1]张敏恒.咪唑啉酮类除草剂的结构-活性关系及合成进展[J].农药,1991,30(3):36-39.
[2]顾林玲,王欣欣.全球除草剂市场、发展概况及趋势(Ⅰ)[J].现代农药,2016,15(2):8-12.
[3]Singer M S.Imidazolidinedione Herbicides:US,3655689[P].1972-04-11.
[4]Thibault T D.2,4-Imidazolidinediones,Compositions and Herbicidal Method:US,4345935[P].1982-08-24.
[5]Prisbylla M P.Novel 5-Aminomethylene-2,4-imidazolidinediones and5-Aminomethylene-2-thionoimidazolidine-4-ones:US,4859228[P].1989-08-22.
[6]Schaefer M.Herbicidal Bicyclic Hydantoins:WO,9523509[P].1995-09-08.
[7]Nakajima M,Itoi K,Takamatsu Y,et al.Hydantocidin:A New Compound with Herbicidal Activity from Streptomyces hygroscopicus[J].Antibiot,1991,44(3):293-300.
[8]汪月鹏,王明安,杜凤沛,等.腺苷酸琥珀酸合成酶与其抑制剂的分子机制研究[J].高等学校化学学报,2010,31(2):336-342.
[9]韩金涛,王进敏,王明安,等.5-(4-羟基苯基)-2,4-咪唑啉二酮酯类化合物合成及生物活性[J].有机化学,2010,30(5):691-697.
[10]韩金涛,王进敏,董宏波,等.含咪唑啉2,4-二酮的新型磷酰胺酯类化合物的合成和生物活性 [J].有机化学,2013,33(3):596-601.
[11]Han J T,Wang J M,Dong H B,et al.Synthesis and Herbicidal Activity of 5-(4-Hydroxybenzyl)-2-thioxoimidazolidin-4-one Esters[J].Molecules,2011,16(4):2833-2845.
[12]王向辉,贺永宁,盘茂东.三光气法合成苯基异氰酸酯 [J].应用化工,2008,39(9):1019-1021.
[13]SauliM.Processforthe Preparation of1-Carbamoyl-3-(3,5-dichlorophenyl)-hydantoins:US,4076941[P].1978-02-28.
[14]信建峰,马吉海,张树芬,等.酰氯制备方法综述 [J].河北化工,2006,29(11):16-18.

