细菌对电化学发光免疫分析法检测乙型肝炎指标结果的影响
(皖南医学院第一附属医院 弋矶山医院 检验科,安徽 芜湖 241001)
·临床医学·
细菌对电化学发光免疫分析法检测乙型肝炎指标结果的影响
李 婕,方 芳,李小宁
(皖南医学院第一附属医院 弋矶山医院 检验科,安徽 芜湖 241001)
目的:探讨细菌对电化学发光免疫分析法检测乙型肝炎指标结果的影响。方法收集我院临床确诊为乙型肝炎患者45例的血液标本,按照加入菌种和浓度的不同,分为1个对照组和9个实验组,通过电化学发光免疫分析法检测HBsAg、HBeAg、HBcAb三项指标。结果加入不同浓度梯度、不同菌种的血清标本检测结果与对照组相比,差异均无统计学意义(P>0.05)。结论细菌对电化学发光免疫分析法检测乙型肝炎指标结果无影响,提示电化学免疫分析法可能不受细菌因素的干扰。
乙型肝炎;细菌;电化学发光免疫分析
随着临床检验技术的不断发展,近年来出现的电化学发光免疫分析技术[1](electrochemiluminescence immunoassay,ECLIA)是继酶免疫测定法(enzyme immunoassay,EIA)、放射免疫测定法(radioimmunoassay,RIA)、荧光免疫测定法(fluorescence immunoassay,FIA)、时间分辨荧光免疫测定法(time-resolved fluorescence immunoassay,TRFIA)之后的新一代标记免疫测定技术,被广泛运用于临床检验诊断领域,是目前较先进的标记免疫测定技术之一。该方法是将标本中待测抗原、生物素化特异性单克隆抗体和钌复合物标记的特异性抗体形成夹心复合物,然后结合到链霉亲和素包被的微粒上,微粒被吸附到电极上,电极加压后产生化学发光,通过光电倍增原理进行测量[2]。ECLIA法具有反应可控、灵敏度高、易于与分离技术联用等特点,且经大量临床试验论证,该方法不受黄疸、溶血、乳糜血和生物素的干扰。但是细菌是否对ECLIA法的检测结果产生干扰,目前国内外尚无相关的研究文献。在临床采集血液过程中,不乏有炎症感染甚至是菌血症患者,或出现血液样本接触到空气中或定植在人体表面细菌的情况,因此研究细菌对ECLIA法检测结果的影响就显得尤为重要。本文拟采用ECLIA法分别定量检测乙型肝炎大三阳患者的HBsAg、HBeAg、HBcAb三项指标,分析不同浓度的细菌和不同细菌之间的检测结果是否存在差异[3-5],旨在探讨细菌是否对ECLIA检测结果产生干扰,为临床选择合理的检验方法提供理论依据。
1 资料与方法
1.1 标本来源 收集弋矶山医院2016年10~12月经临床确诊为乙型肝炎(HBsAg、HBeAg、HBcAb三项指标都为阳性)门诊或住院患者的血液,离心分离血清,-20 ℃密闭保存[4]。共纳入近1个月内无炎症、感染、菌血症病史的成年男性患者23例和女性患者22例。
1.2 仪器与试剂 仪器:电热恒温水槽DK-600型(上海三发科学仪器有限公司),二氧化碳培养箱(上海力申科学仪器有限公司),Roche cobas 8000系列电化学自动分析仪cobas e 602(德国罗氏)。试剂:乙型肝炎病毒表面抗原、e抗原、核心抗体检测试剂盒均来自罗氏诊断产品(上海)有限公司。
1.3 方法 将冷冻标本放置37 ℃电热恒温水槽中解冻,室温下每例标本均设立1个对照组和9个实验组,对照组加入200 μL血清和200 μL生理盐水,实验组每组加入200 μL血清后,再分别依次加入等量0.5、2.0、3.0麦氏单位的表皮葡萄球菌菌液、大肠埃希菌菌液、鲍曼不动杆菌菌液,放入37℃二氧化碳培养箱内培养24 h后,混匀,然后用电化学发光免疫分析仪进行检测,标本信号/Cut-off。实验前校正仪器,机器运行状态良好,所有操作均严格按照仪器及试剂盒说明书进行,质控和样本准确性和精密性均符合要求。
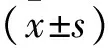
2 结果
2.1 不同浓度表皮葡萄球菌菌液组与对照组的检测结果比较 对3种不同浓度表皮葡萄球菌菌液组的HBsAg、HBeAg、HBcAb三项指标和对照组的检测结果进行比较,发现不同浓度的表皮葡萄球菌菌液组分别与对照组相比,以及不同浓度菌液组之间比较,差异均无统计学意义(P>0.05),见表1。
2.2 同一浓度下不同菌液组与对照组的检测结果比较 通过对相同浓度(2.0麦氏单位)的表皮葡萄球菌菌液组、大肠埃希菌菌液组、鲍曼不动杆菌菌液组和对照组的HBsAg、HBeAg、HBcAb结果分析,发现3种不同菌液组分别与对照组相比,以及不同菌液组之间比较,差异均无统计学意义(P>0.05),见表2。
表1 不同浓度表皮葡萄球菌菌液组HBsAg、HBeAg、HBcAb与对照组比较
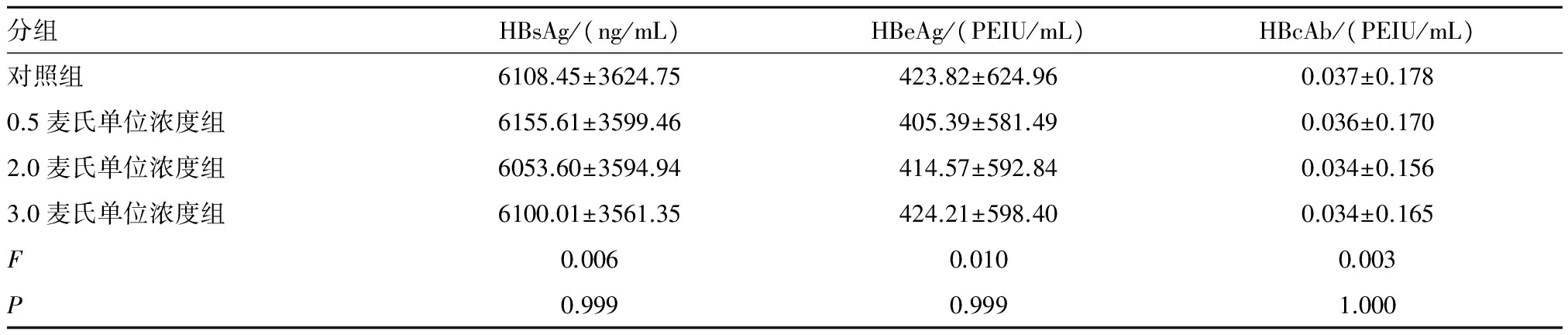
分组HBsAg/(ng/mL)HBeAg/(PEIU/mL)HBcAb/(PEIU/mL)对照组6108.45±3624.75423.82±624.960.037±0.1780.5麦氏单位浓度组6155.61±3599.46405.39±581.490.036±0.1702.0麦氏单位浓度组6053.60±3594.94414.57±592.840.034±0.1563.0麦氏单位浓度组6100.01±3561.35424.21±598.400.034±0.165F0.0060.0100.003P0.9990.9991.000
表2 2.0麦氏单位的不同菌液组检测HBsAg、HBeAg、HBcAb与对照组的比较
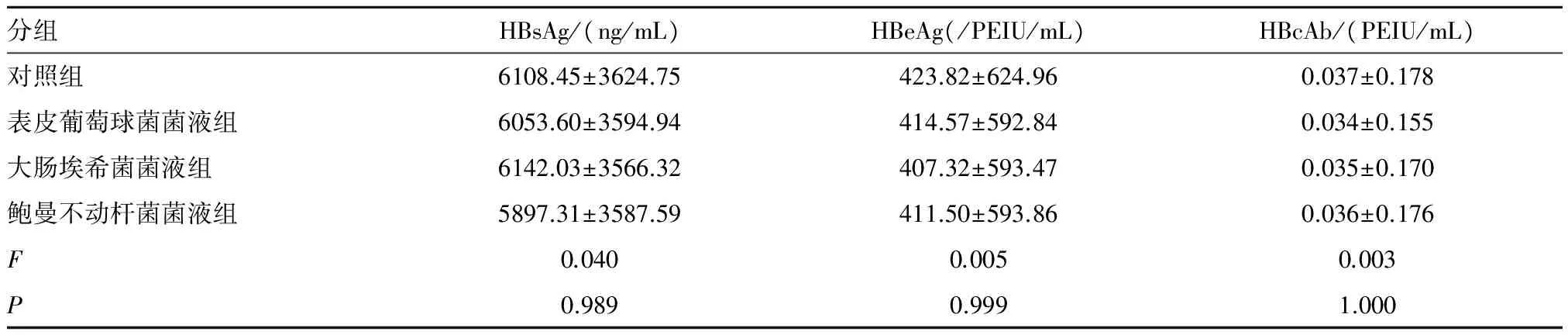
分组HBsAg/(ng/mL)HBeAg(/PEIU/mL)HBcAb/(PEIU/mL)对照组6108.45±3624.75423.82±624.960.037±0.178表皮葡萄球菌菌液组6053.60±3594.94414.57±592.840.034±0.155大肠埃希菌菌液组6142.03±3566.32407.32±593.470.035±0.170鲍曼不动杆菌菌液组5897.31±3587.59411.50±593.860.036±0.176F0.0400.0050.003P0.9890.9991.000
3 讨论
ECLIA发展于1996年,它在发光反应中加入了电化学反应,是继放射免疫、酶免疫、化学发光免疫测定之后的新一代标记免疫测定技术,是电化学和免疫测定相结合的产物,也是现阶段医疗界公认的较先进的临床免疫检测技术之一。目前应用范围延伸至DNA单分子检测、药物分析、免疫分析、生物活性物质分析及活体分析等领域。电化学发光免疫分析仪临床应用于甲状腺激素检测,贫血病因的判断(铁蛋白测定),肿瘤标志物以及性激素检测,输血前常规检测和TORCH实验。
ECLIA基本原理为电化学发光过程中产生的光信号强度与二价的三氯联吡啶钌[Rubpy 3]2+的浓度呈线性关系。将二价的[Rubpy 3]2+与免疫反应体系中的一种物质结合,经免疫反应、分离后,检测免疫反应体系中剩余二价的三氯联吡啶钌[Rubpy 3]2+经上述过程后的激发光,即可得知待检物的浓度。ECLIA法检测灵敏度高、特异性强,线性范围宽;而传统的酶免疫测定法(ELA)、酶联免疫吸附试验(ELISA)法为既往临床常用检查乙肝病毒血清标志物的方法,易受溶血、黄疸、乳糜血、类风湿因子、高浓度非特异性免疫球蛋白、药物、血液抗凝剂及细菌等多种因素的影响,导致ELISA法检测结果判断错误[6-8]。纪晓花[9]认为标本被细菌污染后,菌体中可能含有内源性过氧化物酶,因此,被污染的标本同溶血标本一样,亦可产生非特异性显色而干扰测定结果。如大肠埃希菌的β-半乳糖苷酶本身会对用相应酶作标记的测定方法产生非特异性干扰。其次谭立明[10]认为乳糜血会使吸光度A值增高出现假阳性,而细菌细胞膜含有脂质成分,裂解入血造成检测结果假阳性。化学发光酶免疫测定(CLEIA)因为需要采用催化发光反应的酶标记抗原或抗体,如辣根过氧化物酶(HRP)、碱性磷酸酶(ALP),所以细菌也会对此检测方法产生一定的干扰[11]。放射免疫分析技术(RIA)反应时间较慢,敏感度较低,放射性废物的储存和销毁,均会对环境造成一定放射性污染;时间分辨荧光免疫测定方法(TRFIA)易受环境、试剂和容器中的镧系元素离子的污染,致使检测的本底增高。
正因上述传统的检测方法或多或少都存在各自的缺点,因此寻求新的质量可信、安全可靠的检测方法就显得尤为重要。由于ECLIA设计的是生物素包被,已经证实具有容易测定和控制、结合稳定、不影响标记物的理化性质、试剂灵敏度高、稳定性好等特点。检测仪器说明书上明确指出ECLIA不受标本溶血、胆红素(一定浓度范围内)、乳糜血、抗凝剂因素影响,但是并没有指出会不会受到菌血症的影响。本实验初步探究此因素对电化学发光方法检测肝炎指标结果的影响,选择表皮葡萄球菌是因为该细菌定植于皮肤表面,在采血过程中会污染标本,大肠埃希菌会产生内源性过氧化物酶,鲍曼不动杆菌则是在医院感染患者,尤其重症ICU患者感染中最常见,所以这三种细菌的选择均有代表性意义。本文研究结果也显示不同浓度的不同细菌对电化学发光方法检测乙型肝炎患者的HBsAg、HBeAg、HBcAb指标结果都没有影响,从而为推断电化学自动免疫分析方法检测血清中乙型肝炎病毒是不受细菌干扰的结论提供理论依据。然而,细菌是否对电化学发光免疫分析法检则其他项目如激素、甲状腺功能,HIV相应指标产生影响,有待于下一步试验的继续探索。
总之,检验医师在选择检验方法时,不仅要考虑检验成本和生物安全,还要评估分析所有干扰因素,从而保证检验结果的准确性和重复性,确保检测结果的真实可靠,从而为临床的准确诊断、病情分析、疗效判断及预后评估等方面提供科学依据。
【参考文献】
[1] 牛春波,陈帅,龚纯贵.全自动电化学发光免疫分析仪的日常使用维护[J].中国医疗器械信息,2016,22(17):73-75.
[2] 归国风,宋鹏.电致化学发光适体传感器的研究进展[J].化学传感器,2015,35(4):17-24.
[3] XU W,LI Y,WANG M,etal.Comparison of two immunoassays for determining hepatitis B virus serum markers[J].Clin Chem Lab Med,2011,50(1):153-157.
[4] 邓雪莲,陈辉,王新梅,等.电化学发光法进行HBsAg阳性确认的可行性及应用研究[J].中国输血杂志,2016,29(8):806-811.
[5] 聂尚燕,宋欢欢,王敏,等.HBsAg与慢性乙型肝炎患者血清HBV DNA水平的相关性研究[J].现代中西医结合杂志,2016,2(9):978-979.
[6] 刘玮,郭苗,赵文娜.ECLIA定量检测乙肝血清标志物的临床应用分析[J].基层医学论坛,2016,20(7):950-951.
[7] FEI CR,YE AQ,ZHANG J.Evaluation of different methods in determination of low level HBsAg[J].Journal of Zhejiang University Medical Sciences,2011,40(4):436-439.
[8] 何应中,郑国波,邹焰,等.ECLIA和ELISA检测乙肝病毒血清标志物对比探讨[J].遵义医学院学报,2010,33(5):439-442.
[9] 纪晓花.标本因素对ELISA测定结果的影响[J].中国医学创新,2011,8(7):133-134.
[10] 谭立明.ELISA法检测的影响因素及其对策[J].实验与检验医学,2013,31(4):300-305.
[11] 张利,于冬男.化学发光酶免疫分析法及ELISA检测抗-HCV的结果比较[J].检验医学与临床,2016,13(1):18-20.
EffectofbacteriaontheresultsofelectrochemiluminescenceimmunoassayindetermininghepatitisBvirusserummarkers
LIJie,FANGFang,LIXiaoning
Department of Clinical Laboratory,The First Affiliated Hospital of Wannan Medical College,Wuhu 241001, China
Objective:To observe the interference of bacteria with the results of electrochemiluminescence immunoassay in determining the serum markers of hepatitis B virus.Methods:Serum samples were collected in 45 patients confirmed as hepatitis B. Then the samples were divided into one control group and 9 experimental groups by applying diverse concentration of different bacterium. Electrochemiluminescence immunoassay was performed to detect HBsAg, HBeAg and HbcAb.Results:The serum markers were not significantly varied between the control group and experimental group after using diverse concentration and species of bacterium (P>0.05).Conclusion:The findings indicate that bacteria will produce no interference with the results of electrochemiluminescence immunoassay in determining the serum markers of hepatitis B virus.
hepatitis B;bacterium;electrochemiluminescence immunoassay
1002-0217(2017)06-0567-03
2017-05-02
李 婕(1992-),女,2016级硕士研究生,(电话)18355350249,(电子信箱)1982684407@qq.com;
李小宁,男,主任技师,副教授,硕士生导师,(电子信箱)lixiaoning19702006@126.com,通信作者。
R 512.62;R 392.11
A
10.3969/j.issn.1002-0217.2017.06.017

