Flotillin-1在黑腹果蝇不同发育阶段的表达
张叶军, 王旭研, 王 赢, 李洪艳, 崔玉影, 邹 伟
(辽宁师范大学 生命科学学院,辽宁 大连 116081)
Flotillin-1在黑腹果蝇不同发育阶段的表达
张叶军*, 王旭研*, 王 赢, 李洪艳, 崔玉影, 邹 伟
(辽宁师范大学 生命科学学院,辽宁 大连 116081)
脂筏(Lipid raft)是质膜上富含胆固醇和鞘磷脂以及特定蛋白的微结构域,浮舰蛋白-1(Flotillin-1)是脂筏标记蛋白,与轴突再生、学习记忆和肿瘤形成等过程相关.近年发现,从无脊椎动物到脊椎动物的很多种类都有Flotillin-1的表达,且在进化上高度保守.果蝇属于完全变态昆虫,是一种重要的模式生物,含有人类疾病相关基因中65%同源基因.因此,研究这些基因在果蝇不同发育阶段的表达分布特征,对深入阐明人体病理机制具有重要意义.以黑腹果蝇(Drosophilamelanogaster)为研究对象,通过Western blot和免疫荧光方法检测Flotillin-1在果蝇不同发育阶段的表达.结果如下:Flotillin-1在果蝇不同发育阶段的表达水平和分布不同:幼虫期仅脂肪体中少量表达;蛹期消化道和脂肪体中有少量表达;成虫期主要在脑、复眼、消化道、生殖腺中表达,肌肉中也有少量表达;该蛋白在成虫中的表达量显著高于幼虫和蛹.
黑腹果蝇;Flotillin-1;表达分布
黑腹果蝇(Drosophilamelanogaster)作为模式动物被普遍应用于遗传现象、行为和发育分子机制的研究.科学家在2000年已完成对果蝇13 600个基因的测序.研究发现,果蝇与人类在基因组中有接近80%的同源基因,而且在果蝇的遗传物质里找到了大约65%的人类致癌基因[1].果蝇为完成人类基因和疾病变异功能注释提供了一个强大平台,为遗传和基因组工程高效快速发展提供了最先进的工具和资源.通过研究果蝇中某些基因如何影响特定的细胞过程,为深入探讨神经、心血管、新陈代谢和肾系统等分子机制提供理论基础和实验依据[2].
脂筏(Lipid raft)是质膜上富含胆固醇和鞘磷脂以及特定蛋白的微结构域,浮舰蛋白-1(Flotillin-1)是脂筏标记蛋白,是高度保守的质膜内在蛋白和雌激素应答基因,存在于大多数动物中,尤其在哺乳动物中广泛表达,而且在神经系统、肌肉、脂肪组织以及红细胞中特别丰富,其同源蛋白也存在于原核生物和植物中[3].Flotillin-1在神经发育早期发挥重要作用[4-6],神经元发育对学习和记忆是非常重要的.哺乳动物中Flotillin-1与记忆相关过程有关,然而其在记忆形成和人类相关疾病中的作用还有待进一步研究.从细菌到人类中的Flotillin-1都是保守蛋白,Flotillin-1可能作为质膜微区脚手架蛋白参与多种生命过程,如信号转导、胞吞胞吐、蛋白质运输、细胞转运和细胞分裂等,但其在上述过程中的分子机制和具体功能目前仍不十分清楚[7].
另外,Flotillin-1在质膜受体信号转导等多种细胞过程中发挥重要作用,也参与人类肿瘤的发生发展阶段.最近研究发现,Flotillin-1在人类乳腺癌、大肠癌、食管鳞状细胞癌等上皮来源的癌症中表达水平显著上调,敲低Flotillin-1可显著抑制癌细胞增殖和致瘤性,但其确切分子机制仍不清楚[8].
本文以黑腹果蝇为研究对象,利用Western blot和免疫荧光共聚焦方法检测Flotillin-1在果蝇幼虫、蛹和成虫时期的表达变化,旨在阐明Flotillin-1蛋白在黑腹果蝇不同发育阶段的表达分布模式,探讨Flotillin-1在果蝇发育过程中的作用,为进一步研究其作用的分子机制提供实验依据.
1 材料与方法
1.1 材料
野生型黑腹果蝇品系,由辽宁师范大学遗传学实验室提供.果蝇培养基(杭州基础生物科技有限公司);Flotillin-1单克隆二抗抗兔抗体(武汉三鹰生物技术有限公司);FITC标记山羊抗兔IgG、辣根酶标记山羊抗兔IgG(ZB2301)、GAPDH单克隆二抗抗鼠抗体(北京中杉金桥生物技术有限公司);DAPI染色液、荧光防淬灭剂、BCA蛋白浓度测定试剂盒(上海碧云天生物技术有限公司);ECLTM化学发光试剂盒(美国Thermo Scientific公司);ExpressPlusTM预制胶(南京金斯瑞生物科技有限公司);其他所用试剂均为国产分析纯.
1.2 果蝇培养
将果蝇于室温下培养在玉米培养基中,培养基配方为:酵母粉9.2 g/L,琼脂8.2 g/L,蔗糖81.5 g/L,玉米粉108.5 g/L,苯甲酸钠1.3 g/L.
1.3 果蝇石蜡切片的制备
配制试剂.分别取果蝇幼虫、蛹和成虫投入Bouin液中固定数小时.将固定的材料直接移入70%酒精中冲洗,直至材料无黄色为止.脱水,透明,浸蜡,包埋,切片,切片厚度为4 μm,贴片和烤片.将载玻片编号,室温保存.
1.4 免疫荧光和共聚焦技术
在二甲苯和无水乙醇浓度梯度溶液中脱蜡、脱水,流水冲洗 5 min,3次,磷酸缓冲液PBS充分淋洗5 min,3次.1% BSA,37 ℃避光封闭30 min,4 ℃孵育Flotillin-1一抗48 h.PBS充分淋洗5 min,3次,室温避光孵育二抗IgG-TRITC 1.5 h.PBS充分淋洗5 min,3次,室温避光孵育Hoechst 33342 5 min.PBS充分淋洗5 min,3次,双蒸水冲洗5 min,加防淬灭剂封片.激光扫描共聚焦显微镜镜检切片.
1.5 蛋白质免疫印迹
分别提取果蝇幼虫、蛹和成虫中总蛋白.10%(质量分数)SDS聚丙烯酰胺凝胶电泳,转膜,5%(质量分数)脱脂奶粉室温封闭1 h.根据不同抗体的最佳作用效价,用PBST稀释一抗,将封闭好的PVDF膜置于稀释后的一抗中,4 ℃孵育过夜.室温PBST洗膜3次,每次10 min,与对应辣根过氧化物酶标记的二抗(1∶8 000)室温孵育90 min;PBST洗膜3次.ECL显色,进行X光胶片感光,冲洗胶片.扫描仪和凝胶成像系统记录相应条带的透色光积分吸光度值.Gapdh条带作为内参.
1.6 统计学分析
所有实验均为3次以上(n≥3)独立重复实验.实验结果应用统计学处理,数据分析采用组间t检验和方差分析,数据均以mean±SD表示,*P<0.05表示对比2组之间差异显著性,**P<0.01表示极显著性差异.
2 结 果
2.1 Flotillin-1蛋白在果蝇不同发育阶段的表达分布
分别选取果蝇幼虫石蜡切片的第4、10张,蛹切片的第2、6、11张以及成虫切片的第3、13、24张进行免疫荧光实验,在共聚焦显微镜下观察Flotillin-1蛋白的表达分布情况.结果如图1所示,Flotillin-1蛋白在果蝇的不同生长发育时期表达分布不同:幼虫期仅脂肪体中少量表达(图1A);蛹期肠壁和脂肪体中有少量表达(图1B);成虫期主要在脑、复眼、肠壁、生殖腺中表达,肌肉中也有少量表达(图1C).
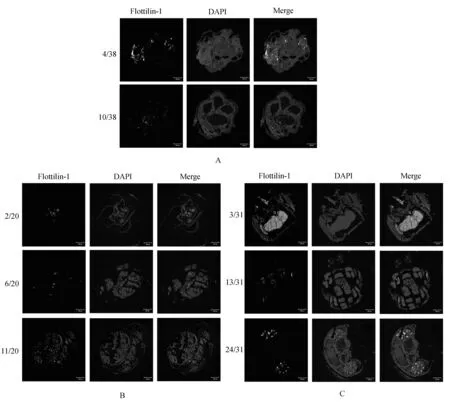
图1 Flotillin-1蛋白在果蝇不同发育阶段的表达分布 Fig.1 The distribution of Flotillin-1 in different developmental stages of the D. melanogasterLarva (A), pupa (B) and adult (C) were fixed and immuno-stained with antibodies against Flotillin-1 (green) and nuclei were counter-stained with DAPI (blue), respectively. Original magnification, 100×
2.2 Flotillin-1蛋白在果蝇不同发育阶段的表达水平
运用蛋白免疫印迹方法,结果如图2所示,Flotillin-1蛋白在黑腹果蝇不同发育时期的表达量不同,主要在果蝇成虫中表达,幼虫和蛹中少量表达,而且Flotillin-1蛋白在成虫中的表达量比幼虫和蛹中显著增加.
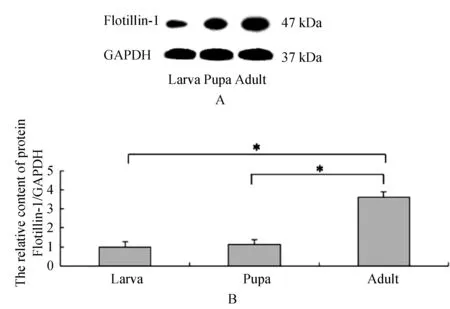
图2 Flotillin-1蛋白在果蝇不同发育阶段的表达水平Fig. 2 The expression level of Flotillin-1 protein at different developmental stages in D. melanogaster A.The band intensities for Flotillin-1 protein were normalized against that of the GAPDH protein. B. Values were expressed as arbitrary units of relative value. Significant differences of different developmental stages (n=3, *P<0.05, **P<0.01) were analyzed by one-way analysis of variance (ANOVA)
3 讨 论
Flotillin-1蛋白是一种重要的脂筏标记蛋白,而脂筏是质膜上的一个动态微结构域,并且Flotillin-1在进化上高度保守.目前,已发现从无脊椎动物到脊椎动物的多个种类普遍有Flotillin-1的表达,而且在进化上高度保守,不同物种之间Flotillin-1的相似度超过60%[9-11].利用DNA Star软件对果蝇Flotillin-1的氨基酸序列与其他物种该蛋白的氨基酸序列进行同源比对,发现果蝇Flotillin-1蛋白的氨基酸序列与其他物种的同源性非常高;同时利用Mega 4.0软件构建系统进化树,发现此蛋白在物种进化过程中具有协同性,因此,进一步验证Flotillin-1蛋白具有高度保守性(结果尚未发表).
质膜脂筏区域优先募集膜蛋白和脂质促进其相互作用,从而调节跨膜信号转导和细胞内稳态[12].Flotillin-1作为质膜微区脚手架蛋白,在多种信号转导通路和生理过程中发挥重要作用.Flotillin-1广泛表达在所有脊椎动物中,尤其在神经系统、肌肉、脂肪组织和红细胞中特别丰富[13-14].最近研究发现在同种生物的不同部位,Flotillin-1的表达量相差很多,其在脑中高表达并显著高于其他组织,在心脏、肺、脊髓、胎盘和睾丸等组织有表达,在胰腺和肝脏中低表达[9].然而,Flotillin-1在昆虫个体发育的细胞和亚细胞分布模式的变化尚不清楚.
为研究Flotillin-1在果蝇发育体系中的组织结构定位,利用免疫荧光共聚焦方法检测Flotillin-1蛋白在其不同发育阶段的表达分布变化.结果发现,Flotillin-1蛋白在果蝇的不同生长发育时期表达分布不同:幼虫期仅脂肪体中少量表达;蛹期肠壁和脂肪体中有少量表达;成虫期主要在脑、复眼、肠壁、生殖腺中表达,肌肉中也有少量表达.果蝇Flotillin-1的表达主要受限于神经系统的发育,这与哺乳动物中Flotillin-1的mRNA和蛋白在神经系统、脂肪组织和肌肉中广泛表达,尤其在脑组织中大量表达的结果一致[15].von Philipsborn等研究发现,在模式生物斑马鱼(Zebra fish)胚胎中枢神经系统中,Flotillin-1强烈表达,尤其在轴突处,这个位置是视神经交叉等轴突束发生的地方,与Flotillin-1在果蝇成虫复眼中高度表达相一致[16].由于昆虫的脂肪体类似于哺乳动物的脂肪和肝脏,因此在果蝇幼虫、蛹和成虫脂肪体中均观察到Flotillin-1表达.
Flotillin-1是进化上高度保守的记忆相关蛋白质[17].最近报道,Flotillin-1在神经系统中发挥不同功能,其对轴突再生、海马神经元分化和神经递质转运蛋白内化非常重要[4].海洋无脊椎动物海兔的鳃和管形口器退缩反射是研究学习和记忆突触可塑性的理想应用模型系统之一.Monje等通过鳃和管形口器退缩反射行为敏感化训练海兔后发现,Flotillin-1在其腹部神经节处的表达水平上调;利用水迷宫训练小鼠后,发现Flotillin-1在其海马组织中的表达水平显著提高,表明Flotillin-1与哺乳动物系统中记忆相关过程有关[17].推测Flotillin-1在果蝇中可能也发挥相似的功能.
进一步实验应使用基因敲除动物模型来确定Flotillin-1在果蝇神经、消化、生殖系统等中的确切功能,并研究其作用的分子机制,这些结果将为研究Flotillin-1在人类学习记忆形成和相关疾病中的作用提供依据.
[1] YAMAMOTO S,JAISWAL M,CHARNG W L,et al.A drosophila genetic resource of mutants to study mechanisms underlying human genetic diseases[J].Cell,2014,159(1):200-214.
[2] UGUR B,CHEN K,BELLEN H J.Drosophilatools and assays for the study of human diseases[J].Disease Models & Mechanisms,2016,9(3):235-244.
[3] WINSHIP A L,RAINCZUK K,DIMITRIADIS E.Flotillin-1 protein is upregulated in human endometrial cancer and localization shifts from epithelial to stromal with increasing tumor grade[J].Cancer Investigation,2016,34(1):26-31.
[4] CARCEA I,MA′AYAN A,MESIAS R,et al.Flotillin-mediated endocytic events dictate cell typespecific responses to semaphorin 3A[J].Journal of Neuroscience,2010,30(45):15317-15329.
[5] SWANWICK C C,SHAPIRO M E,VICINI S,et al.Flotillin-1 mediates neurite branching induced by synaptic adhesion-like molecule 4 in hippocampal neurons[J].Molecular and Cellular Neuroscience,2010,45(3):213-225.
[6] SWANWICK C C,SHAPIRO M E,VICINI S,et al.Flotillin-1 promotes formation of glutamatergic synapses in hippocampal neurons[J].Developmental Neurobiology,2010,70(13):875-883.
[7] BANNING A,TOMASOVIC A,TIKKANEN R.Functional aspects of membrane association of reggie/flotillin proteins[J].Current Protein & Peptide Science,2011,12(8):725-735.
[8] BANNING A,KURRLE N,MEISTER M,et al.Flotillins in receptor tyrosine kinase signaling and cancer[J].Cells,2014,3(1):129-149. doi:10.3390/cells3010129.
[9] VOLONTE D,GALBIATI F,LI S,et al.Flotillins/cavatellins are differentially expressed in cells and tissues and form a hetero-oligomeric complex with caveolinsinvivo. Characterization and epitope-mapping of a novel flotillin-1 monoclonal antibody probe[J].Journal of Biological Chemistry,1999,274(18):12702-12709.
[10] BICKEL P E,SCHERER P E,SCHNITZER J E,et al.Flotillin and epidermal surface antigen define a new family of caveolae-associated integral membrane proteins[J].Journal of Biological Chemistry,1997,272(21):13793-13802.
[11] GALBIATI F,VOLONTE D,GOLTZ J S,et al.Identification, sequene and developmental expression of invertebrate flotillins fromDrosophilamelanogvaster[J].Gene,1998,210(2):229-237.
[12] LORENT J H,LEVENTAL I.Structural determinants of protein partitioning into ordered membrane domains and lipid rafts[J].Chemistry and Physics of Lipids,2015,192(1):23-32.
[13] SALZER U,AHORN H,PROHASKA R.Identification of the phosphorylation site on human erythrocyte band 7 integral membrane protein:implications for amonotopic protein structure[J].Biochimica et Biophysica Acta,1993,1151(2):149-152.
[14] ROSELLI S,GRIBOUVAL O,BOUTE N,et al.Podocin localizes in the kidney to the slit diaphragmarea[J].American Journal of Pathology,2002,160(1):131-139.
[15] FERNOW I,ICKING A,TIKKANEN R.Reggie-1 and reggie-2 localize in non-caveolar rafts in epithelial cells:cellular localization is not dependent on the expression of caveolin proteins[J].European Journal of Cell Biology,2007,86(6):345-352.
[16] VON PHILIPSBORN A C,FERRER-VAQUER A,RIVERA-MILLA E,et al.Restricted expression of reggie genes and proteins during early zebrafish development[J].Journal of Comparative Neurology,2005,482(3):257-272.
[17] MONJE F J,DIVISCH I,DEMIT M,et al.Flotillin-1 is an evolutionary-conserved memory-related protein up-regulated in implicit and explicit learning paradigms[J].Annals of Medicine,2013,45(4):301-307.
TheexpressionofFlotillin-1indifferentdevelopmentalstagesofDrosophilamelanogaster
ZHANGYejun,WANGXuyan,WANGYing,LIHongyan,CUIYuying,ZOUWei
(School of Life Science, Liaoning Normal University, Dalian 116081, China)
Lipid rafts microdomains of the plasma membrane that are rich in cholesterol, sphingomyelin as well as specific proteins on the plasma membrane. Flotillin-1 is a marker protein of lipid rafts, it is related to axonal growth, learning-memory and tumor formation. It has been found that Flotillin-1 expresses in various types of invertebrates and vertebrates and it is highly conserved in evolution.D.melanogasteris a complete metamorphosis insect, as a kind of important model organism, it contains at least 65% homologous genes of the human disease related genes. Therefore, studying the expression and distribution of these genes in different developmental stages ofDrosophilais of great significance to further clarify the mechanism of human pathology. In this paper, the expression levels and distributions of Flotillin-1 in different developmental stages ofD.melanogasterwere detected utilizing Western blot and immunofluorescence. The results were as follows:The expression levels and distributions of Flotillin-1 varied in different developmental stages ofD.melanogaster:the vivo distribution of Flotillin-1 was very little only in the fat bodies in larval stage, a little in the alimentary canal and fat bodies in pupa stage, mainly in the brain, ommateum, alimentary canal, genital gland and a little in the muscles in adult stage. While, the expression levels of Flotillin-1 in adults were significantly higher than those of the larvae and pupae.
Drosophilamelanogaster;Flotillin-1;expression and distribution
Q71
A
2017-06-09
辽宁省自然科学基金资助项目(2015020568);辽宁教育厅科学研究一般项目(L201783647)
张叶军(1979- ),女,河北怀安人,辽宁师范大学讲师,博士;
王旭研(1993- ),女(满族),内蒙古扎兰屯人,辽宁师范大学硕士研究生.
*共同第一作者
1000-1735(2017)04-0513-06
10.11679/lsxblk2017040513

