临床免疫检验质量控制对检验结果可靠性和准确性的影响
韩洁琼
·论著·
临床免疫检验质量控制对检验结果可靠性和准确性的影响
韩洁琼
目的:探析临床免疫检验质量控制的相关性措施对检验结果的可靠性和准确性的影响。方法选择在某院接受治疗的152例患者为观察对象,按照随机分配的原则将患者分为2组,分别为对照组和研究组,每组各76例。对照组患者选择常规方法完成血液样本检测,研究组患者在对照检测方法基础上采取相关性措施,加强临床免疫检验质量控制。本资料将乙肝五项检验结果作为观察指标,分析其检测结果的准确度,同时记录2组患者各项指标平均变异指数,此外对2组患者检出率进行对比。结果比较2组患者乙肝检测结果准确性可知,研究组检测准确性明显高于对照组(P<0.05)。对比2组患者各项指标平均变异指数数据可知,研究组患者检验结果变异指数明显低于对照组(P<0.05),乙型肝炎、乙型肝炎肝硬化以及原发性胆汁性肝硬化检出率方面,2组比较差异有统计学意义(P<0.05)。结论临床免疫检验质量控制举措对检测结果具有积极作用,一方面有效提高检测准确度,另一方面对提升患者治疗有效率具有积极影响。
临床免疫检验; 质量控制; 相关性措施; 检验结果; 可靠性; 准确性
质量控制是临床免疫检测重要环节之一,通常包括室内和室间两大板块。室内质量控制主要指检验人员对临床免疫检验数据实施高效、准确的分析和评价;室间质量控制主要指以临床免疫检验数据标准值为基准对实际检验结果相关指标值的误差进行合理校对[1]。由此可见临床免疫检验数据的准确、可靠性对检验结果和治疗方案制定、实施的重要程度,是确保理想治疗效果的重要前提条件[2]。本次资料采用对比研究的方式观察临床免疫检验质量控制的相关性措施对检验结果的可靠性和准确性的影响,取得理想效果,现报告如下。
1 资料与方法
1.1 一般资料 选择2016年1月-2017年1月在本院接受治疗的152例患者作为观察对象,所有患者经临床检查均符合以下标准。纳入标准:75岁以下在我院接受治疗的患者,其自身机能允许其完成临床免疫检验;患者均符合西安会议在2000年修订的《病毒性肝炎防治方案》中关于肝硬化代偿期的诊断标准[3];所有患者的HBV和DNA的检测呈阳性。排除标准:患者存在重度脏器类疾病,或者伴随出现其他重度疾病;处于妊娠期或者哺乳期的女性患者。按照随机分配的原则将患者平均分为2组分别为对照组和研究组,研究组76例,其中男39例,女37例,年龄26~73岁,平均年龄(44.3±5.6)岁,乙型肝炎患者24例,乙型肝炎肝硬化患者22例,原发性胆汁性肝硬化患者30例;对照组76例,其中男35例,女41例,年龄31~72岁,平均年龄(44.1±4.9)岁,乙型肝炎患者24例,乙型肝炎肝硬化患者23例,原发性胆汁性肝硬化患者29例。2组患者一般资料比较,差异无统计学意义,具有可比性(P>0.05)。患者均知情同意本研究,并经过医院伦理委员会批准。
1.2 方法 对照组患者选择常规方法完成血液样本检测,研究组患者在对照检测方法基础上采取相关性措施加强临床免疫检验质量控制,质量控制在血样检测的各个阶段均有体现,具体体现在以下几个方面[4]。(1)血样免疫检测前控制。检测前样本需要经过采集、储藏、传递和接受四个环节的流通,整个过程对血样检测效果具有较大影响,因此针对该四个环节采取治疗控制显得尤为必要[3]。首先针对样本采集实施相关举措可以通过对采集工作展开的时间控制、选择合适的血液抗凝剂,采集过程体位选择、止血带使用时间等方面均对血液样本的采集效果及质量具有一定影响[5]。因此在血样采集前要对操作人员进行注意事项知情通知,血液采集完成后要科学储藏和保管,对血样对应患者的基本信息进行正确记录。实验室接受到血样后需要对样本进行全面检查,对不符合标准的样本原因进行说明,同时记录送检人员信息和检查项目,以便于相关人员自查[6]。日常采购和维修时尽量采用同一供应商,必须更换配件和设备时应首先与之前使用的相关设备进行比对试验,在保证设备运转稳定性。同时还要注意操作人员的技能培训,采用理论和实践相结合的方式对操作人员进行实训和考核[7]。(2)血样免疫检测过程控制。操作人员在选择合适检验试剂时应注意试剂是否在使用期限内,同时应严格按照相关操作准则和流程,最大程度提升检测结果的准确性和可靠性。(3)血样免疫检测后控制。检验人员完成所有血样检测步骤后,对检测结果数据进行二次审核,一旦发现可疑数据,第一时间联系相关科室负责人,对检测工作进行核查和记录,同时对记录的数据信息进行分类处理[8]。
1.3 观察指标 对比2组患者的乙肝指标检测结果,包括乙肝表面抗体(HBsAb)、乙肝核心抗原(HBcAg)、乙肝表面抗原(HBsAg)、乙肝核心抗体(HBcAb)。同时应用电化学发光法(ECLIA)对比2组患者的指标平均变异指数[9]。对比2组患者乙型肝炎、乙型肝炎肝硬化以及原发性胆汁性肝硬化的检出情况[10]。
应用SPSS 13.0统计软件进行,计量资料以均值±标准差表示,采用t检验,计数资料用百分比(%)表示,采用卡方(χ2)检验,等级资料用秩和检验;生存分析用 Kaplan-Meier 法。取P<0.05时差异具有统计学意义。
2.1 2组患者乙肝检测结果准确度比较 比较2组患者乙肝检测结果准确性可知,研究组检测准确性明显高于对照组,2组比较差异有统计学意义(P<0.05),即临床免疫质量控制的相关举措对提高检测准确度具有积极作用。见表1。

2 结果
反观《红楼梦》大观园里那一群“小善微才”的“异样女子”们,她们的关系甚至可以用“亲密无间”来形容了。从本质上分析,大观园里的女人们没有根本的利益关系方面的冲突,最尖锐的矛盾是妻妾之间的争风吃醋,这也没有发展到你死我活的斗争程度,最多算是一种争强好胜掐尖要强。例如王夫人和赵姨娘的矛盾,王熙凤和尤二姐的矛盾,夏金桂和香莲的矛盾,等等。

表1 2组患者乙肝检测结果准确度比较
2.3 2组患者检出率比较 乙型肝炎、乙型肝炎肝硬化以及原发性胆汁性肝硬化检出率方面,研究组患者均高于对照组,2组比较差异有统计学意义(P<0.05)。见表3。

表2 2组患者各项指标平均变异指数比较
2.2 2组患者各项指标平均变异指数比较 对比2组患者各项指标平均变异指数数据可知,研究组患者检验结果变异指数明显低于对照组,差异有统计学意义(P<0.05)。见表2。
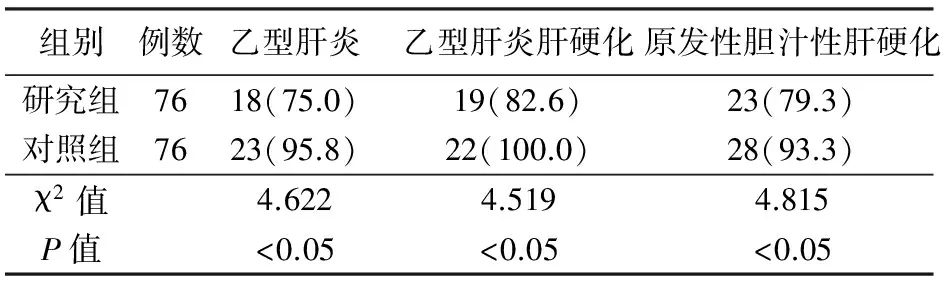
表3 2组患者检出率比较
注:()内数字为检出率/%。
3 讨论
随着我国医疗检测水平的不断提升,相关检测质量控制标准也在不断提升,临床免疫检验质量控制也不例外[11]。临床免疫检验的质量管控是免疫检验工作的核心环节,直接决定了整个免疫检验工作能否正常完成。免疫检验质量评估指标主要体现在可靠性和准确性两个方面,本次实验主要从化验室内部环境、检验者职业素养、检测试剂治疗、检验设备精密度、数据记录和分析效率等方面进行质量控制举措干预,2组患者各项指标平均变异指数比较证实,研究组患者七项检验结果变异指数明显低于对照组(P<0.05),由此可见该系列相关举措可有效提升检验结果安全性[12]。影响免疫检验结果的因素比较繁多,大致分为内源性因素和外源性因素两类,外源性因素通常为血样凝固不完全、血样出现感染、血样保管时间长、血样发生溶血现象等;内源性因素通常包括类风湿因子、高浓度非特异免疫球蛋白及某些影响检验的自身抗体等等[13]。为了确保检验免疫结果质量,应特别注意从血液样本采集、储藏、传递和检测四个方面进行相关举措干预,降低人为因素对检验结果可靠性和准确性带来的不利影响。例如采集工作时提醒接受血液采集的患者在采集前15 d内保证规律、健康的作息,采集前3 d禁止入食高脂肪类食品,采集前1d戒烟、戒酒,且采集当天保持空腹状态完成血样采集[14]。待血样完成采集和信息记录后第一时间送往实验室进行检测,以确保该阶段对血样性质的影响。同时实验室人员需对各项检测设备进行定期保养和维护,确保仪器精密度,最大程度降低检测误差[15]。此外相关操作人员需要不断更新、学习操作知识,以此提升自身职业素养,最大程度保证临床免疫检验的质量。本资料中2组患者乙肝检测结果准确性对比结果显示,研究组检测准确性明显高于对照组(P<0.05),同时乙型肝炎、乙型肝炎肝硬化以及原发性胆汁性肝硬化检出率方面,研究组患者均高于对照组,差异有统计学意义(P<0.05),由此可见临床免疫质量控制的相关举措对提高检测准确度具有积极作用。
3.2 缺乏系统的、专业的康复指导 加强社区康复护理人才的培养是推动社区康复护理的有力保证。然而我国从事老年人康复护理的专业人士很少,大都是社区护士进行简单的康复指导,我国社区护理从业护士主体年龄偏大,且多由普通护理学专业毕业的医院护士转岗而来,较少受过专业康复知识的训练,存在对康复知识认识不充分的问题[20],不能将康复对象当作整体来考虑,忽略将社区康复护理作为与预防、医疗、保健、健康教育和计划生育指导为一体的综合性服务[21]。
综上所述,临床免疫检验质量控制可以有效的提升临床免疫质量控制安全性和准确度,为治疗方案的制定和实施提供了前提条件,值得临床推广。
[1] 武国华,王志云.浅析基层医院临床免疫学检验结果影响因素及控制方法[J].山西医药杂志,2015,2(1):54-55.
[2] 蔡德建,田玫玲,吴殿水,等.临床免疫检验的质量影响因素及相应对策研究[J].检验医学与临床,2015,3(13):1939-1940.
[3] 周睿,秦妍妍,郭健,等.北京地区142家医疗机构互认实验室临床化学和临床免疫及临床检验专业室内质量控制现况调查[J].中华检验医学杂志,2016,39(12):922-929.
[4] CHATCHATEE P,FURANGSEROJ T,SURATANNON N,et al.The Effect of Pediatric Food Allergy on Caregiver Quality of Life:A Study in Asian Population[J].Journal of Allergy & Clinical Immunology,2015,135(2):AB257.
[5] HAMILTON RG,MATSSON PN,HOVANEC-BURNS DL,et al.Analytical Performance Characteristics,Quality Assurance and Clinical Utility of Immunological Assays for Human IgE Antibodies of Defined Allergen Specificities.(CLSI-ILA20-A3)[J].Journal of Allergy & Clinical Immunology,2015,135(2):AB8.
[6] 李艳珍.重视检验前质量控制确保检验结果准确可靠[J].山西医药杂志,2015,8(11):1328-1329.
[7] 巴哈尔古力麦麦提.临床检验质量控制指标的现状分析[J].中国妇幼健康研究,2016,27(1):288-289.
[8] CINGI C,GEVAERT P,MOSGES R,et al.Multi-morbidities of allergic rhinitis in adults:European Academy of Allergy and Clinical Immunology Task Force Report[J].Clinical & Translational Allergy,2017,7(1):17-18.
[9] 费阳,康凤凤,王薇,等.2015年全国临床检验质量指标室间质量评价[J].中华检验医学杂志,2016,39(6):433-437.
[10] TARSI S,LEHMAN HK.Evaluation of a Quality Improvement Tool to Initiate Referral of Hospitalized Asthmatics to Specialist Care[J].Journal of Allergy & Clinical Immunology,2015,135(2):AB51.
[11] 钟堃,王薇,何法霖,等.全国医院检验科临床检验项目基本情况现状调查与分析[J].中华检验医学杂志,2015,38(9):637-641.
[12] 张波,南铁贵,孙晴,等.免疫检测技术在中药质量快速评价中的应用[J].中国中药杂志,2017,42(3):420-427.
[13] 张维,梁先念,沈秀芬.以免疫检验中的临床案例浅析与临床沟通的重要性[J].世界中医药,2015,1(A02):1475-1476.
[14] 刘芳,王璐,阮晓慧,等.质量指标在临床生物化学、免疫分析前检测中的应用分析[J].检验医学与临床,2016,13(6):858-859.
[15] ARMISEN M,GUSPI R,ALFAYA T,et al.Cross-Sectional Validation of a Quality of Life Questionnaire in Spanish for Patients Allergic to Hymenoptera Venom[J].J investig Allergol clin immuno,2015,25(3):176-182.
Effectofimmunologicaltestqualitycontrolonreliabilityandaccuracyoftestresults
HANJie-qiong.
(TheSecondAffiliatedHospitalofHenanTraditionalChineseMedicineUniversity,Zhengzhou,Henan450008,China)
Objective:To explore the effect of clinical immunoassay quality control on the reliability and accuracy of the test results.Methods152 patients were enrolled in this study. The patients were randomly divided into two groups: a control group and a study group, each with 76 cases. Blood samples were tested and the patients in the study group were treated with relevant control measures to strengthen the quality control of clinical immunological tests.Quality control was reflected in all stages of the blood test. The contents of the treatment control were related to the internal environment of the laboratory.The indexes of 5 items of hepatitis B and the accuracy of the test results were recorded.The mutation indexes as well as the treatment results of the two groups were compared.ResultsThe comparison of hepatitis B test results of the two groups showed the detection accuracy of the study group was significantly higher than that of the control group (P<0.05). Moreover, the mutation indexes of test result of the study group were significantly lower than those of the control group (P<0.05).As for the detection rate of hepatitis B, cirrhosis and primary bile of liver cirrhosis, it was significantly higher in the study group than in the control group(P<0.05).ConclusionThe quality control measures of clinical immunoassay have a positive effect on the test results. On the one hand, the accuracy of detection is improved effectively, and on the other hand, it has a positive effect on improving the treatment efficiency.
Immunological test; Quality control; Relevant measures; Test result; Reliability; Accuracy
河南中医药大学第三附属医院 检验科,河南 郑州 450008
韩洁琼(1984-),女,检验师,研究生。
10.14126/j.cnki.1008-7044.2017.06.007
R 446.6
A
1008-7044(2017)06-0647-03
2017-06-23)

